Новые требования к введению в обращение медицинских изделий: оценка соответствия техническим регламентам презентация
Содержание
- 2. Реформа в сфере обращения медицинских изделий Реформа состоит в переходе от государственной регистрации ИМН к оценке
- 3. Технический регламент VS Гос.регистрация ПРИНЦИПИАЛЬНЫЕ ОТЛИЧИЯ изменение статуса некоторых продуктов, которые стали немедицинскими; изменение документации, которая
- 4. Статус: НЕМЕДИЦИНСКАЯ продукция Определение термина «медицинское изделие» в Техническом регламенте относительно медицинских изделий (Постановление КМУ №
- 5. Разрешительные документы: Декларация соответствия. Выдает: производитель медицинского изделия или его уполномоченный представитель в Украине. «Декларирование соответствия
- 6. Разрешительные документы: ОБЯЗАТЕЛЬНАЯ информация в декларации: 1) название, код или другие идентификационные обозначения изделия или группы
- 7. Изменение органов, назначенных для проведения процедуры Раньше - ГЛС. Сейчас - «назначенные органы» (10 органов государственной
- 8. Уполномоченный представитель Обязательным требованием технических регламентов для всех классов изделий, и для всех видов процедур оценки
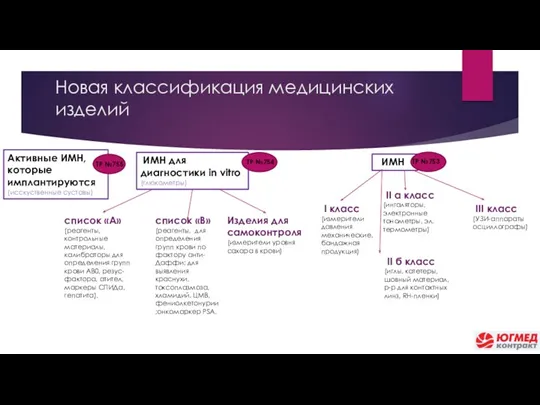
- 9. ИМН ИМН для диагностики in vitro (глюкометры) Новая классификация медицинских изделий Активные ИМН, которые имплантируются (исскуственные
- 10. Новая классификация медицинских изделий В зависимости от сферы применения медицинские изделия подпадают под действие одного из
- 11. Процедура оценки соответствия ИМН I класса (нестерильных, без функций измерения). Самодекларирование Для соответствия требованиям технических регламентов
- 12. Процедура оценки соответствия требованиям технических регламентов для остальных ИМН Оценка соответствия с привлечением назначенного органа. I
- 13. Оценка соответствия путем аудита завода является более обстоятельной, длительной и затратной процедурой по сравнению с попартийной
- 14. Дополнительная процедура оценки соотвествия для ИМН с измерительной функцией (ТР №94 метрология) Назначенный орган проводит метрологическую
- 15. Требования к маркировке Все изделия, декларируемые, как соотвествующие требованиям ТР маркируются национальным знаком соответствия: Если оценка
- 16. Требования к маркировке Все изделия, с измерительной функцией маркируются еще ДОПОЛНИТЕЛЬНЫМ МЕТРОЛОГИЧЕСКИМ ЗНАКОМ. В квадрате рядом
- 17. Упаковка изделия должна иметь информацию (письменно или в форме символов) Название изделия, торговая марка; Производитель: название,
- 18. Изменения требований к инструкции 1) Нанесение маркировки соответствия ТР (трилистник + метрологический знак); 2) Наличие даты
- 19. ВАЖНО ЗНАТЬ!!! Действие технических регламентов не распространяется на медицинские изделия, которые прошли государственную регистрацию и были
- 20. ВАЖНО ЗНАТЬ!!! Действие Технического регламента по электромагнитной совместимости (№785, от 29.07.2009) для ИМН, работающих от внешних
- 21. ВАЖНО ЗНАТЬ!!! ИМН - источники ионизирующего излучения, подлежат дополнительной оценке соответствия ТР закрытых источников ионизирующего излучения
- 22. ВАЖНО ЗНАТЬ!!! Если ИМН определяется производителем, как средство индивидуальной защиты, такое ИМН должно еще соответствовать ТР
- 23. ВАЖНО ЗНАТЬ!!! Если ИМН содержит, как неотъемлемую часть вещество, которое в случае отдельного использования может рассматирваться
- 24. Рыночный надзор. Органом рыночного надзора за медицинскими изделиями, прошедшими процедуру оценки соответствия, является Гослекслужба Украины и
- 25. Формальное несоответствие Державний ринковий нагляд і контроль засобів вимірювальної техніки 100. Державний ринковий нагляд за відповідністю
- 27. Скачать презентацию























 Основы кибербезопасности
Основы кибербезопасности Партии, партийные системы, избирательные системы
Партии, партийные системы, избирательные системы Организационно- правовые основы внедрения и функционирования медицинского страхования в РК
Организационно- правовые основы внедрения и функционирования медицинского страхования в РК Договорное право
Договорное право Еңбек. Еңбек нарығы. Еңбек тәртібі. Еңбек демалысы
Еңбек. Еңбек нарығы. Еңбек тәртібі. Еңбек демалысы Документационное обеспечение управления
Документационное обеспечение управления Конституция – основной Закон Республики Казахстан
Конституция – основной Закон Республики Казахстан Обязательное подтверждение соответствия товаров требованиям технических регламентов
Обязательное подтверждение соответствия товаров требованиям технических регламентов Избирательная кампания в РФ
Избирательная кампания в РФ История развития типологии теоретического правопонимания
История развития типологии теоретического правопонимания Объективная сторона преступления. (Тема 6)
Объективная сторона преступления. (Тема 6) Исковое требование о возмещении ущерба. Пример
Исковое требование о возмещении ущерба. Пример Поощрение и дисциплинарная ответственность муниципального служащего
Поощрение и дисциплинарная ответственность муниципального служащего Продовольственная и сельскохозяйственная организация ООН
Продовольственная и сельскохозяйственная организация ООН Трудоустройство вожатого
Трудоустройство вожатого Государственное управление охраной труда и законодательная база безопасных условий труда
Государственное управление охраной труда и законодательная база безопасных условий труда Трудовое право
Трудовое право Судебная система Российской Федерации
Судебная система Российской Федерации Жеке сот орындаушысының қызметін ұйымдастыру
Жеке сот орындаушысының қызметін ұйымдастыру Порядок внесення змін та доповнень до митної декларації. Особливості подання аркушу коррегування
Порядок внесення змін та доповнень до митної декларації. Особливості подання аркушу коррегування Подсудность уголовных дел. Подготовка к судебному заседанию. Лекция 18
Подсудность уголовных дел. Подготовка к судебному заседанию. Лекция 18 Проблемы реализации конституционного принципа разделения властей в РФ
Проблемы реализации конституционного принципа разделения властей в РФ Методы управления в органах внутренних дел. Тема №4
Методы управления в органах внутренних дел. Тема №4 Децентралізація системи влади в Україні: аналіз основних засад та напрямів
Децентралізація системи влади в Україні: аналіз основних засад та напрямів Классификация сроков в российском гражданском праве
Классификация сроков в российском гражданском праве Государственные услуги и сервисы росреестра для физических и юридических лиц
Государственные услуги и сервисы росреестра для физических и юридических лиц Понятие объекта преступления, его сущность и значение. Тема 3
Понятие объекта преступления, его сущность и значение. Тема 3 Заңды жауапкершілік
Заңды жауапкершілік