Содержание
- 2. Дыхательная цепь. В 1961 – 1966г.г. английский биохимик П.Митчел описал теорию окислительного фосфорилирования, связанную с транспортом
- 3. Дыхательная цепь является частью процесса окислительного фосфорилирования. Компоненты дыхательной цепи катализируют перенос электронов от НАДН +
- 4. Из-за большой разности окислительно-восстановительных потенциалов донора (НАДН + Н+ и, соответственно, КоQH2) и акцептора (О2) реакция
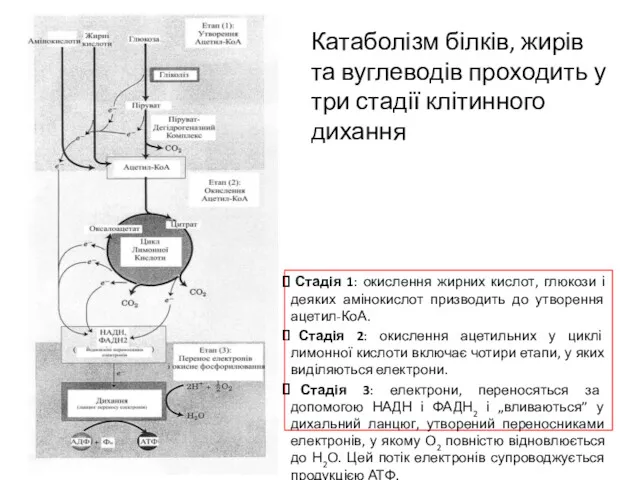
- 7. Стадія 1: окислення жирних кислот, глюкози і деяких амінокислот призводить до утворення ацетил-КоА. Стадія 2: окислення
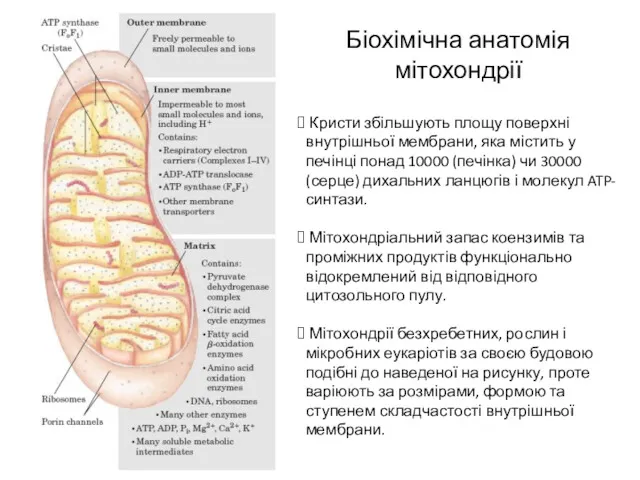
- 8. Біохімічна анатомія мітохондрії Кристи збільшують площу поверхні внутрішньої мембрани, яка містить у печінці понад 10000 (печінка)
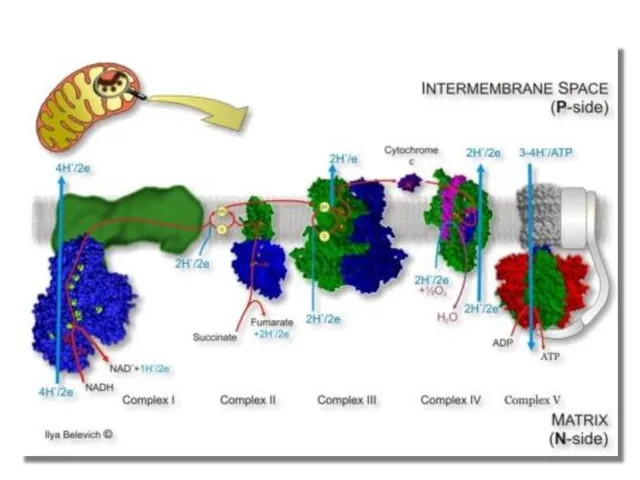
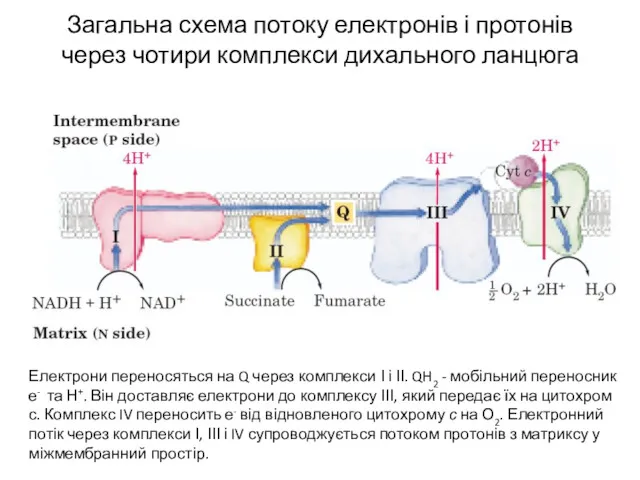
- 9. Загальна схема потоку електронів і протонів через чотири комплекси дихального ланцюга Електрони переносяться на Q через
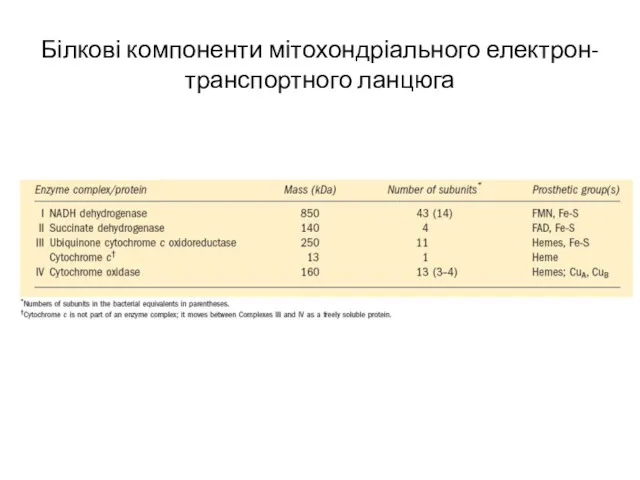
- 10. Білкові компоненти мітохондріального електрон-транспортного ланцюга
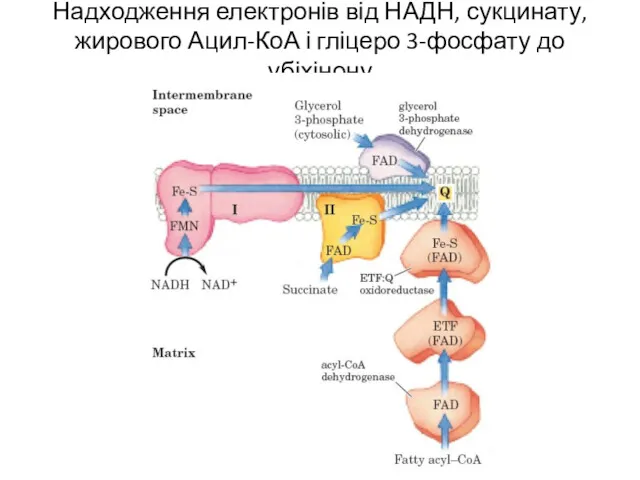
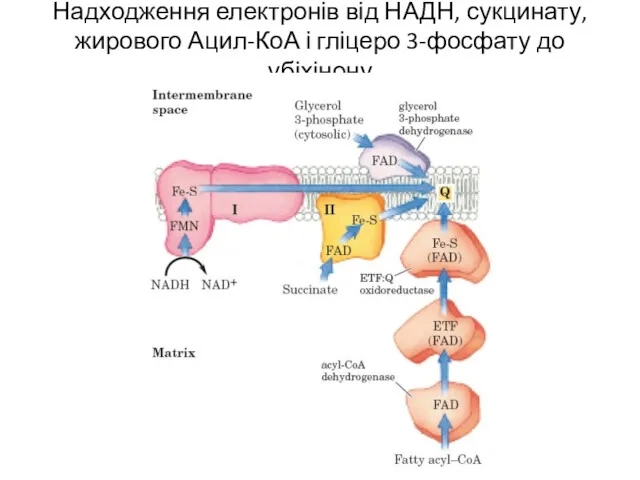
- 11. Надходження електронів від НАДН, сукцинату, жирового Ацил-КоА і гліцеро 3-фосфату до убіхінону
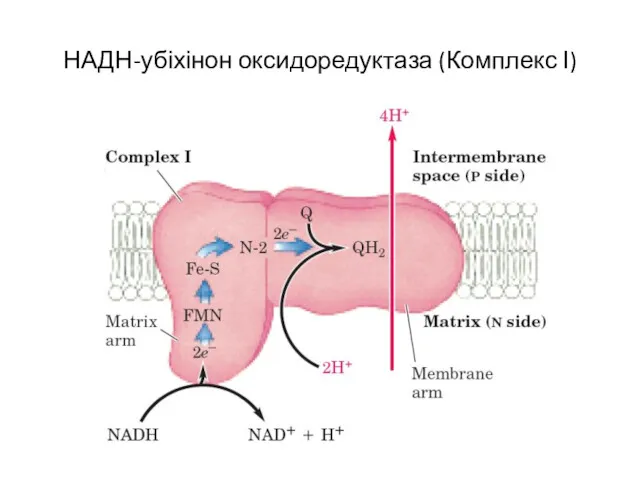
- 12. НАДН-убіхінон оксидоредуктаза (Комплекс І)
- 13. Деякі важливі реакції, що каталізуються НАД(Ф)Н-дегідрогеназами
- 14. Надходження електронів від НАДН, сукцинату, жирового Ацил-КоА і гліцеро 3-фосфату до убіхінону
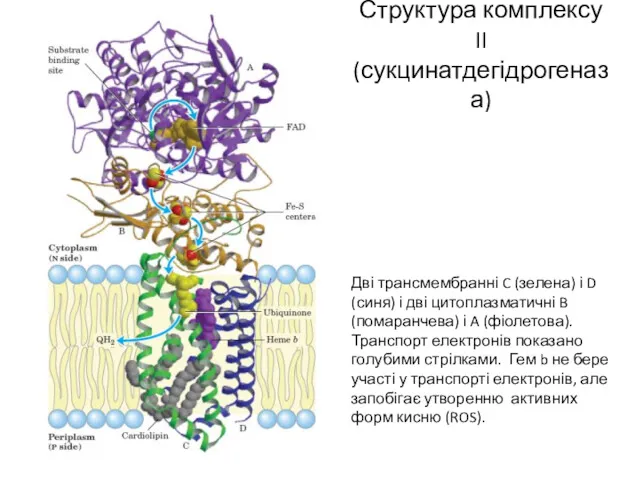
- 15. Структура комплексу II (сукцинатдегідрогеназа) Дві трансмембранні C (зелена) і D (синя) і дві цитоплазматичні B (помаранчева)
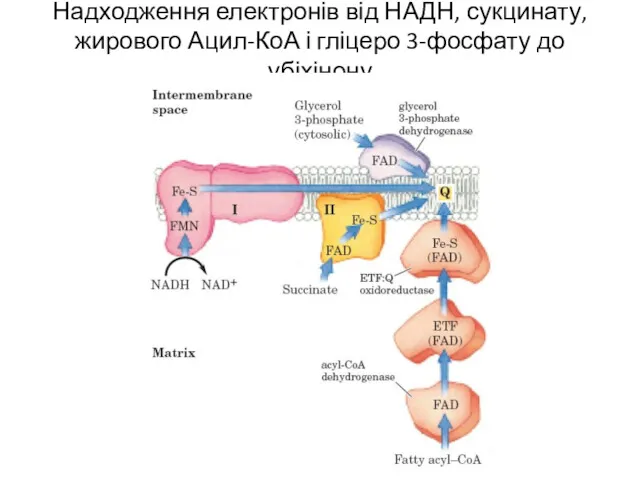
- 16. Надходження електронів від НАДН, сукцинату, жирового Ацил-КоА і гліцеро 3-фосфату до убіхінону
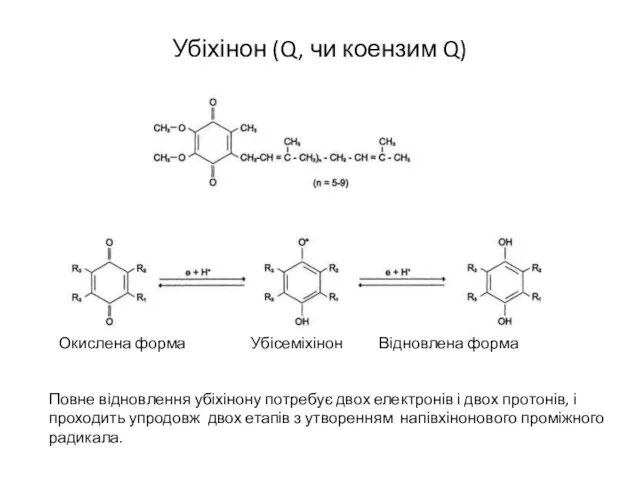
- 17. Убіхінон (Q, чи коензим Q) Повне відновлення убіхінону потребує двох електронів і двох протонів, і проходить
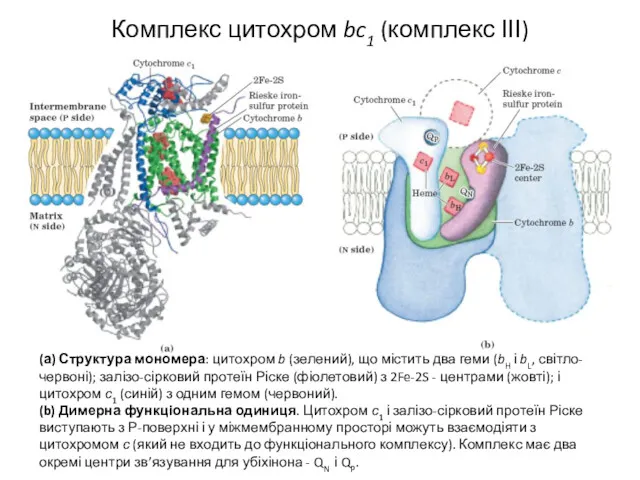
- 18. Комплекс цитохром bc1 (комплекс ІІІ) (а) Структура мономера: цитохром b (зелений), що містить два геми (bH
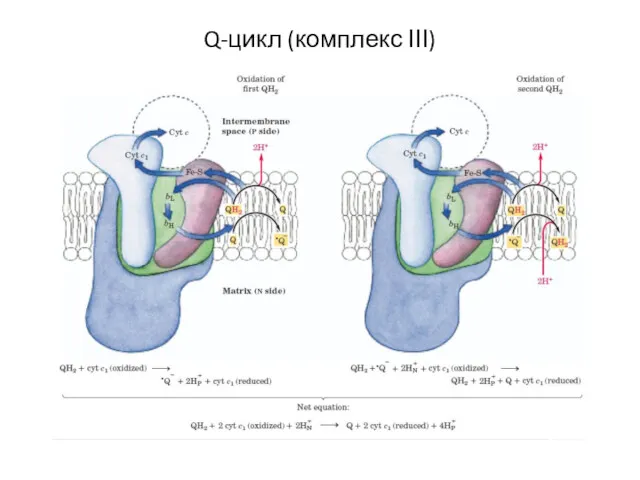
- 19. Q-цикл (комплекс ІІІ)
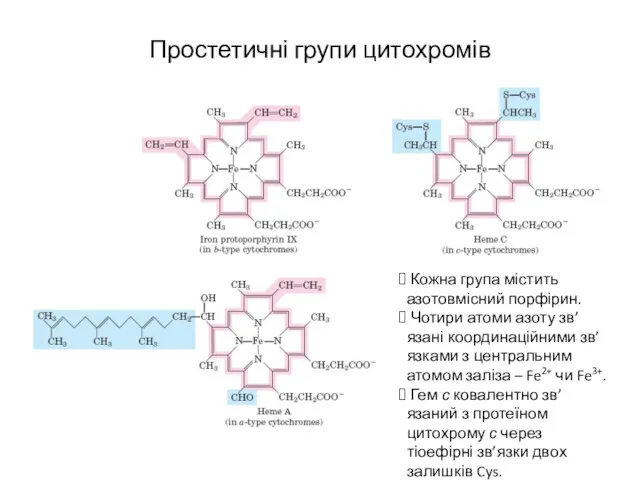
- 20. Простетичні групи цитохромів Кожна група містить азотовмісний порфірин. Чотири атоми азоту зв’язані координаційними зв’язками з центральним
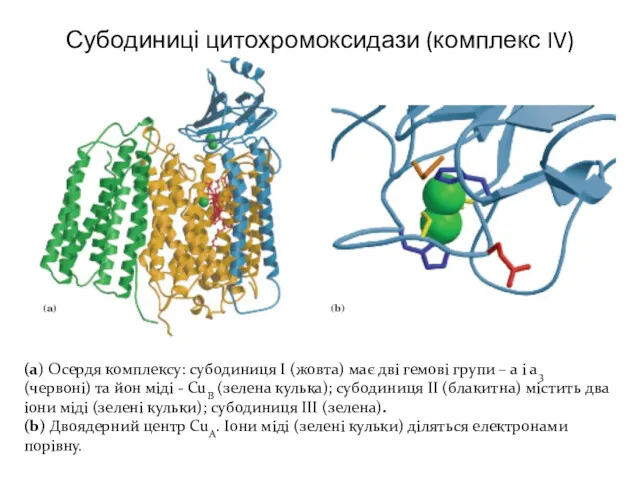
- 21. Субодиниці цитохромоксидази (комплекс IV) (а) Осердя комплексу: субодиниця І (жовта) має дві гемові групи – а
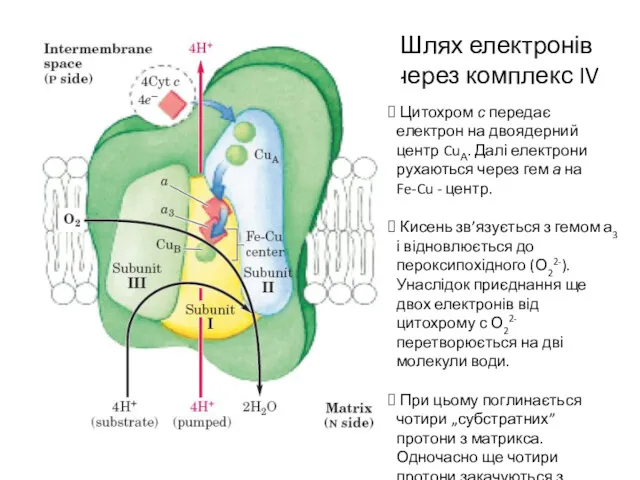
- 22. Шлях електронів через комплекс IV Цитохром с передає електрон на двоядерний центр CuА. Далі електрони рухаються
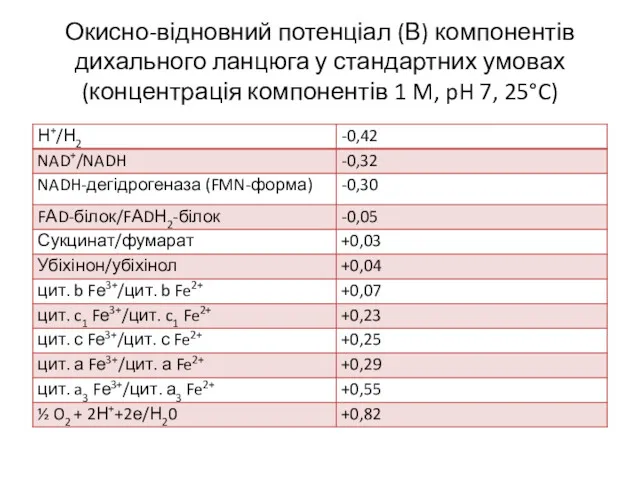
- 23. Окисно-відновний потенціал (В) компонентів дихального ланцюга у стандартних умовах (концентрація компонентів 1 M, pH 7, 25°C)
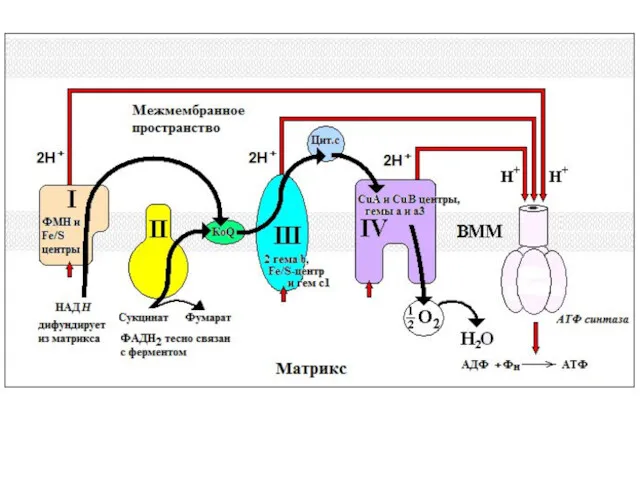
- 24. Схема електрон-транспортного ланцюга
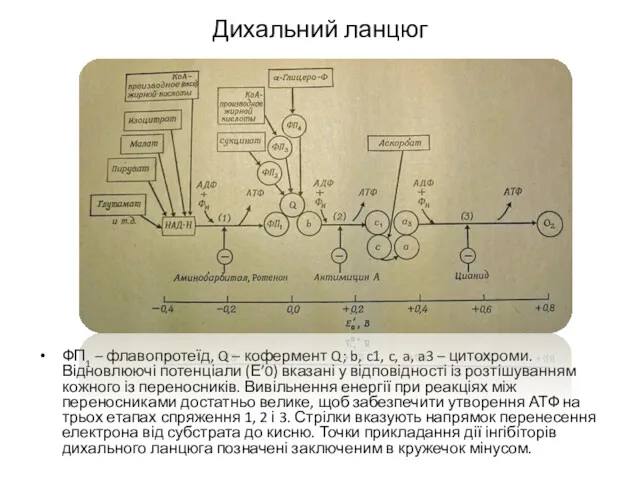
- 25. Дихальний ланцюг ФП1 – флавопротеїд, Q – кофермент Q; b, c1, c, a, a3 – цитохроми.
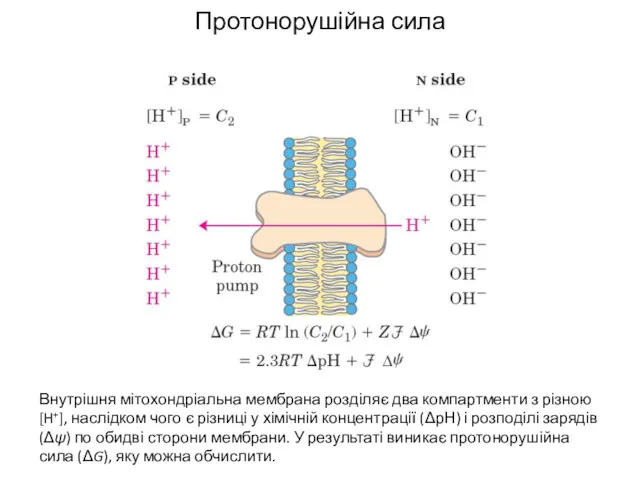
- 26. Протонорушійна сила Внутрішня мітохондріальна мембрана розділяє два компартменти з різною [H+], наслідком чого є різниці у
- 27. Sir Peter D. Mitchell (1920 – 1992) Nobel prize in chemistry (1978) "for his contribution to
- 29. Скачать презентацию






 Легенды и были о цветах
Легенды и были о цветах ДНК-содержащие онкогенные вирусы
ДНК-содержащие онкогенные вирусы Тип Хордовые
Тип Хордовые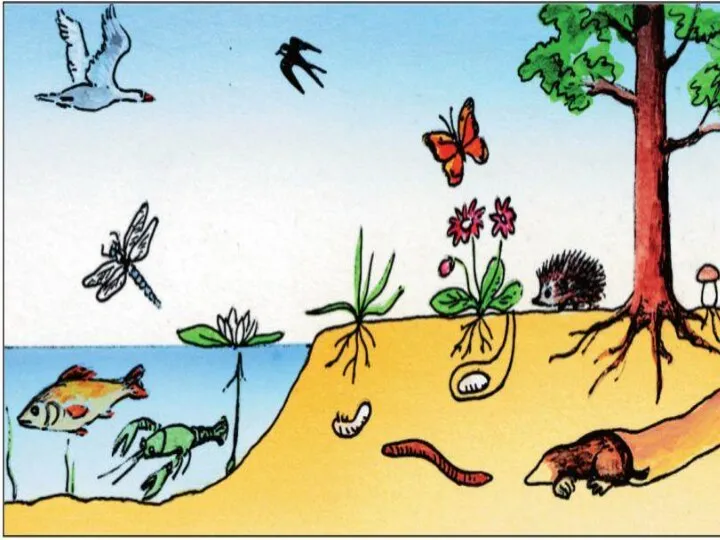 Среда обитания
Среда обитания Гіпофіз, епіфіз, щитоподібна залоза
Гіпофіз, епіфіз, щитоподібна залоза ПРЕЗЕНТАЦИЯ ДЛЯ ИНТЕРАКТИВНОЙ ДОСКИ. Тест Рыбы 7 класс.
ПРЕЗЕНТАЦИЯ ДЛЯ ИНТЕРАКТИВНОЙ ДОСКИ. Тест Рыбы 7 класс. презентация Пушистый доктор
презентация Пушистый доктор Cladocera
Cladocera Класс млекопитающие. (7)
Класс млекопитающие. (7) Сүйекті балықтар класы
Сүйекті балықтар класы Деление клетки
Деление клетки Приспособленность живых организмов к среде обитания
Приспособленность живых организмов к среде обитания Биологическая викторина для 6 класса
Биологическая викторина для 6 класса Брюхоногие моллюски
Брюхоногие моллюски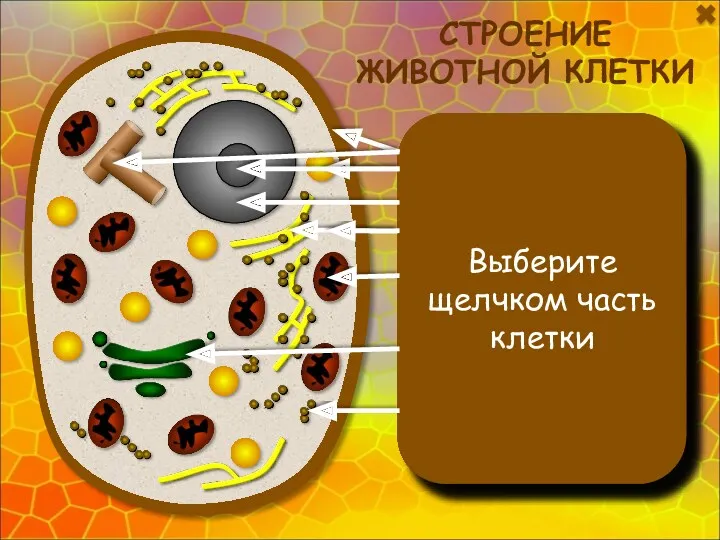 Интерактивная модель по биологии Строение животной клетки для 7 (8) классов
Интерактивная модель по биологии Строение животной клетки для 7 (8) классов Функциональная морфология аппарата внутриклеточного переваривания и энергетического аппарата
Функциональная морфология аппарата внутриклеточного переваривания и энергетического аппарата Brucella (Brucellosis, Bang’s Disease). Occurrence and classification
Brucella (Brucellosis, Bang’s Disease). Occurrence and classification Отряд Зайцеобразные класса Млекопитающие
Отряд Зайцеобразные класса Млекопитающие Папоротники. Размножение
Папоротники. Размножение Тимофеев-Ресовский Н.В (1900-1981)
Тимофеев-Ресовский Н.В (1900-1981) Сенсорные системы
Сенсорные системы Анатомо-физиологические особенности органа слуха и равновесия
Анатомо-физиологические особенности органа слуха и равновесия Вегетативное размножение растений
Вегетативное размножение растений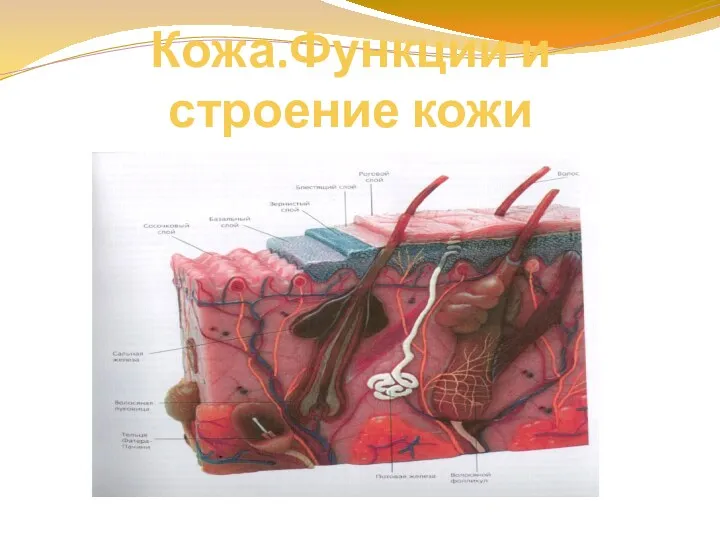 Кожа. Функции и строение кожи
Кожа. Функции и строение кожи Строение волос
Строение волос Строение и функции белков-2
Строение и функции белков-2 Animal reproduction
Animal reproduction Изучение внешнего строения травянистого цветкового растения
Изучение внешнего строения травянистого цветкового растения