Содержание
- 2. Оглавление 1.Определение 2.Строение ферментов 3.Номенклатура ферментов 4.Свойства ферментов 5.Роль ферментов в жизнедеятельности организмов 6.Особенности ферментов 7.Применение
- 3. Определение Ферменты – биологические катализаторы белковой природы, ускоряющие химические реакции в живых организмах и вне их.
- 4. Строение ферментов 1.двухкомпонентными - сложными белками Характерной особенностью двухкомпонентного фермента является то, что ни белковая часть,
- 5. Номенклатура ферментов Сейчас используется новая номенклатура ферментов, принятая в 1961 году. В связи со значительным усложнением
- 6. Свойства ферментов Ферменты обладают такими общими для всех белков свойствами, как: Способность к растворению в воде
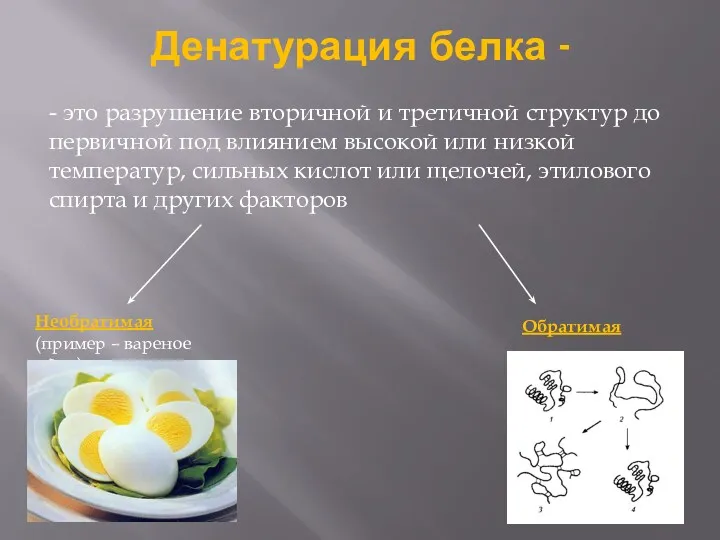
- 7. Денатурация белка - - это разрушение вторичной и третичной структур до первичной под влиянием высокой или
- 8. Свойства ферментов Ферменты обладают также уникальными свойствами: Необычно высокая каталитическая активность. Так, добавка незначительных количеств фермента
- 9. Свойства ферментов Высокая специфичность ферментов. Благодаря данному свойству в организме не воцаряется хаос: каждый из них
- 10. Роль ферментов в жизнедеятельности организмов можно проиллюстрировать схемой:
- 11. Особенности ферментов Многие ферменты наиболее эффективны при температуре человеческого тела (35-42 С). При температуре, отличной от
- 12. Особенности ферментов Ферменты наиболее эффективно действуют при строго определенной среде раствора, при определенных показателях т.н. водородного
- 13. Применение Ферменты используются в производстве: Пищи и напитков(вино, хлеб, сыр) Медикаментов («Пепсин», «Мезим», «Фестал») Моющих средств
- 14. Проверь себя: ТЕСТ
- 15. 1.(3 балла). Класс соединений, к которому относятся ферменты: А. Белки Б. Жиры В. Углеводы. Г. Нуклеиновые
- 16. 1.(3 балла). Класс соединений, к которому относятся ферменты: А. Белки Б. Жиры В. Углеводы. Г. Нуклеиновые
- 17. 2.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению: А. Аминокислоты Б. Углеводороды. В. Углеводы. Г. Высшие
- 18. 2.(3 балла). Вещества, подвергающиеся в организме ферментативному разложению: А. Аминокислоты Б. Углеводороды. В. Углеводы. Г. Высшие
- 19. 3.(3 балла). Продуктами гидролиза белков являются: А. Глюкоза. Б. Аминокислоты. В. Глицерин и жирные кислоты. Г.
- 20. 3.(3 балла). Продуктами гидролиза белков являются: А. Глюкоза. Б. Аминокислоты. В. Глицерин и жирные кислоты. Г.
- 21. 4. (3 балла). Температура, при которой ферменты в организме человека наиболее эффективны: А. 10 °С. Б.
- 22. 4. (3 балла). Температура, при которой ферменты в организме человека наиболее эффективны: А. 10 °С. Б.
- 23. 5.(3 балла). Селективностью (избирательностью) действия ферментов называется: А. Способность фермента ускорять одну или группу однотипных реакций.
- 24. 5.(3 балла). Селективностью (избирательностью) действия ферментов называется: А. Способность фермента ускорять одну или группу однотипных реакций.
- 25. 6.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее активен: А. 1,5—2,0. Б. 3,0—4,0.
- 26. 6.(3 балла). Значение рН желудочного сока, при котором фермент пепсин наиболее активен: А. 1,5—2,0. Б. 3,0—4,0.
- 27. 7.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета: А. Амилаза. Б. Пепсин. В.
- 28. 7.(3 балла). Фермент, добавляемый к зубным пастам для удаления зубного налета: А. Амилаза. Б. Пепсин. В.
- 29. 8.(3 балла). Фермент трипсин расщепляет: А. Углеводы. Б. Белки. В. Жиры. Г. Нуклеиновые кислоты.
- 30. 8.(3 балла). Фермент трипсин расщепляет: А. Углеводы. Б. Белки. В. Жиры. Г. Нуклеиновые кислоты.
- 31. 9.(3 балла). Высокая эффективность ферментов объясняется: А. Быстрым восстановлением их молекул в процессе работы. Б. Многообразием
- 32. 9.(3 балла). Высокая эффективность ферментов объясняется: А. Быстрым восстановлением их молекул в процессе работы. Б. Многообразием
- 33. 10.(3 балла). Отдел желудка жвачных животных, в котором вырабатывается фермент реннин, используемый в сыроделии: А. Сетка.
- 34. 10.(3 балла). Отдел желудка жвачных животных, в котором вырабатывается фермент реннин, используемый в сыроделии: А. Сетка.
- 35. Домашнее задание. § 19 учебника. Ответить на вопросы и выполнить задания после текста § 19 учебника
- 36. Список литературы 1. Габриелян О.С.,А.В.Яшукова Методическое пособие. Химия. 10 класс.(базовый уровень) , М.Дрофа,2008 2. Габриелян О.С.Химия.10
- 38. Скачать презентацию


































 Обеспечение человечества продовольствием
Обеспечение человечества продовольствием Розмноження тварин у природі
Розмноження тварин у природі презентация Цветок
презентация Цветок Анатомия человека
Анатомия человека Язык животных
Язык животных Тварини та рослини Червоної Книги України
Тварини та рослини Червоної Книги України Химические элементы и неорганические вещества клетки
Химические элементы и неорганические вещества клетки Пищеварительная система. Тонкий кишечник
Пищеварительная система. Тонкий кишечник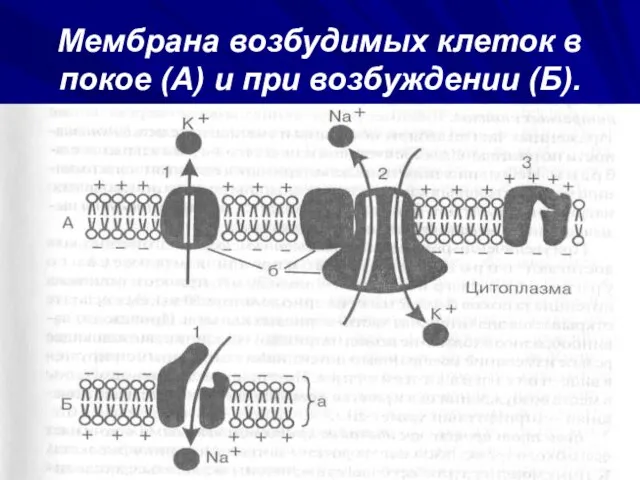 Мембрана возбудимых клеток в покое (А) и при возбуждении (Б)
Мембрана возбудимых клеток в покое (А) и при возбуждении (Б) Побег, его строение и развитие.
Побег, его строение и развитие. Көмірсулары алмасуының бұзылыстары
Көмірсулары алмасуының бұзылыстары Опыление и его виды
Опыление и его виды Общая характеристика Голосеменных
Общая характеристика Голосеменных Функциональная анатомия костей туловища. Соединения костей туловища
Функциональная анатомия костей туловища. Соединения костей туловища e066e089db59f3addec16ce3c001bf5
e066e089db59f3addec16ce3c001bf5 Масти лошадей
Масти лошадей Геномика. Разделы геномики
Геномика. Разделы геномики Как появился человек на Земле
Как появился человек на Земле презентация Амфибии
презентация Амфибии Культивирование отдельных (одиночных) клеток
Культивирование отдельных (одиночных) клеток Споровые растения
Споровые растения Липиды: обмен, переваривание, окисление
Липиды: обмен, переваривание, окисление Движение крови и лимфы
Движение крови и лимфы Общий обзор организма человека
Общий обзор организма человека В ходе каких реакций в природе получаются: глюкоза, фруктоза, сахароза, крахмал, целлюлоза. Области их применения
В ходе каких реакций в природе получаются: глюкоза, фруктоза, сахароза, крахмал, целлюлоза. Области их применения Життя в морях та океані. Океан та людина
Життя в морях та океані. Океан та людина Деградація ксенобіотиків за допомогою мікроорганізмів
Деградація ксенобіотиків за допомогою мікроорганізмів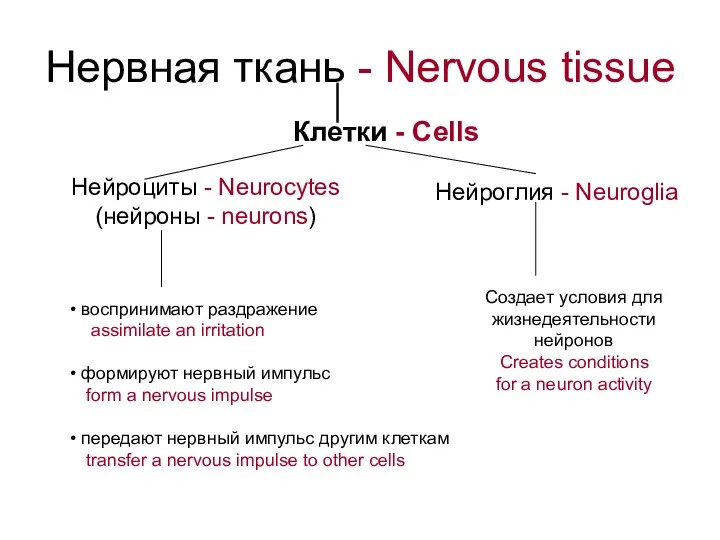 Нервная ткань
Нервная ткань