Слайд 2

Фотосинтетическое фосфорилирование (ФФ)
ФФ – это синтез молекулы АТФ за счет энергии
трансмембранного потенциала (ΔμН+) тилакоидной мембраны.
ΔμН+
АДФ + Фн АТФ + Н2О
Слайд 3

Типы фотофосфорилирования
Нециклическое фотофосфорилирование.
2АДФ + Фн + 2НАДФ+ + 2 Н2О 2АТФ
+ + О2 + 2НАДФН
Осуществляют фотосистемы ФСI и ФСII.
2. Циклическое фотофосфорилирование
АДФ + Фн АТФ + Н2О
Осуществляет ФСI.
Слайд 4
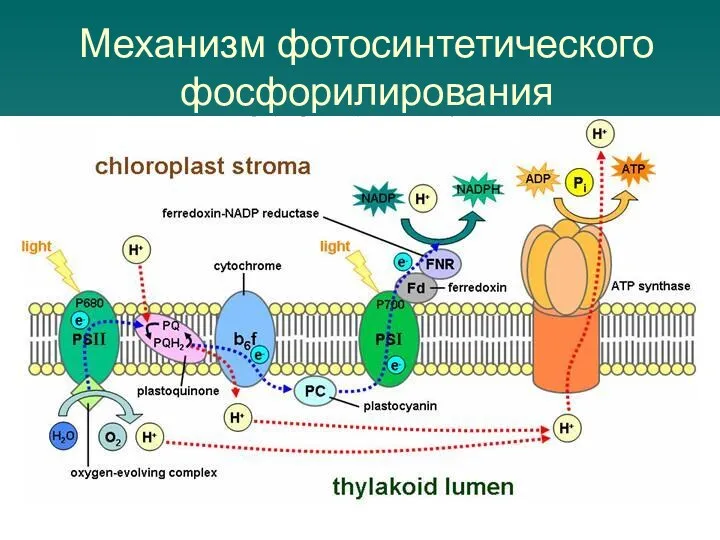
Механизм фотосинтетического фосфорилирования
Слайд 5
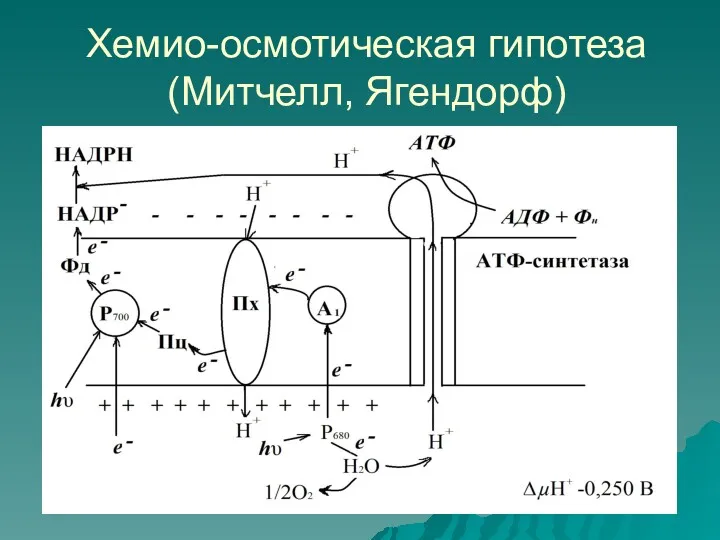
Хемио-осмотическая гипотеза (Митчелл, Ягендорф)
Слайд 6
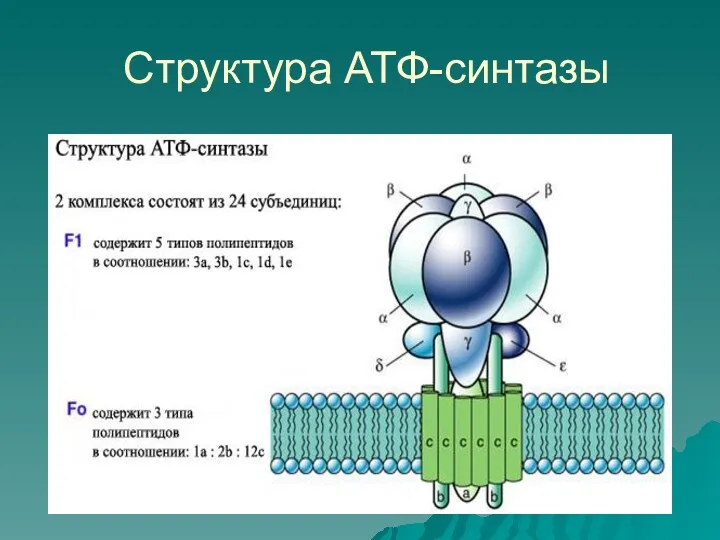
Слайд 7

Биохимия фотосинтеза
Сущность темновой фазы фотосинтеза заключается в трансформации макроэргической связи АТФ
и НАДФН в стабильную форму энергии – органическую связь.
СО2 + АТФ + НАДФН
[СН2О] + АДФ + Фн + НАДФ
Слайд 8

Цикл Кальвина
В 1957 году Кальвин предложил биохимический механизм превращения СО2 в
фосфоглицериновый альдегид (ФГА).
1 сек
*СО2 СН2ОН-СНОН-*СООН
ФГК
Это С3-путь или восстановительный пентозофосфатный путь (ВПФП).
Слайд 9

Методы Кальвина
В лаборатории Кальвина, Басхэма и Бенсона впервые использовали методы:
1.
Для фотосинтеза использовали *СО2 с радиоактивным углеродом – С14.
2. Фиксация растительного образца кипящим этиловым спиртом.
3. Бумажная хроматография.
4. Радиоавтография, необходимая для идентификации изотопных молекул.
5. Фотостатированная камера (фитотрон).
Слайд 10

Цикл Кальвина
Включение СО2 в цикл
1) Активирование первичного акцептора
(рибулозомонофосфат)
РМФ + АТФ →
РБФ + АДФ
РБФ – рибулозо-1,5-бисфосфат
Слайд 11
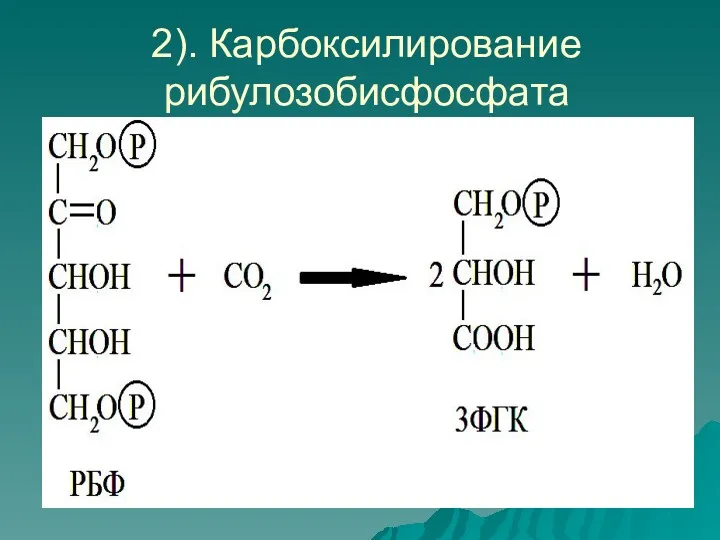
2). Карбоксилирование рибулозобисфосфата
Слайд 12

Свойства рибулозобисфосфаткарбоксилазы
РБФ-карбоксилаза (Rubisco)
КФ 4.1.1.39 – самый распространенный белок биосферы:
а)
50% от общего количества белков в хлоропласте;
б) 70% составляют растительные белки в биосфере;
в) 20% всех белков биосферы являются РБФ-карбоксилазой, т.е. каждый пятый белок в природе это Rubisco.
Слайд 13

Свойства Rubisco
2. Фермент двойного кодирования.
Rubisco имеет молекулярную массу 550 кДа. Состоит
из 8 больших (L) c Mr 51-58 кДа
и 8 малых (S) с Mr 12-18 кДа.
Формула комплекса L8-S8.
Большие субъединицы кодируются хлоропластной ДНК (rbcL), малые ядерные ДНК (rbcS).
Слайд 14

Свойства Rubisco
Сборка белка происходит в хлоропластах при участии белка шаперона (Hsc60),
который кодируется в ядре. Для сборки функционально активного фермента необходима четкая регуляция работы двух геномов (ядерного и хлоропластного).
Каталитический центр фермента формируют аминокислотные остатки C- и N-концов полипептидов двух больших субъединиц. У Rubisco высших растений имеется 8 каталитических центров.
Слайд 15

Свойства Rubisco
Димеры больших субъединиц каталитически активны и в отсутствие малых субъединиц.
Малые субъединицы играют регуляторную роль.
3. Бифункциональность РБФ-карбоксилазы. Фермент катализирует карбоксилазную активность (функционирование ВПФП) и оксигеназную (функционирование фотодыхательного метаболизма).
Слайд 16
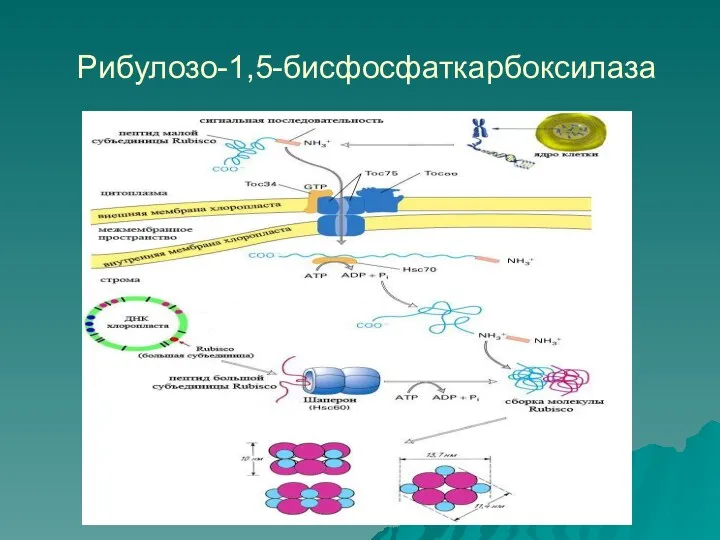
Рибулозо-1,5-бисфосфаткарбоксилаза
Слайд 17

II. Фаза восстановления
Осуществляется с помощью двух реакций:
А) активирование 3ФГК:
3ФГК
+ АТФ → 1,3ФГК + АДФ (фермент киназа)
Б) восстановление ФГК до ФГА
1,3ФГК + НАДФН → ФГА + НАДФ+
(фермент глицероальдегиддегидрогеназа)
Слайд 18
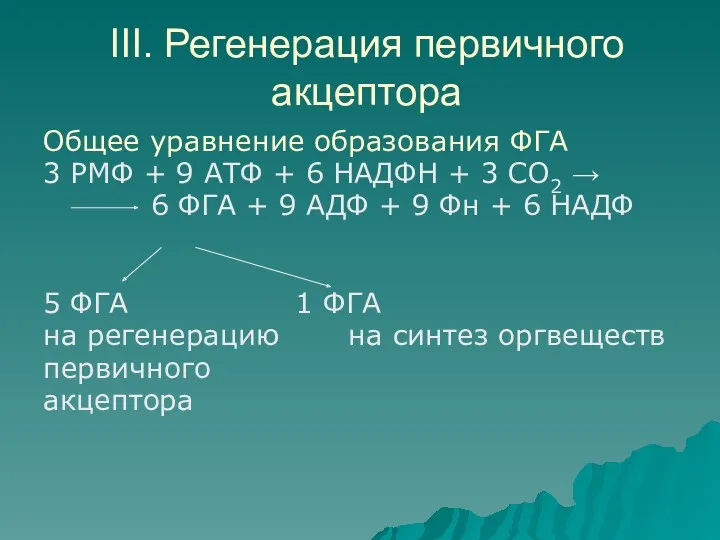
III. Регенерация первичного акцептора
Общее уравнение образования ФГА
3 РМФ + 9
АТФ + 6 НАДФН + 3 СО2 →
6 ФГА + 9 АДФ + 9 Фн + 6 НАДФ
5 ФГА 1 ФГА
на регенерацию на синтез оргвеществ
первичного
акцептора
Слайд 19
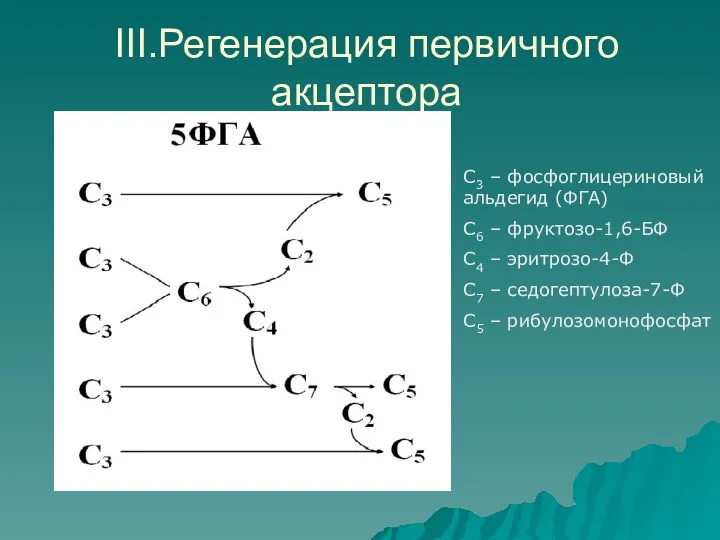
III.Регенерация первичного акцептора
С3 – фосфоглицериновый альдегид (ФГА)
С6 – фруктозо-1,6-БФ
С4 – эритрозо-4-Ф
С7
– седогептулоза-7-Ф
С5 – рибулозомонофосфат
Слайд 20

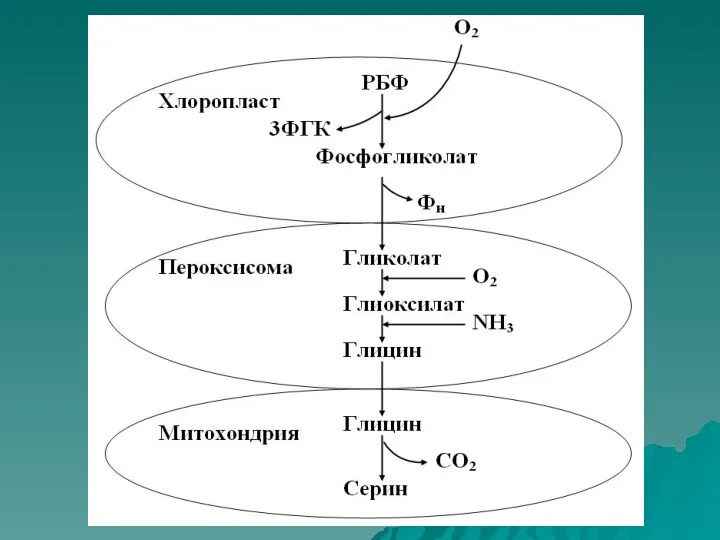
Фотодыхание
Фотодыхание – это светоиндуцируемое выделение углекислого газа зелеными листьями растений.
Фотодыхание
обнаружено в 1965 году. Его осуществляет комплекс органоидов: хлоропласт, пероксисома, митохондрия.
Слайд 21
Слайд 22

Причины фотодыхания
1. Наличие оксигеназной функции у рибулозобисфосфаткарбоксилазы.
2. Высокая концентрация кислорода в
атмосфере, составляющая 21%.
3. Значительные количества кислорода, проникающие в ткань растений, индуцируют оксигеназную функцию Rubisco.
Слайд 23

Значение фотодыхания
На фотодыхательный метаболизм у С3-растений тратится до 55% продуктов фотосинтеза.
1.
Фотодыхание выступает как футильный цикл, обеспечивающий защиту органических веществ (ДНК-белков) от фотодеструкции.
2. Образование протеиногенных аминокислот (глицина и серина).
3. Обеспечивает синтез сахарозы (с небольшой скоростью).
Слайд 24

Значение фотодыхания
Фотодыхание – это «расплата» растений за созданную ими кислородную атмосферу.
Потеря 40-50% продуктов фотосинтеза является необходимой «данью» для выживания в условиях кислородного стресса.
Слайд 25

Цикл Хэтча-Слэйка
Карпилов И.С. в 1963 году обнаружил включение 14СО2 в яблочную
кислоту в листьях кукурузы.
Коржик в 1964 году установил в сахарном тростнике функционирование ФЕП-карбоксилазы.
Хэтч и Слэйк в 1969 году создали цикл ассимиляции СО2 по С4-типу фотосинтеза.
Слайд 26
Анатомия листа у С4 - растений
Слайд 27

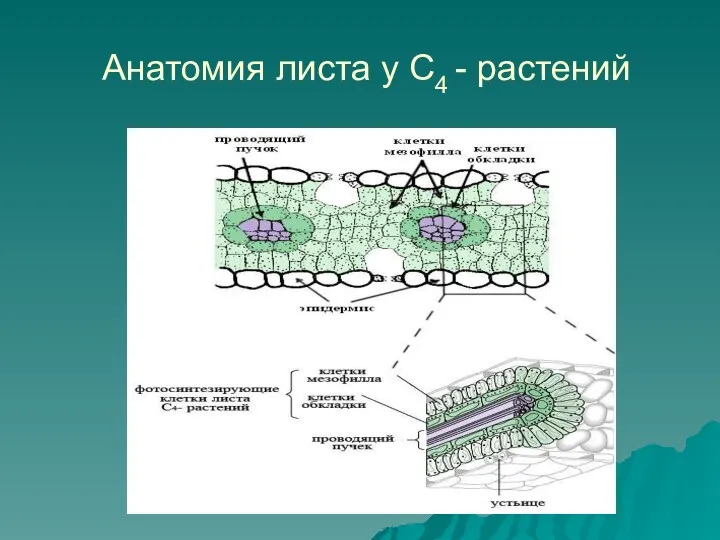
Анатомия листа у С4 - растений
Для С4-растений характерна кранц-анатомия листа.
Внутреннее
кольцо (обкладка) изолировано клетками мезофилла.
В клетках обкладки локализован цикл Кальвина.
В мезофильной ткани протекает специфический С4-путь ассимиляции углерода.
Слайд 28
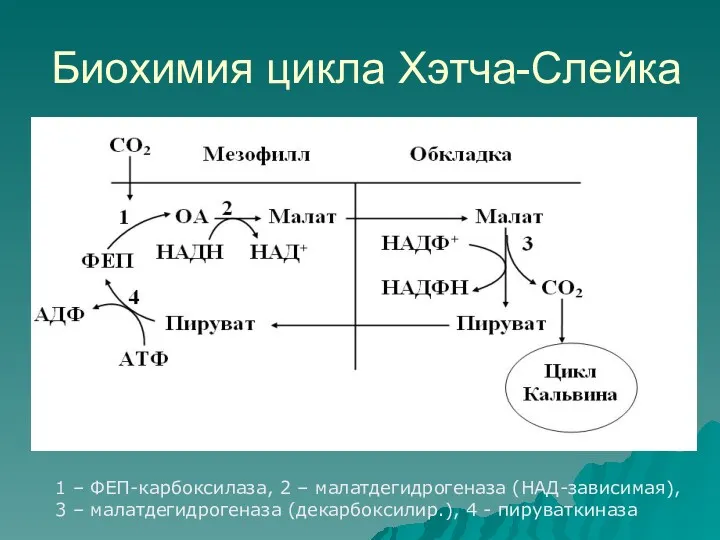
Биохимия цикла Хэтча-Слейка
1 – ФЕП-карбоксилаза, 2 – малатдегидрогеназа (НАД-зависимая), 3 –
малатдегидрогеназа (декарбоксилир.), 4 - пируваткиназа
Слайд 29

Физиологическая роль цикла Хэтча-Слэйка
Физиологическое значение цикла:
1) Увеличение концентрации СО2 в клетках
обкладки.
Используется новый фермент ФЕП-карбоксилаза, обладающий высоким сродством к углекислому газу.
2) Рибулозо-бисфосфат-карбоксилаза «спрятана» в клетках обкладки, где концентрация кислорода минимальна.
Фотодыхание отсутствует или слабо выражено.
Слайд 30

Физиологическая роль цикла Хэтча-Слэйка
3) ФЕП-карбоксилаза является уникальным ферментом, обладающим большим сродством
к СО2, что имеет важное значение в условиях низкой концентрации СО2 в атмосфере (0,035 %).
4) ФЕП-карбоксилаза является термофильным ферментом (оптимум t = 30-40оС, что обеспечивает эффективное карбоксилирование при высоких температурах.
Слайд 31

Эволюция фотосинтеза
Причины эволюции в последние 600 млн. лет обусловлены резким изменением
факторов внешней среды.
1. Концентрация кислорода выросла с 1% до 21%.
2. Количество углекислого газа уменьшилось с 10% до 0,03% (углерод использовался на синтез органических веществ).
3. Нарушение гидробиологического режима. Резкое уменьшение содержания воды в биосфере.
Ксероморфогенез – основной путь эволюции.
Слайд 32

Метаболизм органических кислот по типу толстянковых
Растения, осуществляющие метаболизм по типу толстянковых,
являются суккулентами. Большинство принадлежат к сем.Crassulaceae, отсюда САМ-метаболизм. Представители: колланхое, седум и др.
Слайд 33

САМ-метаболизм
Данные растения адаптировались к дефициту воды на биохимическом уровне. Днем устьица
у этих растений закрываются, чтобы снизить потерю воды. Ночью у них устьица открываются.
Следовательно, СО2 может проникать в ткани только ночью и накапливаться в виде органических кислот.
Слайд 34
Слайд 35

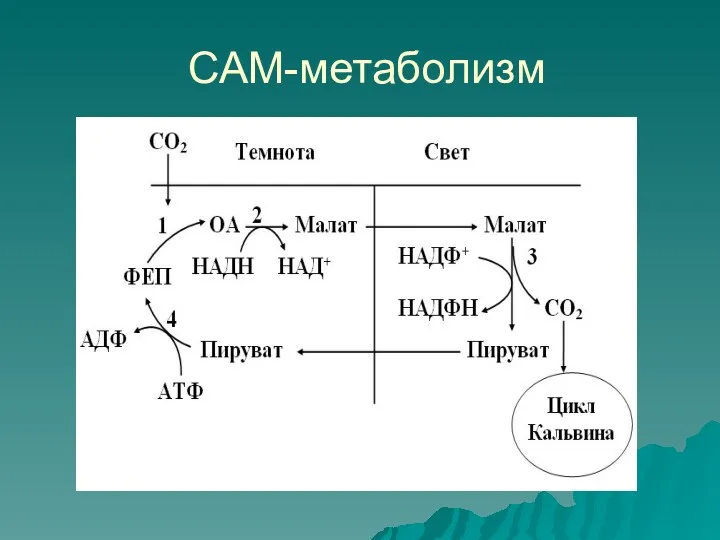
Сущность САМ-метаболизма
1. САМ-фотосинтез осуществляет разделение ассимиляции СО2 и цикла Кальвина не
в пространстве, а во времени.
2. Первичная фиксация СО2 осуществляется в темноте, где ФЕП-карбоксилаза присоединяет его к ФЕПу.
3. Днем устьица закрыты (предотвращение потери воды), и проникновение СО2 невозможно. Малат служит источником эндогенного СО2 (декарбоксилирование).
4. Образовавшийся СО2 диффундирует в хлоропласты и включается в цикл Кальвина.
Слайд 36
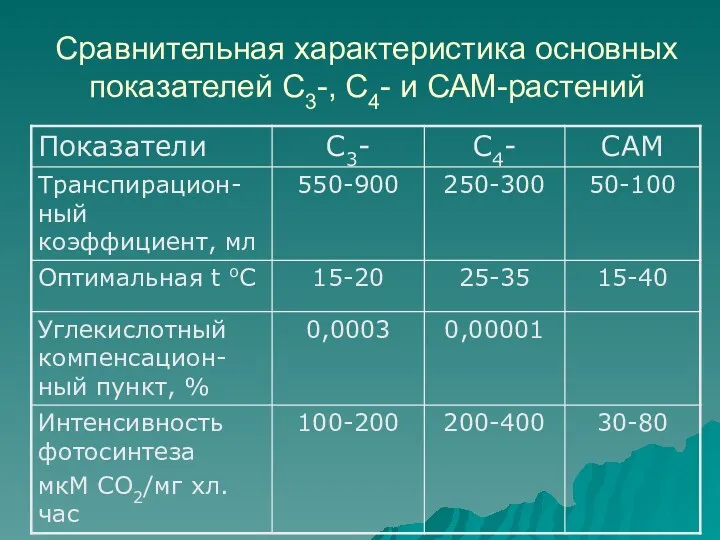
Сравнительная характеристика основных показателей С3-, С4- и САМ-растений
Слайд 37

Фотоокисление воды
До 1931 года доминировала формальдегидная гипотеза происхождения кислорода.
СО2 С +
О2
С + Н2О СН2О
То есть, кислород образовывался по формальдегидной гипотезе из углекислого газа.
Слайд 38

Происхождение кислорода
Ван-Ниль в 1931 году предположил, что кислород образуется из воды.
СО2
+ Н218О СН2О + 18О2
18О – изотоп кислорода.
С помощью изотопа кислорода 18О была доказана справедливость этого утверждения.
Слайд 39

Механизм выделения кислорода
Согласно Кутюрину (1968), молекула кислорода образуется из воды, в
окислении которой участвует непосредственно хлорофилл.
Современная гипотеза предполагает участие марганец-содержащего фермента в окислении воды и формировании молекулы кислорода.
Слайд 40

Механизм выделения кислорода
Mn-содержащий ферментный комплекс







































 Нормальная анатомия легких, плевры и средостения
Нормальная анатомия легких, плевры и средостения Черенкование комнатных растений
Черенкование комнатных растений Такие разные жуки. Коллекции. Занятие № 2. Консультация. Планирование деятельности
Такие разные жуки. Коллекции. Занятие № 2. Консультация. Планирование деятельности Введение в системную биологию
Введение в системную биологию Разнообразие животных
Разнообразие животных Болезни органов дыхания и их предупреждение. Гигиена дыхания
Болезни органов дыхания и их предупреждение. Гигиена дыхания Развитие низших хордовых. Амфибии
Развитие низших хордовых. Амфибии Специфика энергетических систем растительной клетки
Специфика энергетических систем растительной клетки Летучие мыши
Летучие мыши Анатомо-физиологические особенности сердечно сосудистой системы
Анатомо-физиологические особенности сердечно сосудистой системы Презентация у уроку Строение и функции пищеварительной системы человека 8 класс
Презентация у уроку Строение и функции пищеварительной системы человека 8 класс Вопросы экзамена по нервной системе
Вопросы экзамена по нервной системе Устройство речевого аппарата
Устройство речевого аппарата Жизнь и научная деятельность Ж.Б.Ламарка (1744-1829)
Жизнь и научная деятельность Ж.Б.Ламарка (1744-1829) Мышцы шеи
Мышцы шеи Половое размножение у покрытосеменных растений
Половое размножение у покрытосеменных растений Матричные биосинтезы
Матричные биосинтезы Мендель Грегор Иоганн
Мендель Грегор Иоганн Растения-рекордсмены
Растения-рекордсмены Выделительная система человека
Выделительная система человека Онтогенез. Лекция 14
Онтогенез. Лекция 14 Биологиялық тыңайтқыштар
Биологиялық тыңайтқыштар Все о грибах
Все о грибах Биологический метод исследования. Определение патогенности и вирулентности микроорганизмов
Биологический метод исследования. Определение патогенности и вирулентности микроорганизмов Научно-исследовательский проект Удивительные свойства сахара
Научно-исследовательский проект Удивительные свойства сахара Процеси гниття. Хімізм процесу гниття
Процеси гниття. Хімізм процесу гниття Ұлпаның және ағзаның электростимуляциясы
Ұлпаның және ағзаның электростимуляциясы Лабораторная диагностика стафилококковой инфекции
Лабораторная диагностика стафилококковой инфекции