Содержание
- 2. Фосфор «элемент жизни и мысли» (А. Е. Ферсман) В организме человека на долю фосфора приходится 1,16%.
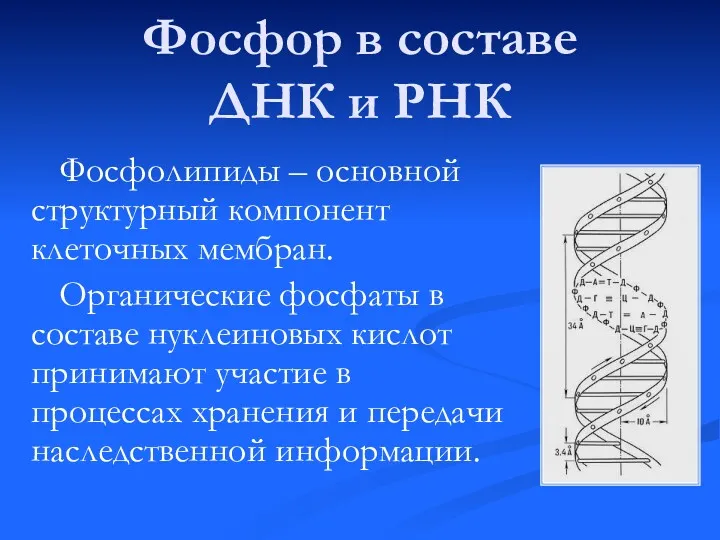
- 3. Фосфор в составе ДНК и РНК Фосфолипиды – основной структурный компонент клеточных мембран. Органические фосфаты в
- 4. АТФ – единица энергии в клетке В молекуле АТФ содержится три фосфатные группы. При отщеплении одной
- 5. История открытия фосфора В 1669 году Хеннинг Бранд получил новое вещество – фосфор 2Ca3(PO4)2 +10C +
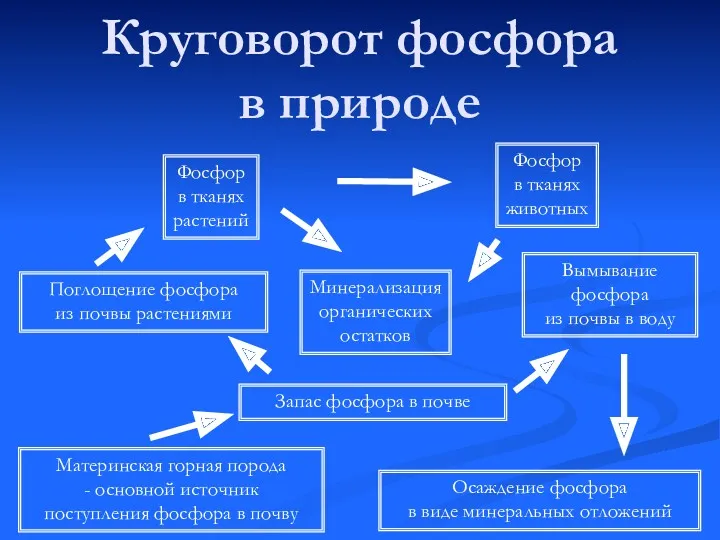
- 6. Круговорот фосфора в природе Материнская горная порода - основной источник поступления фосфора в почву Запас фосфора
- 7. Загадка папоротника Вы когда-нибудь видели цветок папоротника? Уже многие годы его безуспешно ищут в ночь на
- 8. Фосфор в организме человека У детей содержание неорганических фосфорных соединений в крови выше, чем у взрослых
- 9. Потребность в фосфоре Суточная потребность в фосфоре для взрослого человека составляет 1200 мг. Наиболее ценными источниками
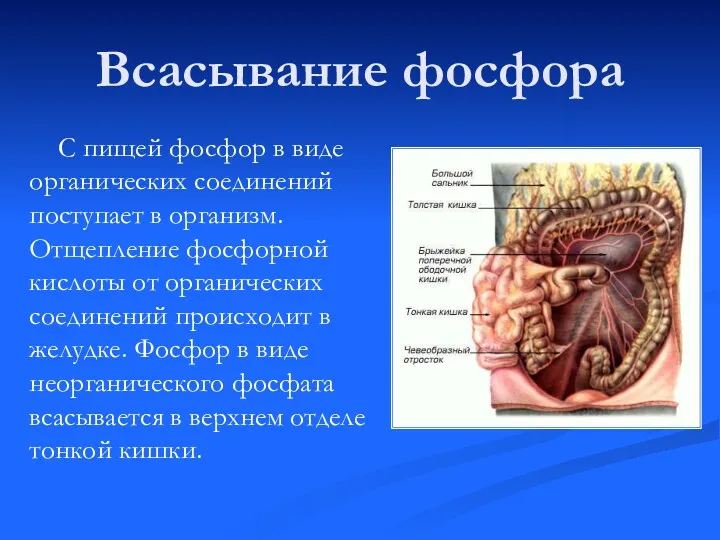
- 10. Всасывание фосфора С пищей фосфор в виде органических соединений поступает в организм. Отщепление фосфорной кислоты от
- 11. «Без фосфора нет мысли…» ( И. Генсинг) Дефицит фосфора в организме приводит к нарушению обмена веществ,
- 12. Aллотропия фосфора Фосфор чёрный Рn t P Фосфор белый Р4 230 О2 Фосфор красный Р8 Фосфор
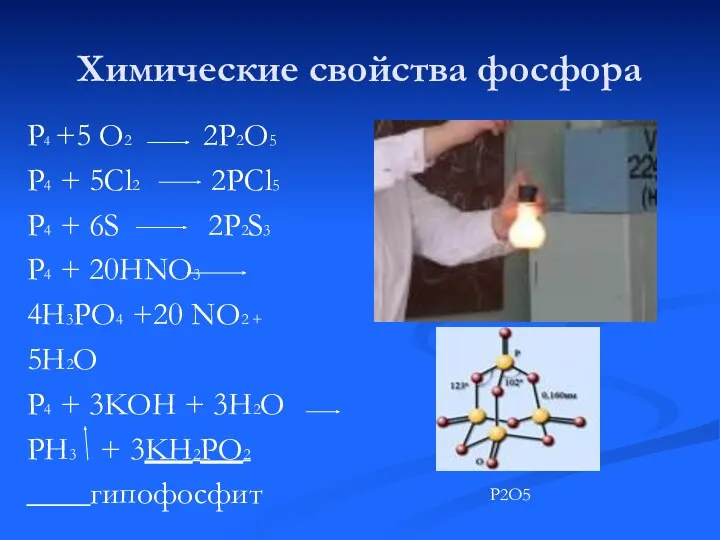
- 13. Химические свойства фосфора P4 +5 O2 2P2O5 P4 + 5Cl2 2PCl5 P4 + 6S 2P2S3 P4
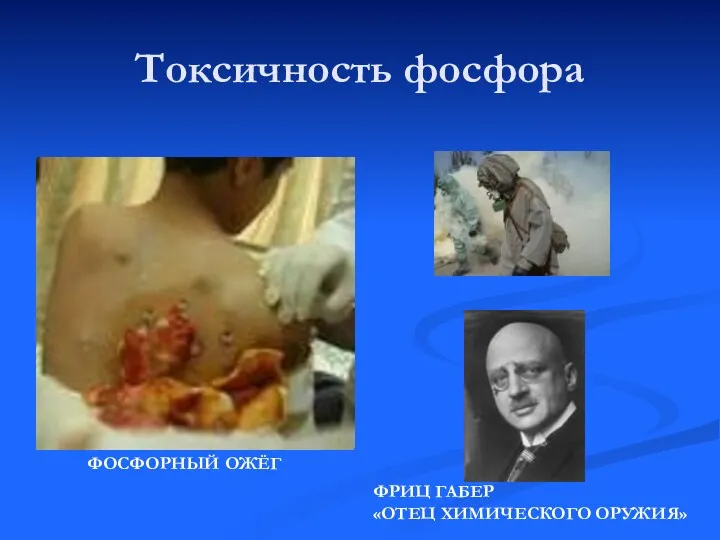
- 14. Токсичность фосфора ФОСФОРНЫЙ ОЖЁГ ФРИЦ ГАБЕР «ОТЕЦ ХИМИЧЕСКОГО ОРУЖИЯ»
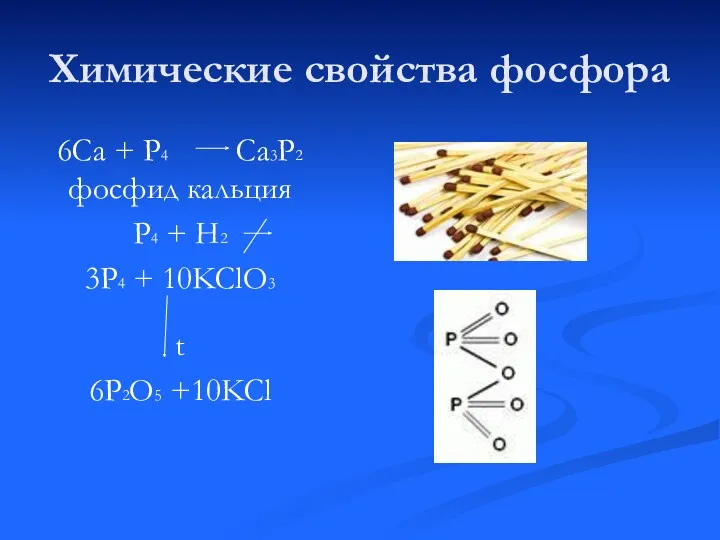
- 15. Химические свойства фосфора 6Са + Р4 Са3Р2 фосфид кальция Р4 + Н2 3Р4 + 10KClO3 t
- 16. Оксид фосфора (v) Кислотный оксид P2O5 + 3H2O 2 H3PO4 (избыток горячей воды) P2O5 + H2O
- 17. Особенности ортофосфорной кислоты твёрдое вещество белого цвета, хорошо растворимо в воде под действием водоотнимающих веществ переходит
- 18. Особенности ортофосфорной кислоты При нагревании переходит в пирофосфорную кислоту 2Н3РО4 Н4Р2О7 + Н2О Со щелочами образует
- 19. Особенности ортофосфатов Легко переходят в кислые соли под действием кислот Ag3PO4 + 2HNO3 AgH 2PO4 +
- 21. Скачать презентацию












 Строение мужской половой системы
Строение мужской половой системы Школьный ботанический сад
Школьный ботанический сад Биогеохимия Оренбургской области
Биогеохимия Оренбургской области Организм человека, как единая биологическая система
Организм человека, как единая биологическая система Общая характеристика типа Моллюски
Общая характеристика типа Моллюски Понятие об организме. Доядерные и ядерные организмы
Понятие об организме. Доядерные и ядерные организмы Физиология растений. ЭТЦ дыхания
Физиология растений. ЭТЦ дыхания Жизнедеятельность клетки. Линия жизни. 6 класс
Жизнедеятельность клетки. Линия жизни. 6 класс Биомеханика двигательной деятельности
Биомеханика двигательной деятельности Место человека в системе органического мира
Место человека в системе органического мира Микориза (грибокорень)
Микориза (грибокорень) Селекція тварин та рослин
Селекція тварин та рослин Органы чувств, их значение и гигиена
Органы чувств, их значение и гигиена Дыхание. Этапы дыхания
Дыхание. Этапы дыхания Викторина Животные
Викторина Животные The story of British zoos
The story of British zoos Овцеводство и козоводство в России
Овцеводство и козоводство в России Уровни организации живой материи
Уровни организации живой материи Анатомия человека. Подготовка к ЕГЭ
Анатомия человека. Подготовка к ЕГЭ Обмен нуклеопротеинов. (Лекция 17)
Обмен нуклеопротеинов. (Лекция 17) Кожа – покровный орган человека
Кожа – покровный орган человека Большие и маленькие улиточки
Большие и маленькие улиточки Экология и человек
Экология и человек Мембраны и компартменты клетки
Мембраны и компартменты клетки Тип Круглые черви
Тип Круглые черви Открытое мероприятие по профилактике вредных привычек
Открытое мероприятие по профилактике вредных привычек Виды птиц
Виды птиц Интересное о растениях
Интересное о растениях