Слайд 2

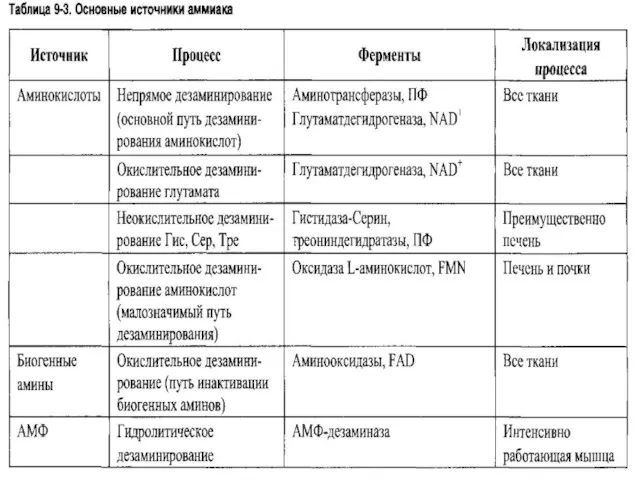
КОНЕЧНЫЕ ПРОДУКТЫ : АММИАК
Деградация аминокислот происходит преимущественно в печени.
При этом освобождается аммиак. Значительные количества аммиака образуются при распаде пуринов и пиримидинов.
Слайд 3
Слайд 4

ТОКСИЧНОСТЬ АММИАКА
Аммиак - NH3 является клеточным ядом. При высоких концентрациях он
повреждает главным образом нервные клетки (гепатаргическая кома).
В норме распад 70 г АК в сутки ведет к концентрации NH3 в крови 60 мкмоль/л.
Слайд 5

Токсичность аммиака
В опытах на кроликах концентрация
NH3 3 ммоль/л вызывала
смерть!
Причины токсичности:
1. при рН крови в виде NH4+, проникает через плазм. и МХ мембраны с большим трудом.
Слайд 6

Нейтр. мол. своб. NH3 легко проходят эти мембраны. При
рН 7,4 только 1% NH3 от общего количества аммиака проникает в клетки мозга и МХ.
Слайд 7

Причины токсичности
2. NH3 + а-КГ + НАДФН2 -?
Глу + НАДФ+
Н2О
Отток альфа- КГ из фонда ЦТК и как следствие – снижение скорости окисления глюкозы
Слайд 8

Токсичность аммиака
Аммиак настолько токсичен, что должен быть немедленно удален посредством экскреторного
механизма, либо путем включения в другое азотсодержащее соединение - менее токсичное.
Слайд 9

Механизмы детоксикации аммиака
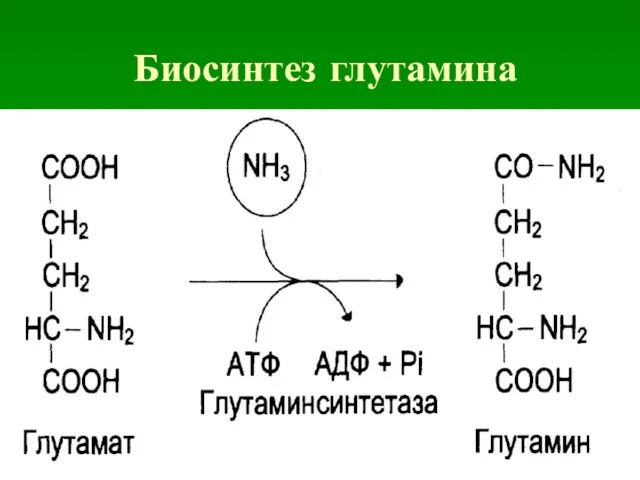
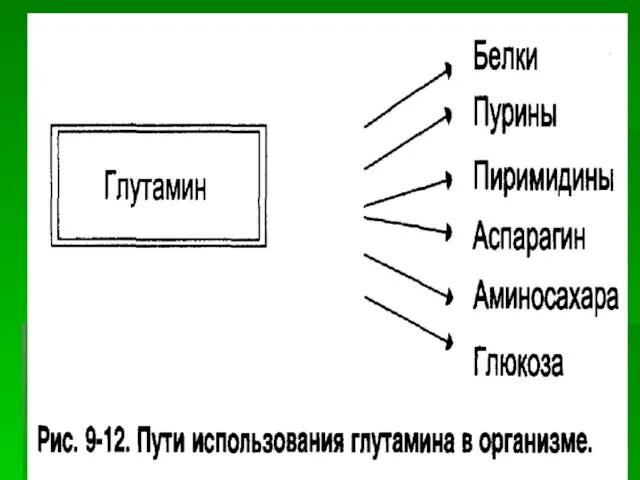
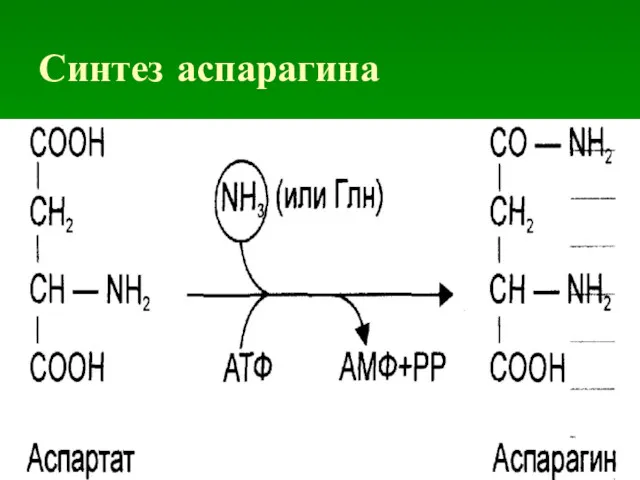
1. Синтез глутамина: Глн, аспарагина: Асн.
2. Синтез мочевины.
3. Аминирование
а-КГ --> Глу.
4. Амидирование белков.
Слайд 10

Механизмы детоксикации аммиака
5.Синтез пурин. и пиримид. структур.
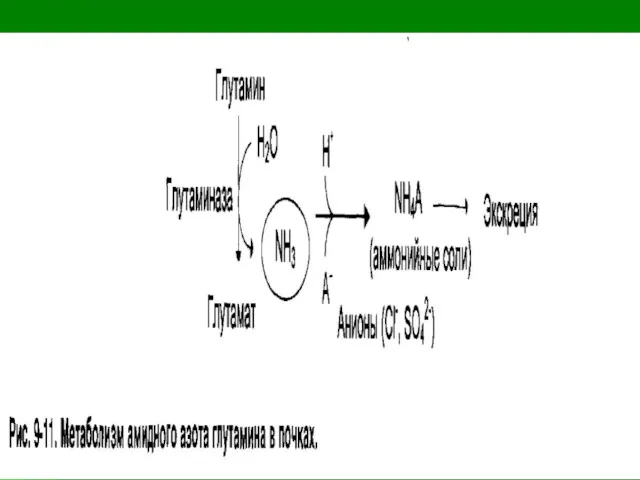
6. Нейтрализация в почках кислотами
и выделение с мочой аммонийных солей.
Слайд 11

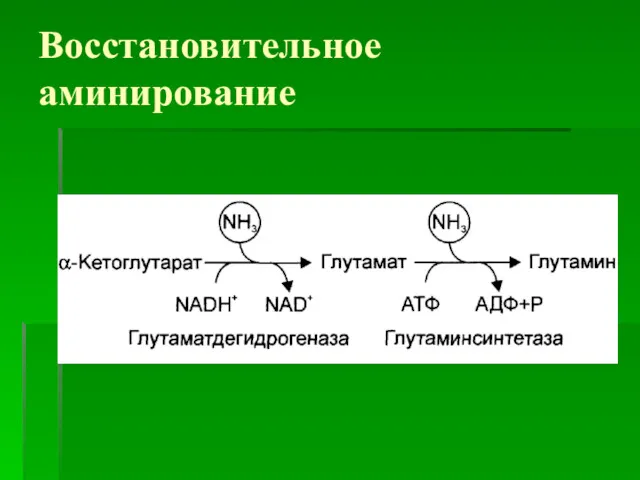
Восстановительное аминирование
Большинство организмов обладает способностью реутилизировать аммиак за счет реакции, катализируемой
глутаматдегидрогеназой.
А-Кетоглутарат + NH3 + НАДФН.Н+ ?
Глутамат + НАДФ+.
Это восстановительное аминирование.
Слайд 12
Восстановительное аминирование
Слайд 13
Слайд 14
Слайд 15
Слайд 16
Слайд 17
Слайд 18

МОЧЕВИНА
У человека инактивация NH3 осуществляется за счет синтеза мочевины, часть
NH3 выводится почками.
Слайд 19

Синтез мочевины
Мочевина - это нейтральное и нетоксичное соединение. Молекула мочевины
может проходить через мембраны, из-за ее хорошей растворимости в воде мочевина легко переносится кровью и выводится с мочой.
Слайд 20

СТАДИИ СИНТЕЗА МОЧЕВИНЫ
Мочевина образуется в результате циклической последовательности реакций, протекающих в
печени.
Оба атома азота берутся из свободного аммиака и за счет дезаминирования аспартата, карбонильная группа — из гидрокарбоната.
Слайд 21

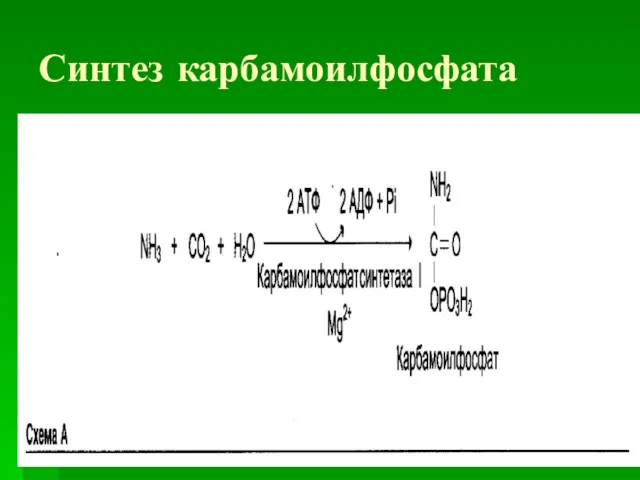
Первая реакция
На первой стадии из гидрокарбоната (НСО3-) и аммиака с потреблением
2 молекул АТФ образуется карбамоилфосфат.
Слайд 22
Слайд 23

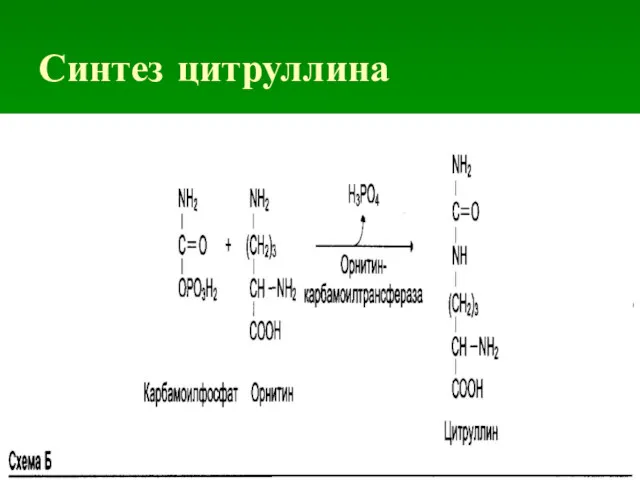
Вторая стадия
Карбамоильный остаток переносится на орнитин с образованием цитруллина. Вновь
необходима энергия в форме АТФ, который при этом расщепляется на АМФ и дифосфат.
Слайд 24
Слайд 25

Третья стадия
Вторая аминогруппа молекулы мочевины поставляется за счет реакции аспартата с
цитруллином.
Слайд 26

Слайд 27

Для обеспечения необратимости реакции дифосфат гидролизуется полностью. Отщепление фумарата от
аргининосукцината приводит к аргинину,
Слайд 28

Слайд 29

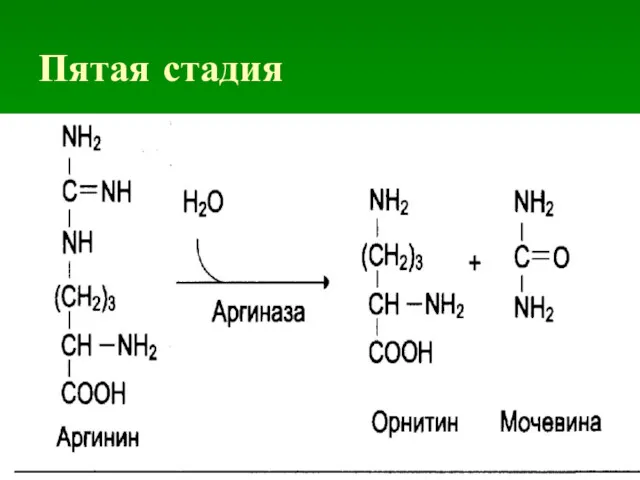
Пятая стадия
из которого в результате гидролиза образуется мочевина. Остающийся орнитин
вновь включается в цикл мочевины.
Слайд 30
Слайд 31
Слайд 32

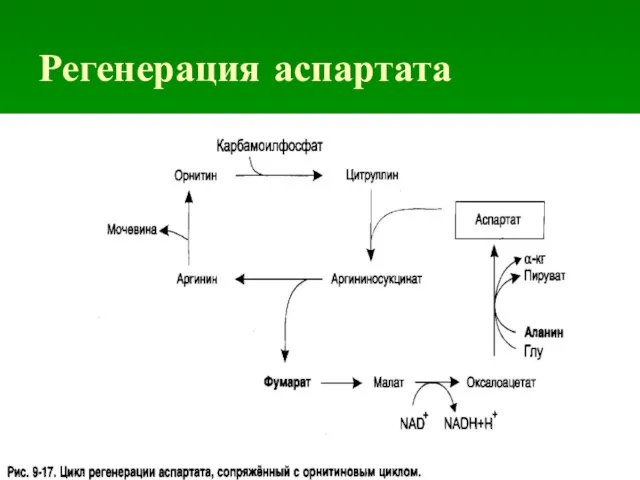
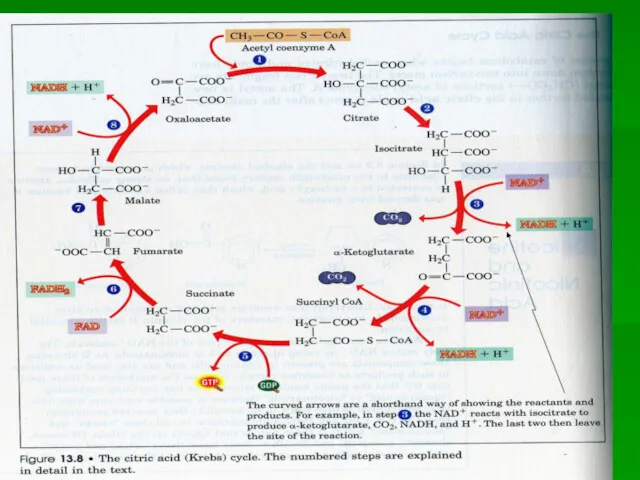
ВЕЛОСИПЕД КРЕБСА
Фумарат, образующийся в цикле мочевины, может в результате двух стадий
цитратного цикла [6, 7] через малат переходить в оксалоацетат, который за счет трансаминирования [9] далее прекращается в аспартат. Последний также вновь вовлекается в цикл мочевины.
Слайд 33
Слайд 34
Слайд 35
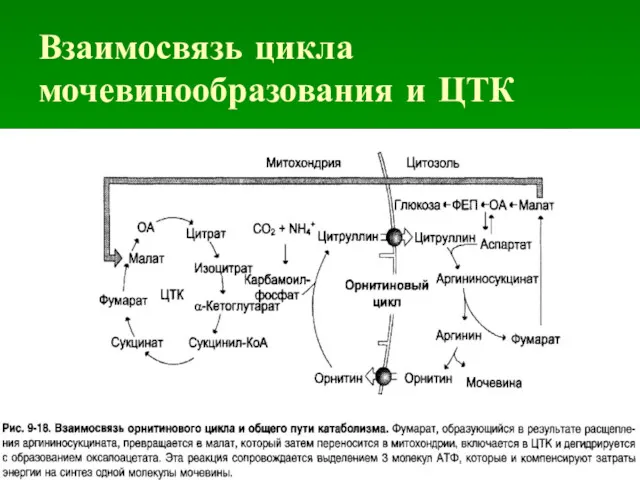
Взаимосвязь цикла мочевинообразования и ЦТК
Слайд 36

ЭНЕРГОЗАВИСИМЫЙ ПРОЦЕСС
Биосинтез мочевины требует больших затрат энергии. Энергия поставляется за счет
расщепления четырех высокоэнергетических связей: двух при синтезе карбамоилфосфата и двух (!) при образовании аргининосукцината (АТФ → АМФ + PPi, РРi → 2Pi).
Слайд 37

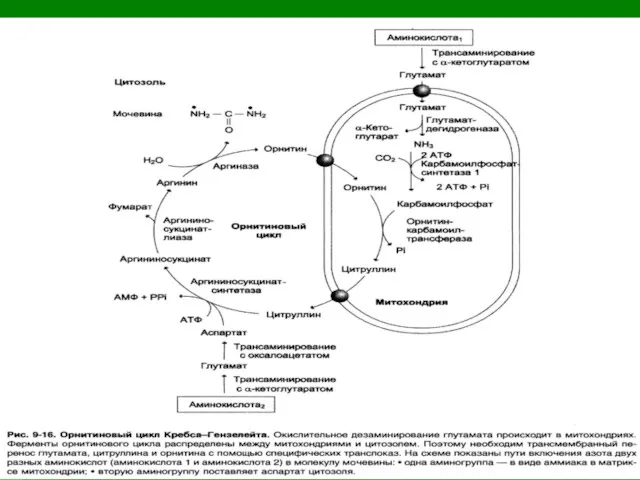
КОМПАРТМЕНТАЛИЗАЦИЯ
Цикл мочевины протекает исключительно в печени. Он разделен на два компартмента:
митохондрии и цитоплазму. Прохождение через мембрану промежуточных соединений цитруллина и орнитина возможно только с помощью переносчиков.
Слайд 38

АЛЛОСТЕРИЧЕСКАЯ РЕГУЛЯЦИЯ СИНТЕЗА МОЧЕВИНЫ
Скорость синтеза мочевины определяется первой реакцией цикла.
Карбамоилфосфатсинтаза активна только в присутствии N-ацетилглутамата. Уровень аргинина и энергоснабжение сильно зависят от концентрации этого аллостерического эффектора.
Слайд 39

Наследственные нарушения орнитинового цикла и их симптомы
Слайд 40

Слайд 41
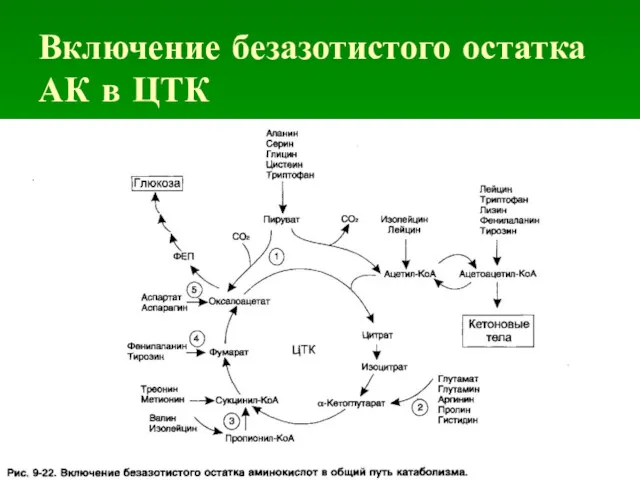
Включение безазотистого остатка АК в ЦТК
Слайд 42

Пути биосинтеза заменимых АК
Слайд 43










































 Роль соли для организма человека
Роль соли для организма человека Мембраналық органоидтар
Мембраналық органоидтар Эволюционная теория Жана Батиста Ламарка
Эволюционная теория Жана Батиста Ламарка Презентация у уроку биологии по теме Тип Кишечнополостные (7 класс)
Презентация у уроку биологии по теме Тип Кишечнополостные (7 класс) Необычные птицы планеты
Необычные птицы планеты Witaminy - są to substancje organiczne niezbędne w niewielkich ilościach do prawidłowego przebiegu procesów
Witaminy - są to substancje organiczne niezbędne w niewielkich ilościach do prawidłowego przebiegu procesów Мутагенные факторы и их влияние на фенотип человека
Мутагенные факторы и их влияние на фенотип человека Паукообразные. Разновидности паукообразных
Паукообразные. Разновидности паукообразных Память и обучение
Память и обучение Презентация Оценка зависимости ЖЕЛ у подростков
Презентация Оценка зависимости ЖЕЛ у подростков Исследовательская работа. Выращивание дуба
Исследовательская работа. Выращивание дуба Животные и растения Астраханского края, занесённые в Красную книгу. 2 класс
Животные и растения Астраханского края, занесённые в Красную книгу. 2 класс Удивительный мир фитодизайна
Удивительный мир фитодизайна Бурый медведь
Бурый медведь Структурные уровни организации живого. Свойства живого
Структурные уровни организации живого. Свойства живого Использование ИКТ на уроках биологии как средство повышения эффективности учебно-воспитательного процесса
Использование ИКТ на уроках биологии как средство повышения эффективности учебно-воспитательного процесса Физиология мышечного сокращения
Физиология мышечного сокращения Способы культивирования вирусов
Способы культивирования вирусов Лаборатория Полимеры для биологии
Лаборатория Полимеры для биологии Развитие эволюционных идей
Развитие эволюционных идей Клеточные и неклеточные формы жизни
Клеточные и неклеточные формы жизни Закономерности влияния окружающей среды на развитие фенотипа животных. (Лекция 1)
Закономерности влияния окружающей среды на развитие фенотипа животных. (Лекция 1) презентация Вид, критерии 11 класс
презентация Вид, критерии 11 класс Врожденные формы поведения. Сравнение врожденных и приобретенных форм поведения
Врожденные формы поведения. Сравнение врожденных и приобретенных форм поведения Химический состав клетки
Химический состав клетки Развитие жизни на Земле в различные периоды
Развитие жизни на Земле в различные периоды Приспособление организмов к среде обитания
Приспособление организмов к среде обитания Клетка — элементарная структурная и функциональная единица живого
Клетка — элементарная структурная и функциональная единица живого