Содержание
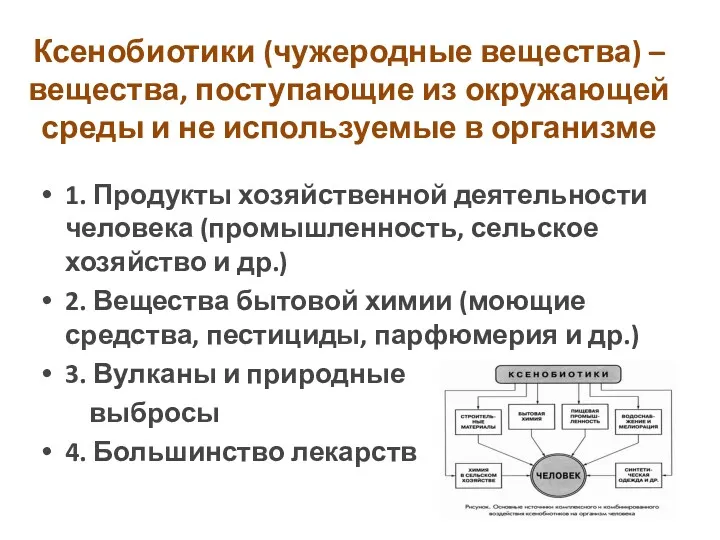
- 2. Ксенобиотики (чужеродные вещества) – вещества, поступающие из окружающей среды и не используемые в организме 1. Продукты
- 3. Детоксикация или обезвреживание ксенобиотиков. Гидрофильные ксенобиотики выводятся с мочой в неизменном виде. Гидрофобные ксенобиотики могут задерживаться
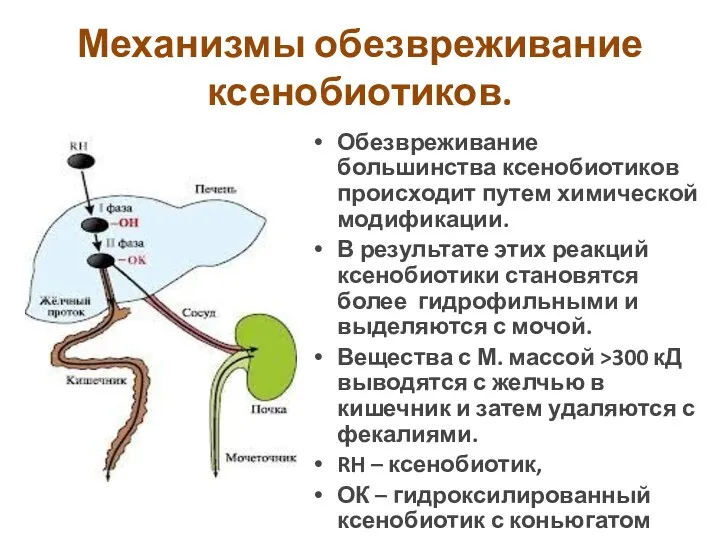
- 4. Механизмы обезвреживание ксенобиотиков. Обезвреживание большинства ксенобиотиков происходит путем химической модификации. В результате этих реакций ксенобиотики становятся
- 5. Система обезвреживания состоит из 2 фаз: Химическая модификация ксенобиотика включает: 1 фаза - Повышение растворимости ксенобиотика.
- 6. Система обезвреживания включает множество микросомальных ферментов, под действием которых практически любой ксенобиотик может быть модифицирован. Микросомальные
- 7. Микросомальное окисление Микросомальное окисление - совокупность реакций первой фазы биотрансформации ксенобиотиков и эндогенных соединений, катализирующихся ферментными
- 8. Семейство цитохромов Р-450 Цитохром Р450-зависимые монооксигеназы катализируют расщепление различных веществ с участием донора электрона НАДФН и
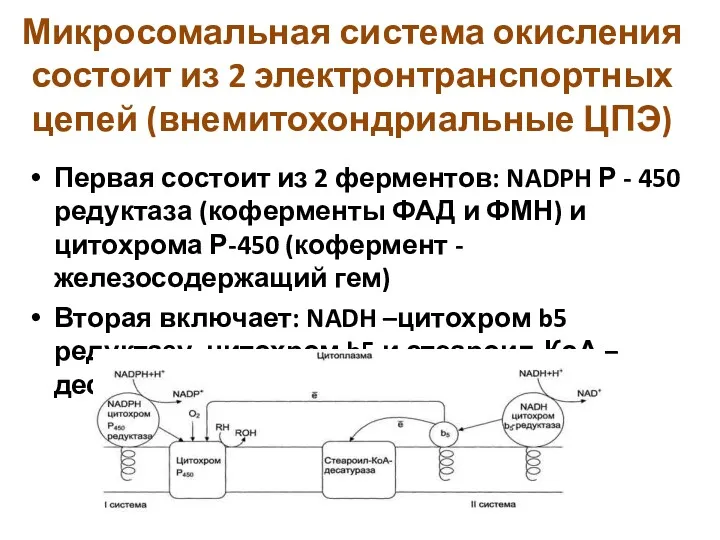
- 9. Микросомальная система окисления состоит из 2 электронтранспортных цепей (внемитохондриальные ЦПЭ) Первая состоит из 2 ферментов: NADPH
- 10. Функционирование первой ЦПЭ Мультиферментный комплекс формирует цепь переноса электронов и протонов, в конце ее происходит активация
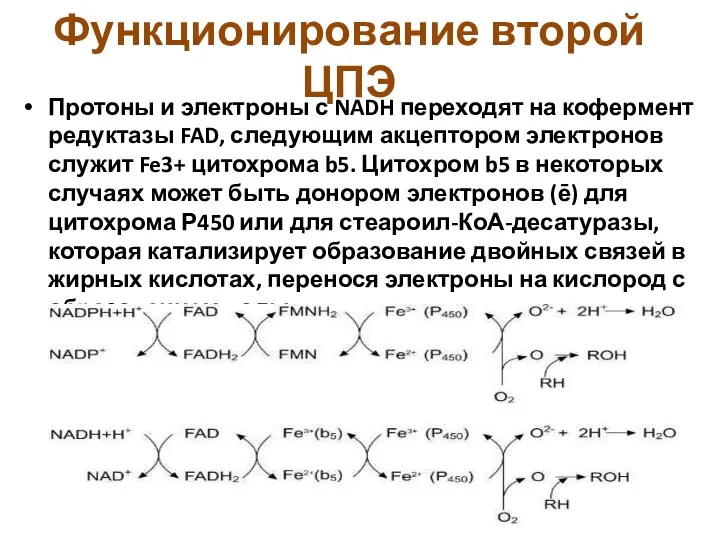
- 11. Функционирование второй ЦПЭ Протоны и электроны с NADH переходят на кофермент редуктазы FAD, следующим акцептором электронов
- 12. Реакции гидроксилирования на цитохроме Р450 Суть реакций заключается в гидроксилировании вещества типа R-H с использованием одного
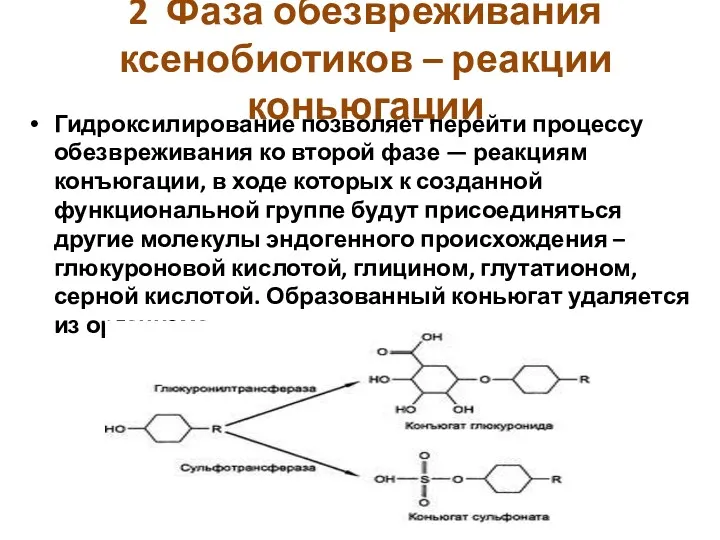
- 13. 2 Фаза обезвреживания ксенобиотиков – реакции коньюгации Гидроксилирование позволяет перейти процессу обезвреживания ко второй фазе —
- 14. Все ферменты, функционирующие во второй фазе обезвреживания ксенобиотиков, относят к классу трансфераз. Они характеризуются широкой субстратной
- 16. Скачать презентацию








 Система органов дыхания
Система органов дыхания Пёсики и их классификации
Пёсики и их классификации Биохимия витаминов. Классификация витаминов. Жирорастворимые витамины
Биохимия витаминов. Классификация витаминов. Жирорастворимые витамины Шляпочные грибы
Шляпочные грибы Зчеплене успадкування і кросинговер. Тема 5
Зчеплене успадкування і кросинговер. Тема 5 Презентация по теме Популяции 9 класс
Презентация по теме Популяции 9 класс Систематика и характеристика голосеменных растений
Систематика и характеристика голосеменных растений Влияние листового опада на состав и биотоп почвы
Влияние листового опада на состав и биотоп почвы Собака в городе: жизнь или выживание?
Собака в городе: жизнь или выживание? Семена
Семена Обмін речовин і енергії
Обмін речовин і енергії Анатомия, физиология и патология органов речи
Анатомия, физиология и патология органов речи Влияние физических упражнений на формирование системы опоры и движения человека
Влияние физических упражнений на формирование системы опоры и движения человека Вода и ее свойства
Вода и ее свойства Гипотезы происхождения жизни
Гипотезы происхождения жизни Обмен липидов
Обмен липидов Вымирающие виды животных
Вымирающие виды животных Амфибии или земноводные
Амфибии или земноводные Выращивание овощей в домашних условиях
Выращивание овощей в домашних условиях Презентация к уроку Общая характеристика класса Млекопитающих
Презентация к уроку Общая характеристика класса Млекопитающих Кровообращение.
Кровообращение. Тип кишечнополостные. (7 класс)
Тип кишечнополостные. (7 класс) Общая биология
Общая биология Виявлення пристосувань до способу життя птахів. Практична робота 3
Виявлення пристосувань до способу життя птахів. Практична робота 3 Ағзалардың тіршілігіндегі бөліп шығарудың маңызы Өсімдіктер мен жануарлардың бөліп шығару өнімдері
Ағзалардың тіршілігіндегі бөліп шығарудың маңызы Өсімдіктер мен жануарлардың бөліп шығару өнімдері Развитие жизни на земле
Развитие жизни на земле Лук – это один из самых полезных овощей
Лук – это один из самых полезных овощей Группы крови. Переливание крови. 8 класс
Группы крови. Переливание крови. 8 класс