Содержание
- 2. Углеводы – это многоатомные альдегидо- или кетоспирты (полиоксикарбонильные соединения) и их производные с общей формулой Сn(H2O)m.
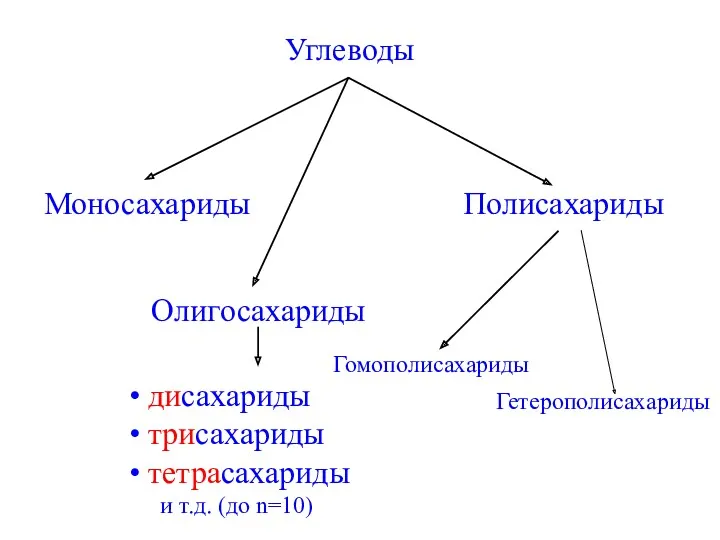
- 3. Углеводы Моносахариды Полисахариды Олигосахариды Гомополисахариды дисахариды трисахариды тетрасахариды и т.д. (до n=10) Гетерополисахариды
- 4. Моносахариды – это простые углеводы, которые в растворе не гидролизируют. Классификация. 1. По количеству атомов С
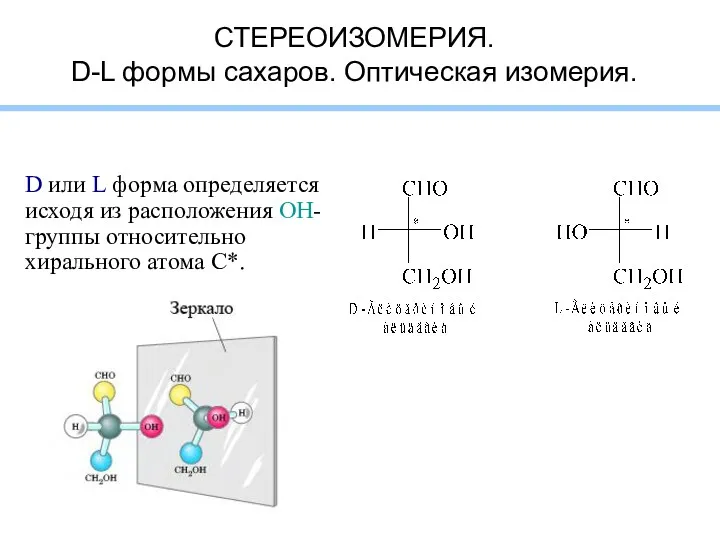
- 5. СТЕРЕОИЗОМЕРИЯ. D-L формы сахаров. Оптическая изомерия. D или L форма определяется исходя из расположения OH-группы относительно
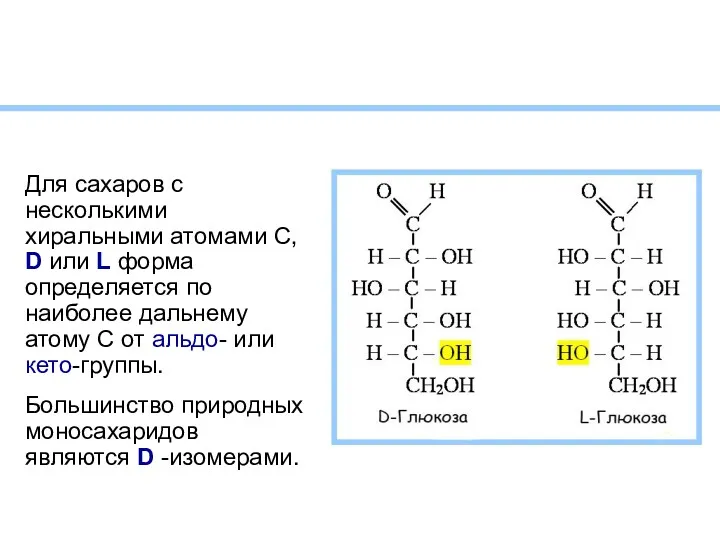
- 6. Для сахаров с несколькими хиральными атомами С, D или L форма определяется по наиболее дальнему атому
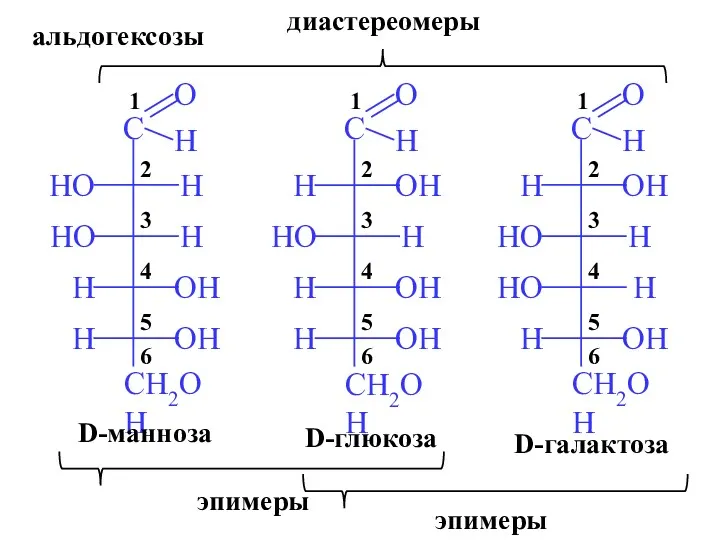
- 7. D-глюкоза D-галактоза D-манноза эпимеры эпимеры диастереомеры альдогексозы
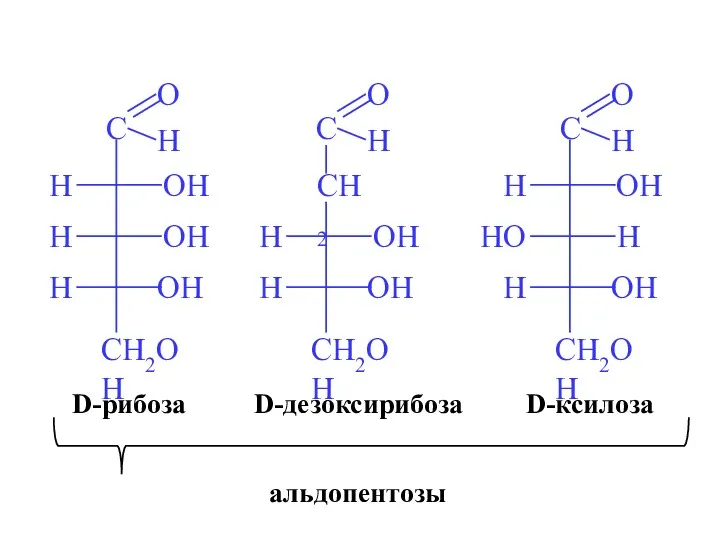
- 8. D-рибоза D-ксилоза D-дезоксирибоза альдопентозы
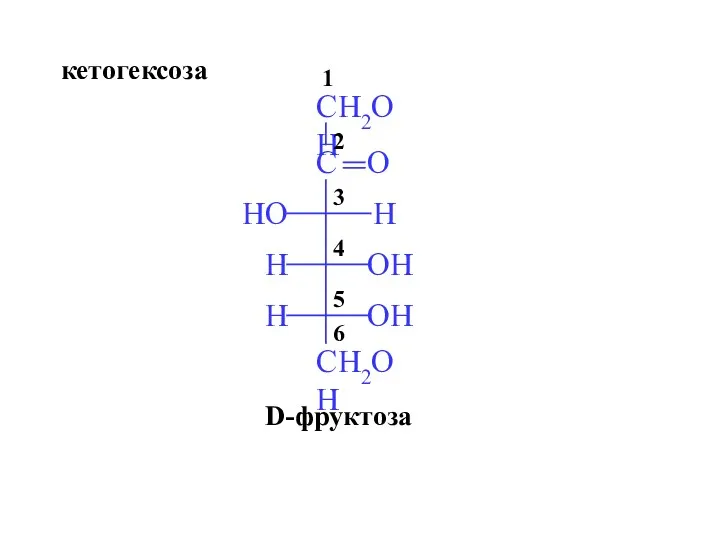
- 9. D-фруктоза кетогексоза
- 10. Цикло-оксо-таутомерия моносахаридов
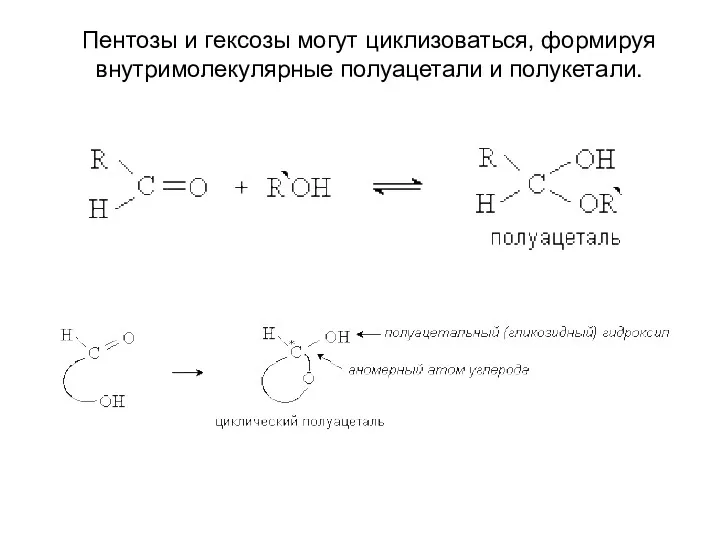
- 11. Пентозы и гексозы могут циклизоваться, формируя внутримолекулярные полуацетали и полукетали.
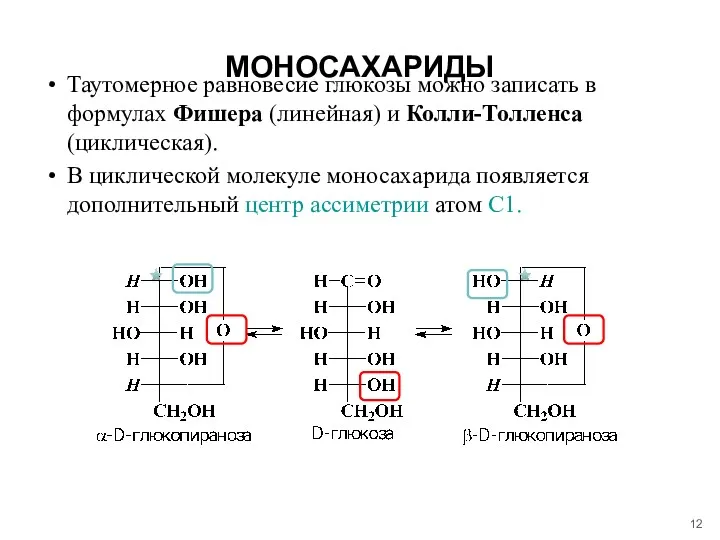
- 12. МОНОСАХАРИДЫ Таутомерное равновесие глюкозы можно записать в формулах Фишера (линейная) и Колли-Толленса (циклическая). В циклической молекуле
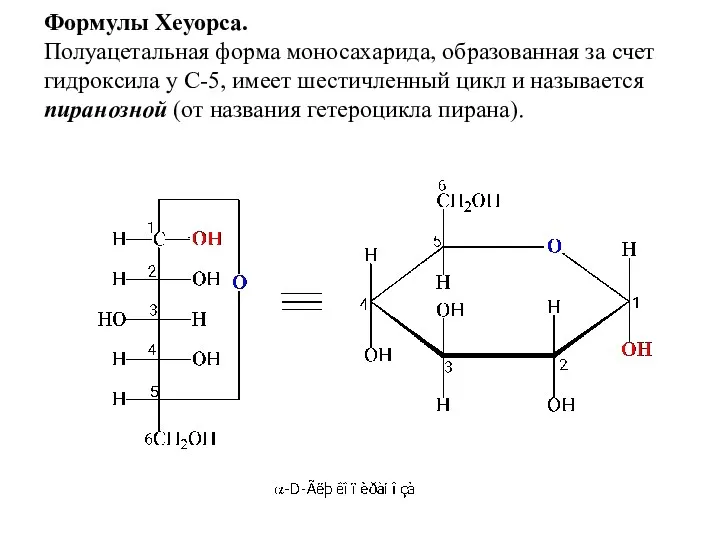
- 13. Формулы Хеуорса. Полуацетальная форма моносахарида, образованная за счет гидроксила у С-5, имеет шестичленный цикл и называется
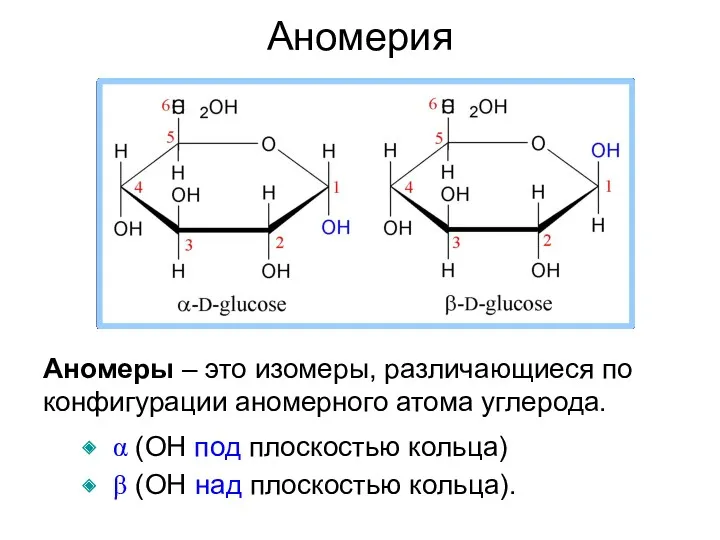
- 14. Аномеры – это изомеры, различающиеся по конфигурации аномерного атома углерода. α (OH под плоскостью кольца) β
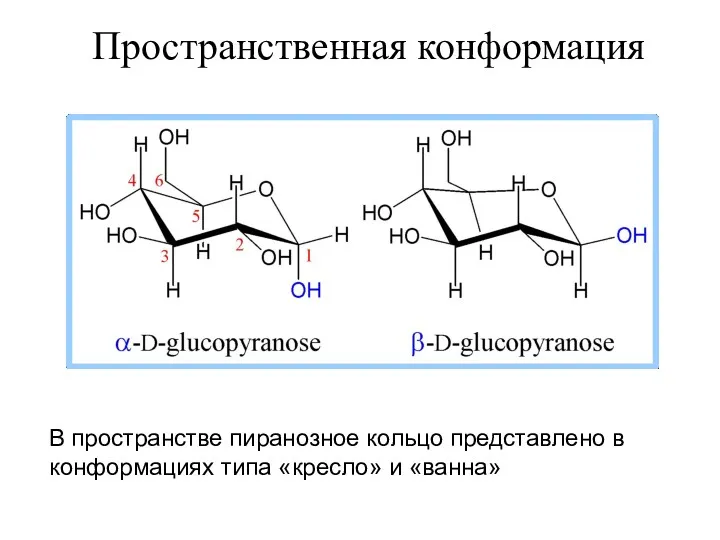
- 15. В пространстве пиранозное кольцо представлено в конформациях типа «кресло» и «ванна» Пространственная конформация
- 16. МОНОСАХАРИДЫ. Химические свойства Основные типы реакционной способности моносахаридов определяются наличием в их таутомерных формах:
- 17. Реакции по карбонильной группе Восстановление моносахаридов [H] D-глюкоза глюцит (сорбит)
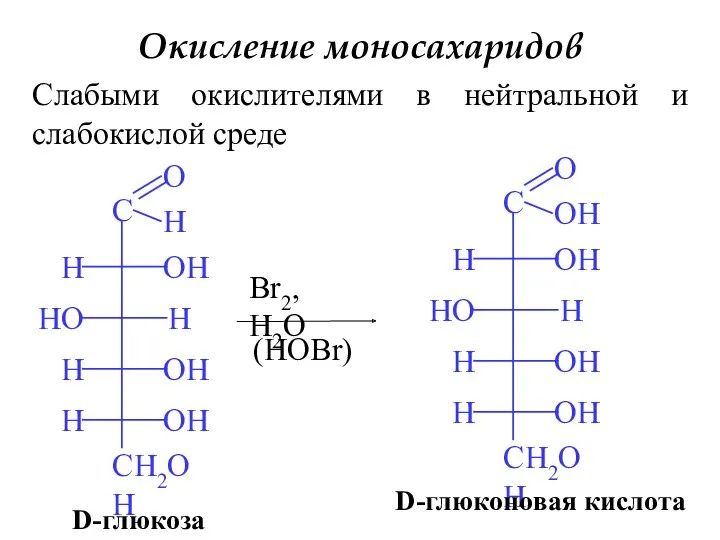
- 18. Окисление моносахаридов Слабыми окислителями в нейтральной и слабокислой среде D-глюкоза Br2, H2O (HOBr) D-глюконовая кислота
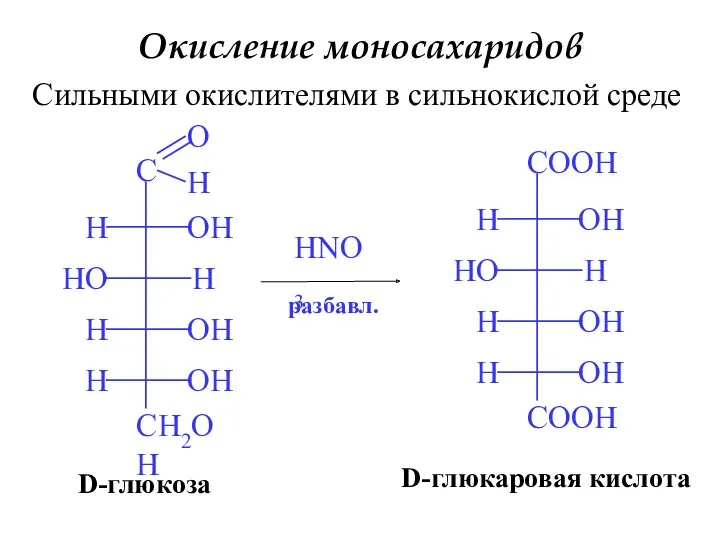
- 19. Окисление моносахаридов Сильными окислителями в сильнокислой среде HNO3 D-глюкаровая кислота D-глюкоза разбавл.
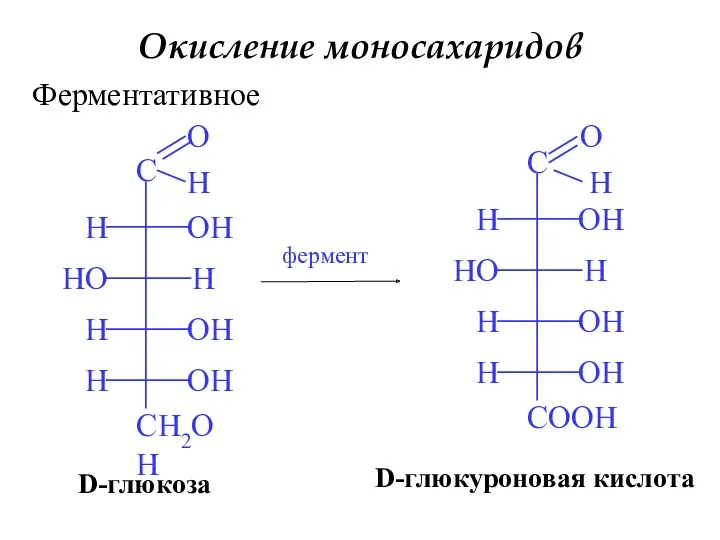
- 20. Окисление моносахаридов Ферментативное фермент D-глюкуроновая кислота D-глюкоза H
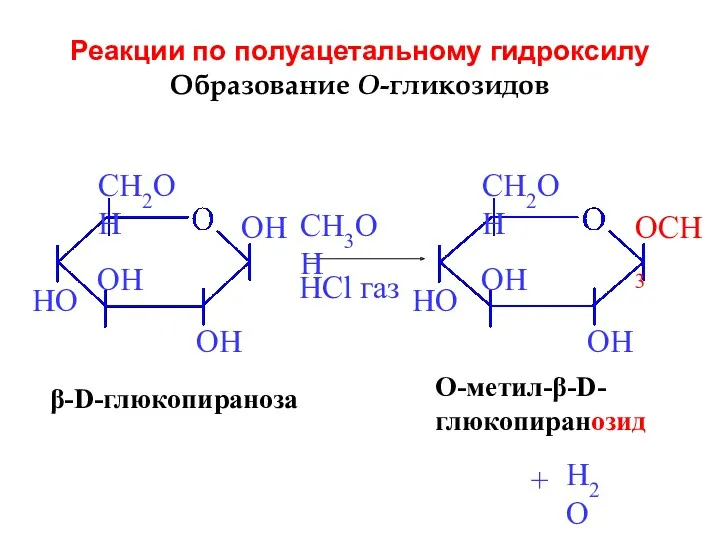
- 21. Реакции по полуацетальному гидроксилу Образование O-гликозидов β-D-глюкопираноза CH3OH HCl газ + O-метил-β-D- глюкопиранозид H2O
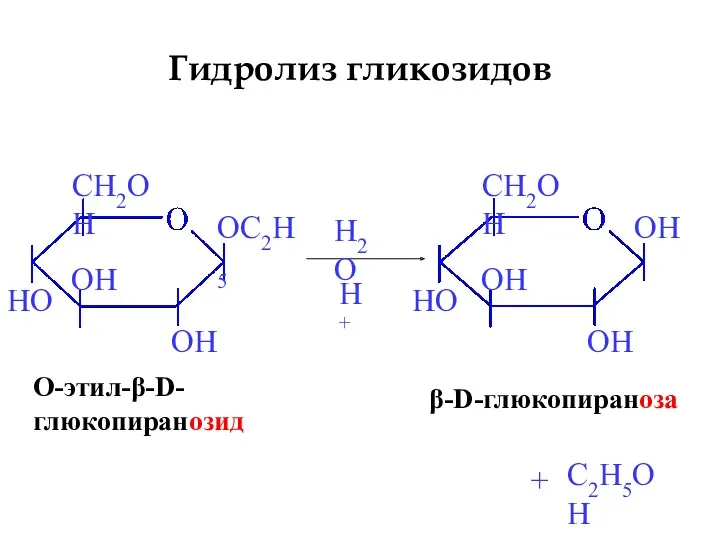
- 22. Гидролиз гликозидов β-D-глюкопираноза H2O H+ + O-этил-β-D- глюкопиранозид C2H5OH
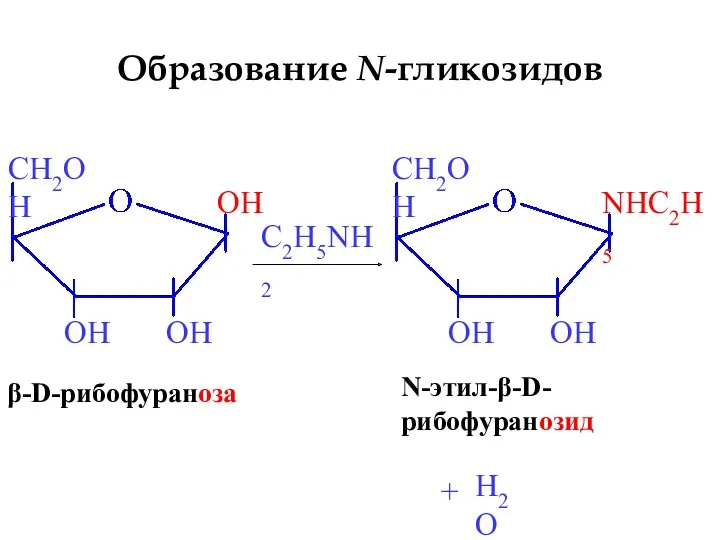
- 23. β-D-рибофураноза C2H5NH2 N-этил-β-D- рибофуранозид + H2O Образование N-гликозидов
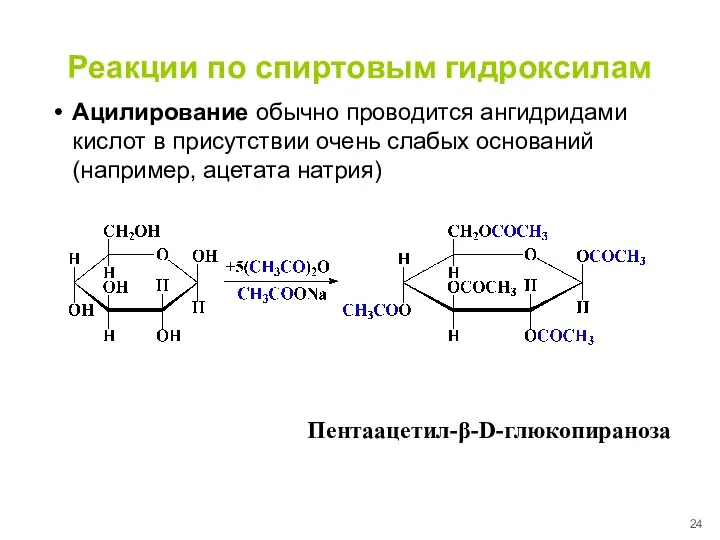
- 24. Реакции по спиртовым гидроксилам Ацилирование обычно проводится ангидридами кислот в присутствии очень слабых оснований (например, ацетата
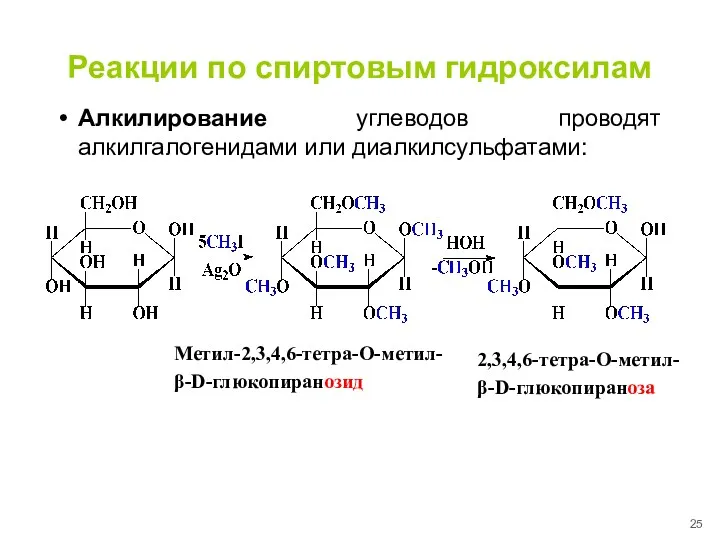
- 25. Реакции по спиртовым гидроксилам Алкилирование углеводов проводят алкилгалогенидами или диалкилсульфатами: 2,3,4,6-тетра-О-метил- β-D-глюкопираноза Метил-2,3,4,6-тетра-О-метил- β-D-глюкопиранозид
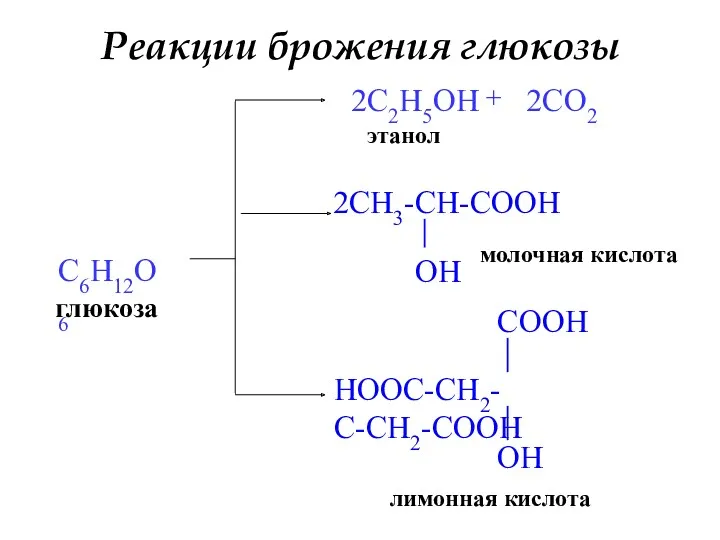
- 26. Реакции брожения глюкозы глюкоза C6H12O6 2C2H5OH этанол + 2CO2 молочная кислота лимонная кислота
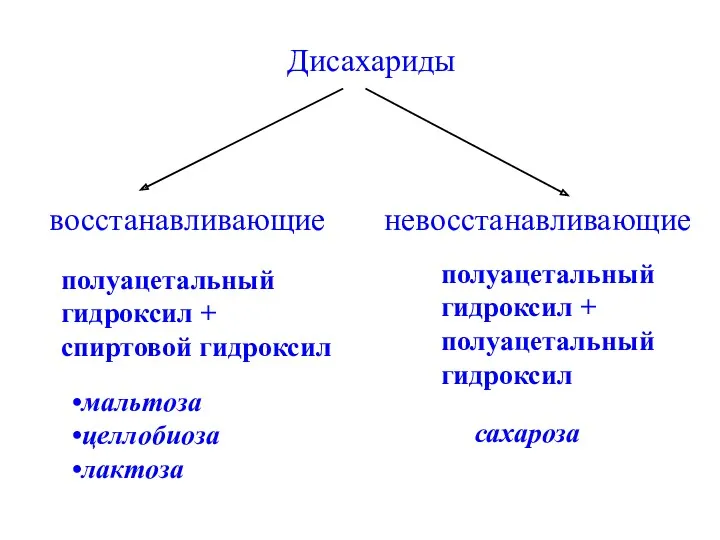
- 27. Дисахариды восстанавливающие невосстанавливающие полуацетальный гидроксил + спиртовой гидроксил полуацетальный гидроксил + полуацетальный гидроксил мальтоза целлобиоза лактоза
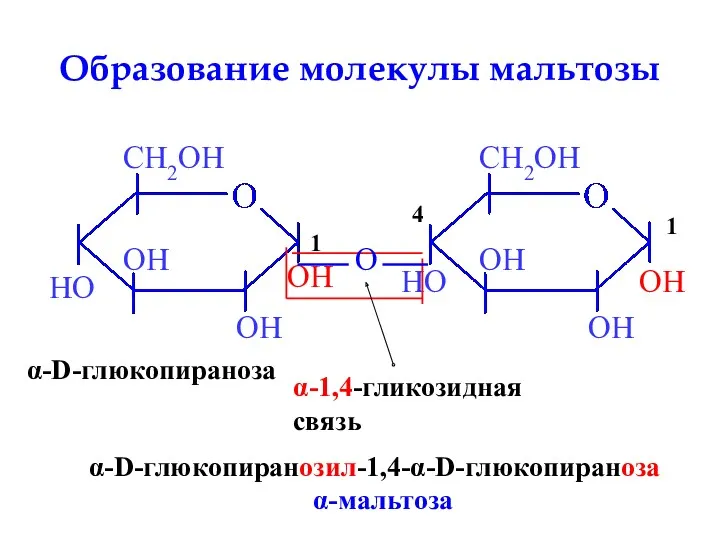
- 28. Образование молекулы мальтозы OH α-D-глюкопираноза HO OH O α-1,4-гликозидная связь α-D-глюкопиранозил-1,4-α-D-глюкопираноза α-мальтоза
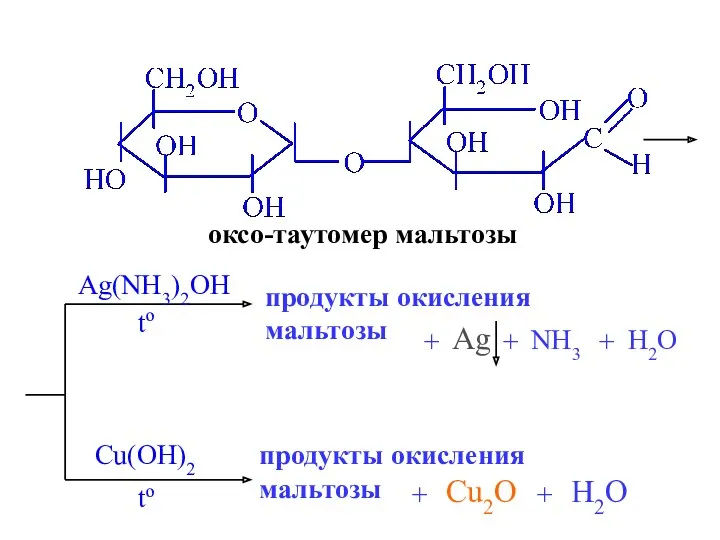
- 29. оксо-таутомер мальтозы Ag(NH3)2OH продукты окисления мальтозы Ag + NH3 + H2O to + Cu(OH)2 to продукты
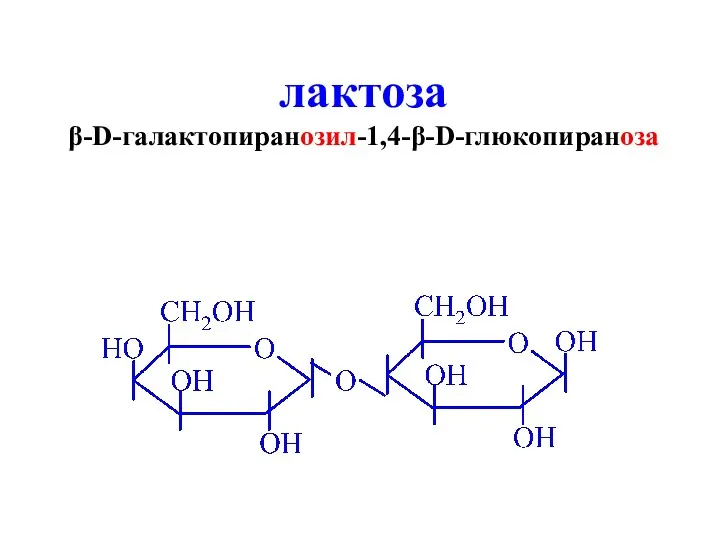
- 30. лактоза β-D-галактопиранозил-1,4-β-D-глюкопираноза
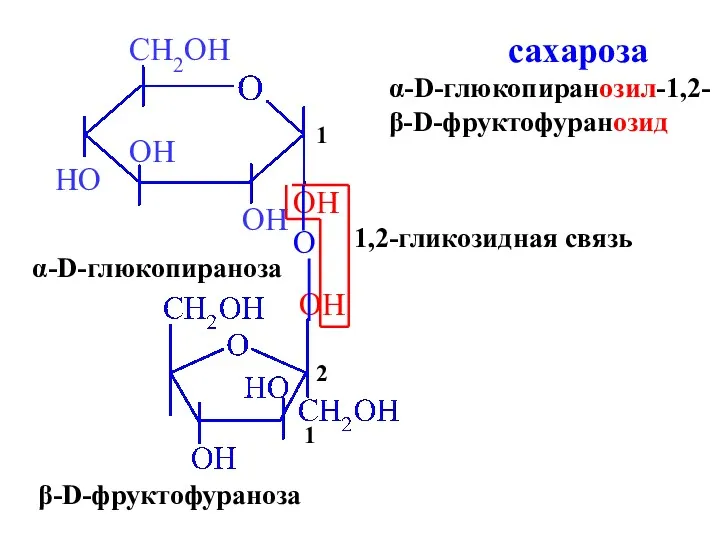
- 31. OH OH α-D-глюкопираноза β-D-фруктофураноза 1 2 O 1,2-гликозидная связь сахароза α-D-глюкопиранозил-1,2- β-D-фруктофуранозид
- 32. Гомополисахариды крахмал целлюлоза гликоген декстран
- 33. Крахмал – гомополимер α-D-глюкозы. Находится в злаках, бобовых, картофеле и некоторых других овощах. Синтезировать крахмал способны
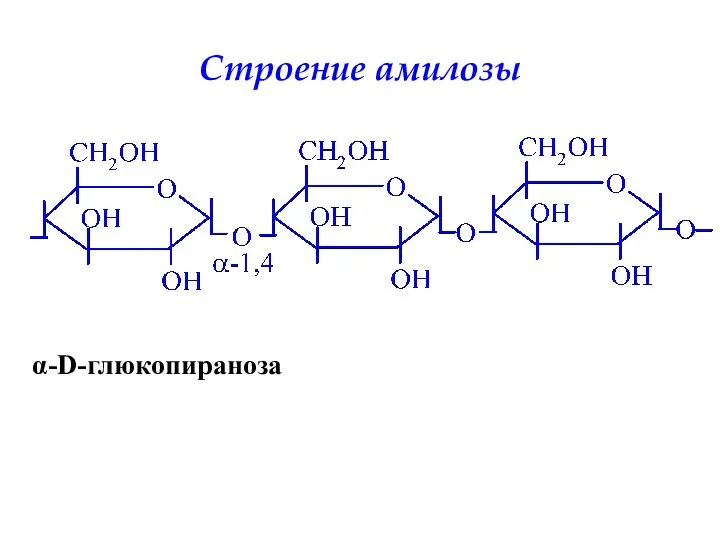
- 34. Строение амилозы α-D-глюкопираноза
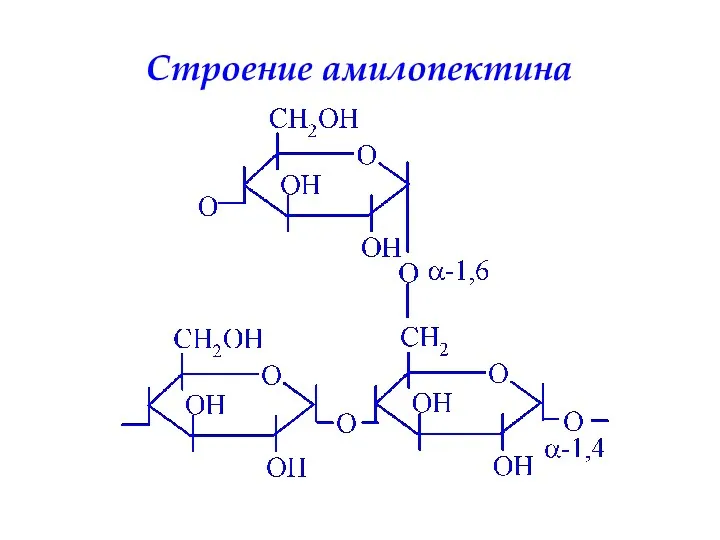
- 35. Строение амилопектина
- 36. Гликоген – резервный полисахарид животных тканей, в наибольшей мере содержится в печени и мышцах. Структурно он
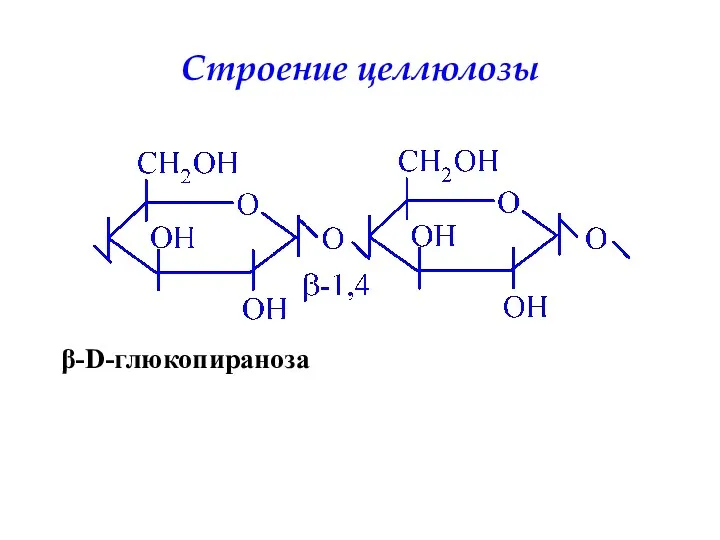
- 37. Целлюлоза является наиболее распространенным органическим соединением биосферы. Около половины всего углерода Земли находится в ее составе.
- 38. Строение целлюлозы β-D-глюкопираноза
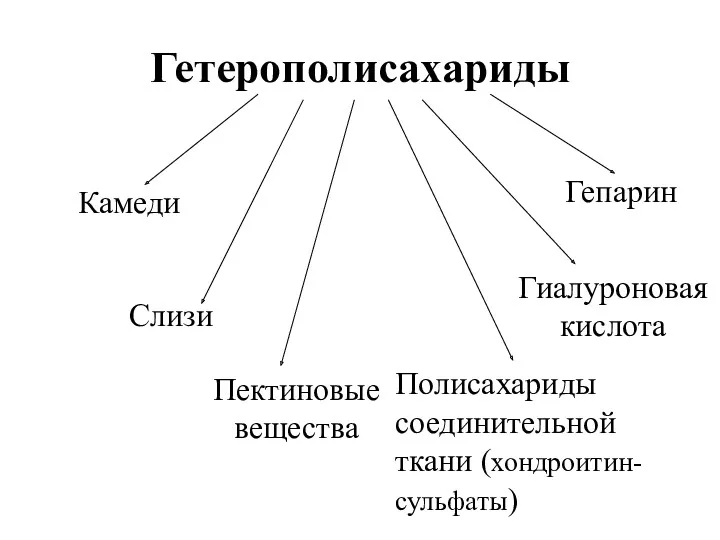
- 39. Гетерополисахариды Камеди Слизи Пектиновые вещества Полисахариды соединительной ткани (хондроитин- сульфаты) Гиалуроновая кислота Гепарин
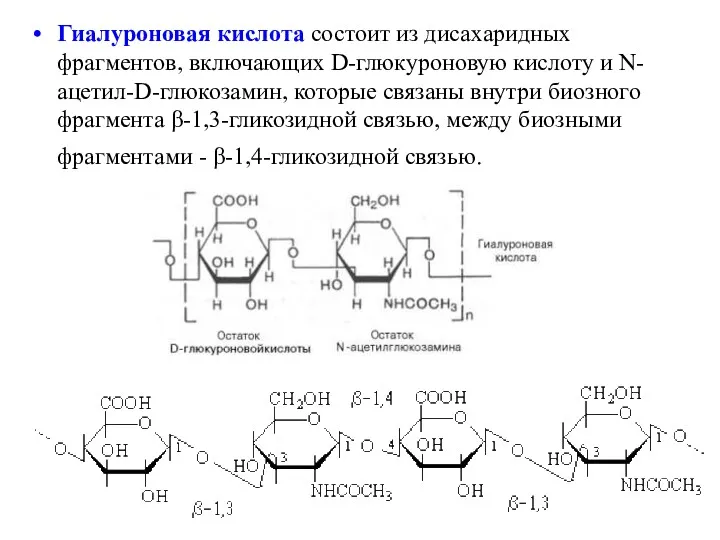
- 40. Гиалуроновая кислота состоит из дисахаридных фрагментов, включающих D-глюкуроновую кислоту и N-ацетил-D-глюкозамин, которые связаны внутри биозного фрагмента
- 42. Скачать презентацию




![Реакции по карбонильной группе Восстановление моносахаридов [H] D-глюкоза глюцит (сорбит)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/261733/slide-16.jpg)



 Химизм фотосинтеза
Химизм фотосинтеза Ядовитые растения. Первая помощь, при отравлении ядовитыми растениями
Ядовитые растения. Первая помощь, при отравлении ядовитыми растениями Продление рода. Органы размножения. 7 класс
Продление рода. Органы размножения. 7 класс Органы и системы органов животных
Органы и системы органов животных Все самое интересное о кошках
Все самое интересное о кошках Вегетативное размножение растений
Вегетативное размножение растений Строение эукариотических клеток
Строение эукариотических клеток Воздушное питание растений. Фотосинтез
Воздушное питание растений. Фотосинтез Загальна будова та функції нервової системи
Загальна будова та функції нервової системи Фитоценоздағы өсімдіктердің ярустық жіктелуі
Фитоценоздағы өсімдіктердің ярустық жіктелуі Желтый Арбуз
Желтый Арбуз Цветы в легендах, поэзии, музыке
Цветы в легендах, поэзии, музыке Происхождение человека (теории происхождения человека)
Происхождение человека (теории происхождения человека) здоровьем дорожить умейте 3 часть
здоровьем дорожить умейте 3 часть Отряд пресмыкающиеся. Черепахи. Крокодилы
Отряд пресмыкающиеся. Черепахи. Крокодилы Обмен веществ и превращение энергии в клетке
Обмен веществ и превращение энергии в клетке Типи онтогенезу та його періодизація
Типи онтогенезу та його періодизація Размножение живых организмов
Размножение живых организмов Операции на голове
Операции на голове Дыхательная функция крови. Кислотно-основное состояние организма
Дыхательная функция крови. Кислотно-основное состояние организма Тип Гребневики (Ctenophora)
Тип Гребневики (Ctenophora) Занятие элективного курса Основы биологии для 11профильного класса.
Занятие элективного курса Основы биологии для 11профильного класса. Генна інженерія
Генна інженерія Репарация ДНК. Спонтанные мутации
Репарация ДНК. Спонтанные мутации Редуценты и их экологическая роль
Редуценты и их экологическая роль Вид и видообразование. (лекция 9-10)
Вид и видообразование. (лекция 9-10) Рысь. Внешний вид
Рысь. Внешний вид Викторина Эти забавные животные
Викторина Эти забавные животные