Содержание
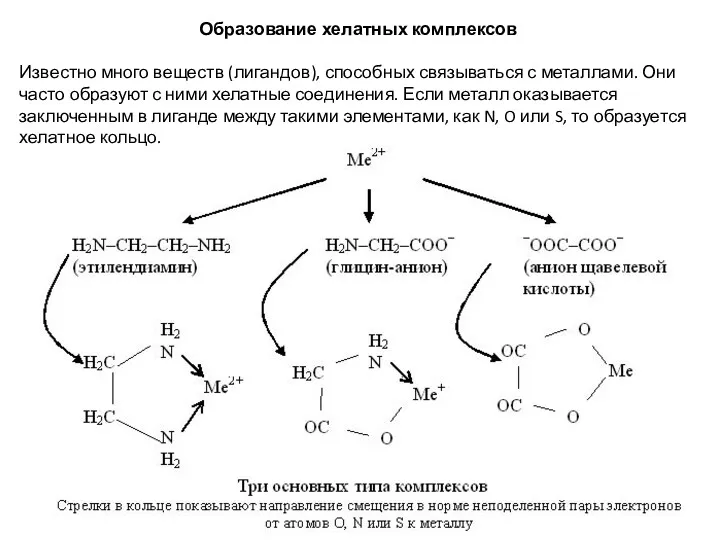
- 2. Образование хелатных комплексов Известно много веществ (лигандов), способных связываться с металлами. Они часто образуют с ними
- 3. При содержании двух электронодонорных групп заряд катиона металла при образовании хелатного соединения не меняется (этилендиамин). Лиганды
- 4. Для оценки прочности связей (варьирующейся в широких пределах для разных комплексов) применяют константы устойчивости, характеризующие равновесие
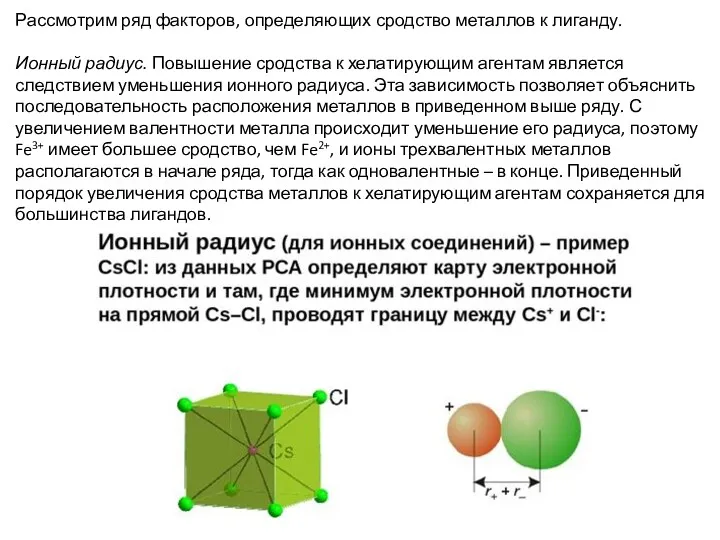
- 5. Рассмотрим ряд факторов, определяющих сродство металлов к лиганду. Ионный радиус. Повышение сродства к хелатирующим агентам является
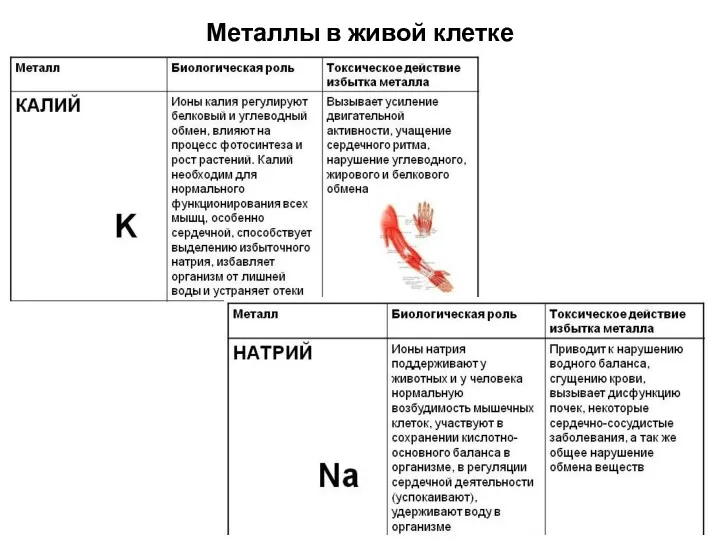
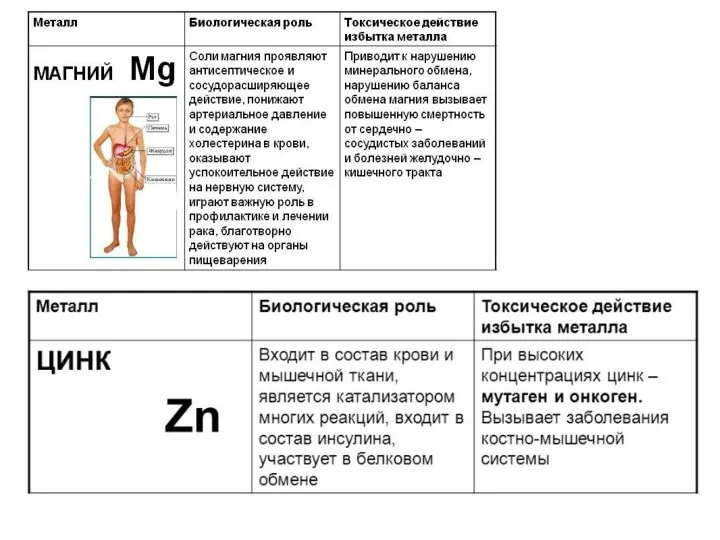
- 6. Металлы в живой клетке
- 8. Механизмы биологического действия хелатирующих агентов Наличие двухфазной реакции организма на металлы свидетельствует о существовании двух разных
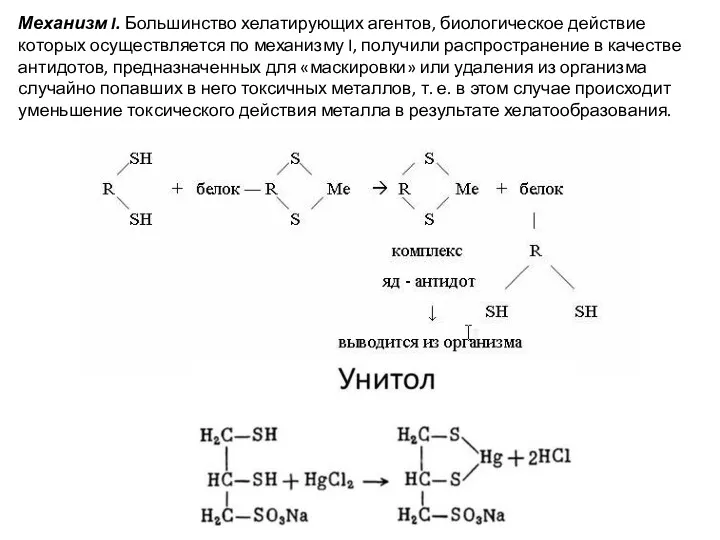
- 9. Механизм I. Большинство хелатирующих агентов, биологическое действие которых осуществляется по механизму I, получили распространение в качестве
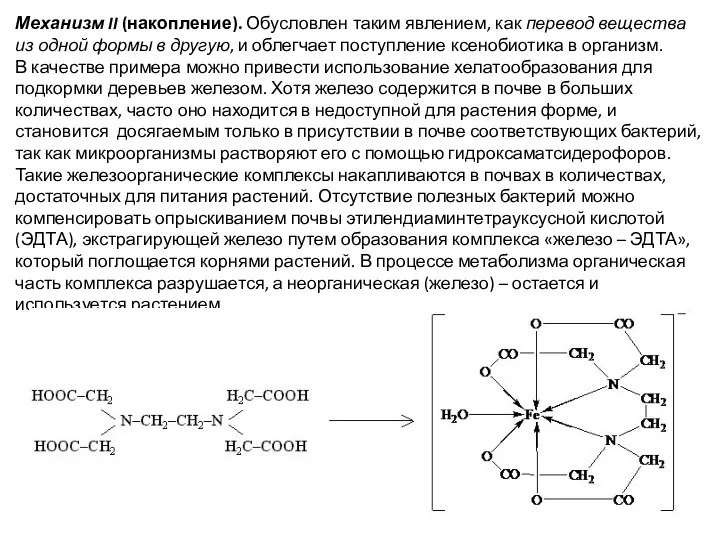
- 10. Механизм II (накопление). Обусловлен таким явлением, как перевод вещества из одной формы в другую, и облегчает
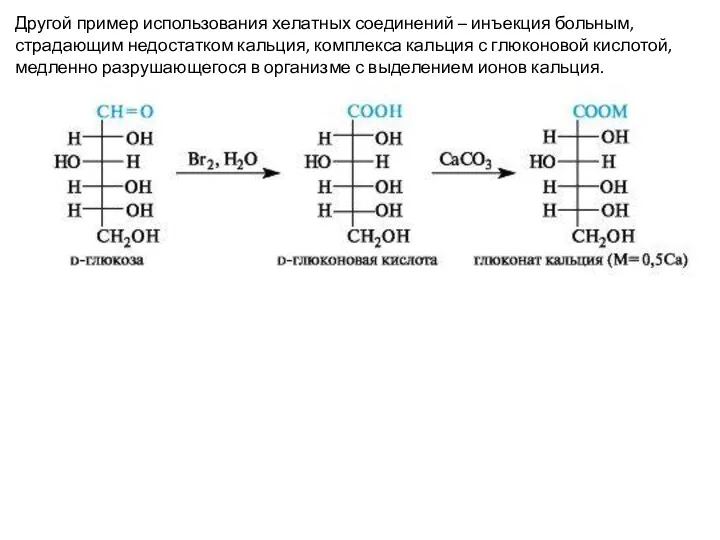
- 11. Другой пример использования хелатных соединений – инъекция больным, страдающим недостатком кальция, комплекса кальция с глюконовой кислотой,
- 12. Кооперативный эффект – явление возрастания химической активности ксенобиотика вследствие хелатообразования. Это можно показать на примере ионов
- 13. Биотрансформация неорганических ксенобиотиков Реакции восстановления атомов с переменной валентностью. Трансформация арсенатов As5+ в арсениты с As3+,
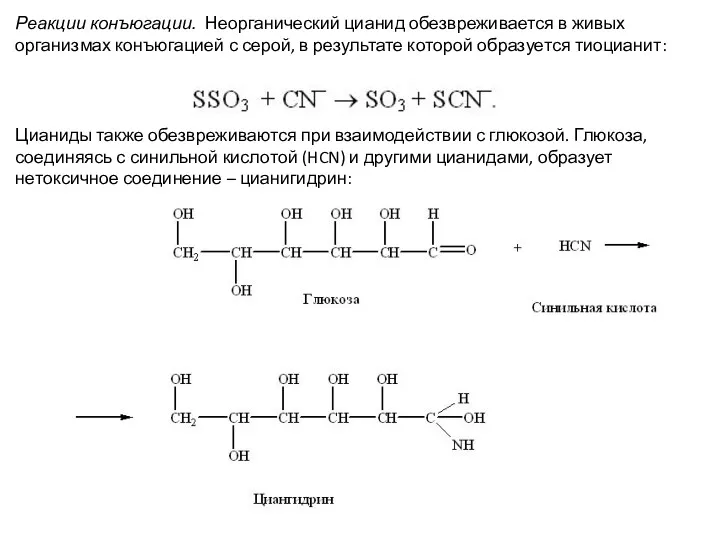
- 14. Реакции конъюгации. Неорганический цианид обезвреживается в живых организмах конъюгацией с серой, в результате которой образуется тиоцианит:
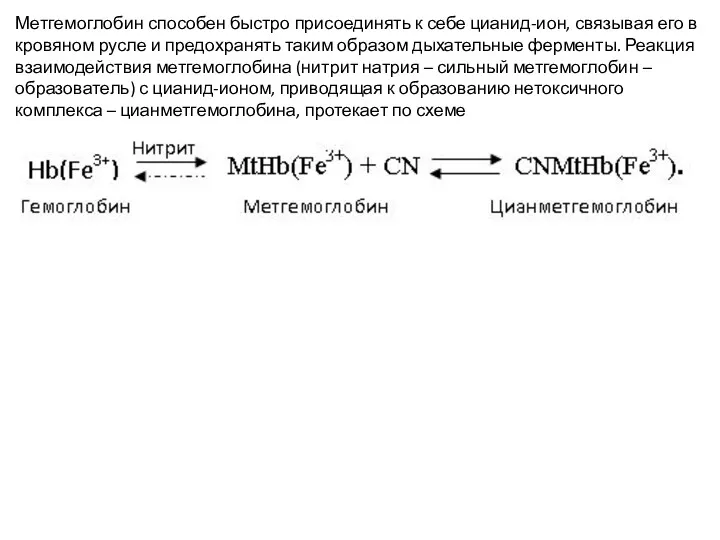
- 15. Метгемоглобин способен быстро присоединять к себе цианид-ион, связывая его в кровяном русле и предохранять таким образом
- 17. Скачать презентацию





 Hedera helix
Hedera helix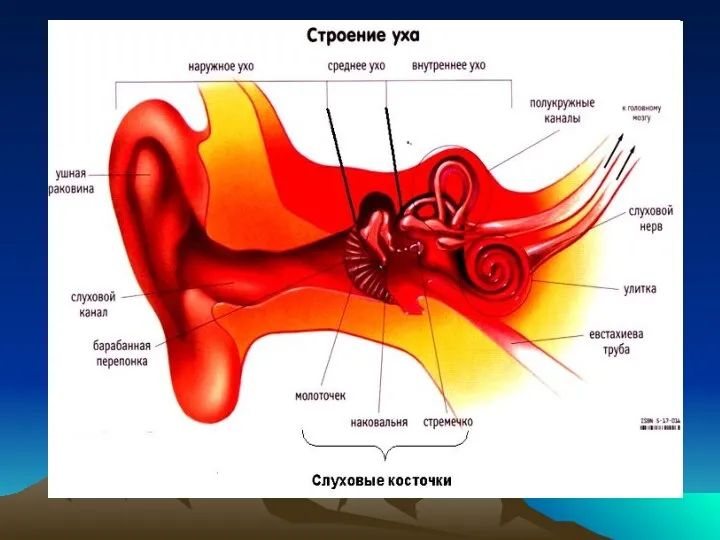 Органы равновесия, обоняния и вкуса
Органы равновесия, обоняния и вкуса Лето на окне или как вырастить огурцы осенью - зимой дома
Лето на окне или как вырастить огурцы осенью - зимой дома Липидтердің құрылымдық компоненттері. Майлардың қасиеттері мен қызметтері
Липидтердің құрылымдық компоненттері. Майлардың қасиеттері мен қызметтері Тварини та їхні особливості. Жираф - найвища тварина на Землі
Тварини та їхні особливості. Жираф - найвища тварина на Землі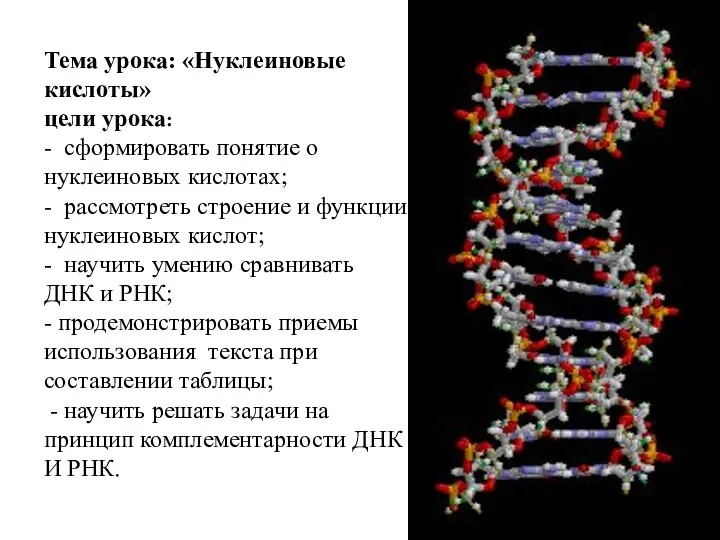 Урок-презентация на тему Нуклеиновые кислоты
Урок-презентация на тему Нуклеиновые кислоты Обмен белка и аминокислот
Обмен белка и аминокислот Красиво цветущие и неприхотливые однолетние растения, которые украсят любой сад
Красиво цветущие и неприхотливые однолетние растения, которые украсят любой сад Межклеточные сигнальные вещества
Межклеточные сигнальные вещества Оплодотворение у цветковых растений
Оплодотворение у цветковых растений Елементний склад живих організмів. Неорганічні речовини: вода і мінеральні солі
Елементний склад живих організмів. Неорганічні речовини: вода і мінеральні солі Невидимые нити в весеннем лесу
Невидимые нити в весеннем лесу Традиційна біотехнологія
Традиційна біотехнологія Электрофорез в полиакриламидном геле
Электрофорез в полиакриламидном геле Brainstem. Cerebellum. Reticular formation
Brainstem. Cerebellum. Reticular formation Презентация Пингвины
Презентация Пингвины Психофизиология сна
Психофизиология сна Органи виділення людини
Органи виділення людини Обмен веществ и превращение энергии
Обмен веществ и превращение энергии Иммунитет. Имунная система (биология, 8 класс)
Иммунитет. Имунная система (биология, 8 класс) Денсаулық сақтау және өндіріс қызметіндегі заманауи генетика мен молекулалық биологияның жетістіктері
Денсаулық сақтау және өндіріс қызметіндегі заманауи генетика мен молекулалық биологияның жетістіктері Трихинеллез. Возбудитель
Трихинеллез. Возбудитель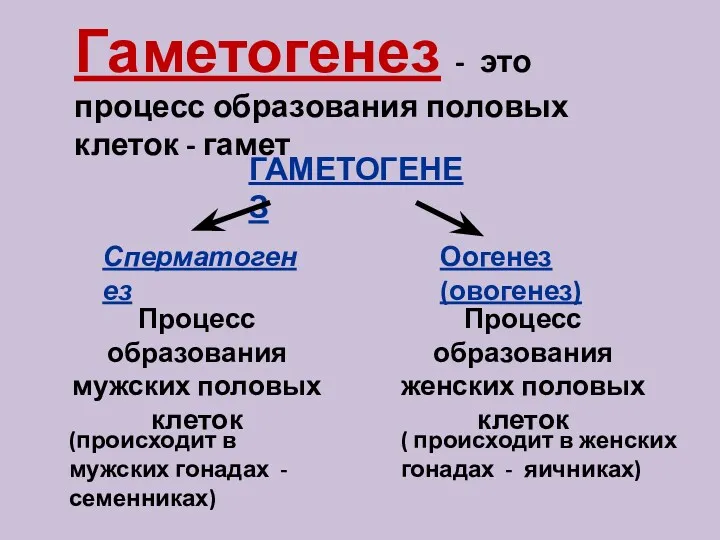 Процесс образования половых клеток - гаметогенез
Процесс образования половых клеток - гаметогенез Транспорт веществ. Термины. 8 класс
Транспорт веществ. Термины. 8 класс Structura morfo-funcţională a aparatului de susţinere şi mişcare
Structura morfo-funcţională a aparatului de susţinere şi mişcare Покрови тіла тварин
Покрови тіла тварин Протерозой
Протерозой Курс зоологии (тип хордовые)
Курс зоологии (тип хордовые)