Содержание
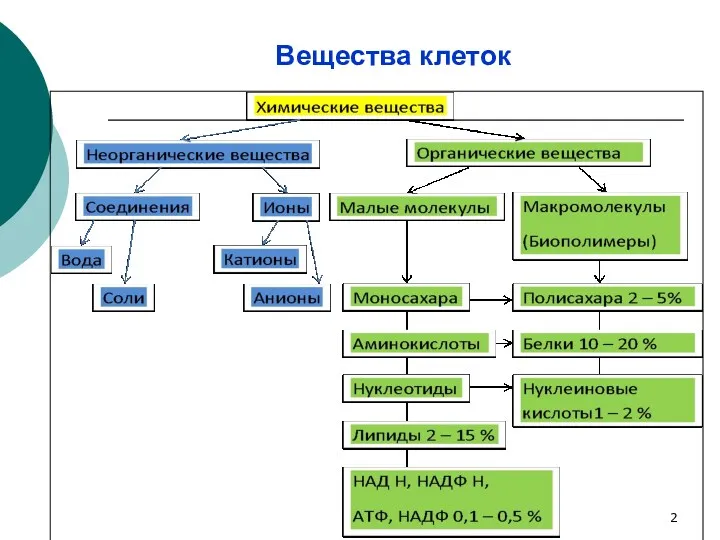
- 2. Вещества клеток
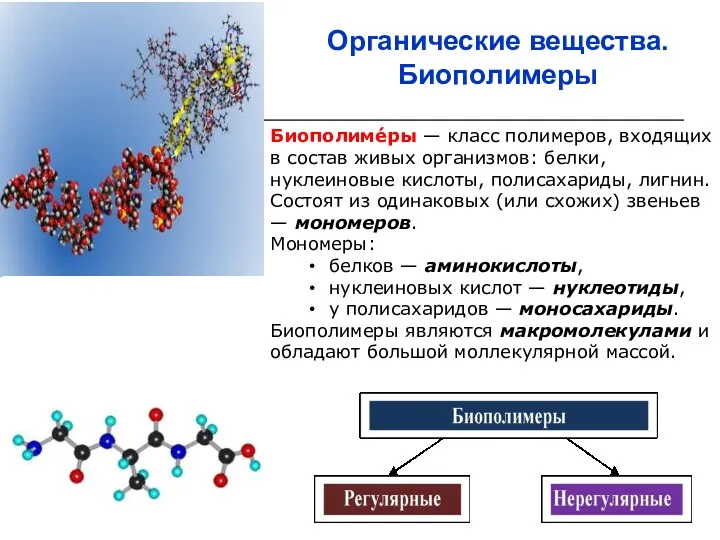
- 3. Органические вещества. Биополимеры Биополиме́ры — класс полимеров, входящих в состав живых организмов: белки, нуклеиновые кислоты, полисахариды,
- 4. Органические вещества: белки «Повсюду, где мы встречаем жизнь, мы находим, что она связана с каким-либо белковым
- 5. История открытия белка Первый белок, очищенный от примесей был получен в 1728 г. Я. Беккари. Это
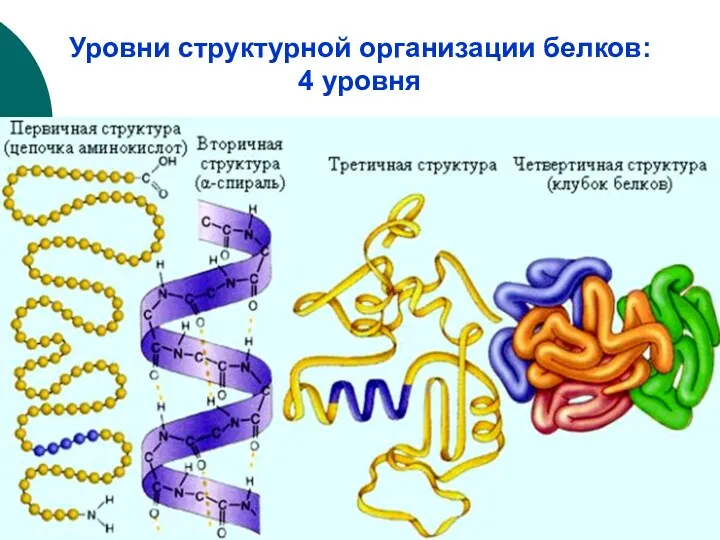
- 6. Уровни структурной организации белков: 4 уровня
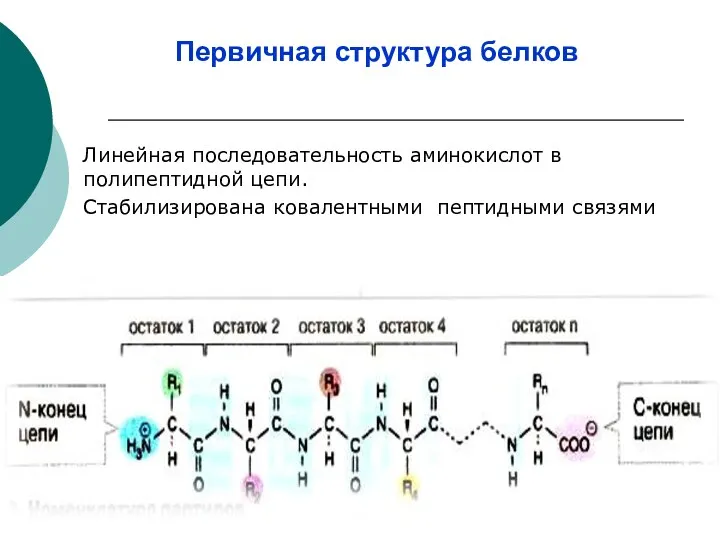
- 7. Первичная структура белков Линейная последовательность аминокислот в полипептидной цепи. Стабилизирована ковалентными пептидными связями
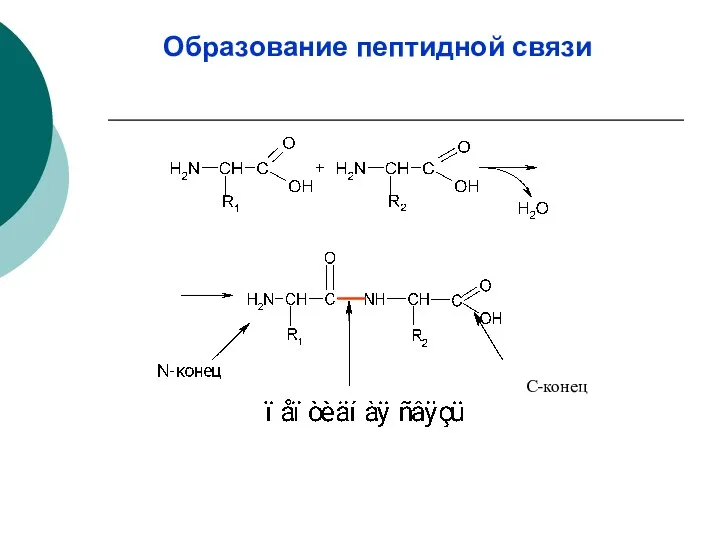
- 8. Образование пептидной связи С-конец
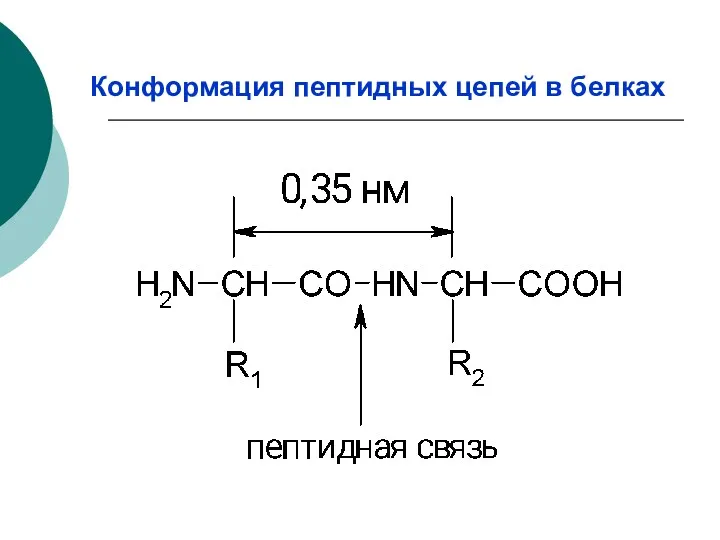
- 9. Конформация пептидных цепей в белках
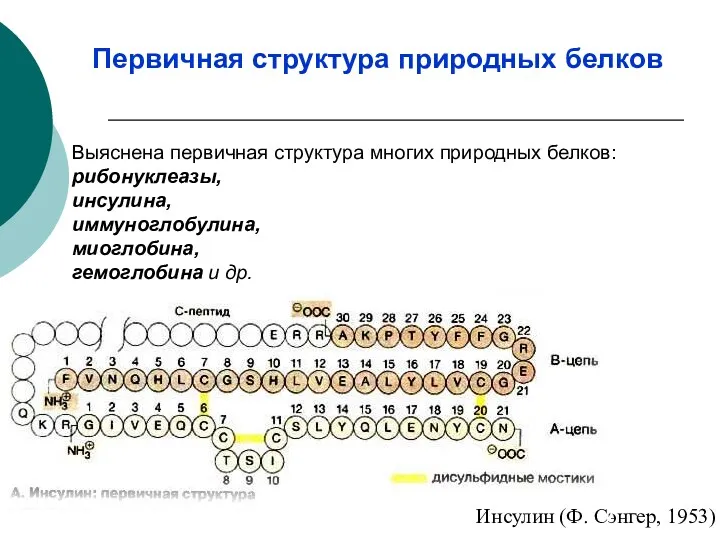
- 10. Выяснена первичная структура многих природных белков: рибонуклеазы, инсулина, иммуноглобулина, миоглобина, гемоглобина и др. Инсулин (Ф. Сэнгер,
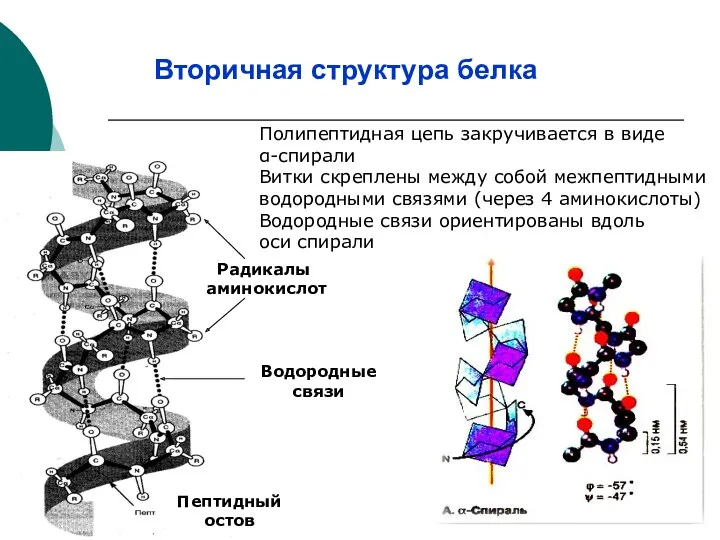
- 11. Вторичная структура белка Полипептидная цепь закручивается в виде α-спирали Витки скреплены между собой межпептидными водородными связями
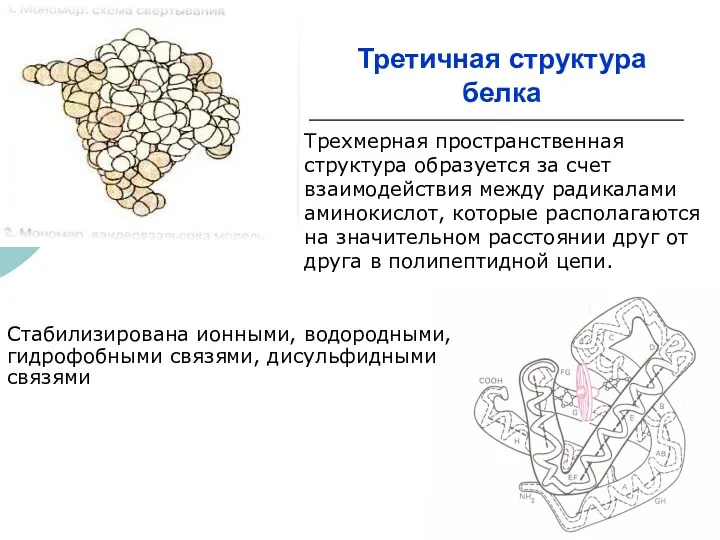
- 12. Третичная структура белка Стабилизирована ионными, водородными, гидрофобными связями, дисульфидными связями Трехмерная пространственная структура образуется за счет
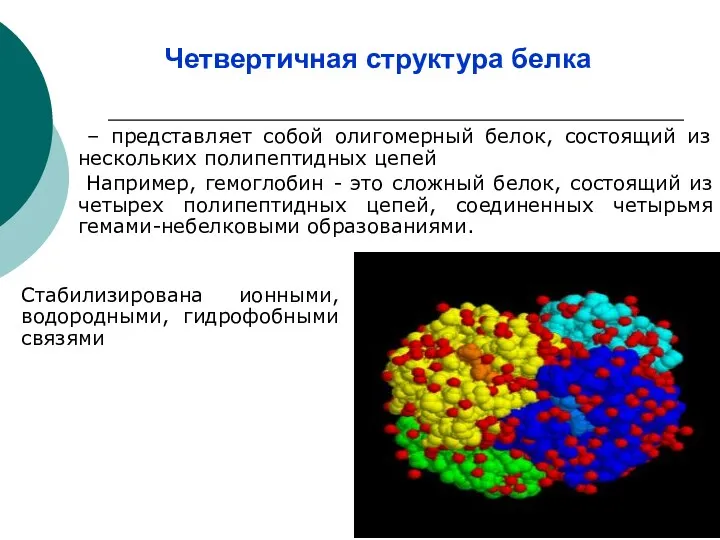
- 13. Четвертичная структура белка – представляет собой олигомерный белок, состоящий из нескольких полипептидных цепей Например, гемоглобин -
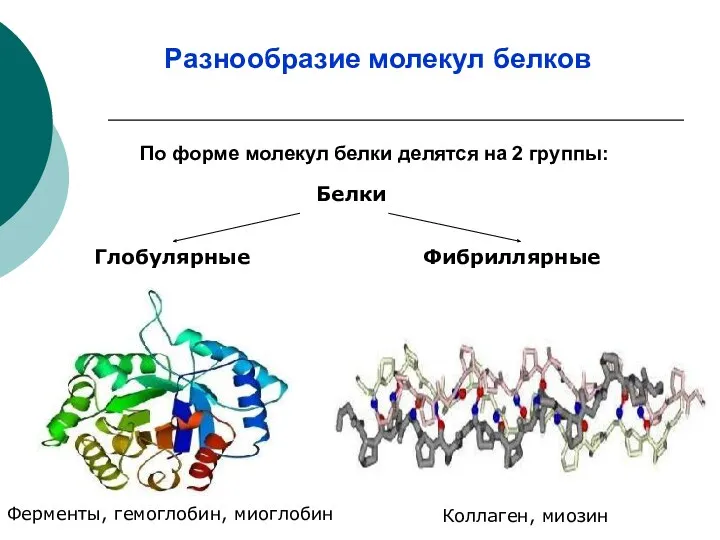
- 14. По форме молекул белки делятся на 2 группы: Фибриллярные Ферменты, гемоглобин, миоглобин Глобулярные Коллаген, миозин Белки
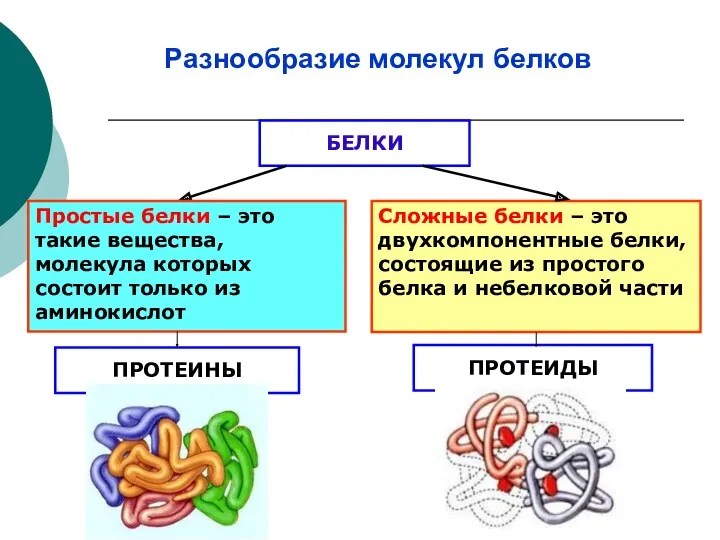
- 15. Разнообразие молекул белков
- 16. Белки представляют собой наиболее сложные коллоидные соединения. 1. В растворах белки обнаруживают очень низкое осмотическое давление
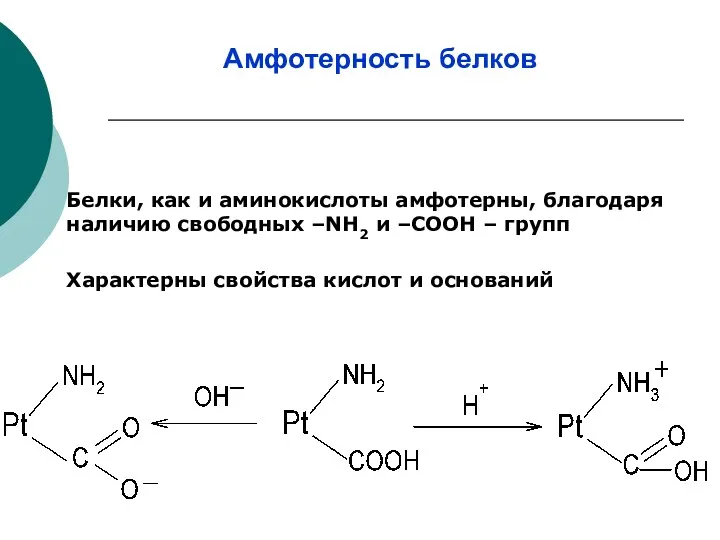
- 17. Амфотерность белков Белки, как и аминокислоты амфотерны, благодаря наличию свободных –NH2 и –СООН – групп Характерны
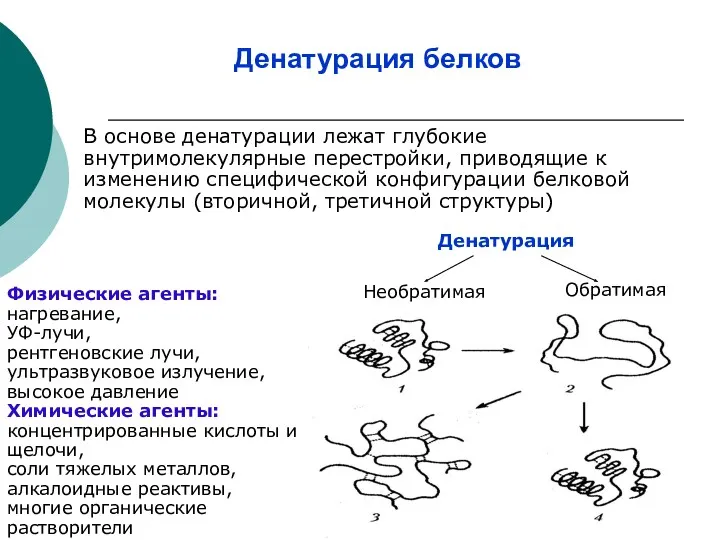
- 18. Денатурация белков В основе денатурации лежат глубокие внутримолекулярные перестройки, приводящие к изменению специфической конфигурации белковой молекулы
- 19. Гидролиз белков Взаимодействие белков с водой, в ходе которого белок утрачивает свою первичную структуру:
- 20. Цветные реакции на белки 1. Биуретовая (реакция Пиотровского) Белок + Cu(OH)2 → фиолетовая окраска → реакция
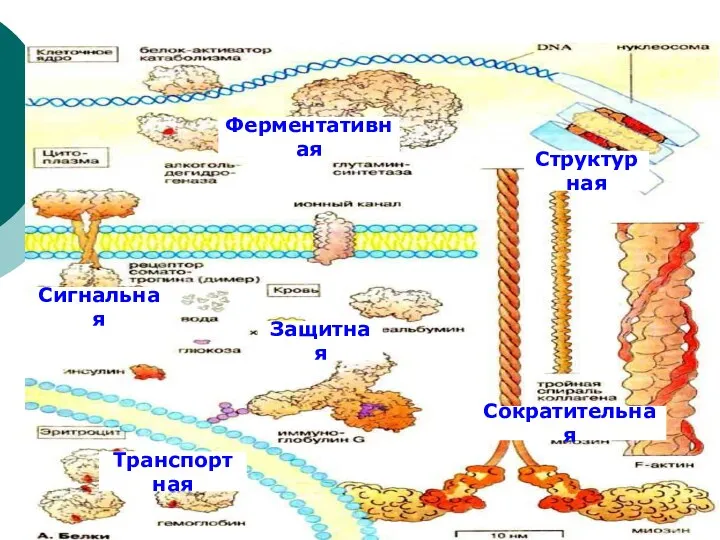
- 21. Биологическое значение белков Структурная Сократительная Защитная Ферментативная Транспортная Сигнальная
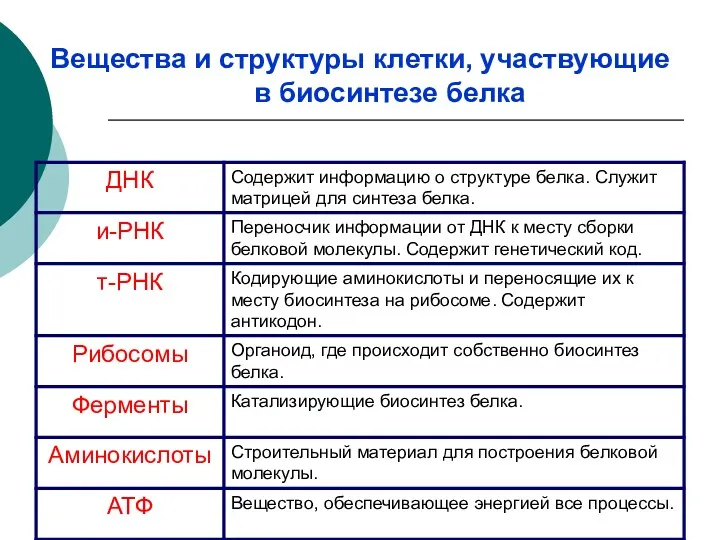
- 22. Вещества и структуры клетки, участвующие в биосинтезе белка
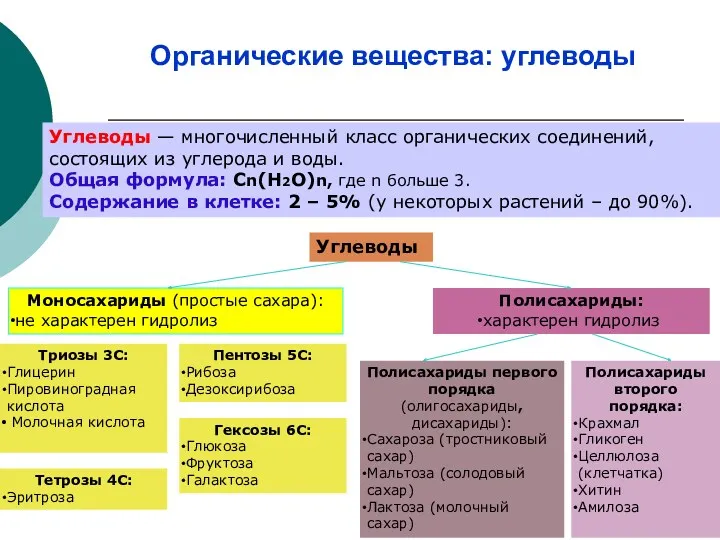
- 23. Органические вещества: углеводы Углеводы — многочисленный класс органических соединений, состоящих из углерода и воды. Общая формула:
- 24. Биологическое значение углеводов Энергетическая функция: 1г. углеводов – 17,6 кДж энергии. Запасающая (крахмал, гликоген). Пластическая функция:
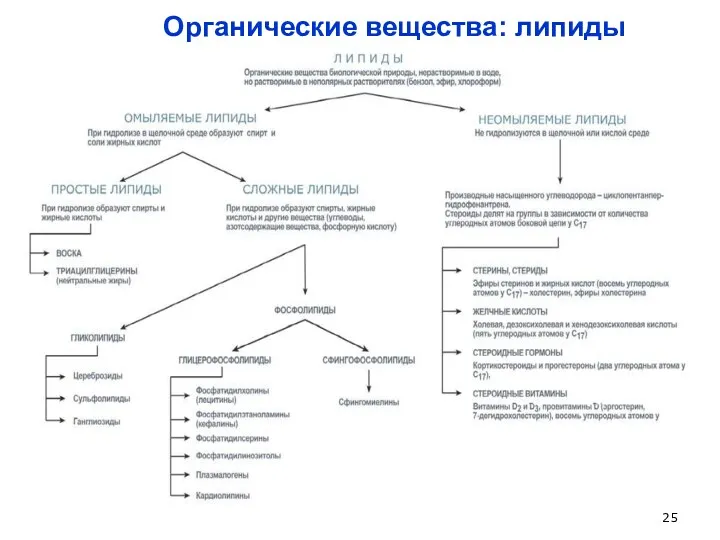
- 25. Органические вещества: липиды
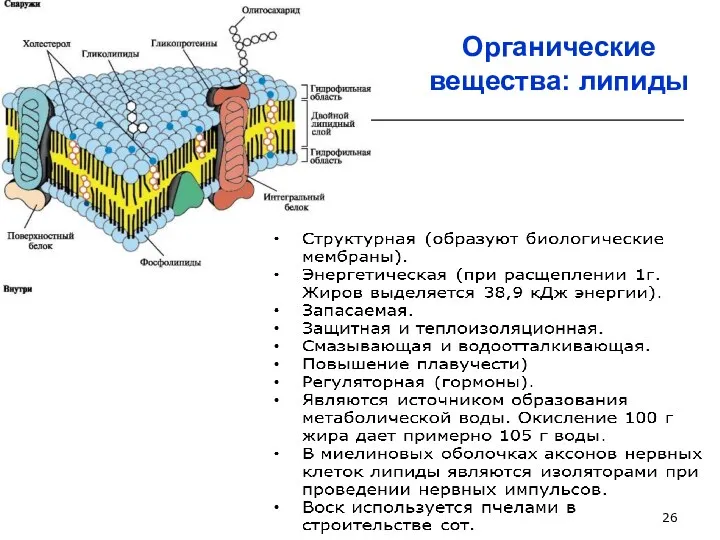
- 26. Органические вещества: липиды
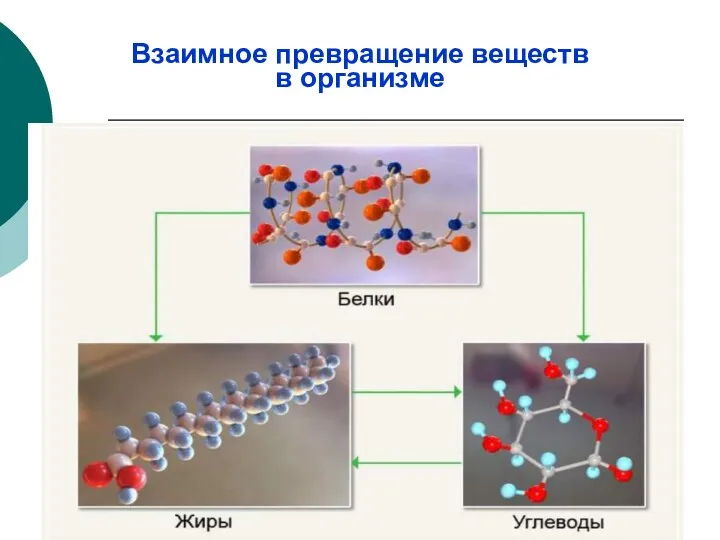
- 27. Взаимное превращение веществ в организме
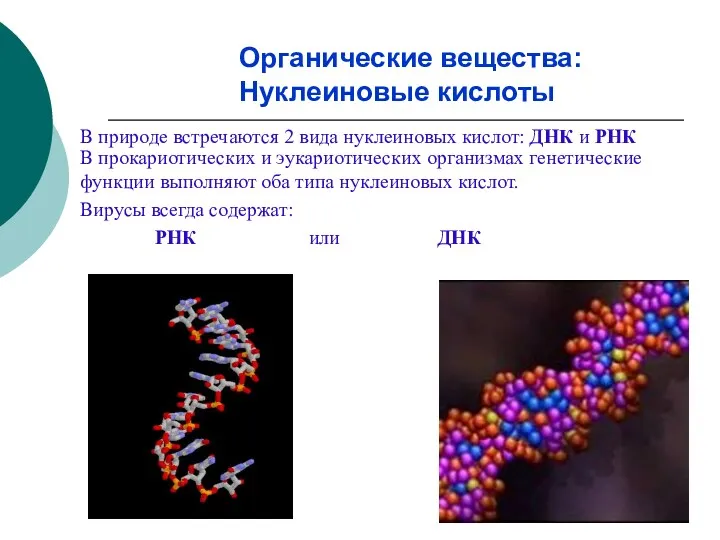
- 28. В природе встречаются 2 вида нуклеиновых кислот: ДНК и РНК В прокариотических и эукариотических организмах генетические
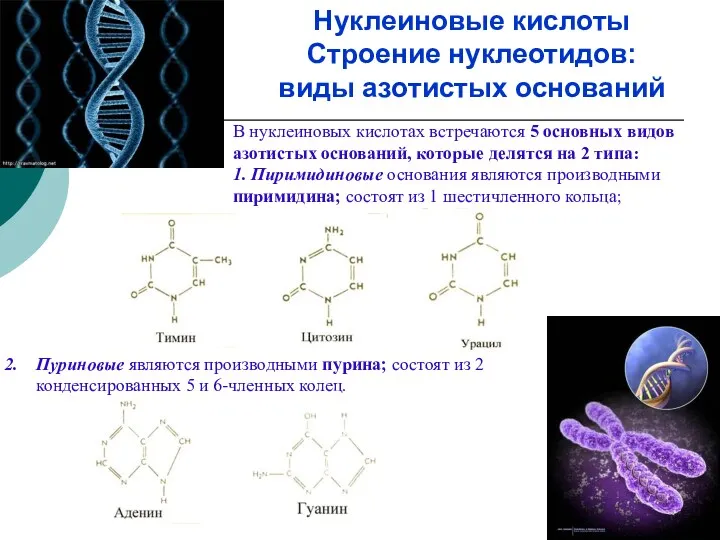
- 29. Нуклеиновые кислоты Строение нуклеотидов: виды азотистых оснований В нуклеиновых кислотах встречаются 5 основных видов азотистых оснований,
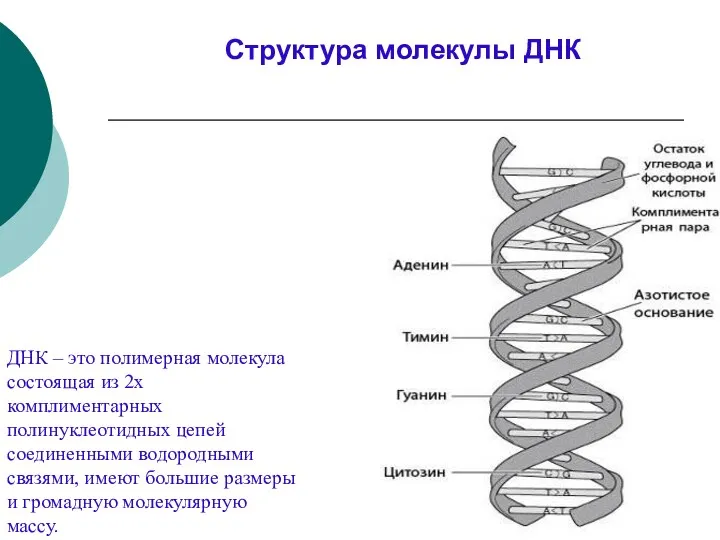
- 30. ДНК – это полимерная молекула состоящая из 2х комплиментарных полинуклеотидных цепей соединенными водородными связями, имеют большие
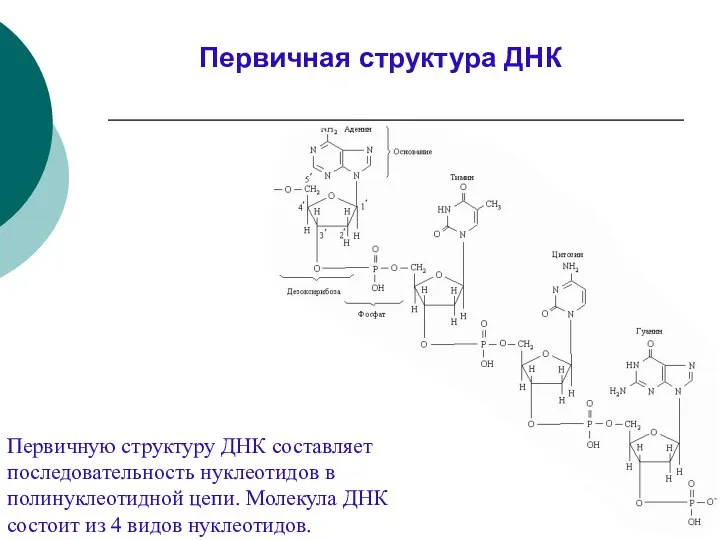
- 31. Первичную структуру ДНК составляет последовательность нуклеотидов в полинуклеотидной цепи. Молекула ДНК состоит из 4 видов нуклеотидов.
- 32. Больших успехов в определении структуры ДНК достигли Эрвин Чаргафф и его сотрудники (1950г.) Используя метод хроматографии
- 33. Вторичная структура ДНК В 1953г. Уотс и Крик установили, что ДНК представляет собой двойную спираль, состоящую
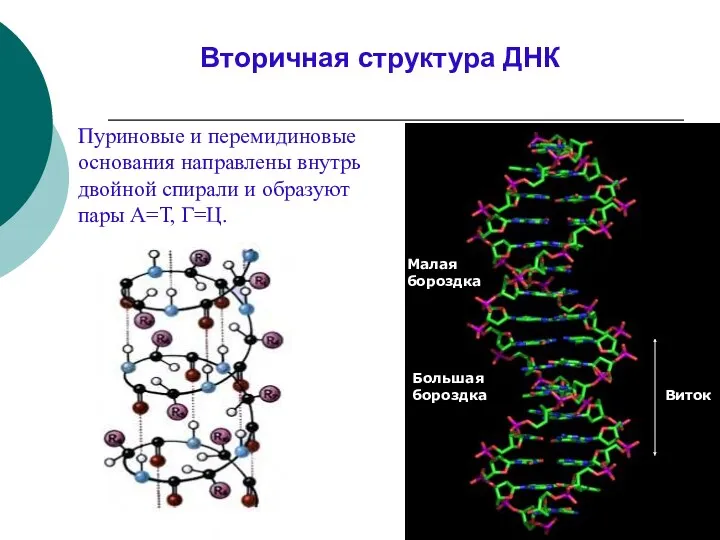
- 34. Виток Большая бороздка Малая бороздка Вторичная структура ДНК Пуриновые и перемидиновые основания направлены внутрь двойной спирали
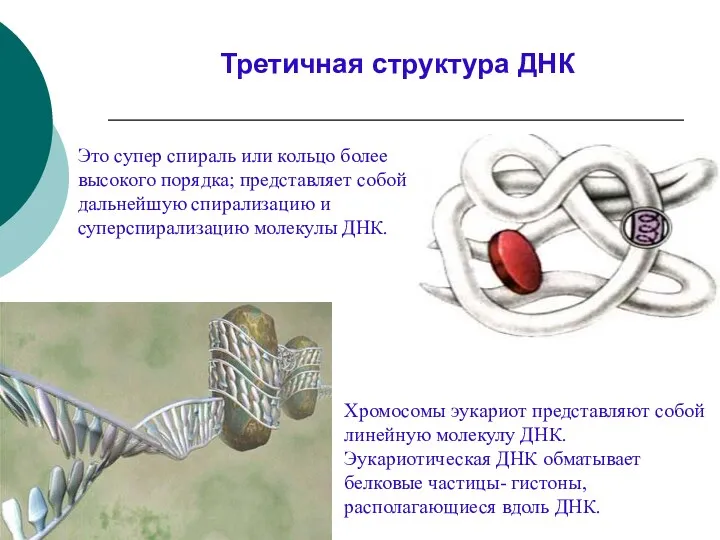
- 35. Это супер спираль или кольцо более высокого порядка; представляет собой дальнейшую спирализацию и суперспирализацию молекулы ДНК.
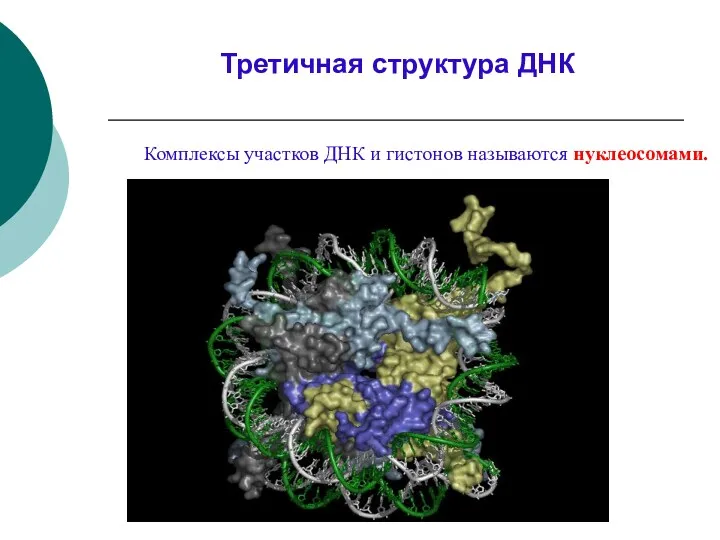
- 36. Комплексы участков ДНК и гистонов называются нуклеосомами. Третичная структура ДНК
- 38. Скачать презентацию








 Лишайники- биоиндикаторы загрязнения воздуха
Лишайники- биоиндикаторы загрязнения воздуха Размножение и развитие организмов
Размножение и развитие организмов Компоненты организма человека
Компоненты организма человека Этнические процессы
Этнические процессы Фотосинтез
Фотосинтез Продление рода. Органы размножения. 7 класс
Продление рода. Органы размножения. 7 класс Дыхательная система
Дыхательная система Сердечно-сосудистая система анатомия и физиология
Сердечно-сосудистая система анатомия и физиология Protein denatu-ration
Protein denatu-ration Онтогенез. 10 класс
Онтогенез. 10 класс Динамика популяций. Экологические стратегии. Факторы, влияющие на рост популяции
Динамика популяций. Экологические стратегии. Факторы, влияющие на рост популяции Строение волос
Строение волос Тип Плоские Черви
Тип Плоские Черви Урок-игра по теме Системы органов животных
Урок-игра по теме Системы органов животных Питательные вещества, необходимые для роста живых организмов
Питательные вещества, необходимые для роста живых организмов evolyuciya_krovenosnoy_sistemy_7_klass_1427359430_105713
evolyuciya_krovenosnoy_sistemy_7_klass_1427359430_105713 Тканини організму людини
Тканини організму людини Презентация к уроку биологии в 6 классе по темеЦветок.Соцветия
Презентация к уроку биологии в 6 классе по темеЦветок.Соцветия Красная книга Глазуновского района
Красная книга Глазуновского района Жизненные циклы семенных растений
Жизненные циклы семенных растений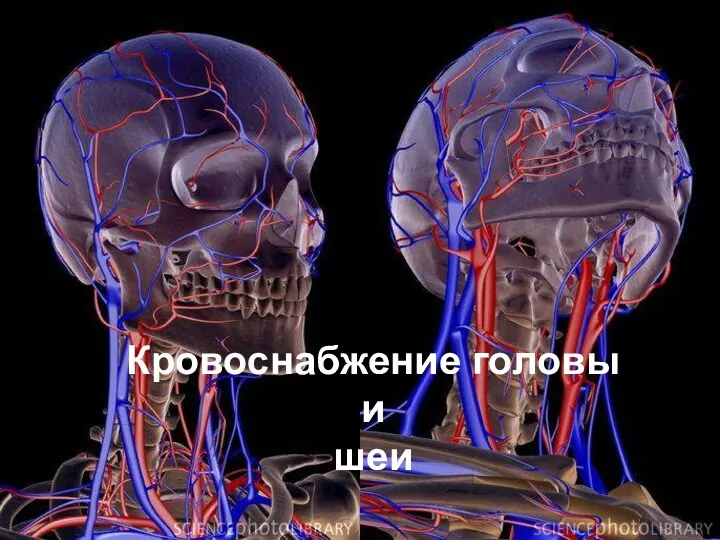 Кровоснабжение головы и шеи
Кровоснабжение головы и шеи Биологические исследования
Биологические исследования Физиология вторичных Мессенджеров
Физиология вторичных Мессенджеров Везикулярлық тасымалдау
Везикулярлық тасымалдау Содержание углекислого газа в школьных помещениях
Содержание углекислого газа в школьных помещениях Закономірності успадкування ознак
Закономірності успадкування ознак Комнатные растения
Комнатные растения Презентация к уроку общей биологии 11 класс Антропогенез
Презентация к уроку общей биологии 11 класс Антропогенез