Санитарно-гигиеническая оценка биологического объекта и готовых продуктов, включающих живые клетки продуцента презентация
Содержание
- 2. Использование биологического объекта в биотехнологических процессах определяет специфику технологии производств, специфику их гигиенической и санитарной оценки.
- 3. Гигиеническому нормированию подлежат штаммы микроорганизмов, используемые или предполагаемые к использованию в биотехнологических процессах. Нормированию также подлежат
- 4. Комплексная оценка промышленных штаммов Изучение штаммов-продуцентов включает изучение их микробиологических, технологических, санитарно-гигиенических и экологических свойств. Схема
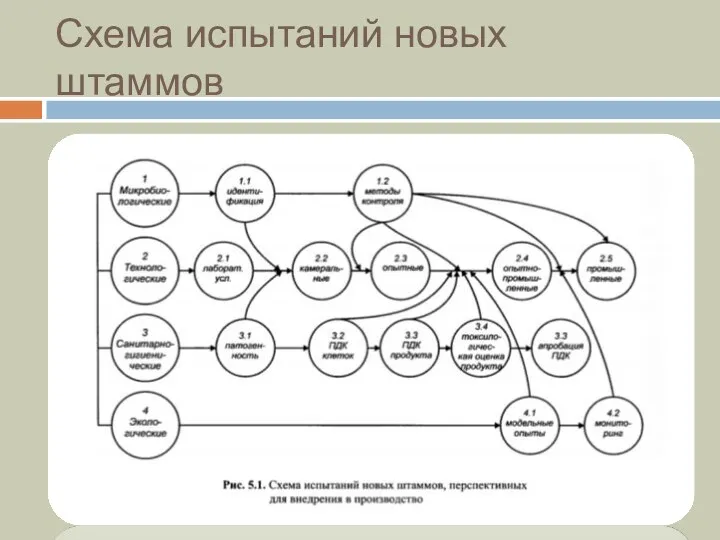
- 5. Схема испытаний новых штаммов
- 6. Этапы исследований На этапе микробиологических исследований (этап 1) определяется таксономическое положение штамма, разрабатываются методы его идентификации
- 7. Эколого-токсикологические исследования (этап 4) включают определение приживаемости клеток продуцента в экосистемах, изучение их влияния на биоценоз
- 8. Гигиеническое нормирование микроорганизмов Гигиеническое нормирование микроорганизмов – продуцентов и содержащих их готовых форм препаратов в объектах
- 9. Концепция и принципы определение ПДК Концепция определения ПДК химических веществ не в полной мере применима к
- 10. Определение патогенности штаммов В соответствии с Методическими указаниями по экспериментальному обоснованию ПДК микроорганизмов-продуцентов и содержащих их
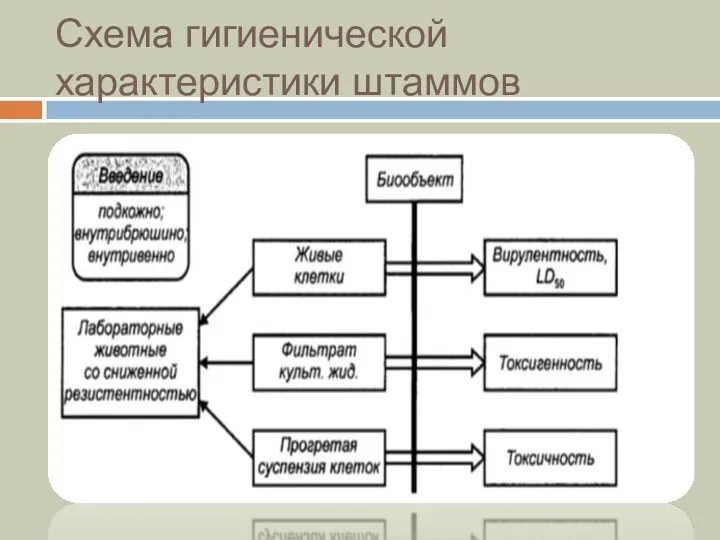
- 11. Схема гигиенической характеристики штаммов
- 12. В исследованиях используются лабораторные животные молодого возраста: белые мыши (масса тела 16-18г), белые крысы (масса тела
- 13. Для определения токсигенности культуры испытывается фильтрат культуральной жидкости при глубинном выращивании штамма. Токсичность культуры определяют при
- 14. При комплексной токсико-гигиенической оценке биологической активности штаммов и продуктов их жизнедеятельности определяется: •токсичность штаммов (острая, подострая,
- 15. •тератогенные свойства – способность вызывать структурные трансформации или дефекты зародыша или плода; •гонадотоксические свойства – способность
- 16. Показателями опасности непатогенных микроорганизмов (не вызывающих инфекционных процессов) является их токсичность, токсигенность, транзиторное микробоносительство (диссеминация во
- 17. Обоснование ПДК живых клеток микроорганизмов в воздухе рабочей зоны и в атмосферном воздухе Схема проведения исследований
- 18. На втором этапе оценивается опасность изучаемого микроорганизма при поступлении в организм лабораторных животных путями, адекватными реальным
- 19. Критерии опасности Критериями высокой опасности штамма (1 класс опасности) являются: •величина LD50 при введении микроорганизма в
- 20. Если гибели животных не наблюдается, то для достоверности оценки степени патогенности штаммов определяется вирулентность и на
- 21. Сенсибилизация Широкие исследования промышленных непатогенных штаммов и продуктов, представляющих биомассу их инактивированных клеток, показали, что в
- 22. Выявление сенсибилизирующего действия микроорганизмов штаммов-продуцентов проводится с живой культурой. При оценке готовых форм препаратов для сенсибилизации
- 23. Сенсибилизирующее действие определяется воспроизведением аллергии при повторном введении аллергена. Мыши (10-20 особей) сенсибилизируются интраназально или энтерально
- 24. Через сутки определяется разница отека двух задних лапок опытных и контрольных групп животных. При определении сенсибилизирующего
- 25. Для установления порога хронического общетоксического действия (Lim Ch) животные, сенсибилизированные суспензией изучаемого микроорганизма, подвергаются в течение
- 26. Порог иммунотоксического действия определяется на основании исследования возможного появления у животных следующих эффектов: сенсибилизации, иммунизации (признак
- 27. Оценка антигенности микроорганизмов осуществляется на основе определения иммунных антител изучаемого микроба в реакциях агглютинации и фагоцитоза
- 28. При реакции фагоцитоза подсчитывается формула крови сенсибилизированных и контрольных животных и определяется доля фагоцитирующих нейтрофилов и
- 29. За пороговую концентрацию микроорганизмов принимается та, которая вызывает сенсибилизацию 30 % животных, увеличениеим имунного ответа организма
- 30. Определение порога диссеминации микроорганизмов во внутренних органах осуществляется в конце хронического эксперимента и через две недели
- 31. За пороговую принимается минимальная доза или концентрация, при которой через 2 недели после окончания хронического эксперимента
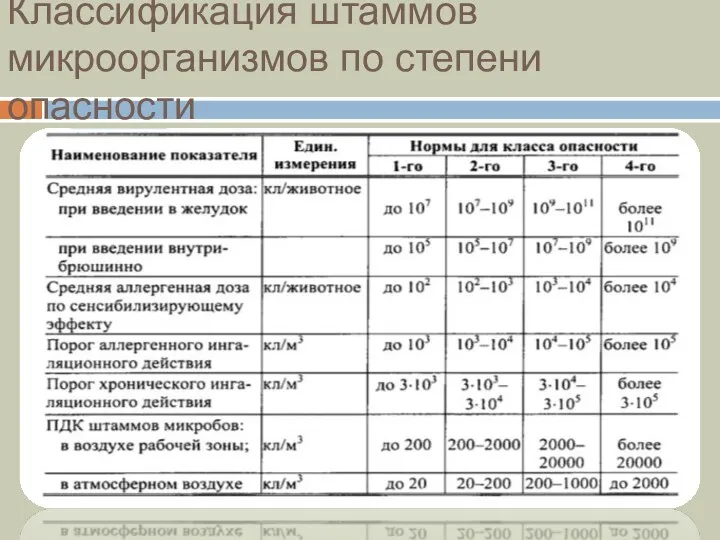
- 32. Класс опасности микроорганизмов устанавливается согласно табл.5.1 и ставится пометка «А» (аллерген), если при нормировании лимитирующим признаком
- 33. Классификация штаммов микроорганизмов по степени опасности
- 34. Классы макроорганизмов Микроорганизмы-продуценты и готовые продукты на их основе, отнесенные к 1 классу опасности не разрешаются
- 35. Наиболее широкие санитарно-гигиенические исследования проведены с дрожжами p. Candida, которые использовались в крупнотоннажных производствах кормового белка
- 36. По данным гигиенических обследований конца XX века, частота обнаружения дрожжей p. Candida на слизистых оболочках у
- 37. Санитарно-гигиенические обследования крупнотоннажных производств, использующих в качестве продуцентов непатогенные штаммы дрожжей p. Candida, показали, что промышленные
- 38. На основании санитарно-гигиенических исследований промышленных углеводород окисляющих штаммов дрожжей p.Candida определена ПДК клеток в воздухе рабочей
- 39. Бактерии метилотрофы Methylococcus capsulatus и Acetobacter methylicus, используемые в качестве продуцентов при культивировании на природном газе
- 40. Вывод Поскольку отдельные патогенные штаммы выявляются среди непатогенных дрожжей одного и того же вида, теоретически возможным
- 42. Скачать презентацию




































 Хромосомный набор соматических клеток
Хромосомный набор соматических клеток Purinergic signaling
Purinergic signaling Тип членистоногие. Класс пауки и насекомые
Тип членистоногие. Класс пауки и насекомые Zoológico de Madrid
Zoológico de Madrid Додарвиновский период развития эволюционных учений.
Додарвиновский период развития эволюционных учений. Презентация урока: Типы соединения костей с лабораторной работой Внешнее строение кости
Презентация урока: Типы соединения костей с лабораторной работой Внешнее строение кости Артерии большого круга кровообращения
Артерии большого круга кровообращения Астық таситын кемелерде және трюмдеріндегі фосфин негізіндегі препараттармен астық өнімдерін зарарсыздандыру
Астық таситын кемелерде және трюмдеріндегі фосфин негізіндегі препараттармен астық өнімдерін зарарсыздандыру Свет в жизни комнатных растений
Свет в жизни комнатных растений Лимфатическая система
Лимфатическая система Сердечно-сосудистая система
Сердечно-сосудистая система Синюха голубая - Polemonium caeruleum
Синюха голубая - Polemonium caeruleum Различия Русской пегой и Русской гончих
Различия Русской пегой и Русской гончих Митохондрия. Лизосомы
Митохондрия. Лизосомы Эпиграф
Эпиграф Открытый урок по биологии тема внешнее строение листа
Открытый урок по биологии тема внешнее строение листа Генеративная часть покрытосеменных растений
Генеративная часть покрытосеменных растений Биоритмы. Сны и сновидения
Биоритмы. Сны и сновидения Основные типы экологических взаимодействий
Основные типы экологических взаимодействий Животные в доме
Животные в доме Autonomic Nervous System
Autonomic Nervous System Экстремалды бактериялар
Экстремалды бактериялар Функциональная анатомия органов мужской половой системы
Функциональная анатомия органов мужской половой системы “Професія” дощового черв’яка
“Професія” дощового черв’яка Понятие о стволовых клетках
Понятие о стволовых клетках Методы микробиологической диагностики вирусных инфекций. Профилактика вирусных инфекций
Методы микробиологической диагностики вирусных инфекций. Профилактика вирусных инфекций Знатоки цветов. Викторина
Знатоки цветов. Викторина Мой первый гербарий. 4 класс
Мой первый гербарий. 4 класс