Содержание
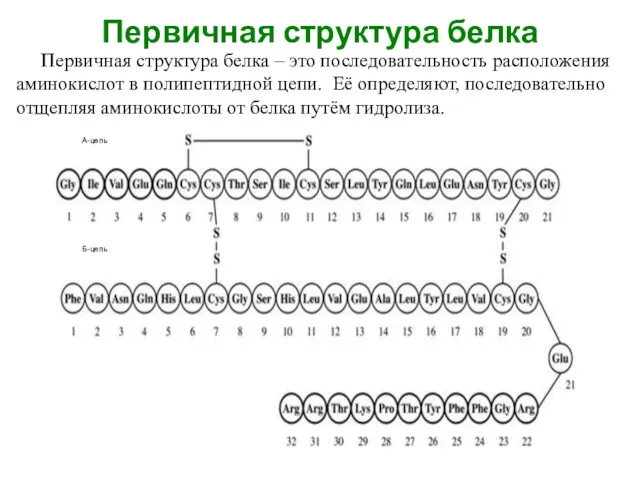
- 2. Первичная структура белка Первичная структура белка – это последовательность расположения аминокислот в полипептидной цепи. Её определяют,
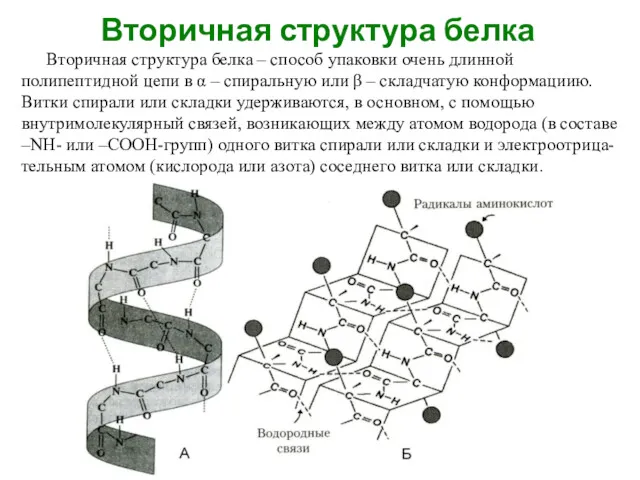
- 3. Вторичная структура белка Вторичная структура белка – способ упаковки очень длинной полипептидной цепи в α –
- 4. Третичная структура белка Третичная структура белка – трёхмерная пространственная ориентация полипептидной спирали или складчатой структуры в
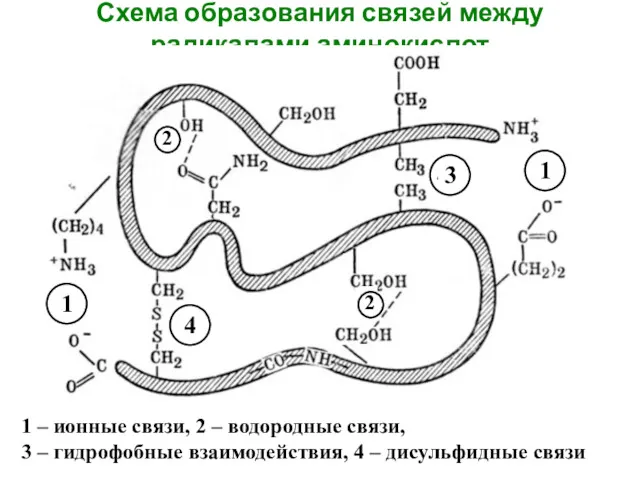
- 5. Схема образования связей между радикалами аминокислот 1 – ионные связи, 2 – водородные связи, 3 –
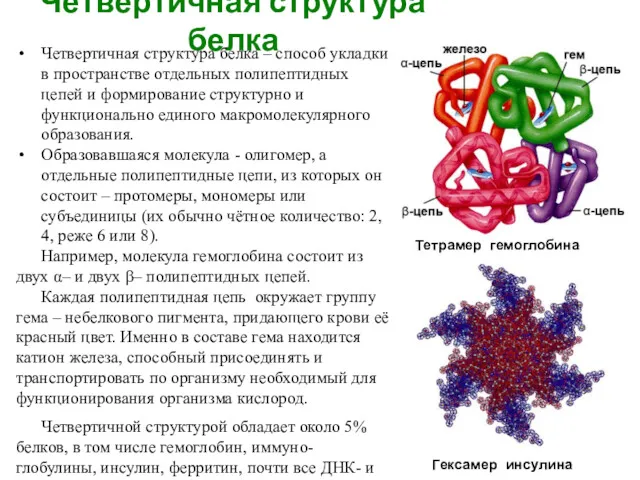
- 6. Четвертичная структура белка Четвертичная структура белка – способ укладки в пространстве отдельных полипептидных цепей и формирование
- 7. Цветные реакции для обнаружения белков и аминокислот Для идентификации пептидов, белков и отдельных аминокислот используют так
- 8. Классификация белков Белки можно классифицировать: – по форме молекул (глобулярные и фибриллярные); – по молекулярной массе
- 9. Классификация простых белков Альбумины. Примерно 75-80% осмотического давления белков сыворотки крови приходится на альбумины; еще одна
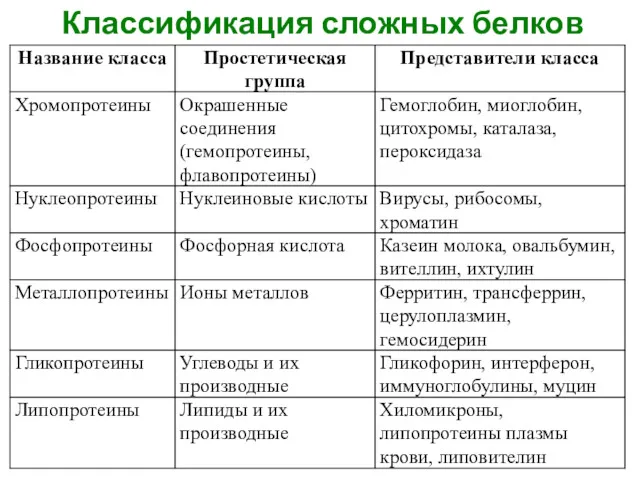
- 10. Классификация сложных белков
- 11. Функции белков
- 12. Скорость биологически важных реакций органических соединений Общая скорость химической реакции определяется (лимитируется) скоростью ее наиболее медленной
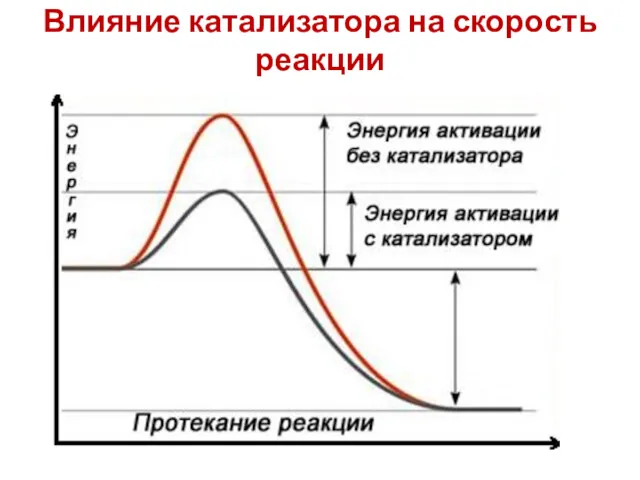
- 13. Влияние катализатора на скорость реакции
- 14. Различают субстрат и действующее на него соединение – реагент (реакционная частица) . Субстрат - вещество, в
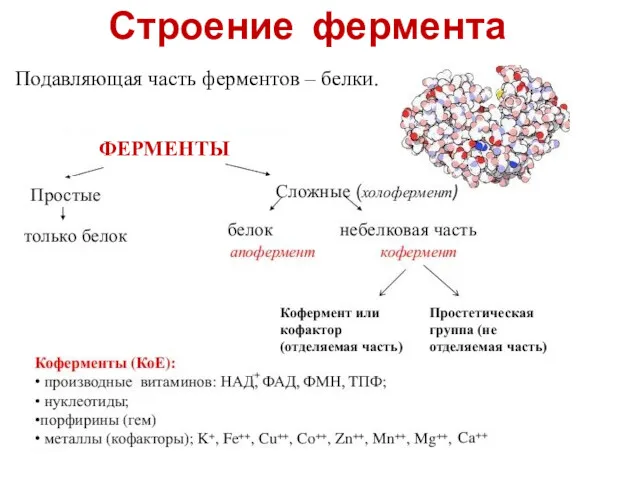
- 15. Строение фермента
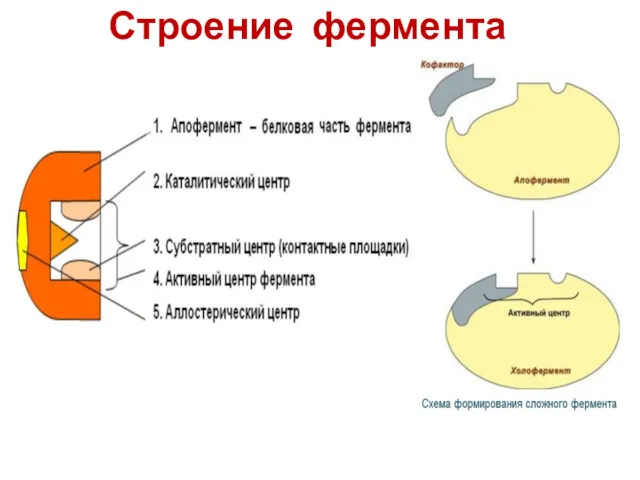
- 16. Строение фермента
- 17. Абсолютная специфичность – фермент катализирует превращение только одного вещества. Например, расщепление мочевины уреазой. Групповая (относительная) специфичность
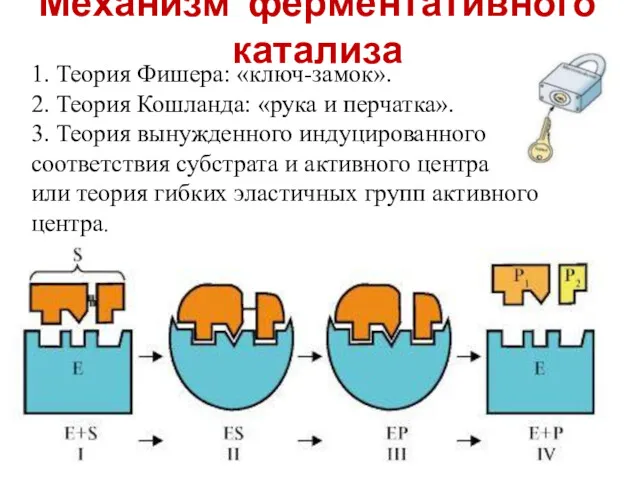
- 18. Механизм ферментативного катализа 1. Теория Фишера: «ключ-замок». 2. Теория Кошланда: «рука и перчатка». 3. Теория вынужденного
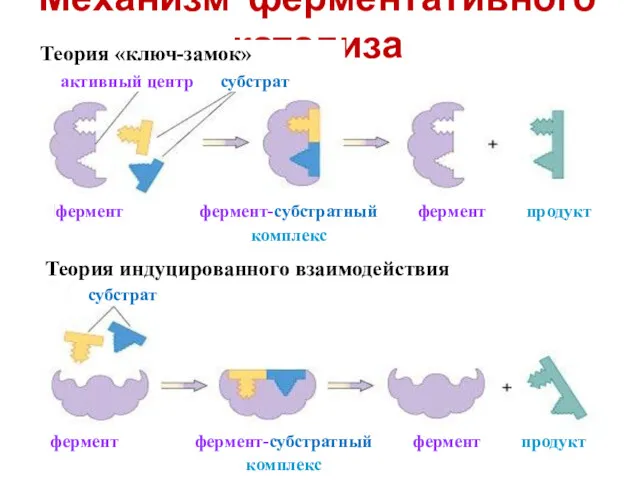
- 19. Механизм ферментативного катализа Теория «ключ-замок» Теория индуцированного взаимодействия активный центр субстрат фермент фермент-субстратный фермент продукт комплекс
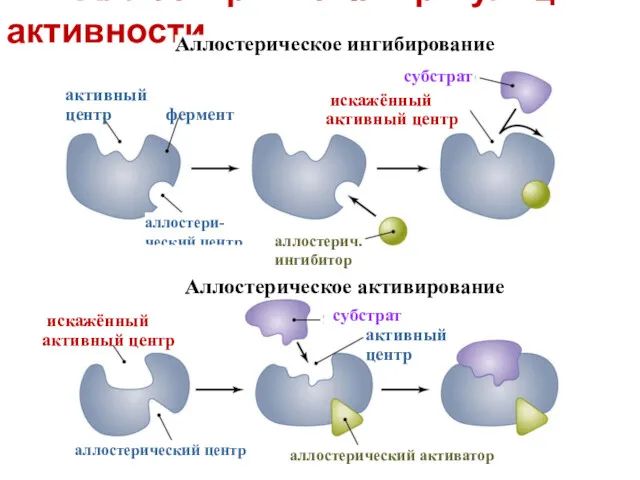
- 20. Аллостерическая регуляция активности
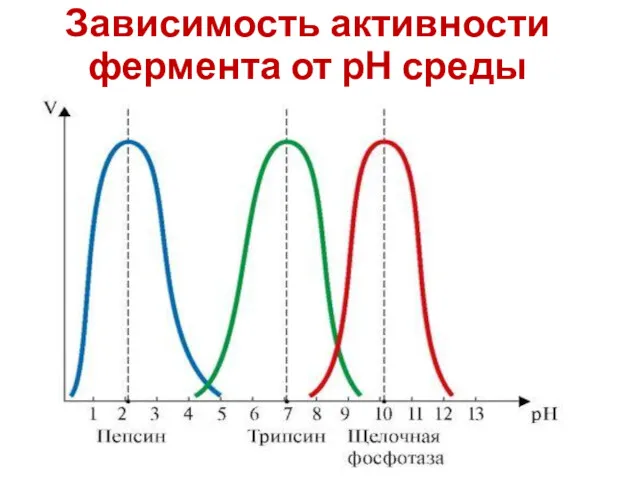
- 21. Зависимость активности фермента от рН среды
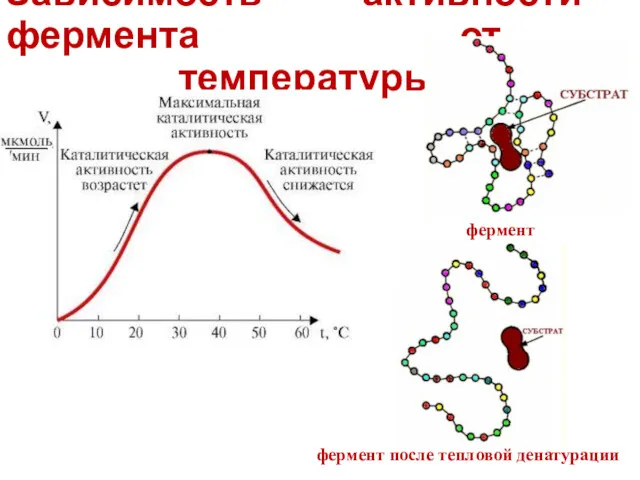
- 22. Зависимость активности фермента от температуры фермент фермент после тепловой денатурации
- 23. Классификация ферментов Согласно современной классификации, выделяют шесть классов ферментов: оксидоредуктазы; трансферазы; гидролазы; лиазы; изомеразы; лигазы.
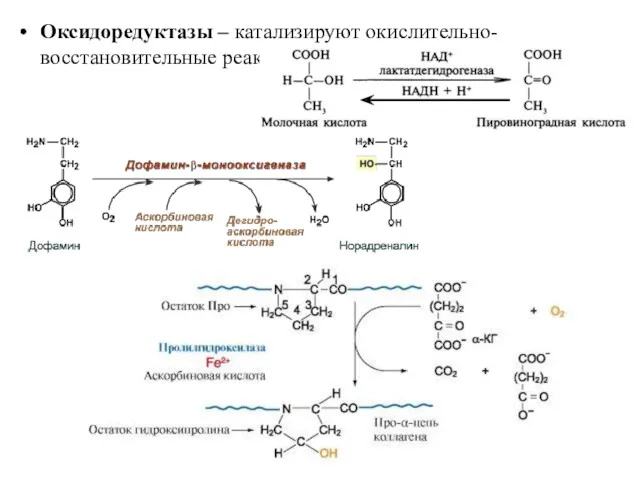
- 24. Оксидоредуктазы – катализируют окислительно-восстановительные реакции:
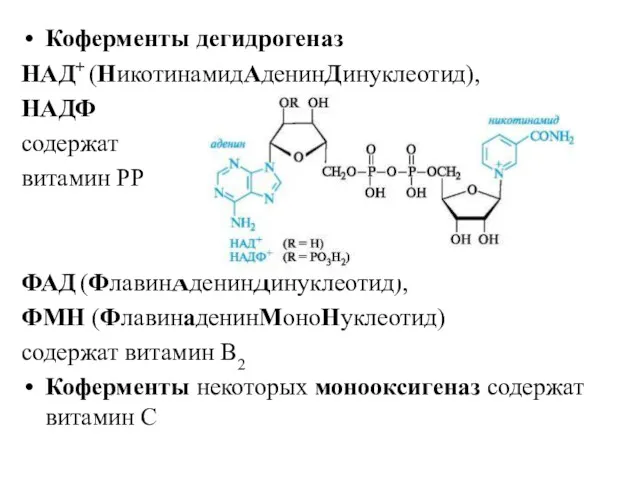
- 25. Коферменты дегидрогеназ НАД+ (НикотинамидАденинДинуклеотид), НАДФ содержат витамин РР ФАД (ФлавинАденинДинуклеотид), ФМН (ФлавинаденинМоноНуклеотид) содержат витамин В2 Коферменты
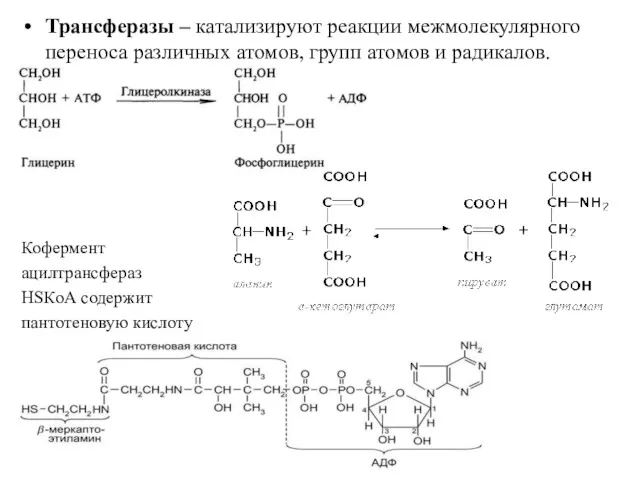
- 26. Трансферазы – катализируют реакции межмолекулярного переноса различных атомов, групп атомов и радикалов. Кофермент ацилтрансфераз HSКоА содержит
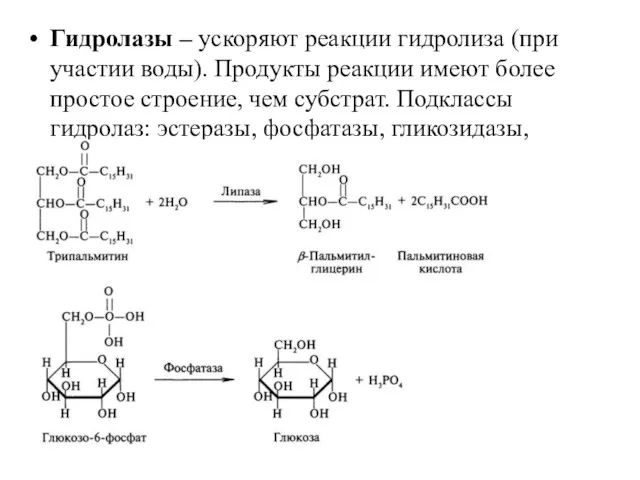
- 27. Гидролазы – ускоряют реакции гидролиза (при участии воды). Продукты реакции имеют более простое строение, чем субстрат.
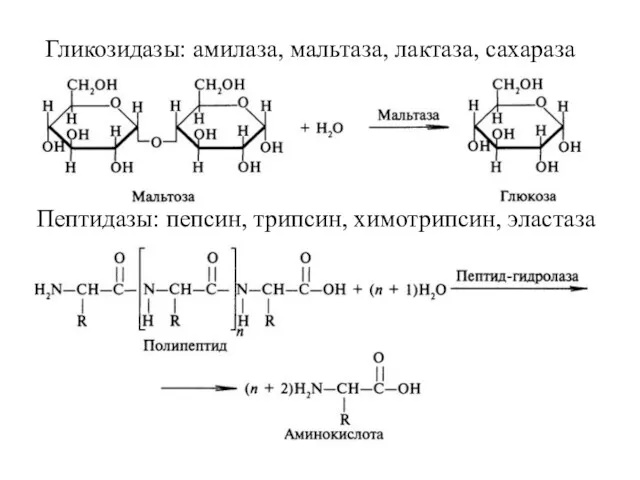
- 28. Гликозидазы: амилаза, мальтаза, лактаза, сахараза Пептидазы: пепсин, трипсин, химотрипсин, эластаза
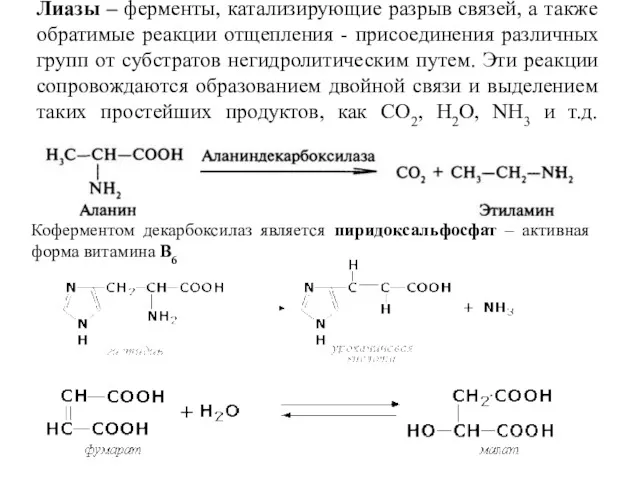
- 29. Лиазы – ферменты, катализирующие разрыв связей, а также обратимые реакции отщепления - присоединения различных групп от
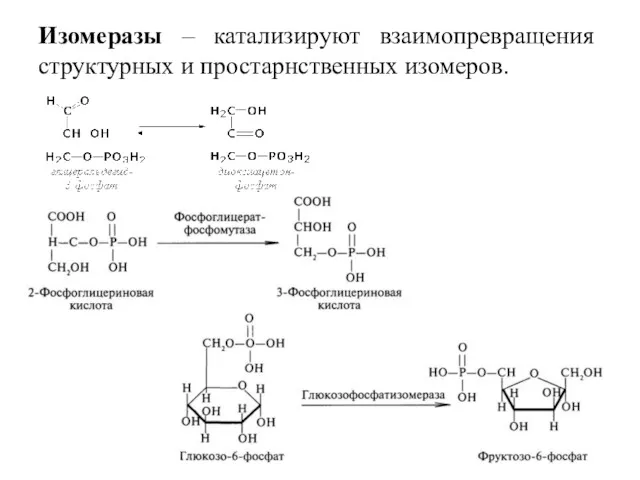
- 30. Изомеразы – катализируют взаимопревращения структурных и простарнственных изомеров.
- 31. Лигазы (синтетазы) – катализируют синтез органических веществ из двух исходных молекул с использованием энергии распада АТФ
- 33. Скачать презентацию










 Селекция и её достижения
Селекция и её достижения Живой мир Австралии
Живой мир Австралии Ведение в вирусологию
Ведение в вирусологию Red Wolf
Red Wolf Обмен белков-3
Обмен белков-3 Строение стебля
Строение стебля Морфология микроорганизмов. Прокариоты
Морфология микроорганизмов. Прокариоты Удивительные деревья
Удивительные деревья Системы органов. Опорно-двигательная. Строение кости. Скелет
Системы органов. Опорно-двигательная. Строение кости. Скелет Основные законы Менделя
Основные законы Менделя Красная книга
Красная книга Адаптация и здоровье.Психотипы человека и их склонность к возникновению заболеваний
Адаптация и здоровье.Психотипы человека и их склонность к возникновению заболеваний Класс Пресмыкающиеся, или рептилии
Класс Пресмыкающиеся, или рептилии Живая и неживая природа
Живая и неживая природа Слюнные железы
Слюнные железы Поленика арктическая и земляника садовая
Поленика арктическая и земляника садовая Цитотехнологія. Клітинна інженерія
Цитотехнологія. Клітинна інженерія Реализация системно-деятельностного подхода в рамках внеурочной деятельности
Реализация системно-деятельностного подхода в рамках внеурочной деятельности Зимующие птицы Башкирии
Зимующие птицы Башкирии Презентация по биологии Мхи, папоротники, хвощи и плауны для 6 класса.
Презентация по биологии Мхи, папоротники, хвощи и плауны для 6 класса. Отряд пресмыкающихся. Черепахи
Отряд пресмыкающихся. Черепахи Социальная психофизиология. Эволюционный путь генеза социальных отношений в сообществах живых организмов
Социальная психофизиология. Эволюционный путь генеза социальных отношений в сообществах живых организмов Что общего у разных растений
Что общего у разных растений Соотношение врожденного и приобретенного в поведении
Соотношение врожденного и приобретенного в поведении Dinoflagellates
Dinoflagellates Сцепленное наследование генов
Сцепленное наследование генов Потенциал действия
Потенциал действия Молекулярные основы наследственности
Молекулярные основы наследственности