Содержание
- 2. Современное представление О стволовых клетках много говорят На стволовые клетки надеются Стволовые клетки спасают жизни Стволовые
- 3. Зачем они нужны? Basic research – определение механизмов/ цепочек событий происходящих при развитии человека. Понимание молекулярных
- 4. Зачем они нужны? Доклинические исследования – стволовые клетки могут позволить создать новые модели для тестирования лекарств
- 5. Зачем они нужны? Клеточная терапия: Регенеративная терапия таких заболеваний как: болезни Паркинсона, Альцгеймера, Боковой амиотрофический склероз,
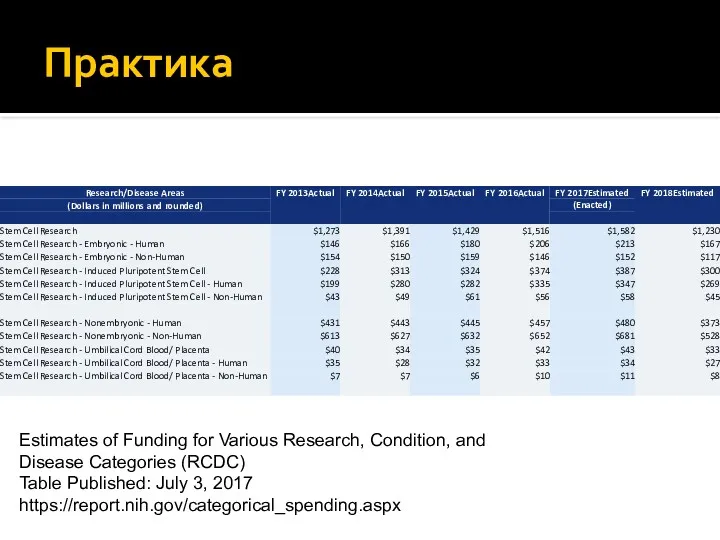
- 6. Практика Estimates of Funding for Various Research, Condition, and Disease Categories (RCDC) Table Published: July 3,
- 7. Практика USD (millions) from the Stem Cell Summit 2007 Fact Sheet: http://www.stemcellsummit.com/2007/stem-cell-fact-sheet.pdf
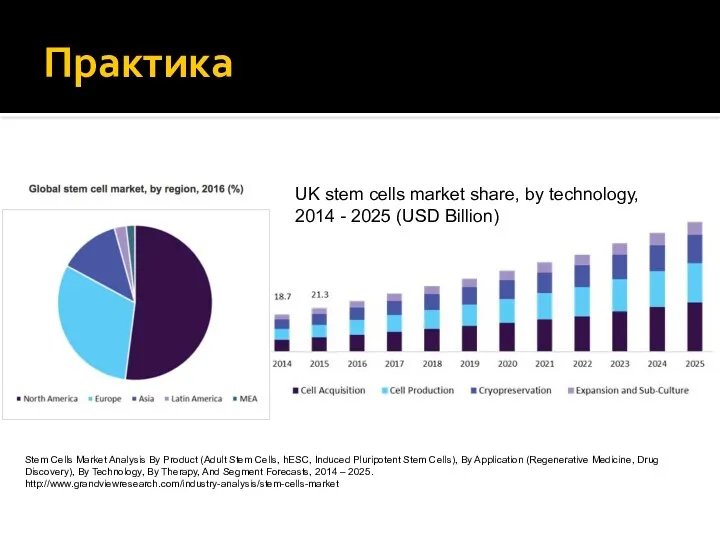
- 8. Практика UK stem cells market share, by technology, 2014 - 2025 (USD Billion) Stem Cells Market
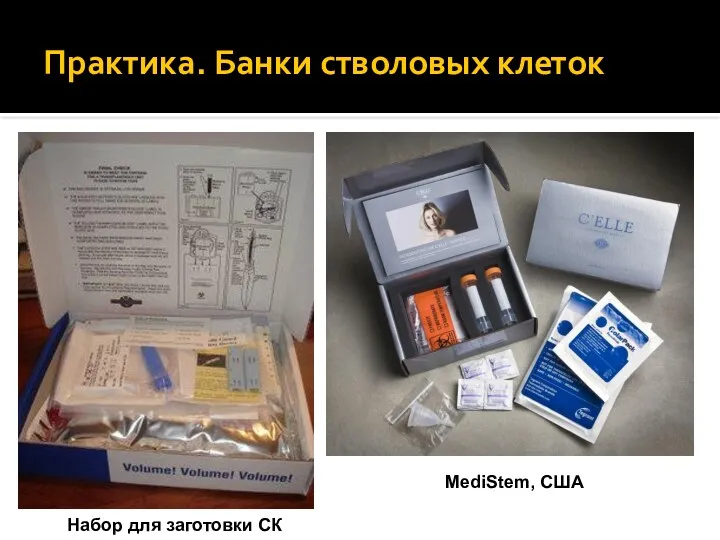
- 9. Практика. Банки стволовых клеток БиоБанк – персональное/неперсональное хранилище образцов СК: Банки пуповинной крови Банки ККМ
- 10. Практика. Банки стволовых клеток MediStem, США Набор для заготовки СК
- 11. Противоречие
- 12. S Korea scientist on fraud charge The South Korean cloning scientist who faked his stem cell
- 13. Успех
- 14. Успех
- 15. Тканевая инженерия Т.И. – раздел биотехнологии, основной целью которого является разработка методов создания тканеподобных структур. Продукты
- 16. Историческая справка 1963 г. – Till и McCulloch доказательство существования ГСК 1968 г. – первая неродственная
- 17. Стволовые клетки
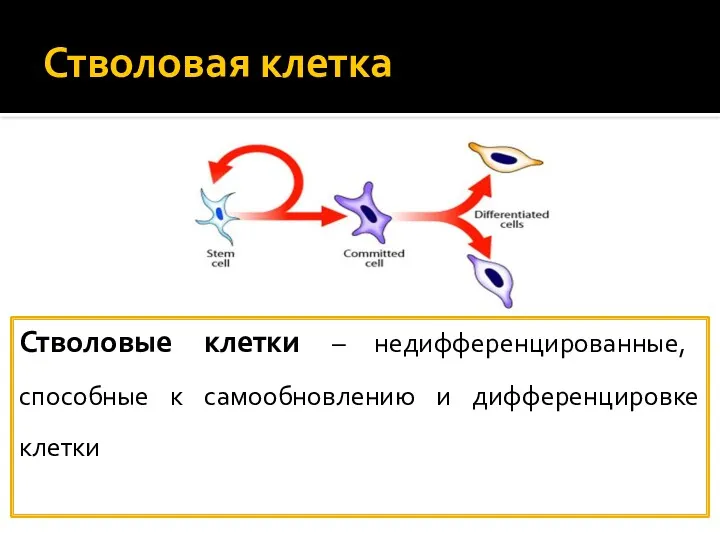
- 18. Стволовая клетка Стволовые клетки – недифференцированные, способные к самообновлению и дифференцировке клетки
- 19. Основные типы
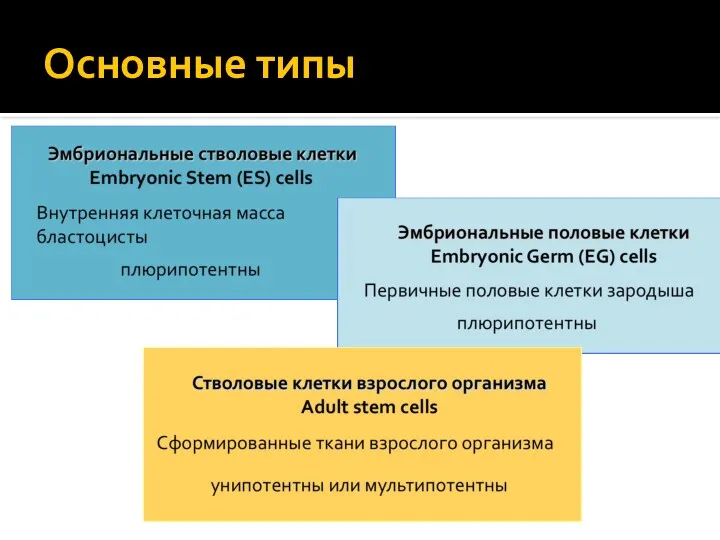
- 20. Основные типы
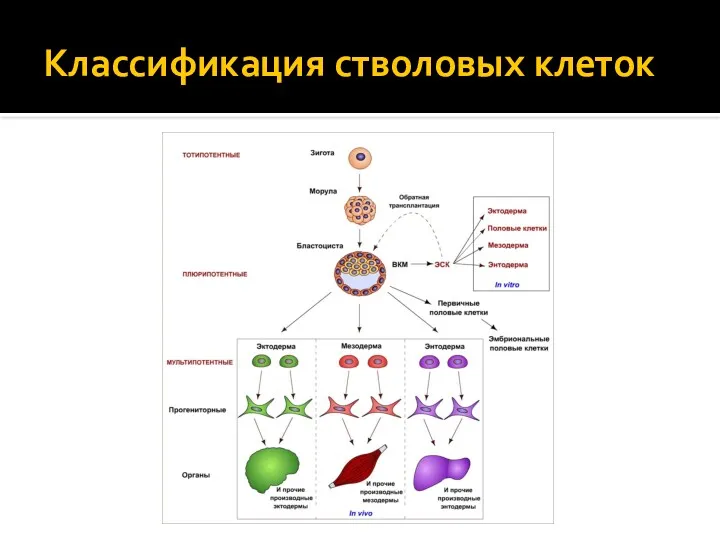
- 21. Классификация стволовых клеток
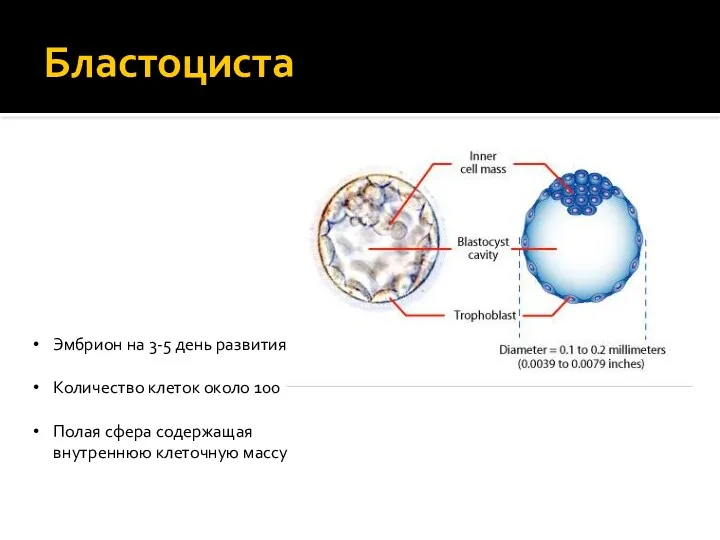
- 22. Бластоциста Эмбрион на 3-5 день развития Количество клеток около 100 Полая сфера содержащая внутреннюю клеточную массу
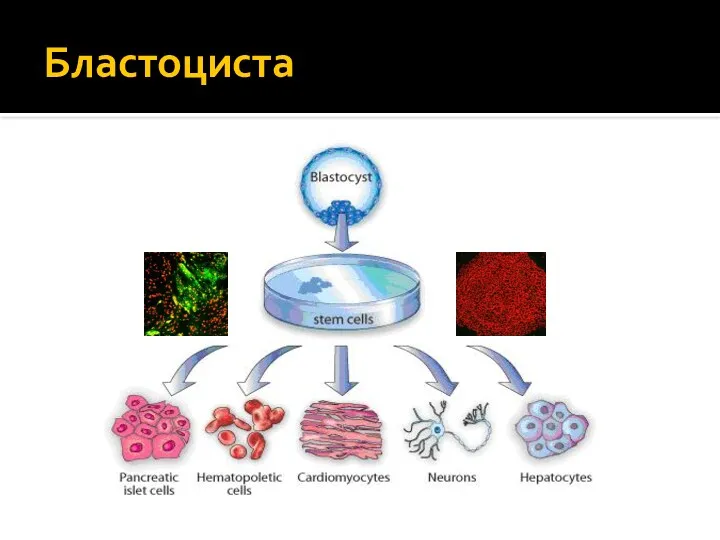
- 23. Бластоциста
- 24. Свойства недифференцированных эмбриональных стволовых клеток 1855: Rudolf Virchow высказал гипотезу об эмбриональном происхождении опухолей На основании
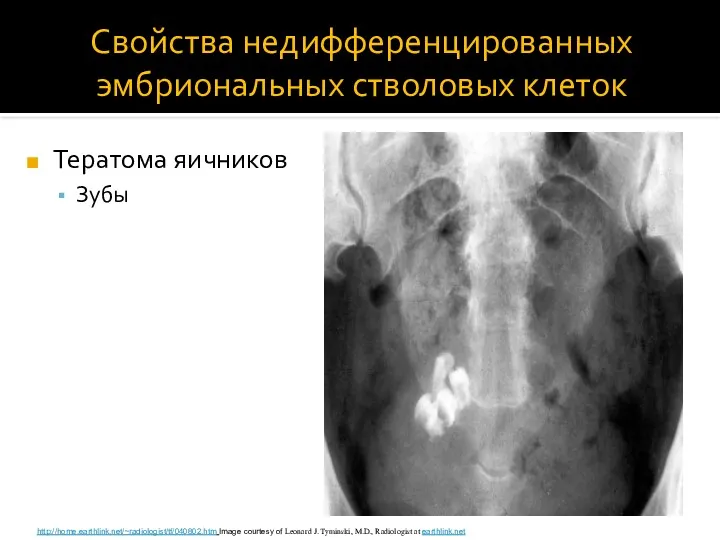
- 25. Свойства недифференцированных эмбриональных стволовых клеток Тератома яичников Зубы http://home.earthlink.net/~radiologist/tf/040802.htm Image courtesy of Leonard J. Tyminski, M.D.,
- 26. Обама разрешил исследования стволовых клеток эмбриона человека Администрация Обамы профинансирует стволовые клетки "Как верующий человек, я
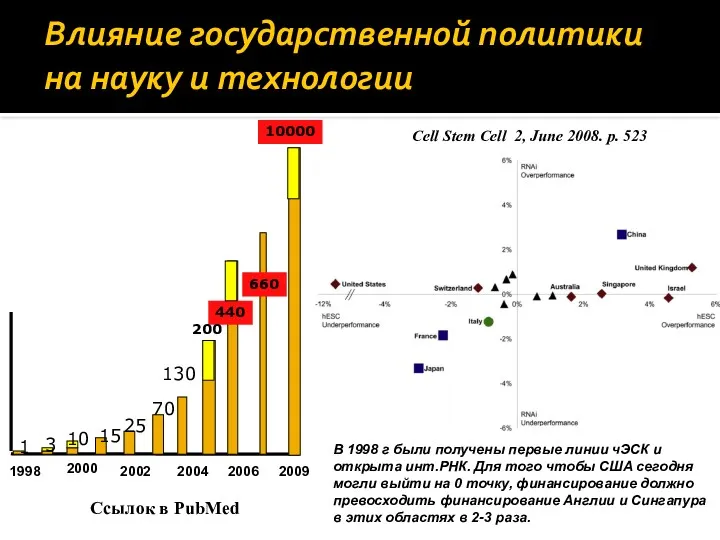
- 27. Влияние государственной политики на науку и технологии 1998 2002 2004 2006 2000 1 15 10 3
- 28. Ислам не против ЭСК Иран Иран достиг значительного прогресса в доклинических исследованиях. Входит в топ 10
- 29. Эмбриональные стволовые клетки 1981 г. – получены линии ES клеток мыши (Martin 1981, PNAS 78:7634-38; Evans
- 30. Эмбриональные стволовые клетки 1987 г. – изменили геном ES клетки путем гомологической рекомбинации (Thomas KR and
- 31. Свойства недифференцированных эмбриональных стволовых клеток
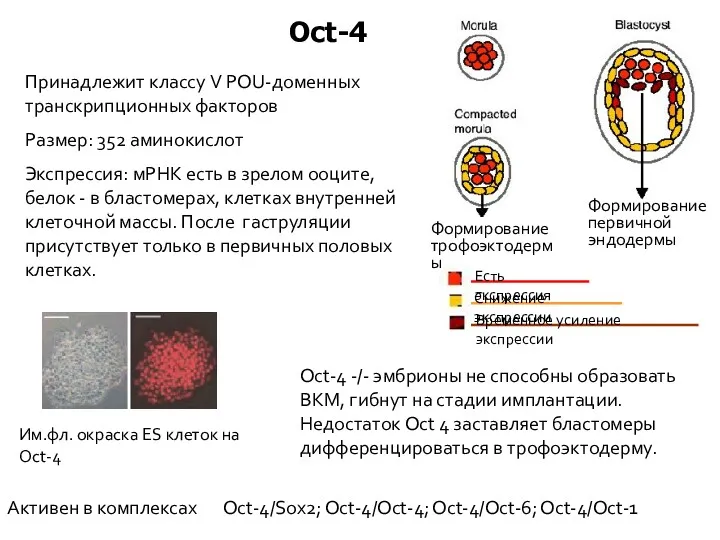
- 32. Oct-4 Принадлежит классу V POU-доменных транскрипционных факторов Размер: 352 аминокислот Экспрессия: мРНК есть в зрелом ооците,
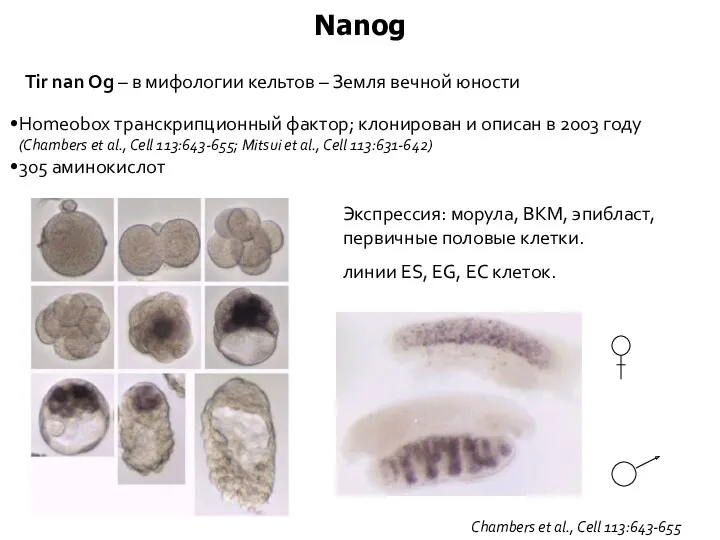
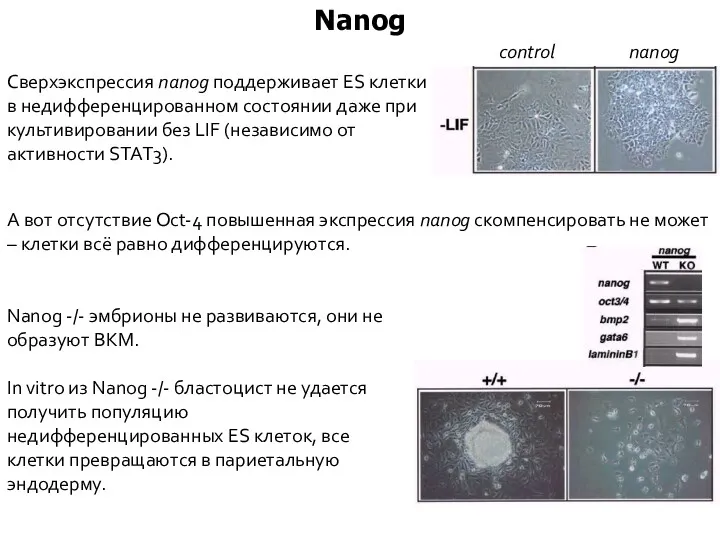
- 33. Nanog Homeobox транскрипционный фактор; клонирован и описан в 2003 году (Chambers et al., Cell 113:643-655; Mitsui
- 34. Nanog А вот отсутствие Oct-4 повышенная экспрессия nanog скомпенсировать не может – клетки всё равно дифференцируются.
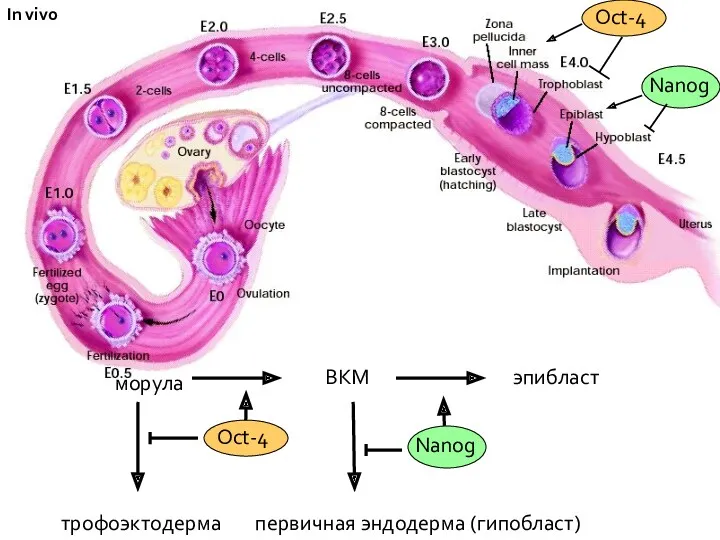
- 35. ВКМ эпибласт первичная эндодерма (гипобласт) трофоэктодерма морула In vivo
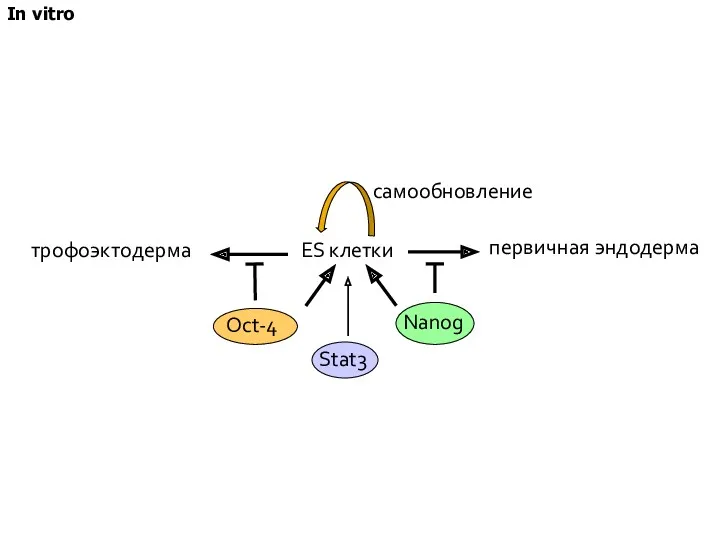
- 36. ES клетки первичная эндодерма трофоэктодерма Oct-4 Nanog самообновление Stat3 In vitro
- 38. Скачать презентацию
















 Устройство речевого аппарата
Устройство речевого аппарата Власне сполучна тканина
Власне сполучна тканина Внешнее строение листа. 6 класс
Внешнее строение листа. 6 класс Морфология прокариот
Морфология прокариот Різноманітність тварин у природі. Звірі. Урок №46. Я досліджую світ
Різноманітність тварин у природі. Звірі. Урок №46. Я досліджую світ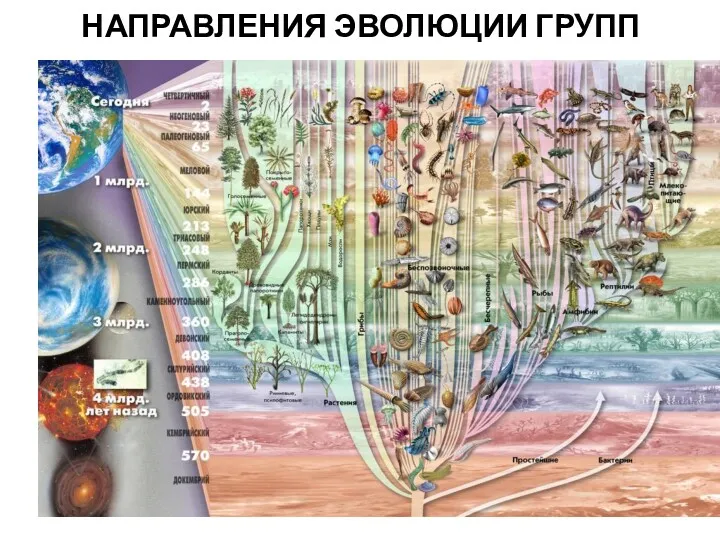 Направления и формы эволюции групп. Лекция 2
Направления и формы эволюции групп. Лекция 2 Пори року. Дні тижня. Доба. Урок №97. Я досліджую світ
Пори року. Дні тижня. Доба. Урок №97. Я досліджую світ Микробы в жизни растений
Микробы в жизни растений Algae. Division: Chlorophyta and Charоphyta
Algae. Division: Chlorophyta and Charоphyta Лимфа жүйесінің құрылысы
Лимфа жүйесінің құрылысы Состав и свойства помидоров
Состав и свойства помидоров Половое размножение
Половое размножение Морфология нервной системы. Часть 1
Морфология нервной системы. Часть 1 Полезные и лекарственные растения Зауралья
Полезные и лекарственные растения Зауралья Гормональная регуляция метаболических процессов
Гормональная регуляция метаболических процессов Плауны. Хвощи. Папоротники
Плауны. Хвощи. Папоротники Генотоксиканты. Классификации мутагенов. Генотоксические поражения и болезни
Генотоксиканты. Классификации мутагенов. Генотоксические поражения и болезни Все о чае
Все о чае КЛЕТКА
КЛЕТКА Bryophyta – моховидные или мхи
Bryophyta – моховидные или мхи Програмированный тест по теме Биогеоценоз
Програмированный тест по теме Биогеоценоз Продуктивность кукурузы в зависимости от приемов выращивания в центральной зоне Краснодарского края
Продуктивность кукурузы в зависимости от приемов выращивания в центральной зоне Краснодарского края Волчеягодник обыкновенный
Волчеягодник обыкновенный Основные методы селекции
Основные методы селекции Жорғалаушылардың сыртқы, ішкі құрылысы мен тіршілік
Жорғалаушылардың сыртқы, ішкі құрылысы мен тіршілік Cladocera
Cladocera Пищеварение в ротовой полости и желудке
Пищеварение в ротовой полости и желудке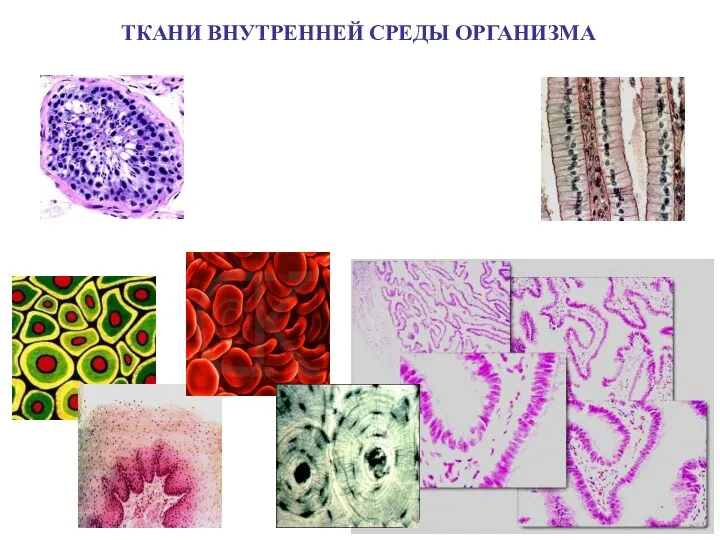 Ткани внутренней среды организма. Костная ткань
Ткани внутренней среды организма. Костная ткань