Содержание
- 2. История кафедры
- 3. История кафедры
- 4. История кафедры
- 5. История кафедры
- 6. История кафедры
- 7. История кафедры
- 8. История кафедры
- 9. История кафедры
- 10. История кафедры
- 11. История кафедры
- 12. История кафедры
- 14. Трудности изучения биохимии Объективные: Знание предметов, на которых базируется изучение дисциплины (общая и органическая химия, физическая
- 15. БИОЛОГИЧЕСКАЯ ХИМИЯ – наука о химическом составе живой ткани и химических процессах, происходящих в живом организме
- 16. Предмет изучения биохимии – живая ткань, познание ее сущности, т.е. качественного отличия живого от неживого.
- 17. Задачи изучения биохимии Стратегическая задача – выяснение вопроса: каким образом система, состоящая из неживых биомолекул приобретает
- 18. В зависимости от подхода к изучению живой ткани биохимия делится на 3 раздела (деление условное): Статическая
- 19. Методы исследования в биохимии Общая их черта – исследуемое химическое соединение или их набор вводится в
- 20. Общие особенности живой ткани Сложный и высокий уровень организации (в состав одноклеточных организмов входит до 5
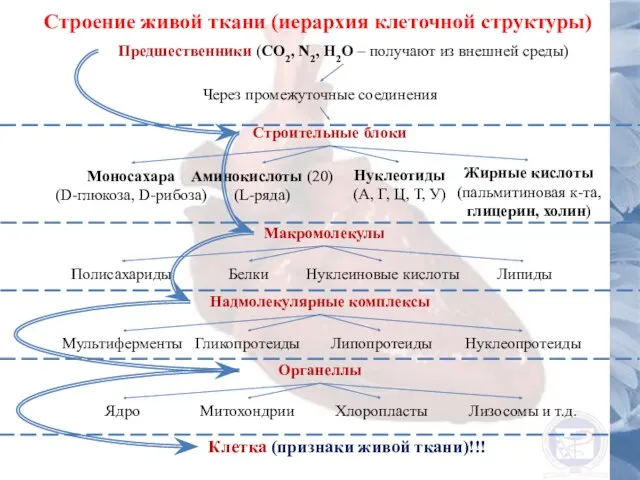
- 21. Строение живой ткани (иерархия клеточной структуры) Предшественники (CO2, N2, H2O – получают из внешней среды) Через
- 22. БЕЛКИ (протеины- «первый, главный» - лат.) – высокомолекулярные соединения, состоящие из L-аминокислот, соединенных пептидными связями. Первым
- 23. Бесконечное разнообразие структуры и вместе с тем высокая видовая специфичность (предопределяет многообразие организмов); Крайнее многообразие физических
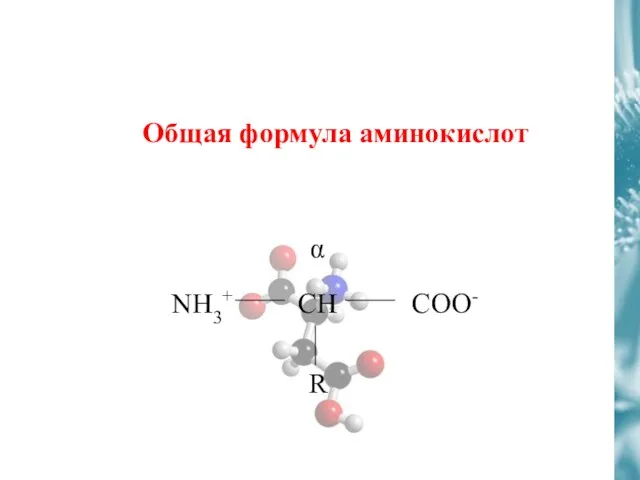
- 24. Общая формула аминокислот
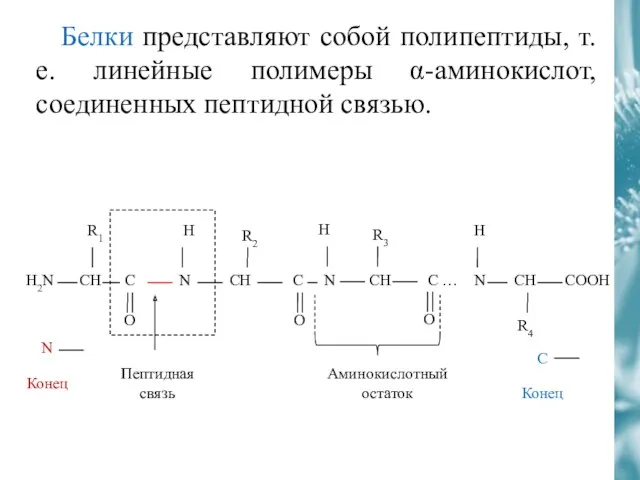
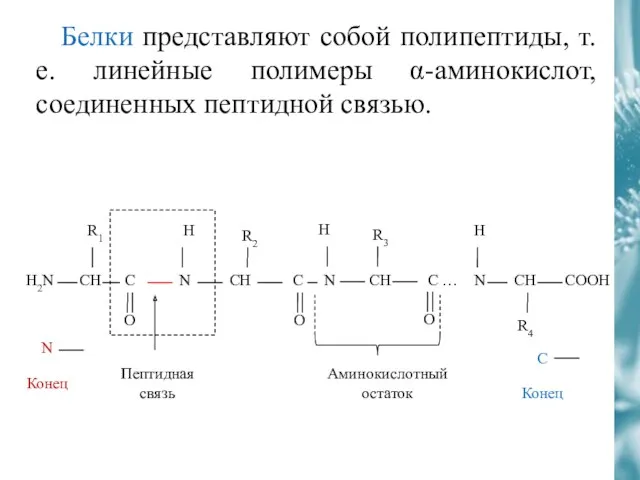
- 25. Белки представляют собой полипептиды, т.е. линейные полимеры α-аминокислот, соединенных пептидной связью. Пептидная связь Аминокислотный остаток
- 26. Закономерности строения полипептидной цепи Остов полипептидной цепи составляет монотонно чередующиеся химические группы -NH-CH-CO-, окруженные разнообразными по
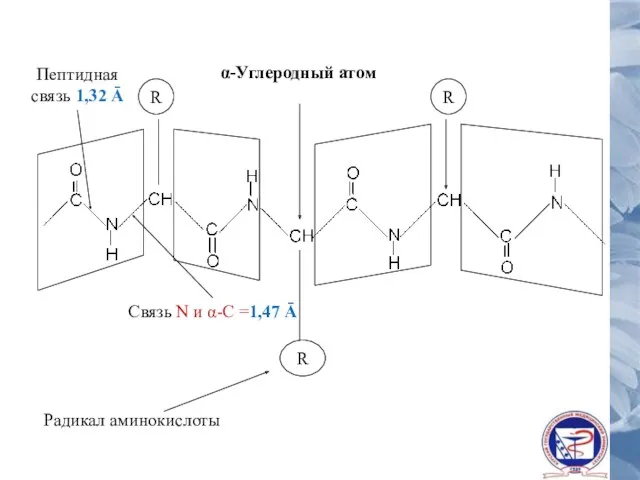
- 27. Радикал аминокислоты α-Углеродный атом R R R Пептидная связь 1,32 Ā Связь N и α-С =1,47
- 28. Уровни организации белковой молекулы Первичная структура белков характеризует линейную последовательность аминокислотных остатков в полипептидной цепи. Закономерности
- 29. Уровни организации белковой молекулы Закономерности первичной структуры белка Первичная структура определена генетически (детерминированность), но точность воспроизведения
- 30. Белки представляют собой полипептиды, т.е. линейные полимеры α-аминокислот, соединенных пептидной связью. Пептидная связь Аминокислотный остаток
- 31. Конформация полипептидной цепи – пространственная трехмерная структура, образующаяся при взаимодействии ее функциональных групп и радикалов аминокислот
- 32. Вторичная структура белков – конформация (пространственная трехмерная структура), образующаяся в результате взаимодействия между функциональными группами, входящими
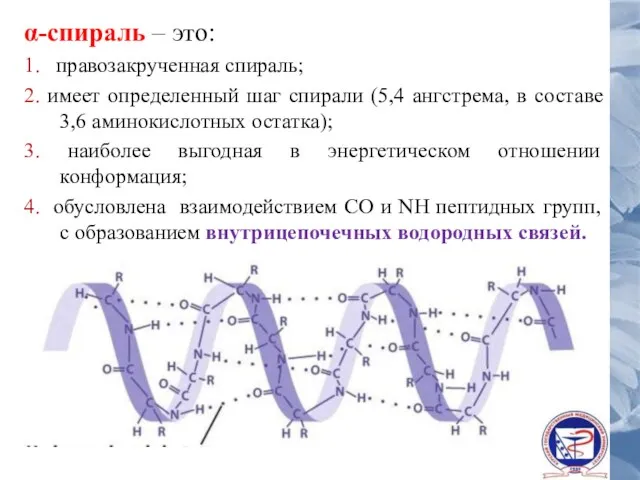
- 33. α-спираль – это: 1. правозакрученная спираль; 2. имеет определенный шаг спирали (5,4 ангстрема, в составе 3,6
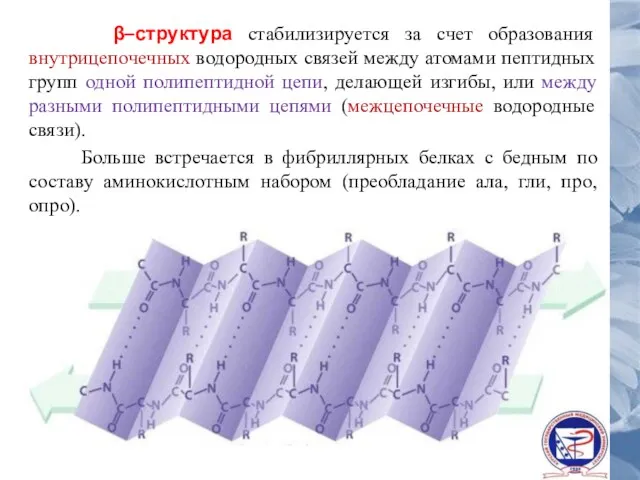
- 34. β–структура стабилизируется за счет образования внутрицепочечных водородных связей между атомами пептидных групп одной полипептидной цепи, делающей
- 35. Полипептидные цепи или их части могут формировать параллельные или антипараллельные β-структуры. В первом случае N- и
- 36. Степень спирализации у различных белков различна (гемоглобин – 75% спирализация, пепсин – 28%, химотрипсин – 11%
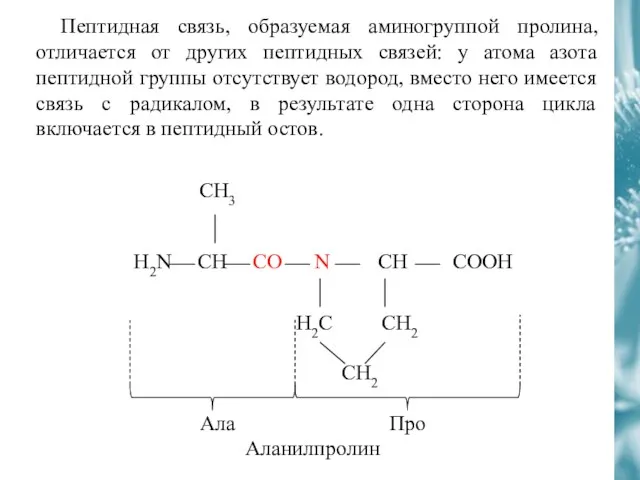
- 37. Пептидная связь, образуемая аминогруппой пролина, отличается от других пептидных связей: у атома азота пептидной группы отсутствует
- 38. Третичная структура белков – конформация, образующаяся за счет взаимодействия между радикалами аминокислот, которые могут находиться на
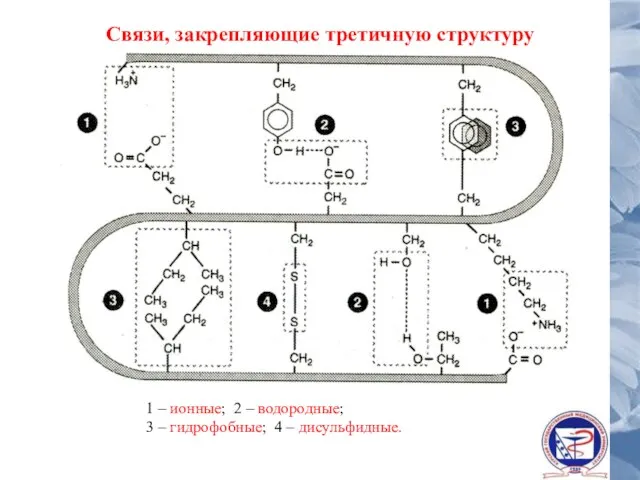
- 39. Связи, закрепляющие третичную структуру 1 – ионные; 2 – водородные; 3 – гидрофобные; 4 – дисульфидные.
- 40. Третичная структура имеет для белков следующие закономерности: Укладка полипептидной цепи очень плотная; Все гидрофильные (полярные) радикалы
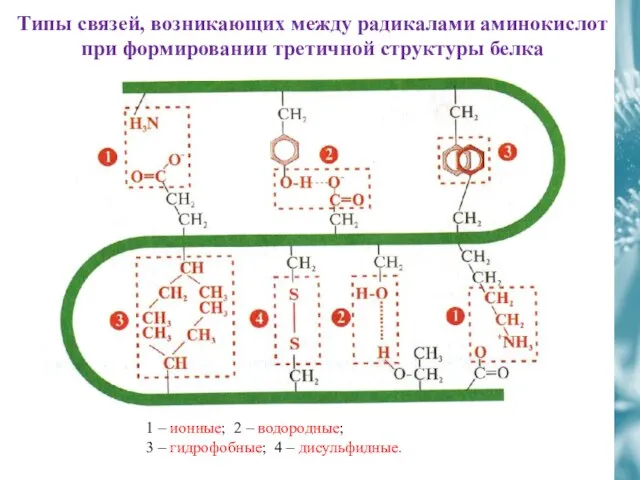
- 41. Типы связей, возникающих между радикалами аминокислот при формировании третичной структуры белка 1 – ионные; 2 –
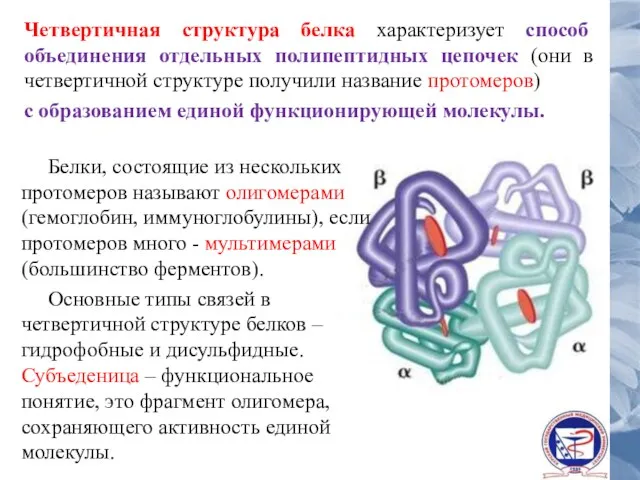
- 42. Четвертичная структура белка характеризует способ объединения отдельных полипептидных цепочек (они в четвертичной структуре получили название протомеров)
- 43. Образование конформации белка – важнейший биологический процесс, т.к. от этого зависит его функция. Процесс ее образования
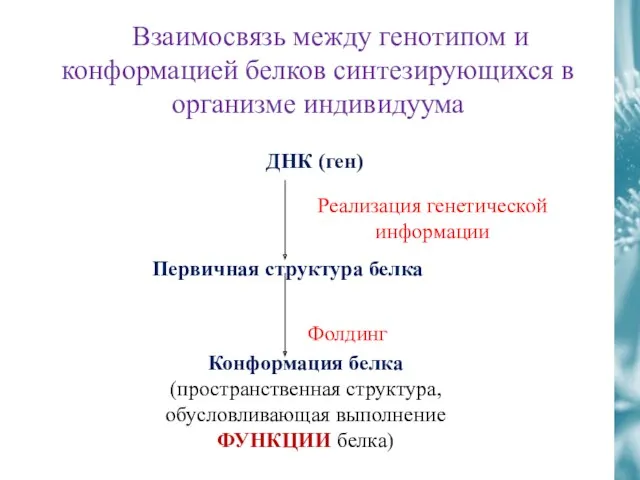
- 44. Взаимосвязь между генотипом и конформацией белков синтезирующихся в организме индивидуума ДНК (ген) Первичная структура белка Реализация
- 45. В процессе синтеза полипептидных белков, транспорта их через мембраны, сборке олиго и мультимеров могут возникать промежуточные
- 46. При нарушении фолдинга белков (возможно это связано с нарушение синтеза шаперонов или усилением активности протеаз) возникают
- 47. 1. В первую категорию включены белки, в которых имеются только α-спирали, например миоглобин и гемоглобин. Вторичная
- 48. По наличию α-спиралей β-структур глобулярные белки могут быть разделены на четыре категории: 2. Во вторую категорию
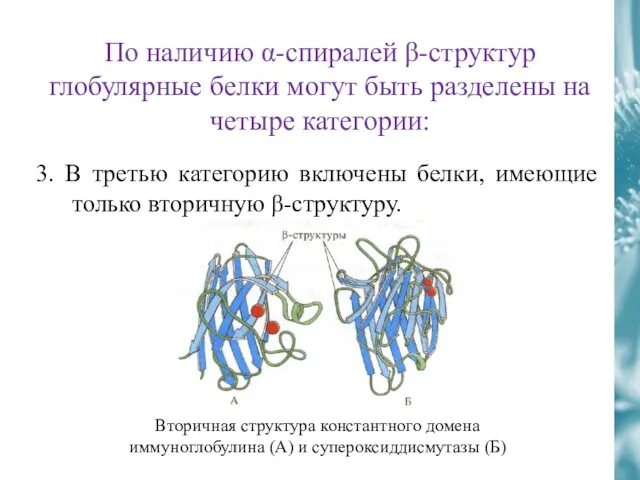
- 49. По наличию α-спиралей β-структур глобулярные белки могут быть разделены на четыре категории: 3. В третью категорию
- 50. По наличию α-спиралей β-структур глобулярные белки могут быть разделены на четыре категории: 4. В четвертую категорию
- 51. Потеря нативной конформации, сопровождающаяся утратой специфической функции белка называется денатурацией белков (необратимая, обратимая). При этом первичная
- 53. Скачать презентацию




































 Происхождение митохондрий
Происхождение митохондрий Практична робота №1. Виявлення прикладів пристосування до способу життя у комах
Практична робота №1. Виявлення прикладів пристосування до способу життя у комах Физиология пищеварения
Физиология пищеварения Дифференцировка зародышевых листов. Гистогенез. Органогенез. Внезародышевые органы
Дифференцировка зародышевых листов. Гистогенез. Органогенез. Внезародышевые органы “Галерея кімнатних рослин”. Орхідеї. Догляд за ними
“Галерея кімнатних рослин”. Орхідеї. Догляд за ними Водоросли
Водоросли Сулы ерітінділер. Тірі ағза сұйықтықтарындағы тепетеңдік
Сулы ерітінділер. Тірі ағза сұйықтықтарындағы тепетеңдік Лекарственные растения в домашней аптечке (2 класс)
Лекарственные растения в домашней аптечке (2 класс) Микроорганизмы в геохимических круговоротах. Вводная лекция
Микроорганизмы в геохимических круговоротах. Вводная лекция Интерактивный кроссворд Плодово-ягодные розоцветные
Интерактивный кроссворд Плодово-ягодные розоцветные Бурые и красные водоросли как объекты биотехнологии
Бурые и красные водоросли как объекты биотехнологии Класс однодольные. Семейство лилейные
Класс однодольные. Семейство лилейные Деревья и кустарники
Деревья и кустарники 20181104_kletochnaya_teoriya_t.shvanna
20181104_kletochnaya_teoriya_t.shvanna Водоросли
Водоросли Надорганизменный уровень биомониторинга
Надорганизменный уровень биомониторинга Эволюция отношения человека к животным
Эволюция отношения человека к животным Обмен веществ и энергии. Метаболизм
Обмен веществ и энергии. Метаболизм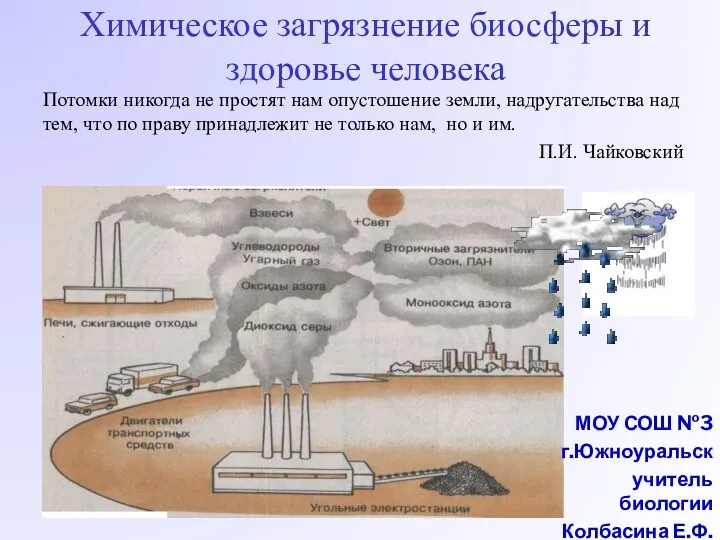 Химическое загрязнение биосферы и здоровье человека
Химическое загрязнение биосферы и здоровье человека Информационная биология. Семантическая и прагматическая информация. (Тема 5)
Информационная биология. Семантическая и прагматическая информация. (Тема 5) Бактерии, грибы, растения. 6 класс
Бактерии, грибы, растения. 6 класс Neuropsychomodulating action of microbiota
Neuropsychomodulating action of microbiota Взаимодействие неаллельных генов. Комплементарность, эпистаз, полимерия
Взаимодействие неаллельных генов. Комплементарность, эпистаз, полимерия Сосна – зелёный символ Кунгура
Сосна – зелёный символ Кунгура Красная книга России
Красная книга России Древесная лягушка
Древесная лягушка Популяционная генетика
Популяционная генетика Виды растительных тканей
Виды растительных тканей