Содержание
- 3. Хроматография как метод разделения, идентификации и определения В основе хроматографии лежит процесс распределения разделяемых компонентов между
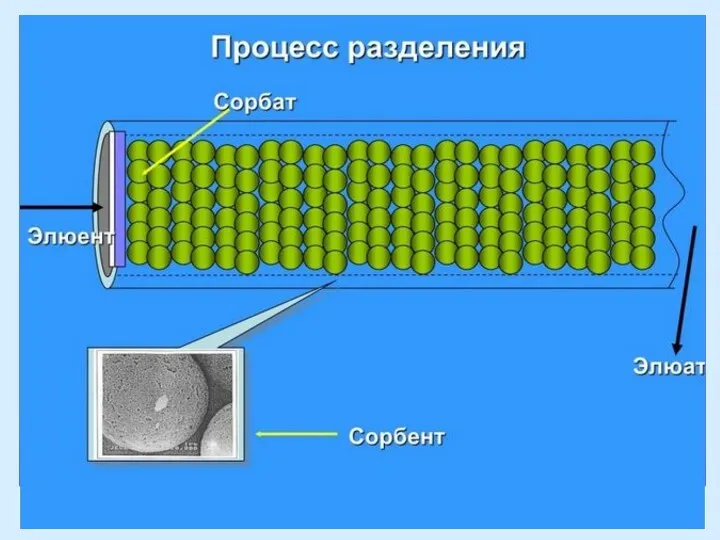
- 5. Сорбция - поглощение твёрдым телом либо жидкостью (сорбент) различных веществ из окружающей среды (сорбат). Процесс сорбции
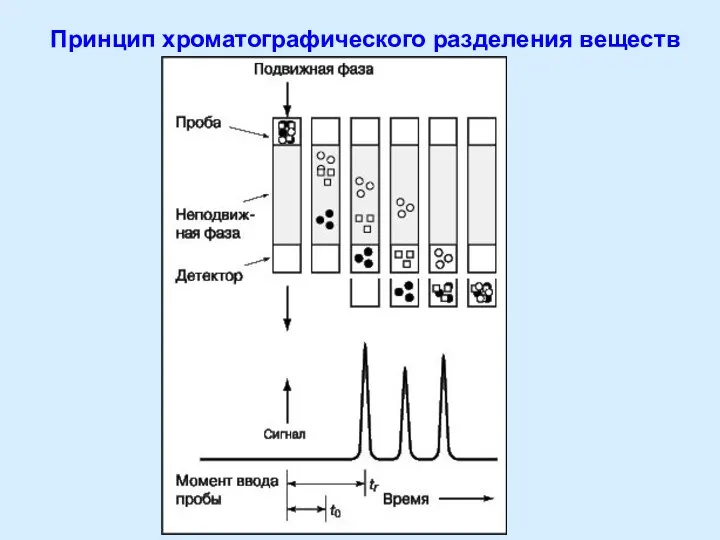
- 6. Принцип хроматографического разделения веществ
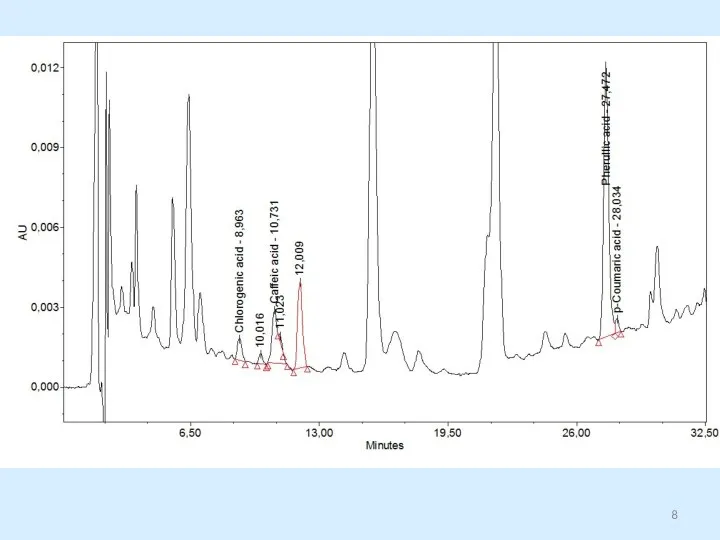
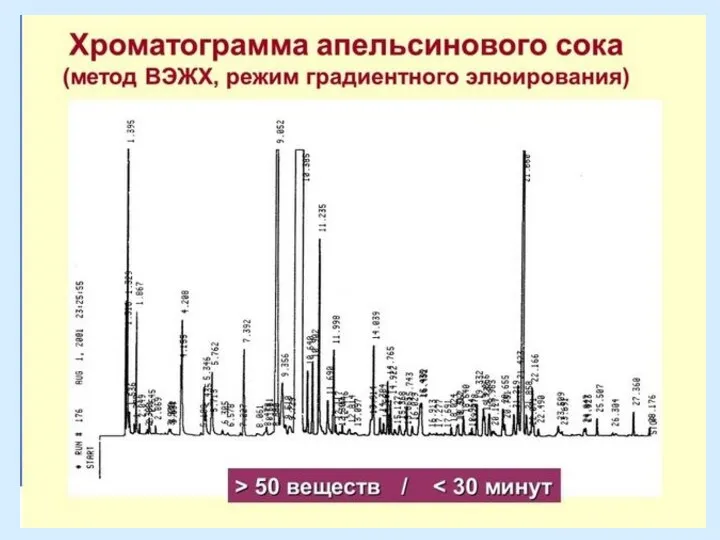
- 7. Хроматограмма - зависимость аналитического сигнала от времени или объема подвижной фазы. Внутренняя хроматограмма – распределение разделяемых
- 9. Экспериментальные данные, получаемые непосредственно из хроматограммы: Мертвое время (tm). Время удерживания инертного вещества, не сорбирующегося на
- 10. Исправленное время удерживания (tR’) Удерживаемый объем (VR ) где F (см3/с) ‑ объемная скорость потока газа-носителя
- 11. Пример 1. Скорость потока газа-носителя гелия составляет 20 мл/мин. Определить удерживаемый объем, исправленный удерживаемый объем и
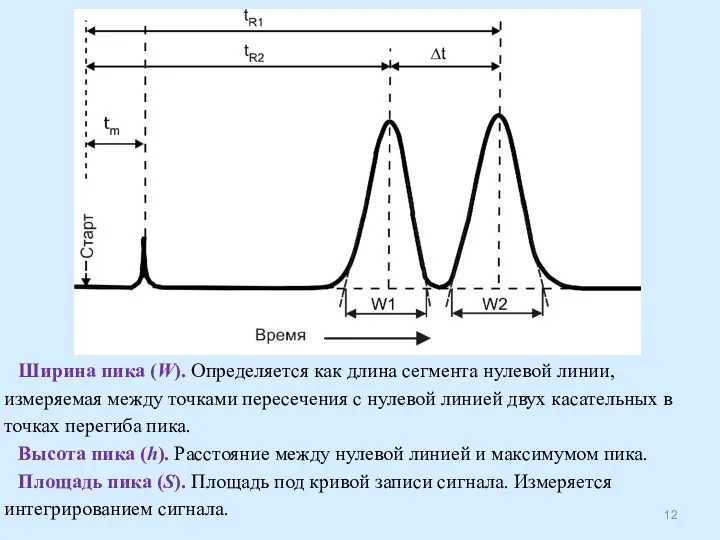
- 12. Ширина пика (W). Определяется как длина сегмента нулевой линии, измеряемая между точками пересечения с нулевой линией
- 13. Если условия выбраны правильно, то каждому из компонентов смеси соответствует отдельная хроматографическая зона на внутренней хроматограмме
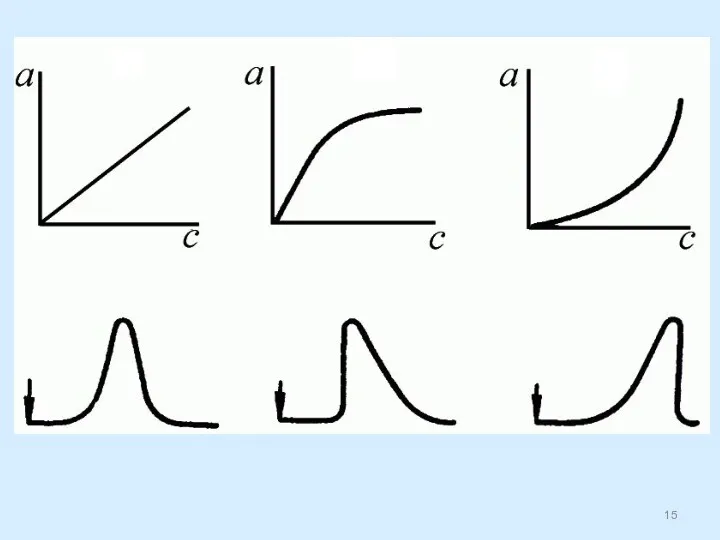
- 14. Теория хроматографического разделения Положение и вид хроматографических зон разделяемых веществ зависят от формы изотермы сорбции, скорости
- 16. Теория теоретических тарелок: 1) каждая хроматографическая колонка состоит из некоторого количества одинаковых по величине абстрактных узких
- 17. Количественной характеристикой хроматографической колонки являются: высота эквивалентная теоретической тарелке (H) и число теоретических тарелок (N). Чем
- 18. Пример 3. Длина хроматографической колонки составляет 2 м. Анализ смеси углеводородов проводился при трех различных линейных
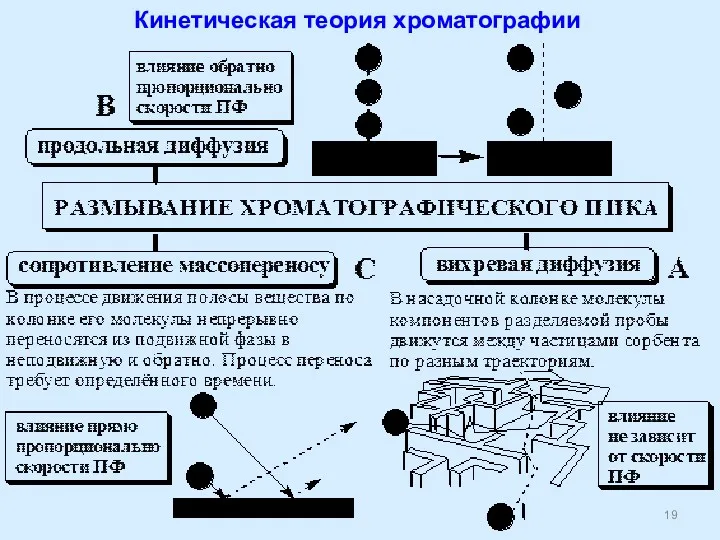
- 19. Кинетическая теория хроматографии
- 20. Суммарное влияние вихревой диффузии, продольной диффузии и сопротивления массопереносу на величину высоты эквивалентной теоретической тарелке описывается
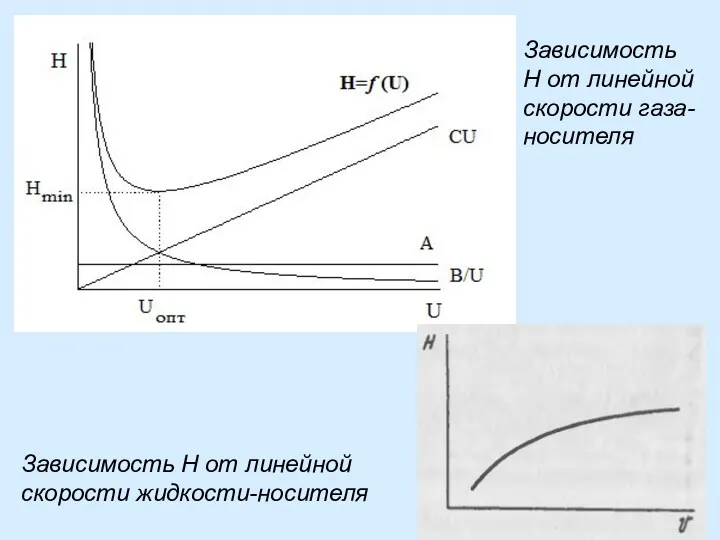
- 21. Зависимость H от линейной скорости жидкости-носителя Зависимость H от линейной скорости газа-носителя
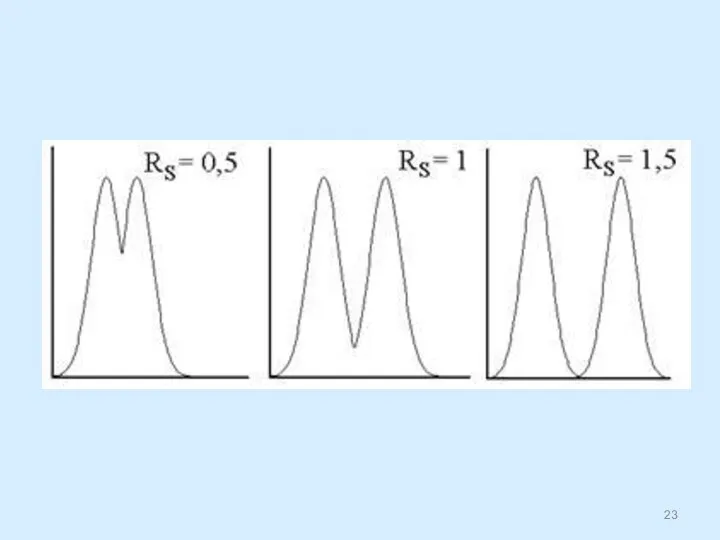
- 22. Эффективность разделения компонентов: Коэффициент разделения (α): Если α = 1, то разделение невозможно. Разрешение (RS) рассчитывается
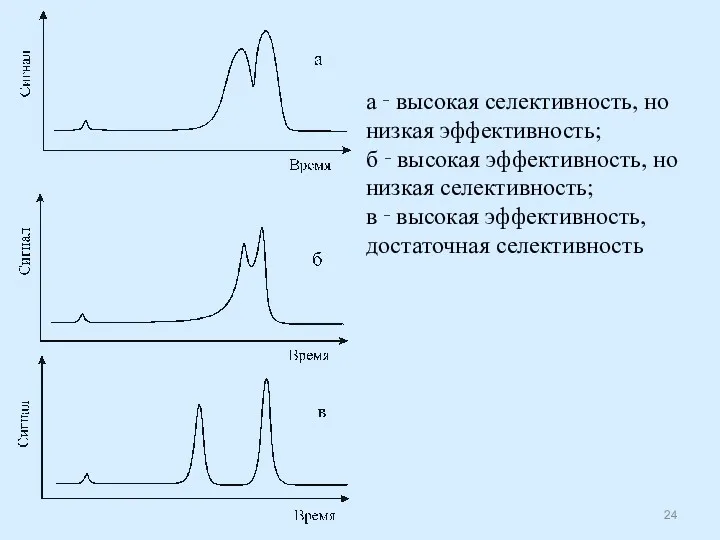
- 24. а ‑ высокая селективность, но низкая эффективность; б ‑ высокая эффективность, но низкая селективность; в ‑
- 25. Пример 4. Длина хроматографической колонки составляет 28,3 см, объем стационарной фазы ‑ 12,3 мл, подвижной фазы
- 27. Классификация хроматографических методов
- 28. Газо-жидкостная хроматография (ГЖХ) Используется для разделения «летучих» соединений, т.е. соединений с молекулярной массой до 500. Чувствительность
- 29. Газо-жидкостная хроматография (ГЖХ) Капиллярные колонки: внутренний диаметр 0.15-0.53 мм; длина 5-150 м.
- 30. Жидкостная колоночная хроматография Классическая: длина колонки 1-2 м, размер частиц сорбента >100 мкм. Метод высокоэффективной жидкостной
- 33. Скачать презентацию




















 Трехфазные цепи
Трехфазные цепи Электронный парамагнитный резонанс
Электронный парамагнитный резонанс Нанохимия и нанотехнологии. Спектральные методы исследования нанообъектов. (Лекция 4)
Нанохимия и нанотехнологии. Спектральные методы исследования нанообъектов. (Лекция 4) Дисперсия света. Интерференция. Применение интерференции. Физика. 11 класс
Дисперсия света. Интерференция. Применение интерференции. Физика. 11 класс Архимед күші. (7-сынып)
Архимед күші. (7-сынып) Размерная слесарная обработка деталей: шлифование ,опиливание. Зенкование, зенкерование, развертка
Размерная слесарная обработка деталей: шлифование ,опиливание. Зенкование, зенкерование, развертка Експлуатація навчального вертольота. Експлуатація трансмісії
Експлуатація навчального вертольота. Експлуатація трансмісії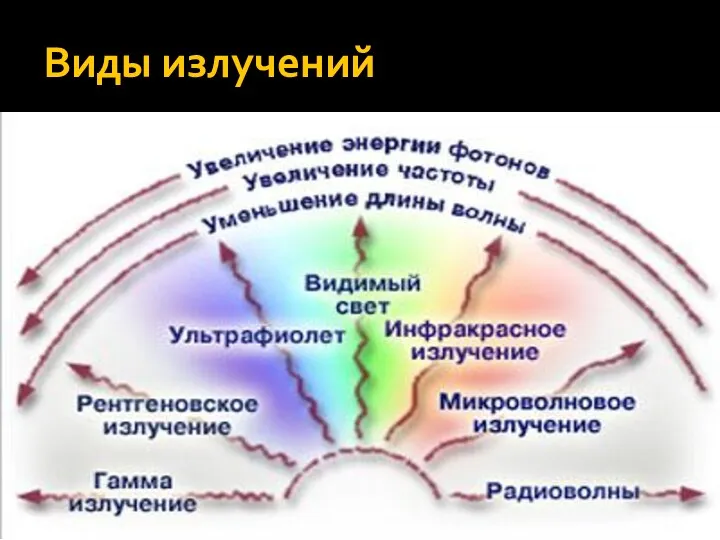 Виды излучений
Виды излучений Мастер-класс Ученик-исследователь
Мастер-класс Ученик-исследователь Решение задач Закон сохранения механической энергии
Решение задач Закон сохранения механической энергии Презентация к уроку 10 класс Положения МКТ
Презентация к уроку 10 класс Положения МКТ Звуковые волны
Звуковые волны Активізація пізнавальної діяльності учнів на уроках фізики шляхом використання проблемних ситуацій
Активізація пізнавальної діяльності учнів на уроках фізики шляхом використання проблемних ситуацій Импульсный сигнал
Импульсный сигнал использование метода мозгового штурма на уроках физики
использование метода мозгового штурма на уроках физики Всероссийский турнир юных физиков. Катание на диске
Всероссийский турнир юных физиков. Катание на диске Явление диффузии в жидкостях
Явление диффузии в жидкостях Проектирование участка диагностики и обслуживания ходовой части автомобиля
Проектирование участка диагностики и обслуживания ходовой части автомобиля Ашық сабақ
Ашық сабақ Звукові коливання 5 клас
Звукові коливання 5 клас Архимедова сила
Архимедова сила Второе и третье начала термодинамики циклические процессы. Лекция № 13
Второе и третье начала термодинамики циклические процессы. Лекция № 13 Композиты - древний материал будущего
Композиты - древний материал будущего Детали машин и механизмов. Основные положения и понятия раздела
Детали машин и механизмов. Основные положения и понятия раздела Изопроцессы в газах
Изопроцессы в газах Изобретение Рентгена
Изобретение Рентгена Световые явления природы
Световые явления природы §8. Плоскопараллельное движение твердого тела (плоское)
§8. Плоскопараллельное движение твердого тела (плоское)