Слайд 2
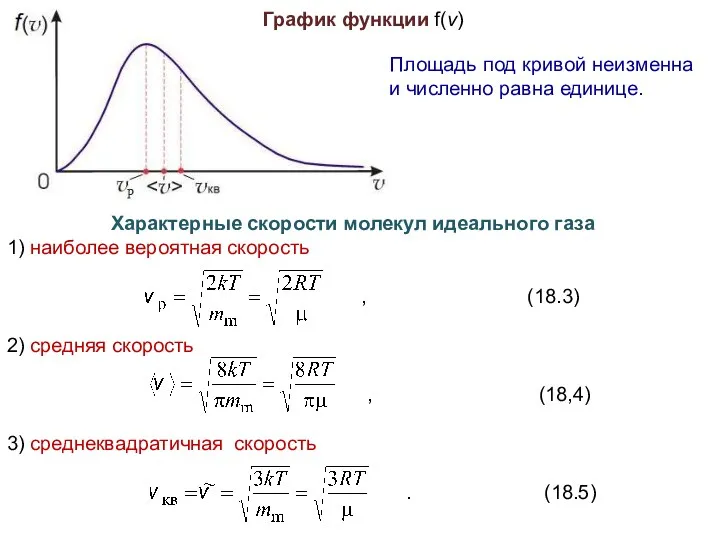
График функции f(v)
Площадь под кривой неизменна и численно равна единице.
Характерные скорости
молекул идеального газа
1) наиболее вероятная скорость
, (18.3)
2) средняя скорость
, (18,4)
3) среднеквадратичная скорость
. (18.5)
Слайд 3
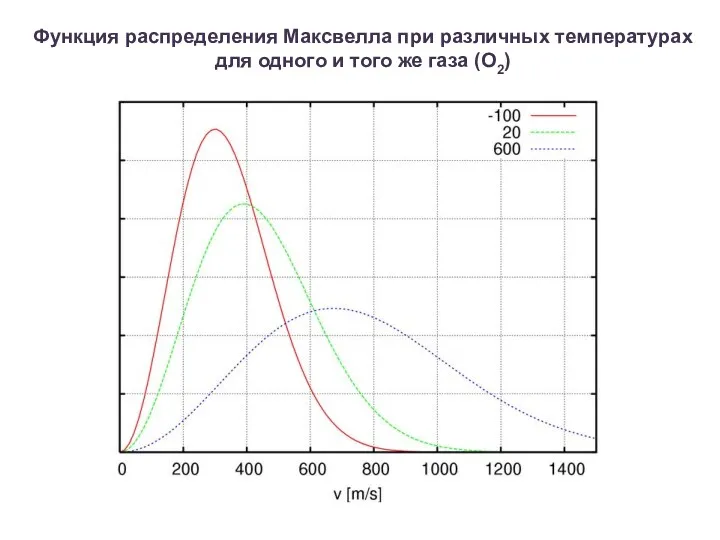
Функция распределения Максвелла при различных температурах для одного и того же
газа (О2)
Слайд 4
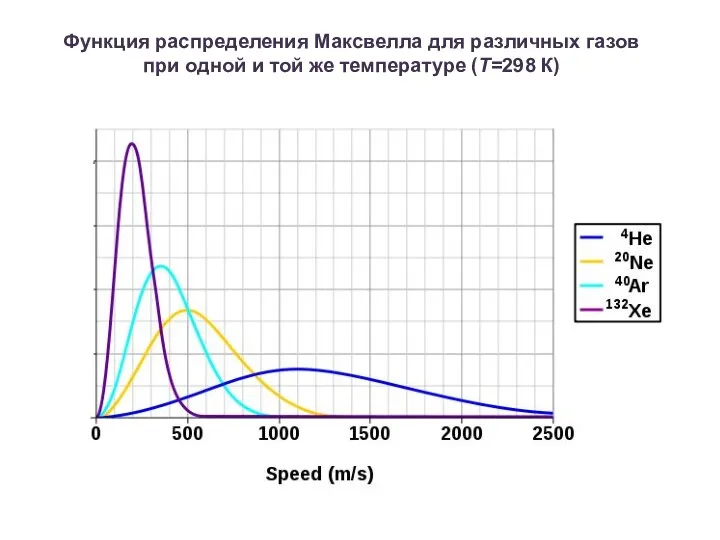
Функция распределения Максвелла для различных газов
при одной и той же температуре
(T=298 К)
Слайд 5

Распределение Больцмана
Распределение Максвелла получено в предположении, что на частицы физической макросистемы
не действуют внешние силы (например, сила тяжести).
Если же макросистема (в частности, идеальный газ) находится во внешнем силовом поле, то распределение частиц по объему описывается законом Больцмана (Людвиг Больцман, 1896 г.).
В соответствии с распределением Больцмана концентрация частиц макросистемы в некоторой ее точке r, определяется выражением
, (18.6)
где n0 – концентрация частиц в отсутствии внешнего поля;
Π(r) – потенциальная энергия частицы в точке r.




 Температура
Температура Сила. Сила тяжести. Сила - векторная величина
Сила. Сила тяжести. Сила - векторная величина Презентация открытого урока по теме Лазеры
Презентация открытого урока по теме Лазеры Принцип суперпозиции полей
Принцип суперпозиции полей Понятие методологической культуры педагога
Понятие методологической культуры педагога Кремний для солнечной энергетики
Кремний для солнечной энергетики Электрический ток в металлах. Действия электрического тока
Электрический ток в металлах. Действия электрического тока Электризация тел. Два рода электрического заряда
Электризация тел. Два рода электрического заряда КПД теплового двигателя
КПД теплового двигателя Презентация к уроку Введение 7 класс
Презентация к уроку Введение 7 класс Физика будущего
Физика будущего Лучистый теплообмен между телами, образующими замкнутую систему
Лучистый теплообмен между телами, образующими замкнутую систему викторина Юный физик
викторина Юный физик Молекулярно-кинетическая теория (МКТ)
Молекулярно-кинетическая теория (МКТ) Презентация к уроку Диффузия. Движение молекул. (7 класс)
Презентация к уроку Диффузия. Движение молекул. (7 класс) Открытый урок по теме Шкала электромагнитных излучений (11 класс)
Открытый урок по теме Шкала электромагнитных излучений (11 класс) Опыт Эрстеда. Магнитное поле. Конфигурации магнитных полей. Характеристики магнитного поля
Опыт Эрстеда. Магнитное поле. Конфигурации магнитных полей. Характеристики магнитного поля Радіоактивність. Прилад для вимірювання радіоактивності-дозиметр
Радіоактивність. Прилад для вимірювання радіоактивності-дозиметр Колебательный контур. Свободные и вынужденные электромагнитные колебания
Колебательный контур. Свободные и вынужденные электромагнитные колебания Волны. Звуковые волны. Звук
Волны. Звуковые волны. Звук Основные понятия нанотехнологий. Оборудование
Основные понятия нанотехнологий. Оборудование История представлений строения атома
История представлений строения атома Общие теоремы динамики точки
Общие теоремы динамики точки Материя, темная материя, вещество, антивещество
Материя, темная материя, вещество, антивещество внеклассное мероприятие Как сберечь воду и уменьшить ее загрязнение для учащихся 6-7 классов
внеклассное мероприятие Как сберечь воду и уменьшить ее загрязнение для учащихся 6-7 классов Электрический заряд
Электрический заряд игра по физике Звездный час
игра по физике Звездный час Проект “Дизельный двигатель”
Проект “Дизельный двигатель”