Содержание
- 2. Тема Реагенты
- 3. Модификация возможна 1) Коллоидная неустойчивость – конденсационно-коагуляционный рост капель в облаке и выпадение дождя из теплых
- 4. Воздействие на фазовый состав облака Основная группа методов АВ на облака различных форм связана с воздействием
- 5. Введение хладореагента или льдореагента в облако жидкий азот с помощью самолетных азотных генераторов мелкодисперсных частиц льда
- 6. Вещества, используемые в качестве реагента, должны удовлетворять следующим основным требованиям. 1. Нерастворимость. При растворении в воде
- 7. 2. Размер. Важной характеристикой является степень дисперсности реагента. Чем меньше размеры частиц реагента, тем большее число
- 8. критический радиус жизнеспособных зародышей зависит от температуры (при механизмах конденсационного, иммерсионного и контактного замерзания) и от
- 9. Исследования показали, что образцы реагента с очень однородной поверхностью (хорошо отполированной) проявляют меньшую льдообразующую способность, чем
- 10. 3. Подобие. Важным условием эффективности реагента является подобие его кристаллической решетки или поверхностных свойств соответствующим характеристикам
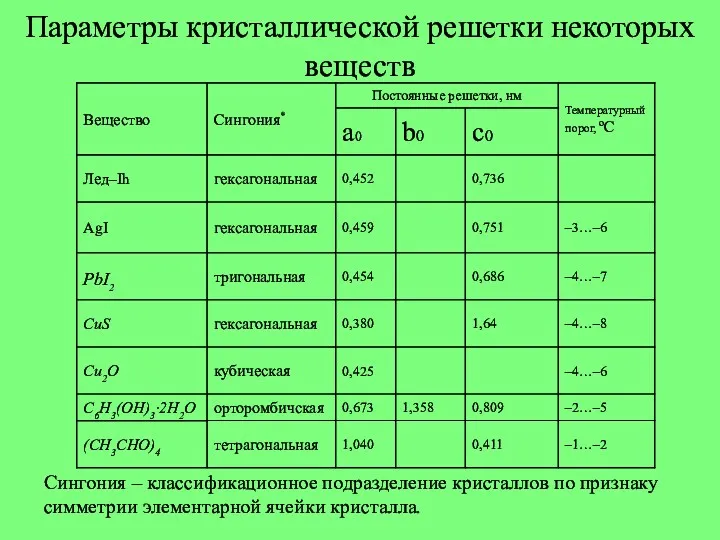
- 11. Параметры кристаллической решетки некоторых веществ Сингония – классификационное подразделение кристаллов по признаку симметрии элементарной ячейки кристалла.
- 12. Если отличаются не только параметры решетки, но и вид сингонии, рост кристаллов не может быть эпитаксийным.
- 13. – Подобие водородных связей. Взаимодействие между молекулами Н2О во льду осуществляется с помощью водородных связей О…Н.
- 14. Цепочка превращений.
- 15. С физической точки зрения мы имеем дело с фазовыми превращениями собственно реагента и гетерогенной нуклеацией льда
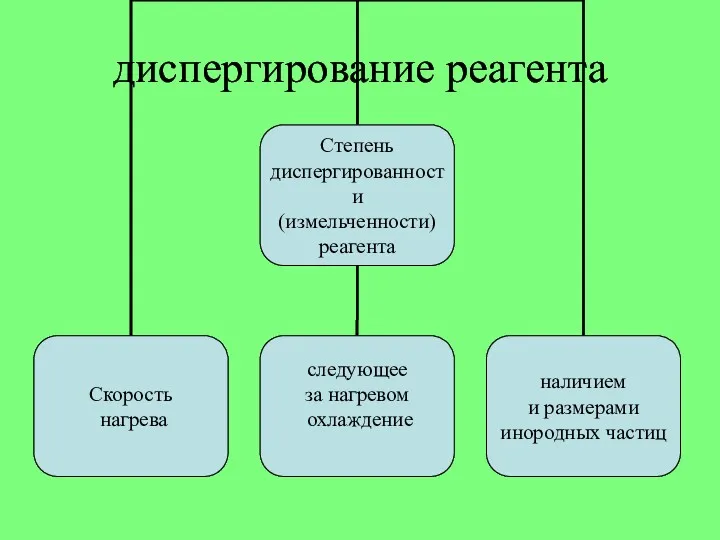
- 16. диспергирование реагента
- 17. На практике способы диспрергирования тесно связаны со средствами доставки реагента в облака. В лабораторных условиях диспергирование
- 18. Широкое распространение получили методы диспергирования, связанные с сжиганием реагента в пиротехнических составах. Эти методы используются при
- 19. При обстреле облаков с поверхности земли с помощью артиллерийских орудий реагент закладывается в снаряд, начиненный взрывчатым
- 20. Используются гранулированная твердая углекислота (сухой лед CO2), гранулы которой имеют температуру -70 °С и жидкий азот
- 22. Скачать презентацию

















 Адиабатическое приближение в твердом теле
Адиабатическое приближение в твердом теле Стабилитроны
Стабилитроны Формы и методы подготовки учащихся к ГИА по физике
Формы и методы подготовки учащихся к ГИА по физике Топ-5 перспективных разработок атомной энергетики
Топ-5 перспективных разработок атомной энергетики ВКР: Получение нанодисперсной магнитной жидкости на полярной основе методом химической конденсации
ВКР: Получение нанодисперсной магнитной жидкости на полярной основе методом химической конденсации Преимущества и недостатки использования оптических волокон в системах связи
Преимущества и недостатки использования оптических волокон в системах связи Импульсные сигналы и переходные процессы. Общие сведения об импульсных сигналах
Импульсные сигналы и переходные процессы. Общие сведения об импульсных сигналах Конвективный теплообмен. (Лекция 10)
Конвективный теплообмен. (Лекция 10) Стандартная модель. Космогония современного мира
Стандартная модель. Космогония современного мира Устройство автомобиля – шасси. Подвеска автомобиля
Устройство автомобиля – шасси. Подвеска автомобиля Как называются частицы, из которых состоят вещества?
Как называются частицы, из которых состоят вещества? 10 класс. Презентация по физике на тему Конденсаторы
10 класс. Презентация по физике на тему Конденсаторы Магнитооптические материалы
Магнитооптические материалы Свойства уравнений Максвелла
Свойства уравнений Максвелла Физика. Молекулярно-кинетическая теория
Физика. Молекулярно-кинетическая теория Статистические и термодинамические свойства макросистем
Статистические и термодинамические свойства макросистем Обертальний рух в природі
Обертальний рух в природі Урок в 8 классе Сила тока.
Урок в 8 классе Сила тока. Внеклассное мероприятие Конкурс изобретателей
Внеклассное мероприятие Конкурс изобретателей использование интерактивного обордования на роках физики
использование интерактивного обордования на роках физики Исследование особенностей проектирования и анализа плавучего отеля с катамаранным корпусом
Исследование особенностей проектирования и анализа плавучего отеля с катамаранным корпусом Теоретические основы электротехники. Основные законы электрических цепей
Теоретические основы электротехники. Основные законы электрических цепей Устройство и безопасная эксплуатация строительных подъемников
Устройство и безопасная эксплуатация строительных подъемников Графики изопроцессов. Решение графических задач
Графики изопроцессов. Решение графических задач Инжекторная система впрыска топлива
Инжекторная система впрыска топлива Зубчатые передачи
Зубчатые передачи Кинетическая энергия
Кинетическая энергия Электрический ток в газах
Электрический ток в газах