Содержание
- 2. Масса фотона Масса покоя фотона равна нулю. Массу движущегося фотона найдем из закона взаимосвязи массы и
- 3. Импульс фотона
- 4. Давление света Петр Николаевич ЛЕБЕДЕВ (1866—1912) Основатель выдающейся школы физиков Московского университета. Блестящий экспериментатор. Первым измерил
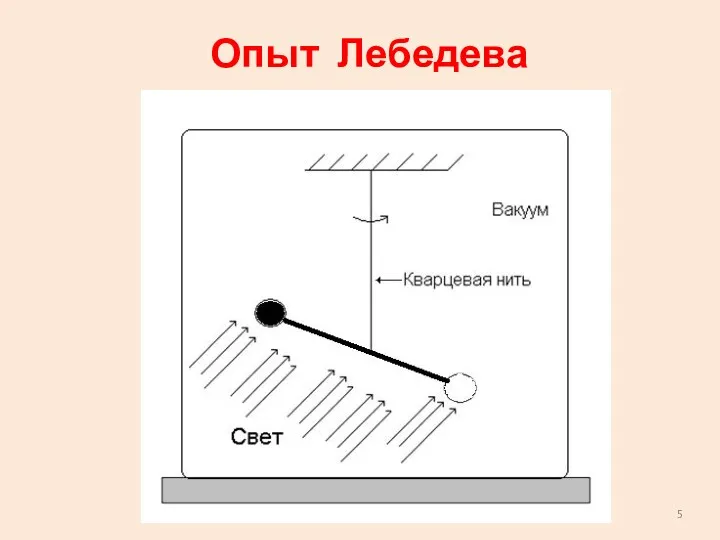
- 5. Опыт Лебедева
- 6. Если в единицу времени на единицу площади поверхности с коэффициентом отражения ρ падает N фотонов, то
- 7. Е - энергия N фотонов, падающих на 1 м2 в 1 с. Давление света
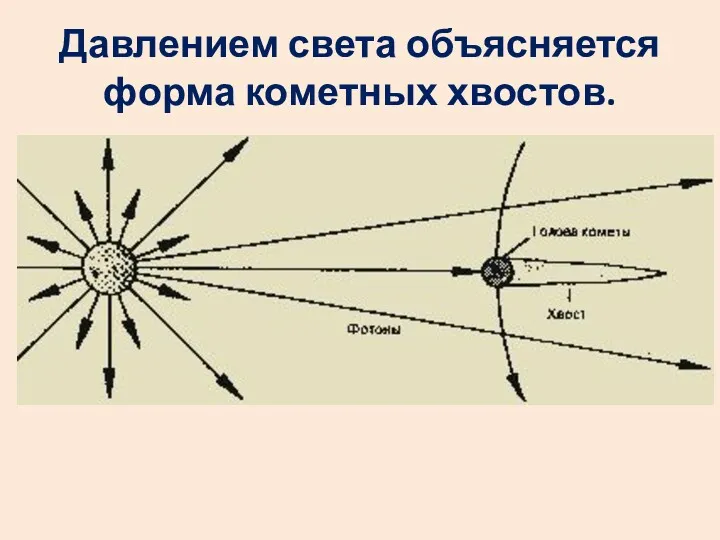
- 8. Давлением света объясняется форма кометных хвостов.
- 9. Солнечный парус
- 10. Гипотеза де Бройля В 1924 г. Луи де Бройль выдвинул гипотезу об универсальности корпускулярно-волнового дуализма: не
- 11. Связь величин, описывающих корпускулярные и волновые свойства частиц та же, что и для фотонов:
- 12. Длина волны де Бройля тем меньше, чем больше масса частицы и ее скорость. Пусть m =
- 13. Для электрона с энергиями от 10 эВ до 104 эВ длины волн де Бройля лежат в
- 14. Первое экспериментальное подтверждение гипотезы де Бройля было получено в 1927 году в опытах К. Дэвиссона и
- 15. Опыт В.А. Фабриканта (1949 г.)
- 16. Дифракция электронов при прохождении через очень тонкий слой серебра
- 17. Дифракция нейтронов
- 18. Соотношение неопределенностей Гейзенберга
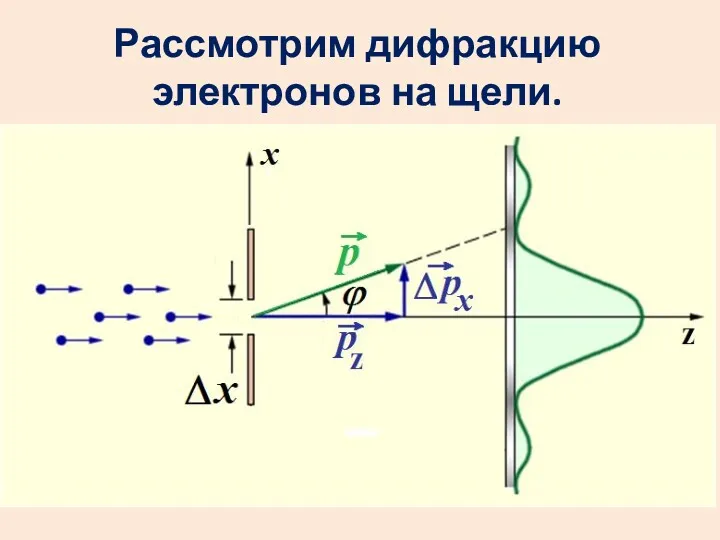
- 19. Рассмотрим дифракцию электронов на щели.
- 20. Пусть условно все электроны летят в центральный максимум. Координата х каждого электрона точно не известна. Неопределенность
- 21. Запишем условие первого минимума:
- 22. Получим: С учетом других максимумов произведение будет больше.
- 23. Соотношения неопределенностей Гейзенберга:
- 24. Для квантовой частицы неправомерно говорить об одновременных значениях ее координаты и импульса. Чем точнее определена какая-либо
- 25. Если ΔX→0, то ΔP→ Если ΔP→0, то ΔX→
- 26. Для энергии частицы W и времени: Если Δt→0, то ΔW→
- 27. ВОДОРОДОПОДОБНЫЕ АТОМЫ
- 28. Гипотеза о том, что вещества состоят из атомов, впервые была высказана Левкиппом и Демокритом примерно в
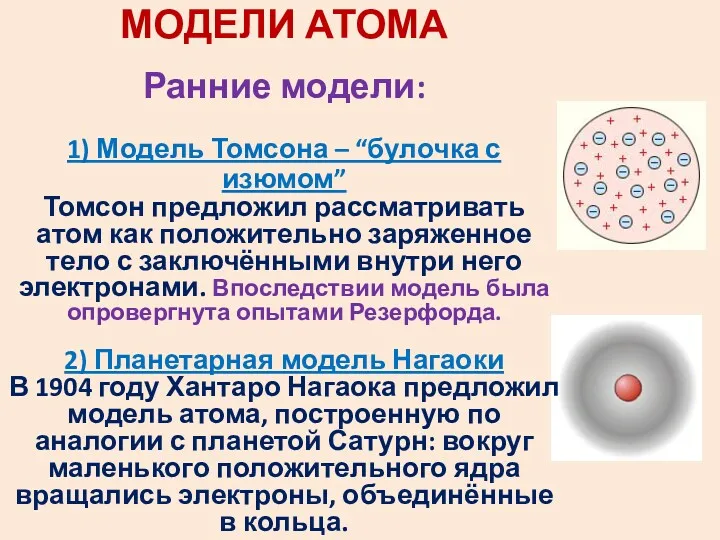
- 29. МОДЕЛИ АТОМА Ранние модели: 1) Модель Томсона – “булочка с изюмом” Томсон предложил рассматривать атом как
- 30. Опыт Резерфорда по рассеянию α-частиц Эрнст Резерфорд
- 31. Альфа-частица образована 2-мя протонами и 2-мя нейтронами, заряжена положительно. Идентична ядру атома гелия (4He2+).
- 32. Резерфорд направил поток α-частиц на золотую фольгу толщиной около 0,1 мкм. Большинство частиц пролетели сквозь фольгу,
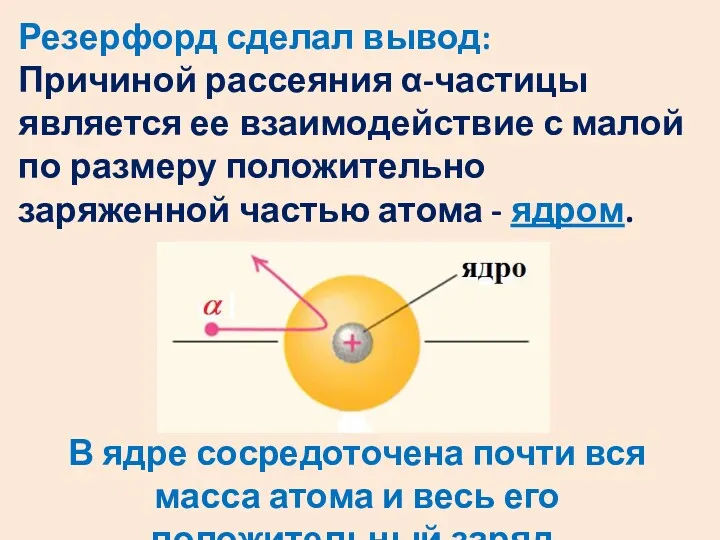
- 33. Резерфорд сделал вывод: Причиной рассеяния α-частицы является ее взаимодействие с малой по размеру положительно заряженной частью
- 34. Планетарная модель атома Резерфорда Атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам
- 35. Неустойчивость атома Резерфорда Согласно классической электродинамике электрон при движении с центростремительным ускорением должен излучать электромагнитные волны
- 36. Для объяснения стабильности атомов Нильсу Бору пришлось ввести особые предположения – постулаты.
- 37. Теория водородоподобного атома по Бору При построении теории Бор опирался на опыт Резерфорда и данные по
- 38. Водородоподобный атом – это атом с одним внешним электроном: Na, K, Rb, Cs. Спектр атома –
- 39. Спектр атома водорода образован сериями линий. Линии сгущаются к высокочастотной границе серии. В видимой области наблюдается
- 40. Бальмер подобрал формулу для частот спектральных линий: Для серии Бальмера m = 2, n = 3,
- 41. Постулаты Бора Атом может находится только в особых стационарных или квантовых состояниях, каждому из которых соответствует
- 42. Второй постулат Бора (правило частот) При переходе атома из одного стационарного состояния с энергией Wn в
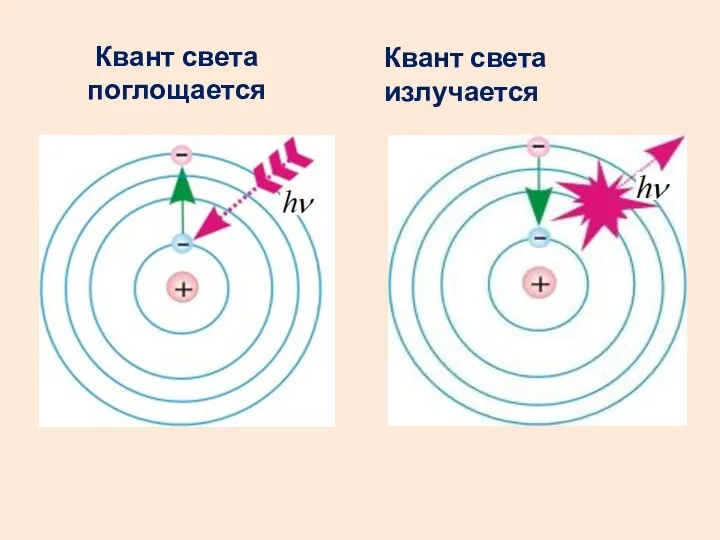
- 43. Квант света поглощается Квант света излучается
- 44. Третий постулат (квантование орбит) Момент импульса электрона в атоме принимает только дискретные значения, кратные постоянной Планка:
- 45. Бор вычислил радиусы орбит:
- 46. Радиус ближайшей к ядру орбиты называют первым боровским радиусом. заряд ядра,
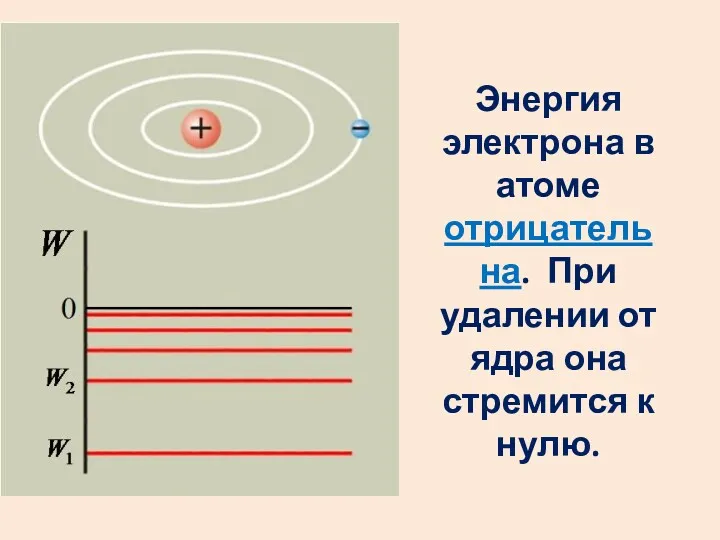
- 47. Полная энергия электрона в атоме: Энергия электрона на первой боровской орбите в атоме водорода:
- 48. Энергия электрона в атоме отрицательна. При удалении от ядра она стремится к нулю.
- 49. Частота излучения при переходе с n-го на m-й уровень энергии: R=3,3∙1015 Гц - частотная константа Ридберга,
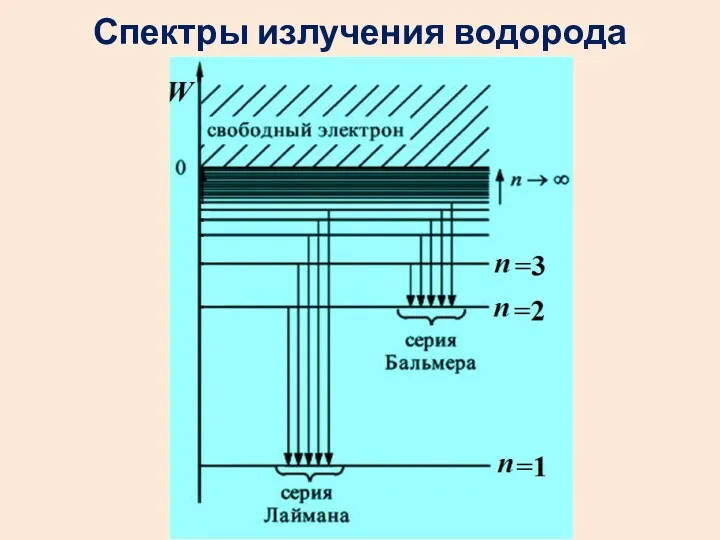
- 50. Спектры излучения водорода
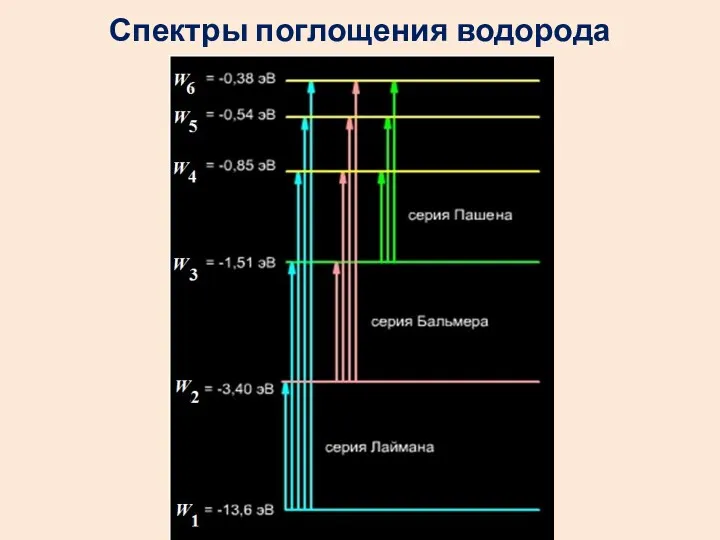
- 51. Спектры поглощения водорода
- 53. Скачать презентацию

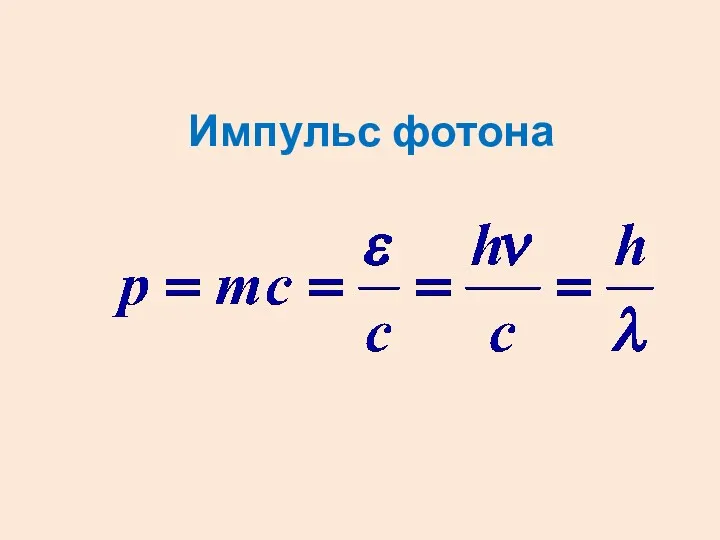


















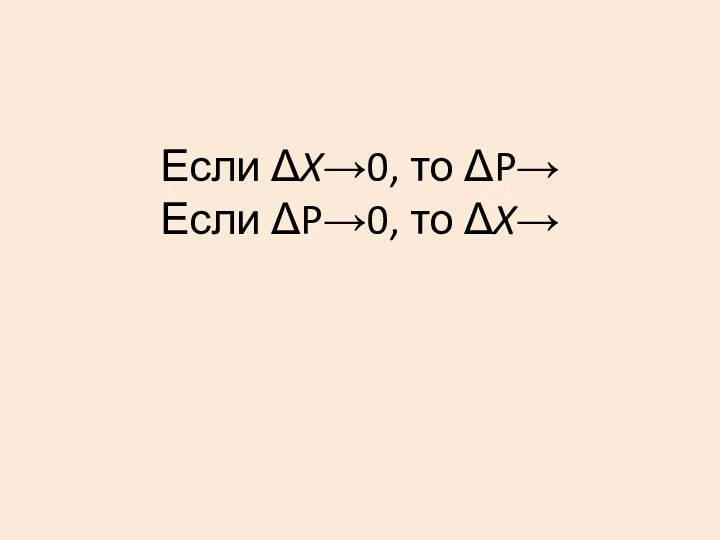




















 Мощностной баланс автомобиля
Мощностной баланс автомобиля Конденсаторы
Конденсаторы Визуальная, квантовая физика
Визуальная, квантовая физика Техническое обслуживание, диагностирование и ремонт газораспределительного механизма автомобиля
Техническое обслуживание, диагностирование и ремонт газораспределительного механизма автомобиля Электрооборудование автомобилей. Системы автоматического управления оборудованием автомобиля. (Урок 12)
Электрооборудование автомобилей. Системы автоматического управления оборудованием автомобиля. (Урок 12) Влияние предварительной деформации на эффект памяти формы в интерметаллиде TiNi
Влияние предварительной деформации на эффект памяти формы в интерметаллиде TiNi Отличия квантовой статистики от классической
Отличия квантовой статистики от классической Люмінесценція і її застосування. (Тема 1)
Люмінесценція і її застосування. (Тема 1) Конвекция. Ламинарный тепловой погранслой при вынужденном движении жидкости вдоль плоской поверхности. (Тема 2. Лекции 8,9)
Конвекция. Ламинарный тепловой погранслой при вынужденном движении жидкости вдоль плоской поверхности. (Тема 2. Лекции 8,9) Теплообмен излучением
Теплообмен излучением Основы молекулярно-кинетической теории
Основы молекулярно-кинетической теории Применение первого закона термодинамики к различным процессам
Применение первого закона термодинамики к различным процессам Проектная деятельность на уроках физики в 7 классе
Проектная деятельность на уроках физики в 7 классе Защита от ионизирующих излучений
Защита от ионизирующих излучений Ходовая автомобиля
Ходовая автомобиля Плотность вещества
Плотность вещества Подшипники качения
Подшипники качения Электронагревательные приборы. Из истории изобретения электрической лампы накаливания
Электронагревательные приборы. Из истории изобретения электрической лампы накаливания Пристеночный закон скоростей в турбулентных течениях
Пристеночный закон скоростей в турбулентных течениях Аэрогазодинамика. Плоские изоэнтропические течения газа (лекции 8, 9)
Аэрогазодинамика. Плоские изоэнтропические течения газа (лекции 8, 9) Опыт Резерфорда
Опыт Резерфорда Токарно-винторезный станок мод. 16К20
Токарно-винторезный станок мод. 16К20 Рулевое управление. Устройство автомобиля
Рулевое управление. Устройство автомобиля Прості механізми
Прості механізми Хроматография. (Лекция 4)
Хроматография. (Лекция 4) Реактивное движение
Реактивное движение Презентация к уроку в 7 классе по теме Масса тела.Измерение массы тела с помощью весов
Презентация к уроку в 7 классе по теме Масса тела.Измерение массы тела с помощью весов Реактивное движение. Ракеты
Реактивное движение. Ракеты