Содержание
- 2. Обратимыми по направлению химическими реакциями называются такие реакции, которые при данных внешних условиях могут самопроизвольно протекать
- 3. Н2(газ) + J2(газ) ↔ 2HJ (газ), ΔGo = 1,6 кДж/моль Hb(р-р) + О2(газ) ↔ НbО2(р-р), ΔGo
- 4. Гульдберг, Вааге и Бекетов открыли закон действующих масс (здм). Он отражает соотношение между равновесными концентрациями реагирующих
- 5. ΔGо р-ции = -RTlnkc, т.к. при равновесии ΔGо р-ции = 0 (стандартные условия) С учетом этого:
- 6. КОНСТАНТЫ РАВНОВЕСИЯ: По способу выражения а) термодинамическая Ка = б) концентрационная в) для газов через давление
- 7. КОНСТАНТЫ РАВНОВЕСИЯ: По типу реакции а) константа диссоциации (ионизации) HNO2 ↔ H+ + NO2- K(HNO2) б)
- 8. Влияние температуры на величину константы химического равновесия выражается уравнением: К2 и К1 – константы равновесия при
- 9. Если на систему, находящуюся в равновесии, воздействовать извне, изменив какое-либо из условий, то в результате протекающих
- 10. Химическая кинетика – учение о закономерностях протекания химических реакций. Она рассматривает скорость и механизм реакций. Их
- 11. По механизму реакции делятся на простые и сложные. Простые реакции осуществляются посредством однотипных элементарных актов. Под
- 12. Для осуществления сложных реакций необходимы два или более элементарных акта (биохимические реакции). V1 а) параллельные А
- 13. Молекулярность реакции – число молекул, участвующих одновременно в элементарном акте. Различают: мономолекулярные (термическое разложение, цис-транс –
- 14. Порядок реакции – это эмпирически установленная зависимость скорости от концентрации реагирующих веществ. Известны реакции: нулевого порядка
- 15. V = ± ΔCA / Δt для реакции А→ В Средняя скорость Истинная скорость Единица измерения
- 16. Гульдберг, Вааге и Бекетов (здм) Скорость простой реакции прямо пропорциональна произведению концентрации реагирующих веществ А +
- 17. Для гетерогенных реакций С(тв.фазы) = const Например: СО2 + С = 2СО V = - d(CO2)
- 18. Кинетическое уравнение реакции – функциональная зависимость концентрации реагирующих веществ от времени. Они получаются из уравнений здм.
- 19. 1) Реакции нулевого порядка (скорость не зависит о концентрации исходных веществ). Это гетерогенные реакции. А →
- 20. 2) Реакции первого порядка А → продукты реакции После интегрирования:
- 21. График зависимости от t – прямая линия, где -tgα=k Для СА = САо/2 имеем t0,5 =
- 22. 3) Реакции второго порядка 2А → продукты реакции или А + В → продукты реакции Интегральное
- 23. Есть реакции псевдопервого порядка, если концентрация одного из веществ большая и практически не меняется. СН3СООС2Н5 +
- 24. Порядок реакции определяется: Физическими методами Химическими методами (по t0,5) Биохимическими методами
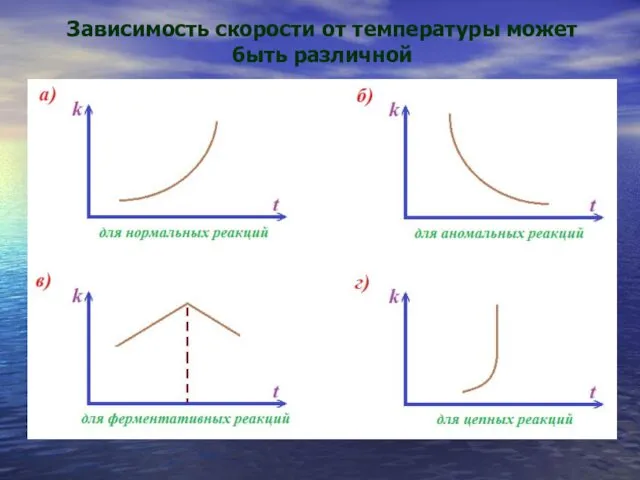
- 26. Зависимость скорости от температуры может быть различной
- 27. Правило Вант-Гоффа (для небольших температур) γ=2÷4 раз Но для биохимических реакций γ = 1,06 – 1,82
- 28. С. Аррениус создал теорию активных соударений. Уравнение Аррениуса: где А – предэкспоненциальный множитель, пропорциональный числу столкновений
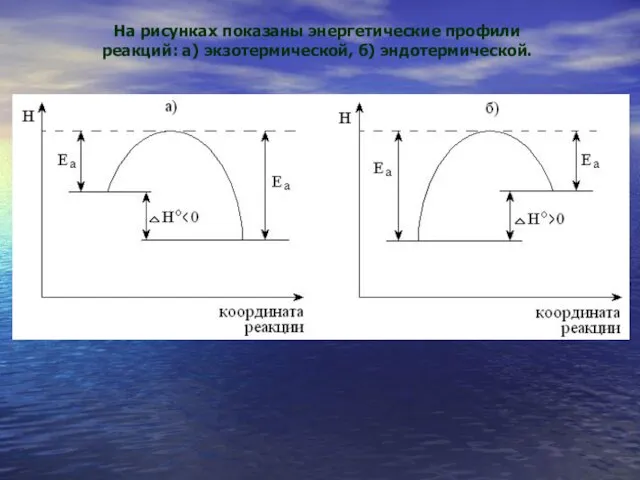
- 29. На рисунках показаны энергетические профили реакций: а) экзотермической, б) эндотермической.
- 30. Энергия активации - тот энергетический барьер, который должны преодолеть исходные вещества по пути превращения в продукты
- 31. Для двух температур уравнение Аррениуса имеет вид: или k1 и k2 – константы скорости при температурах
- 32. Катализ – это явление изменения скорости химических реакций в присутствии веществ, которые после завершения реакции остаются
- 33. Для ферментативных процессов: где Е – энзим (фермент); S – субстрат, вещество на которое действует фермент;
- 34. Михаэлис и Ментен дали уравнение ферментативного катализа (уравнение Михаэлиса – Ментен) Vст – стационарная скорость (она
- 35. Ферменты - белковые вещества. Содержат один или несколько активных центров, где и происходит превращение субстратов. Металлоферменты
- 36. Механизм действия ферментов заключается в изменении пути процесса превращения реагентов в продукты. Новый путь характеризуется меньшим
- 37. Итак, на скорость химических реакций оказывают влияние: природа реагирующих веществ; концентрации исходных веществ; температура; катализаторы; давление
- 39. Скачать презентацию


































 Розв’язування задач з теми Закон збереження імпульсу
Розв’язування задач з теми Закон збереження імпульсу Subjects: forces in mechanics. Dynamics. Newton’s laws
Subjects: forces in mechanics. Dynamics. Newton’s laws Световые кванты
Световые кванты Резьбы, резьбовые изделия и соединения. Разъемные соединения. Неразъемные соединения
Резьбы, резьбовые изделия и соединения. Разъемные соединения. Неразъемные соединения Системы смазки и охлаждения двигателя
Системы смазки и охлаждения двигателя Гидростатика. Давление в жидкости
Гидростатика. Давление в жидкости DSI M78 6-Speed A/T. Overseas service team
DSI M78 6-Speed A/T. Overseas service team Геометрическая оптика
Геометрическая оптика Электромагнитное поле
Электромагнитное поле Отдельные электроприемники в однофазной цепи переменного тока
Отдельные электроприемники в однофазной цепи переменного тока Центрифугирование
Центрифугирование Өз құрылымы мен құрамы болмайтын бөлшекті
Өз құрылымы мен құрамы болмайтын бөлшекті Движение заряженной частицы в электрическом и магнитном полях. Лекция 6
Движение заряженной частицы в электрическом и магнитном полях. Лекция 6 Правило буравчика, правило правой руки
Правило буравчика, правило правой руки Кузнечно-сварочная практика. Специальность 190604 Техническое обслуживание и ремонт автомобильного транспорта
Кузнечно-сварочная практика. Специальность 190604 Техническое обслуживание и ремонт автомобильного транспорта Двигатель внутреннего сгорания. Устройство. Схема. Применение
Двигатель внутреннего сгорания. Устройство. Схема. Применение Движение тела под действием силы трения
Движение тела под действием силы трения Устройство токарного станка для обработки древесины. (Технический труд. 6 класс)
Устройство токарного станка для обработки древесины. (Технический труд. 6 класс) Вещества и явления в окружающем мире
Вещества и явления в окружающем мире Дизельный двигатель
Дизельный двигатель Физика в стихах
Физика в стихах Урок Оптические приборы, физика11 класс
Урок Оптические приборы, физика11 класс Отчет об исследовательской работе
Отчет об исследовательской работе Основы молекулярной физики и термодинамики
Основы молекулярной физики и термодинамики Идеальные газы тождественных частиц. Распределение Ферми-Дирака и Бозе-Эйнштейна
Идеальные газы тождественных частиц. Распределение Ферми-Дирака и Бозе-Эйнштейна Схема сверхзвукового обтекания затупленного тела
Схема сверхзвукового обтекания затупленного тела Оптические методы и приборы контроля качества продукции
Оптические методы и приборы контроля качества продукции Равновесные и неравновесные носители зарядов
Равновесные и неравновесные носители зарядов