Идеальный газ. Давление газа. Средняя кинетическая энергия поступательного движения молекул. Концентрация молекул презентация
Содержание
- 2. Идеальный газ Давление газа Средняя кинетическая энергия поступательного движения молекул Концентрация молекул Понятия и величины:
- 3. Основное уравнение молекулярно-кинетической теории (уравнение Клаузиуса) Уравнение Менделеева - Клапейрона Законы:
- 4. Все тела состоят из мельчайших частиц – атомов и молекул. Атомы и молекулы находятся в состоянии
- 5. Дополнительно для МКТ газа В любом, даже очень малом, объеме газа число молекул очень велико. (При
- 6. При отсутствии внешних сил молекулы газа распределяются равномерно по всему объему, занятому газом. Направления скоростей молекул
- 7. Тепловое движение Хаотическое движение молекул тела называется тепловым движением. Тепловое движение будем характеризовать средней кинетической энергией
- 8. Идеальный газ – простейшая физическая модель реального газа. Газ считается идеальным, если выполнимы следующие допущения: -
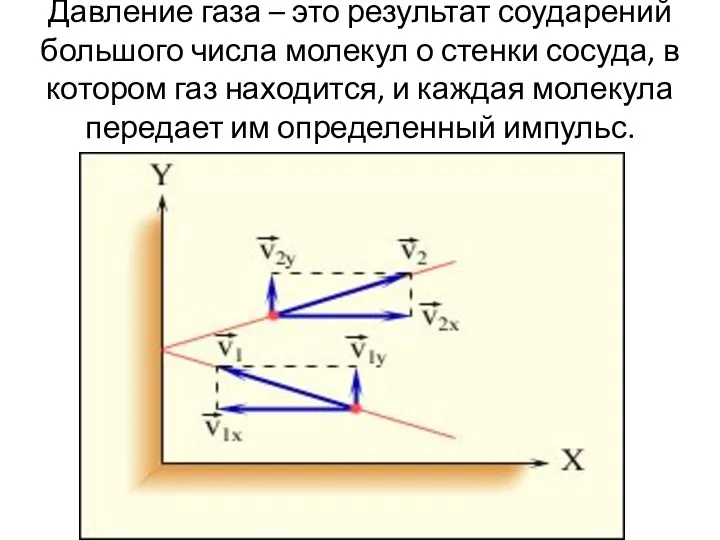
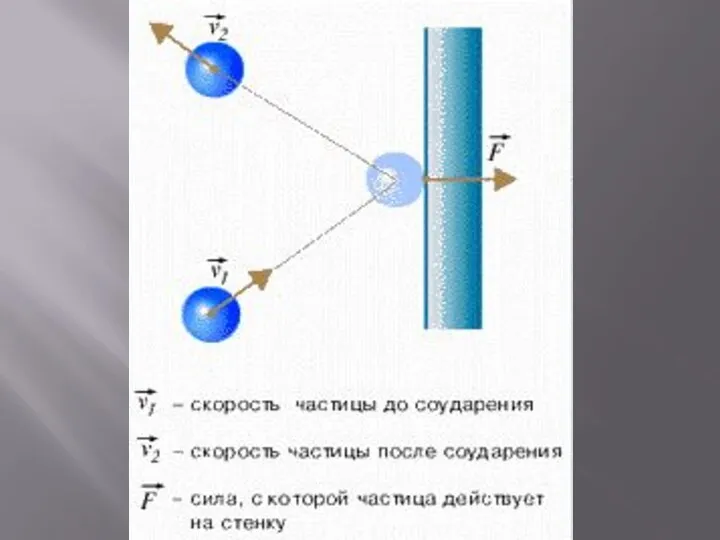
- 10. Давление газа – это результат соударений большого числа молекул о стенки сосуда, в котором газ находится,
- 12. Основное уравнение молекулярно-кинетической теории (уравнение Клаузиуса) Это уравнение устанавливает связь между давлением p идеального газа, массой
- 13. Давление идеального газа p пропорционально произведению массы молекулы m0, концентрации молекул (числу молекул в единице объема)
- 14. Через среднюю кинетическую энергию молекулы это уравнение записывают в виде р = n∙E к Давление газа
- 15. Возникают вопросы: Каким образом можно на опыте изменять среднюю кинетическую энергию движения молекул в сосуде неизменного
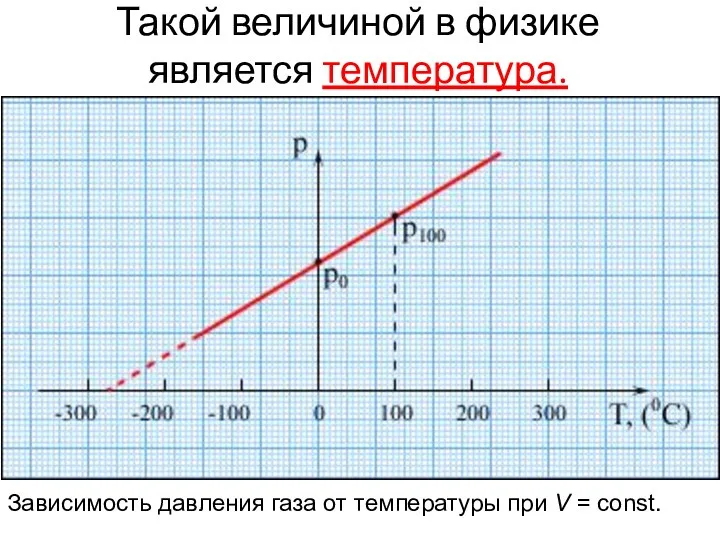
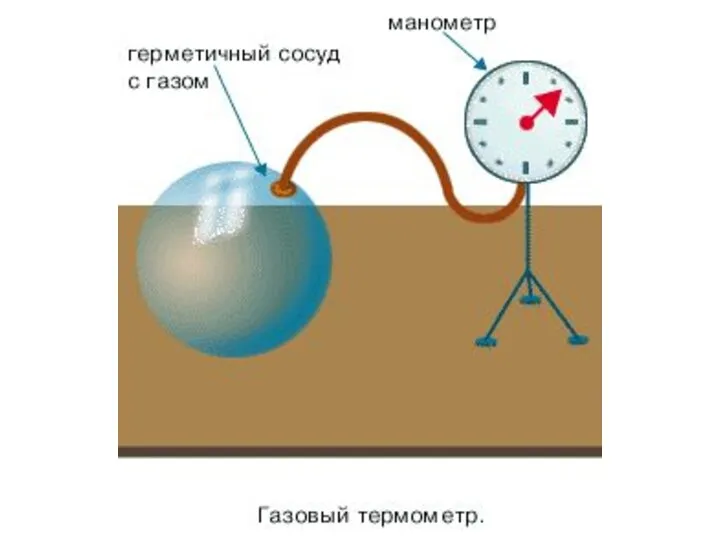
- 16. Такой величиной в физике является температура. Зависимость давления газа от температуры при V = const.
- 17. Английский физик У. Кельвин (Томсон) в 1848 г. предложил использовать точку нулевого давления газа для построения
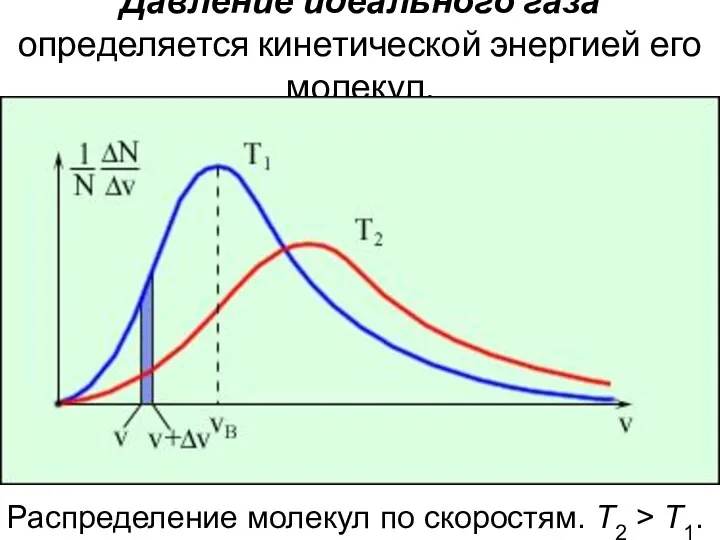
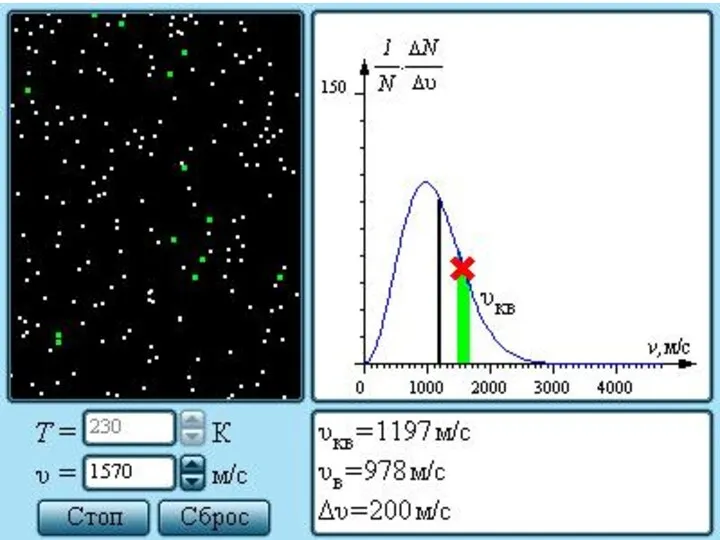
- 19. Давление идеального газа определяется кинетической энергией его молекул. Распределение молекул по скоростям. T2 > T1.
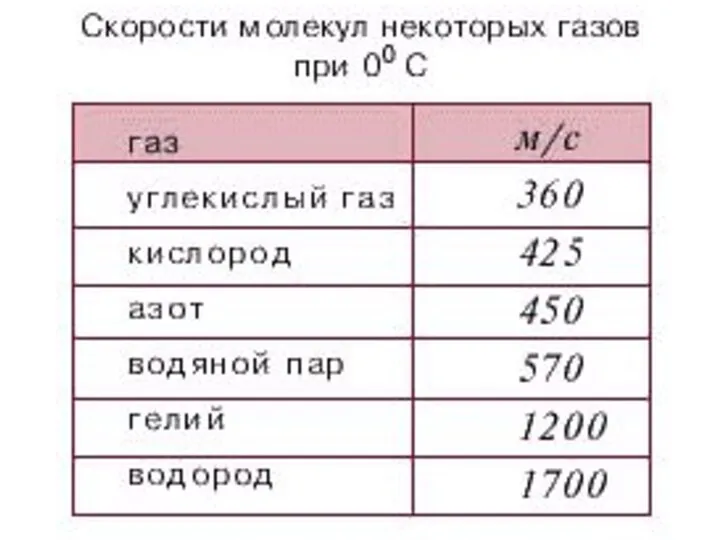
- 20. Характерными параметрами распределения Максвелла являются наиболее вероятная скорость υв, соответствующая максимуму кривой распределения, и среднеквадратичная скорость
- 23. Таким образом, давление разреженного газа в сосуде постоянного объема V изменяется прямо пропорционально его абсолютной температуре:
- 24. Объединяя эти соотношения пропорциональности, можно записать: p = nkT, где k – некоторая универсальная для всех
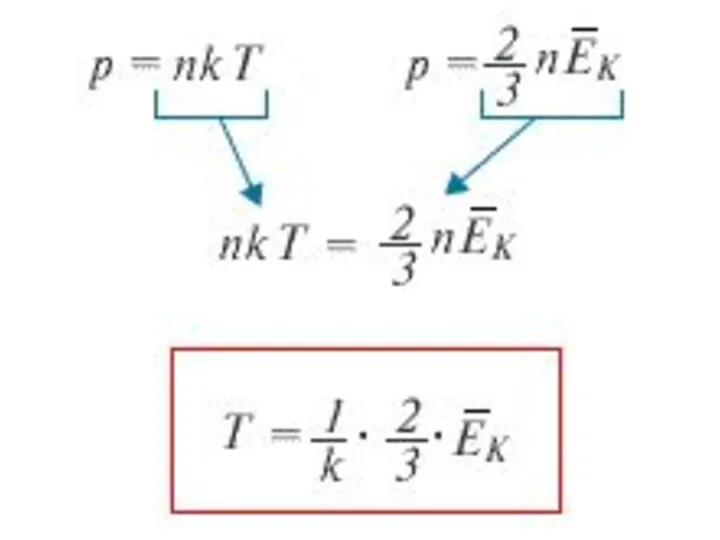
- 25. Сравнивая соотношения p = nkT с основным уравнением молекулярно-кинетической теории газов, можно получить: Средняя кинетическая энергия
- 27. Таким образом, температура есть мера средней кинетической энергии поступательного движения молекул.
- 29. Давление смеси газов на стенки сосуда будет складываться из парциальных давлений каждого газа: p = p1
- 30. уравнение состояния идеального газа. Соотношение p = nkT может быть записано в другой форме, устанавливающей связь
- 31. В итоге получим: Произведение постоянной Авогадро NA на постоянную Больцмана k называется универсальной газовой постоянной и
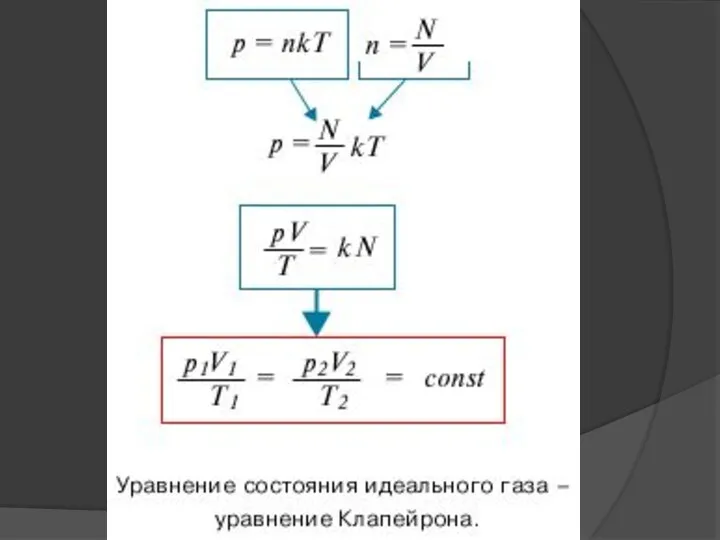
- 32. Уравнение, устанавливающее связь между давлением, объемом и температурой газа было получено в середине XIX века французским
- 33. Клапейрон Бенуа Поль Эмиль (26.I.1799–28.I.1864) Французский физик, член Парижской АН (1858). Окончил Политехническую школу в Париже
- 34. Менделеев Дмитрий Иванович (8.II.1834–2.II.1907) Русский ученый-энциклопедист.. В 1874 вывел общее уравнение состояния идеального газа, обобщив уравнение
- 35. Если температура газа равна Tн = 273,15 К (0 °С), а давление pн = 1 атм
- 36. И последнее, но очень важное: Для постоянной массы идеального газа
- 38. Т.е. для двух любых состояний газа: Есть величина постоянная!!! (Поправьте крыши – у многих уже съезжают!
- 39. Задание не для слабонервных : Попытайтесь рассчитать чему равно соотношение для одного моля газа при нормальных
- 40. Нормальные условия: (напоминаю в последний раз!) температура газа Tн = 273,15 К (0 °С), а давление
- 41. Закон Авогадро: один моль любого газа при нормальных условиях занимает один и тот же объем V0,
- 42. Сравним результат: Никто не ощутил приступа дежа-вю? Эта цифра сегодня уже мелькала! Точно, это она –
- 44. Скачать презентацию
































 Аккумулятор
Аккумулятор Деление атомных ядер. (Тема 2.7)
Деление атомных ядер. (Тема 2.7) Электростатика. Первоначальная энергия электрона
Электростатика. Первоначальная энергия электрона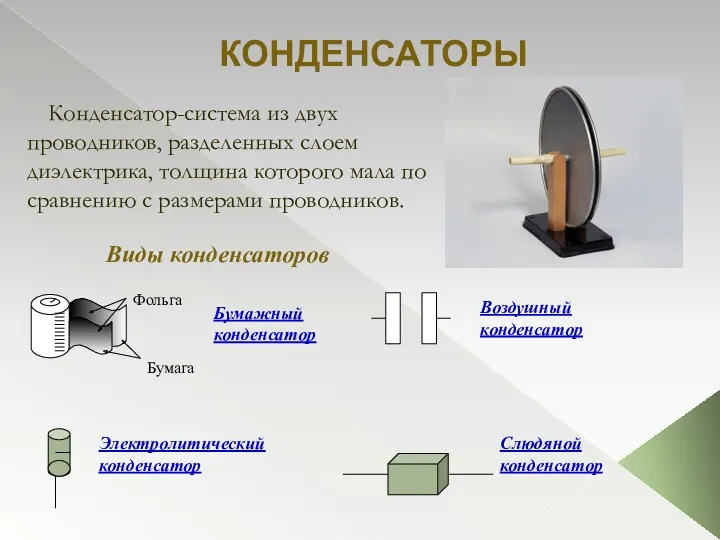 Конденсаторы. Классификация конденсаторов
Конденсаторы. Классификация конденсаторов Свободное движение твердого тела. (Лекция 5, Кафедра теоретической механики)
Свободное движение твердого тела. (Лекция 5, Кафедра теоретической механики) Прочность, совместимость и радиационная стойкость реакторных материалов. Тема 3
Прочность, совместимость и радиационная стойкость реакторных материалов. Тема 3 Расчет сооружений методом конечных элементов. (Лекция 6)
Расчет сооружений методом конечных элементов. (Лекция 6) Физическая игра Интеллектуальный ринг для 5- класса
Физическая игра Интеллектуальный ринг для 5- класса Тепловые явления
Тепловые явления ВКР: Анализ маслосистемы двигателя ПС-90А и её сравнительная характеристика с маслосистемой двигателя SaM-146
ВКР: Анализ маслосистемы двигателя ПС-90А и её сравнительная характеристика с маслосистемой двигателя SaM-146 Делимость электрического заряда
Делимость электрического заряда Технологический процесс изготовления детали Шестерня
Технологический процесс изготовления детали Шестерня Дисперсия света
Дисперсия света Механическая работа. Физика 7 класс
Механическая работа. Физика 7 класс Явление самоиндукции. Индуктивность
Явление самоиндукции. Индуктивность Квантовая физика. Фотоэффект
Квантовая физика. Фотоэффект Оптичні прилади та їх застосування
Оптичні прилади та їх застосування Закон Кулона – основной закон электростатики
Закон Кулона – основной закон электростатики Основы молекулярно-кинетической теории
Основы молекулярно-кинетической теории Отстаивание. Гидравлическая крупность частиц взвешенных веществ
Отстаивание. Гидравлическая крупность частиц взвешенных веществ Special Theory of Relativity
Special Theory of Relativity Тиск рідин і газів. Закон Паскаля. Урок 44
Тиск рідин і газів. Закон Паскаля. Урок 44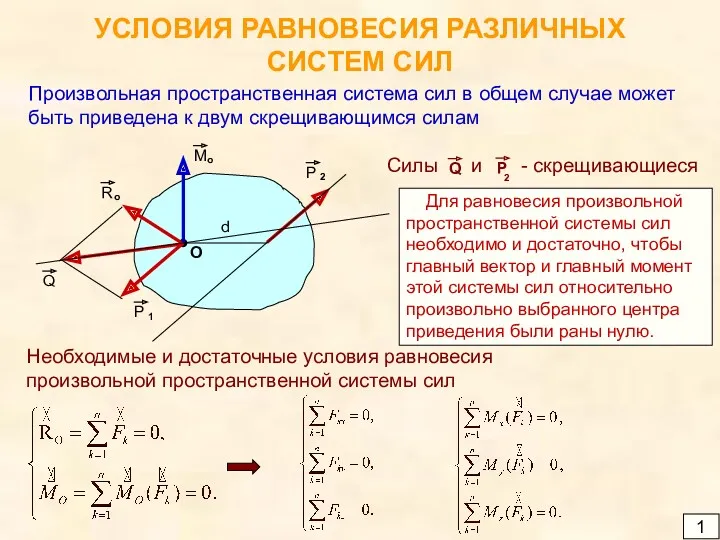 Условия равновесия различных систем сил
Условия равновесия различных систем сил Неединичные обратные связи и инвариантность системы к задающему воздействию
Неединичные обратные связи и инвариантность системы к задающему воздействию Урок по физике на тему Развитие средств связи
Урок по физике на тему Развитие средств связи презентация проектно-исследовательская деятельность
презентация проектно-исследовательская деятельность Активизация познавательной деятельности учащихся при изучении физики
Активизация познавательной деятельности учащихся при изучении физики Барометр-анероид. Атмосферное давление на различных высотах
Барометр-анероид. Атмосферное давление на различных высотах