Содержание
- 2. метод основан на ионизации атомов и молекул вещества и последующем разделении образующихся ионов в соответствии с
- 3. 1. Молекулярную массу вещества. 2. Молекулярную формулу вещества. 3. Строение вещества. МС позволяет определить:
- 4. Масс-спектр уксусной кислоты m/z I,% 50 10 20 30 40 50 60 100 28 60 3
- 5. Масс-спектр уксусной кислоты m/z I,% 50 20 30 40 10 50 60 100 28 60 3
- 6. Типы ионов в масс-спектрах Молекулярный ион – молекула с положительным зарядом (катион-радикал), полученным за счёт отрыва
- 7. Масс-спектрометрия – совокупность трёх отдельных процессов: Ионизация молекулы. Разделение ионов по массам. Детектирование ионов.
- 8. Типы ионизации 1. Электронный удар (ЭУ). катион-радикал - молекулярный ион ABC ABC -e молекула органического вещества
- 9. Достоинства метода дает богатые фрагментами масс-спектры, которые однозначно характеризуют структуру молекулы высокочувствительный метод анализа, позволяет анализировать
- 10. Недостатки метода: Молекулярные ионы образуются лишь у 20% органических соединений Определение легколетучих термически стабильных соединений; Ионы
- 11. Типы ионизации 2. Химическая ионизация. Органическое вещество ионизируется газом реагентом: метаном, аммиаком, изобутаном Определяемые молекулы АВ
- 12. Достоинства: Мягкий метод ионизации, молекуле образца передается около 5 эВ избыточной энергии, что препятствует процессам распада
- 13. Недостатки: Отсутствие распада, очень простые масс-спектры, что не позволяет судить о структуре вещества и сравнить спектр
- 14. Типы ионизации 3. Бомбардировка ускоренными атомами. Ионизация ионами инертных газов: аргона, ксенона. пробу помещают в ионизатор
- 15. Типы ионизации 4. Электроспрей ионизация (ESI). 2002 г. Дж. Фенн – Нобелевская премия. Анализ полимеров белков,
- 16. Достоинства: Метод позволяет работать с веществами, которые нельзя перевести в газовую фазу Удобен для сочетания масс-спектрометра
- 17. Недостатки: Вещество должно быть растворимо в полярных растворителях масс-спектр малоинформативен, как правило, присутствуют лишь пики комплексов
- 18. Типы ионизации 5. Матричная лазерная десорбционная ионизация МЛДИ (MALDI). 2002 г. К. Танаке – Нобелевская премия.
- 19. Взаимодействие лазерного импульса с образцом МЛДИ лазерный импульс (337нм, 3.68эВ, 0.1нс)
- 20. Достоинства: 1. Возможность анализа крупных молекул. 2. Мягкая ионизация образца. 3. Возможность анализа загрязненных примесями образцов
- 21. Типы ионизации 6. Полевая ионизация Ионизация происходит под действием электрического поля высокой напряженности (до 108 В/см).
- 22. Способы ввода пробы: Непрямой способ - пробу вводят в ионизатор в газообразном состоянии. Жидкие и твердые
- 23. Масс-спектрометрия под действием электронного удара
- 25. Движение заряженной частицы в магнитном поле 2 2 m = B r z 2V m –
- 26. В масс-спектрометрии регистрируются только заряженные частицы: катион-радикалы АВС+. и катионы А+, АВ+, С+. Незаряженные радикальные частицы
- 27. Масс –анализатор – устройство для разделения ионов в соответствии с отношением m/z Основные типы масс-анализаторов: 1.
- 28. Изменение траектории заряженной частицы под действием магнитного поля. r = 1 2U m / z H
- 29. Достоинства: высокое разрешение, чувствительность, большой диапазон детектируемых масс Основной недостаток – большой размер приборов и высокая
- 30. Электрический (электростатический) МА
- 31. Квадрупольный анализатор
- 33. Действие времяпролетных масс-анализаторов основано на зависимости скорости движения ионов от их массы. Особенность: ионы движутся в
- 34. Сочетание ВЭЖХ и МС. Анализ смесей труднолетучих, полярных веществ, не поддающихся анализу методом газожидкостной хроматографии. ЖИДКОСТНАЯ
- 36. Сначала использовалась фотопластинка. В настоящее время применяют динодные вторично-электронные умножители, в которых ион, попадая на первый
- 37. Для МС характерны Использование небольших навесок ( 1 мг и меньше) Высокая чувствительность все элементы периодической
- 38. Области применения МС Ядерная энергетика Археология Нефтехимия Геохимия (изотопная геохронология) Агрохимия Химическая промышленность Анализ полупроводниковых материалов,
- 39. Масс-спектрометрическая характеристика различных классов органических соединений
- 40. Алканы Обычно дают малоинтенсивные пики М+. В масс-спектрах характерно присутствие гомологичных ионов [CnH2n+1]+. Самые интенсивные пики
- 41. Циклоалканы ион с m/z = 56 циклогексан M+ = 84 Характерно наличие интенсивных пиков М+. Обычный
- 42. Алкены и алкины Пики М+ обычно более интенсивны, чем у алканов. В масс-спектрах характерно присутствие гомологичных
- 43. Спирты Молекулярные ионы М+ образуются при потере электрона от неподелённой электронной пары атома кислорода. Основные пути
- 44. Масс-спектр бутанола-1 I,% 50 20 30 40 10 50 60 100 43 2 56 = 74
- 45. Простые эфиры Характерен разрыв α- β связи: бутилэтиловый эфир M+ = 102 O α β O
- 46. Альдегиды и кетоны O αC β R' β R R C O R' R' C O
- 47. Для альдегидов и кетонов характерна перегруппировка Мак-Лафферти: O γ H β масса 14n γ α OH
- 48. Масс-спектр пентанона-2 58 продукт перегруппировки Мак-Лафферти I,% 50 40 50 60 100 86 M + m/z
- 49. Карбоновые кислоты и их производные Основные пути распада молекулярных ионов: путь а: Х = OH, NH2;
- 51. Скачать презентацию
 Автоколебания. Природа автоколебаний
Автоколебания. Природа автоколебаний Сила давления жидкости на плоские и криволинейные стенки
Сила давления жидкости на плоские и криволинейные стенки Сборка неподвижных и неразъемных соединений деталей
Сборка неподвижных и неразъемных соединений деталей Силы в механике: сила упругости, сила сухого и вязкого трения.
Силы в механике: сила упругости, сила сухого и вязкого трения.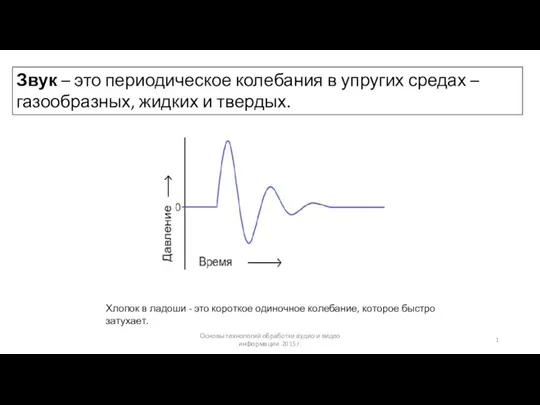 Звук. Периодическое колебание
Звук. Периодическое колебание Первый закон Ньютона. Инерциальные системы отсчёта
Первый закон Ньютона. Инерциальные системы отсчёта урок по физике в 10 классе Силы трения с презентацией
урок по физике в 10 классе Силы трения с презентацией Проекты АЭС с ВВЭР Российские реакторы 3-го поколения
Проекты АЭС с ВВЭР Российские реакторы 3-го поколения Условие равновесия рычагов. Правило моментов
Условие равновесия рычагов. Правило моментов Дисперсия
Дисперсия 135 лет со дня рождения Иоффе Абрама Федоровича.
135 лет со дня рождения Иоффе Абрама Федоровича. Температура, способы ее измерения, температурные шкалы
Температура, способы ее измерения, температурные шкалы Организация эксплуатации и ремонта бронетанковой техники. Ходовая часть
Организация эксплуатации и ремонта бронетанковой техники. Ходовая часть Электрические явления. 8 класс
Электрические явления. 8 класс Уравнения Максвелла. Закон полного тока
Уравнения Максвелла. Закон полного тока Термоэлектрические термометры
Термоэлектрические термометры Испарение и конденсация. Кипение жидкости. 8 класс
Испарение и конденсация. Кипение жидкости. 8 класс Бойове застосування КЗА 86Ж6. Система електроживлення. Апаратура радіаційної та хімічної розвідки. (Тема 9.5)
Бойове застосування КЗА 86Ж6. Система електроживлення. Апаратура радіаційної та хімічної розвідки. (Тема 9.5) Электрическое сопротивление. Закон Ома для участка цепи. Удельное сопротивление проводника
Электрическое сопротивление. Закон Ома для участка цепи. Удельное сопротивление проводника Презентация к уроку по теме Атмосферное давление. Опыт Торричелли
Презентация к уроку по теме Атмосферное давление. Опыт Торричелли Роботизированная коробка передач DSG
Роботизированная коробка передач DSG открытый урок-презентация на тему История Российской атомной энергетики
открытый урок-презентация на тему История Российской атомной энергетики Сила трения
Сила трения Презентация к план-конспекту интегрированного урока по физике 7 класс Путешествие в мир Силы тяжести
Презентация к план-конспекту интегрированного урока по физике 7 класс Путешествие в мир Силы тяжести Автоматтық жүйелер: негізгі анықтамалар, функционалдық схемалар. Ақпарат ұғымы, саны. Хабарлама
Автоматтық жүйелер: негізгі анықтамалар, функционалдық схемалар. Ақпарат ұғымы, саны. Хабарлама Тепловыделение в ядерных реакторах
Тепловыделение в ядерных реакторах Электрический ток в жидкостях
Электрический ток в жидкостях Прості механізми
Прості механізми