Слайд 2

Металлы
План лекции
Общая характеристика металлов: положение в периодической системе, строение атома,
распространение в природе
Общие физические свойства металлов
Общие химические свойства металлов
Общие способы получения металлов
Биологическая роль металлов
Слайд 3

Общая характеристика металлов
Если провести по периодической системе диагональ от бериллия
к астату, то в левом нижнем углу находятся металлы. Вдоль диагонали располагаются элементы с двойственным характером.
Слайд 4

Общие физические свойства металлов
Благодаря металлической кристаллической решетке металлы обладают тепло и
электропроводностью.
Металлы имеют металлический блеск, они непрозрачны
Металлы, плавящиеся при температуре выше 10000 называются тугоплавкими, ниже 10000 – легкоплавкими.
Металлы отличаются твердостью. Самый твердый металл – хром, самые мягкие – щелочные металлы.
Образуют сплавы: сплавы-растворы, сплавы-эмульсии, сплавы-суспензии
Слайд 5

Общие химические свойства металлов
Образование оксидов:
4 Na + O2 = 2
Na2O
2. Образование гидридов:
2 Na + H2 = 2 NaH
3. Образование гидроксидов:
2 Na + 2 HOH = 2 NaOH + H2
4. Образование солей:
Zn + 2 HCL = ZnCL2 + H2
5. Вытеснение металлов из их солей:
СuSO4 + Fe = FeSO4 = Cu
Металлы подвергаются коррозии – окисляются:
Химическая коррозия
Газовая коррозия
Электрокоррозия




 Вихретоковый контроль
Вихретоковый контроль 1-е начало термодинамики. Адиабатический процесс
1-е начало термодинамики. Адиабатический процесс قوة المولد بروفايل
قوة المولد بروفايل Показатели качества устойчивых ЛСС и методы их определения. Точность ЛСС в установившемся режиме
Показатели качества устойчивых ЛСС и методы их определения. Точность ЛСС в установившемся режиме Курс Атомные реакторы и ядерная энергетика. Лекция 3. Ядерная энергетика. Настоящее и будущее
Курс Атомные реакторы и ядерная энергетика. Лекция 3. Ядерная энергетика. Настоящее и будущее Интерференция света
Интерференция света Применение зондовой микроскопии в нанотехнологиях
Применение зондовой микроскопии в нанотехнологиях Рулевое управление
Рулевое управление Дисперсия света
Дисперсия света Что значит минута?
Что значит минута? Приборы для измерения атмосферного давления. Билет 23. Барометры
Приборы для измерения атмосферного давления. Билет 23. Барометры Страницы из жизни 1-ого человека в космосе.
Страницы из жизни 1-ого человека в космосе. Основные положения молекулярно-кинетической теории. Размеры молекул. Количество вещества
Основные положения молекулярно-кинетической теории. Размеры молекул. Количество вещества Определение стоимости и расхода электроэнергии
Определение стоимости и расхода электроэнергии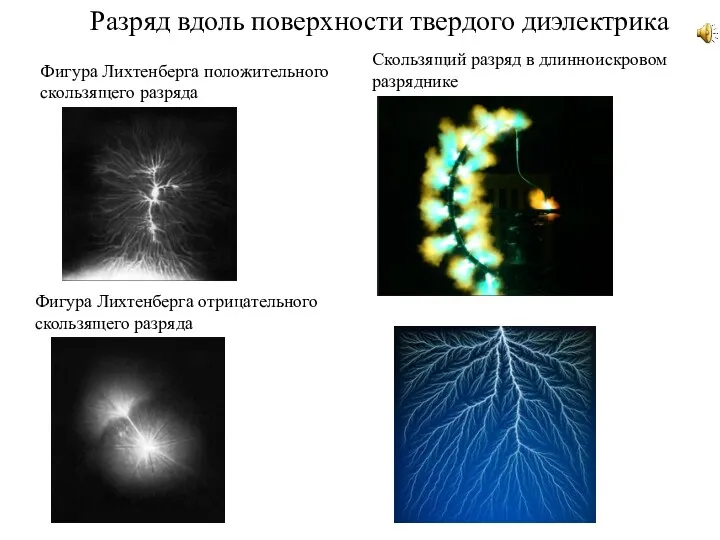 Разряд вдоль поверхности твердого диэлектрика. (Лекция 4)
Разряд вдоль поверхности твердого диэлектрика. (Лекция 4) Бүкіл әлемдік тартылыс заңы
Бүкіл әлемдік тартылыс заңы Подготовка к контрольной работе по теме Механика 10 класс
Подготовка к контрольной работе по теме Механика 10 класс Открытие протона и нейтрона. 9 класс
Открытие протона и нейтрона. 9 класс создание постера Один дома
создание постера Один дома Аэродинамика и летно-технические данные вертолёта. Тема №1. Аэродинамические силы и их коэффициенты. Лекция №3
Аэродинамика и летно-технические данные вертолёта. Тема №1. Аэродинамические силы и их коэффициенты. Лекция №3 Лучистый теплообмен между телами, образующими замкнутую систему
Лучистый теплообмен между телами, образующими замкнутую систему Заттың агрегаттық күйлерінің өзгеруі. 8 сынып
Заттың агрегаттық күйлерінің өзгеруі. 8 сынып Kappa (κ) Engine
Kappa (κ) Engine Действие жидкости и газа на погруженное в них тело
Действие жидкости и газа на погруженное в них тело Поляризация света
Поляризация света Презентация Механическая работа
Презентация Механическая работа Термодинамика бастамасының дүниетанымдық мәні
Термодинамика бастамасының дүниетанымдық мәні Опыт: Огнеупорный шарик (4 класс)
Опыт: Огнеупорный шарик (4 класс)