Содержание
- 3. Концепция атомизма 1.Дихотомия Демокрита
- 4. ? Легенда о яблоке
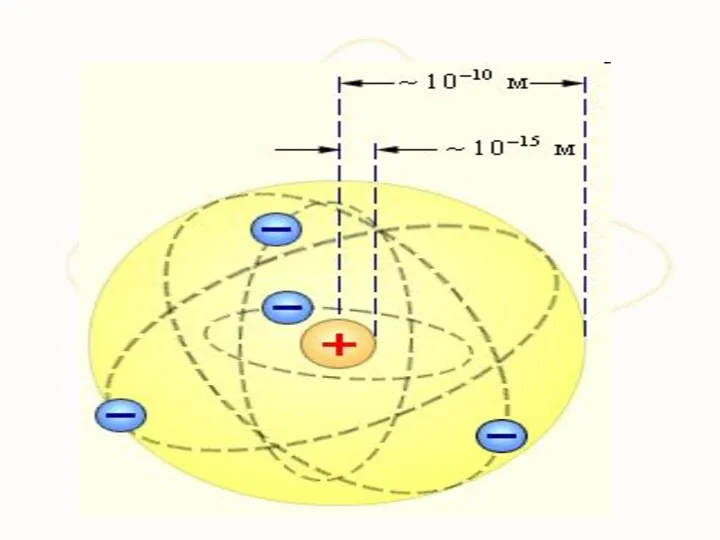
- 5. 1.1. Закономерности в атомных спектрах. х Итак, что же такое атом? Изолированные атомы в виде разреженного
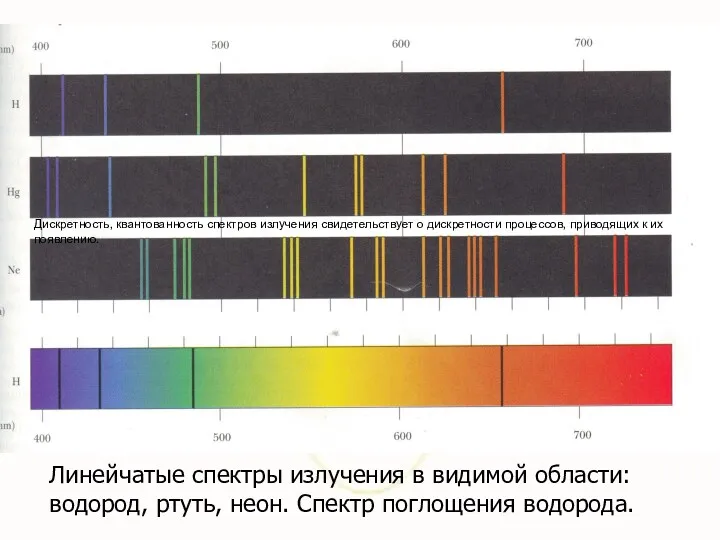
- 6. Линейчатые спектры излучения в видимой области: водород, ртуть, неон. Спектр поглощения водорода. Дискретность, квантованность спектров излучения
- 8. Швейцарский физик Й. Бальмер в 1885 году установил, что длины волн серии в видимой части спектра
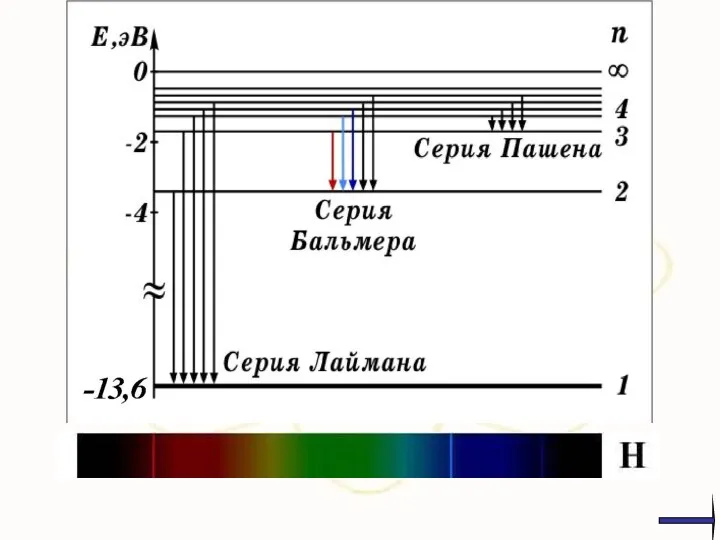
- 9. Дальнейшие исследования показали, что в спектре водорода имеется еще несколько серий: х
- 10. Обобщенная формула Й. Бальмера где k = 1, 2, 3,…, n = k + 1, k
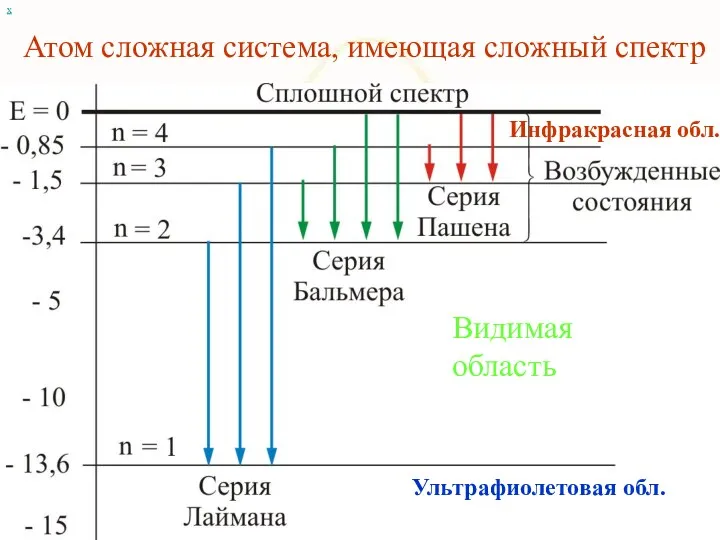
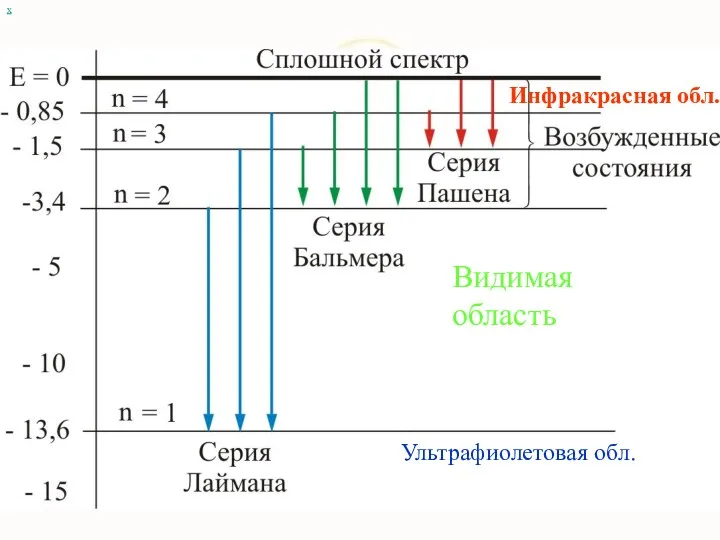
- 11. Атом сложная система, имеющая сложный спектр х Видимая область Инфракрасная обл. Ультрафиолетовая обл.
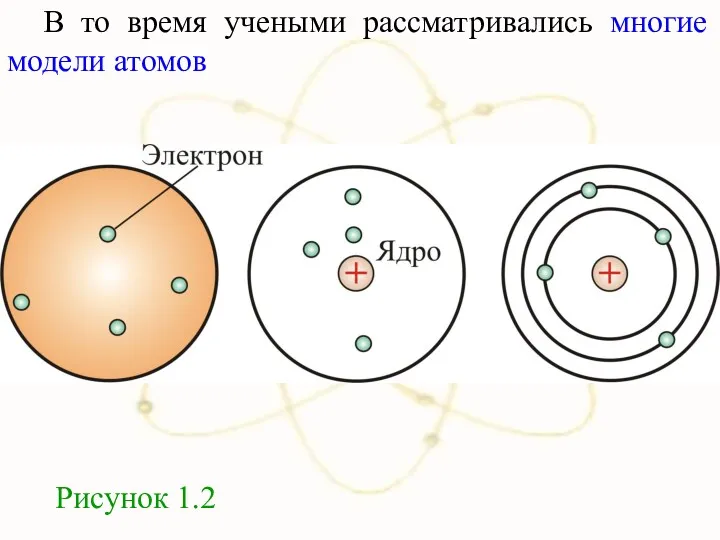
- 12. В то время учеными рассматривались многие модели атомов Рисунок 1.2
- 13. Закон постоянства состава соединений Лавуазье (1743-1794) Открытие атомов в химии
- 15. Интерпретация Дальтона: имеются определенные минимальные количества элементов и веществ (соединений)
- 16. Проблема внутреннего строения атома Открытие электрона Исследование тока в разреженных газах
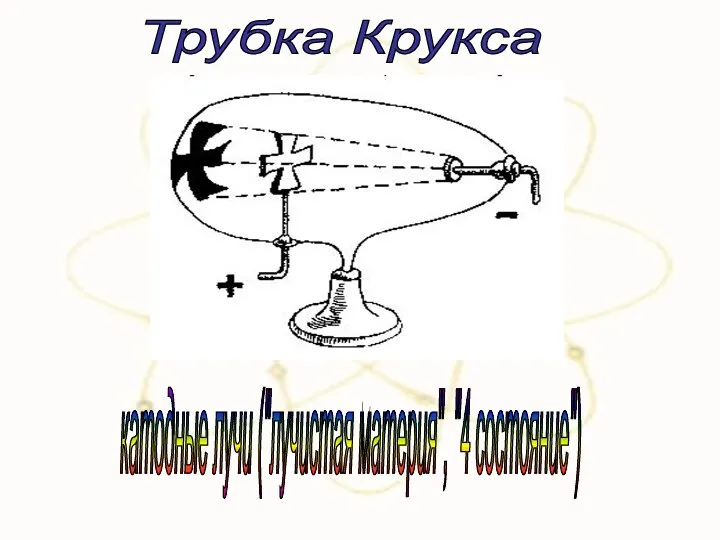
- 17. Трубка Крукса катодные лучи ("лучистая материя", "4 состояние")
- 18. 3- свойства К-лучей не зависят от типа газа 1 - отклоняются в магнитном поле 2 -
- 19. К-лучи - это поток отрицательно заряженных частиц вещества. ВЫВОДЫ:
- 20. Дж.Дж.Томсон в 1897 году определил величину отношения "заряд"/"масса" для этих частиц.
- 21. В состав всех атомов входят частицы малой массы - э л е к т р о
- 22. 1895- открытие Х-лучей Рентгеном 1896- открытие радиоактивности Беккерелем
- 23. 1897 - открытие электрона
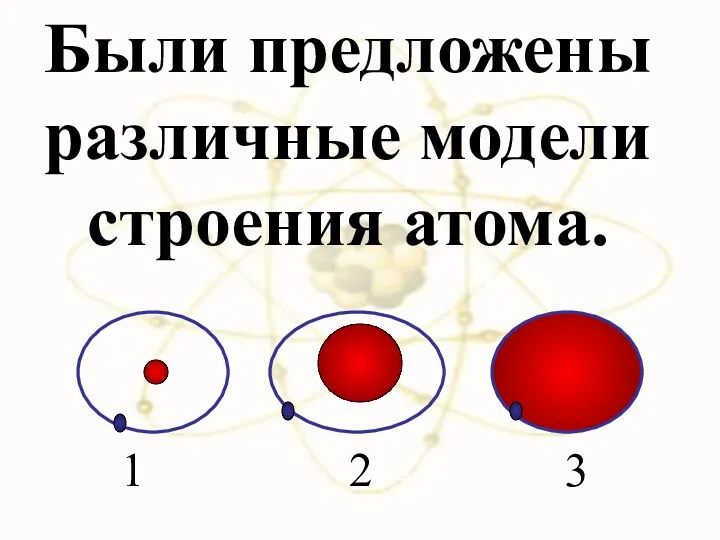
- 24. Были предложены различные модели строения атома. 1 2 3
- 26. х В 1903 году Дж. Дж. Томсон, предложил модель атома: сфера, равномерно заполненная положительным электричеством, внутри
- 27. Модель Дж.Дж Томсона (1904)
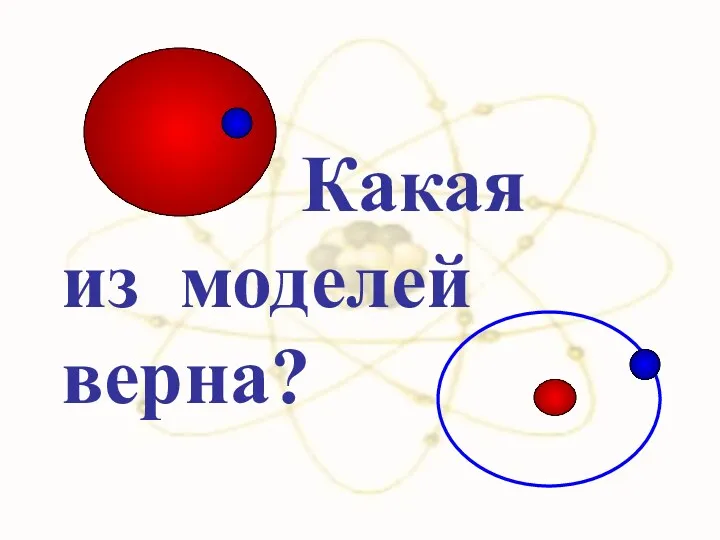
- 28. Какая из моделей верна?
- 29. Своими фундаментальными открытиями в этих областях заложил основы современного учения о радиоактивности и теории строения атома.
- 30. х 1.2. Ядерная модель атома (модель Резерфорда). Скорость α – частиц = 107 м/с = 104
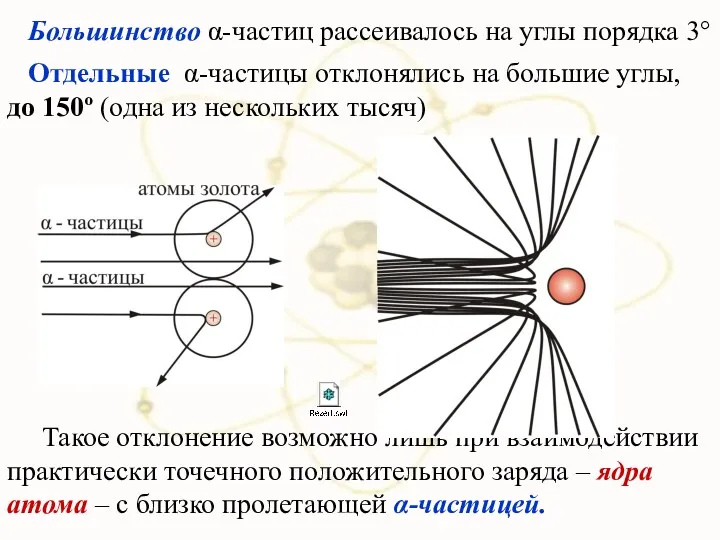
- 31. Большинство α-частиц рассеивалось на углы порядка 3° Отдельные α-частицы отклонялись на большие углы, до 150º (одна
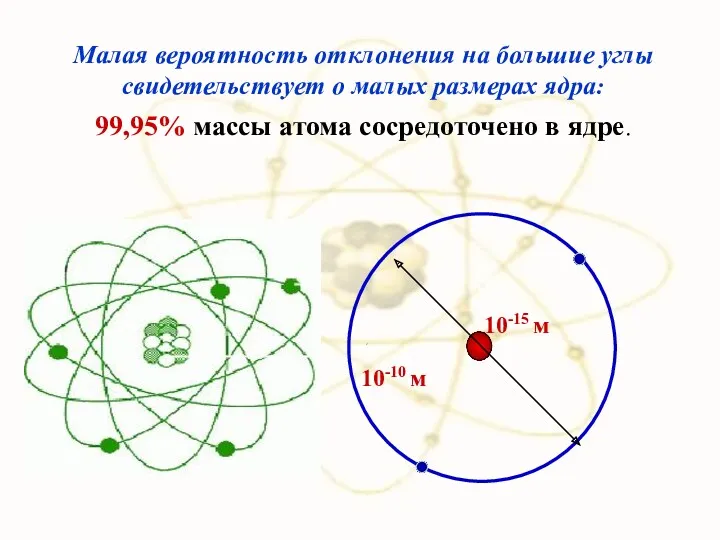
- 32. Малая вероятность отклонения на большие углы свидетельствует о малых размерах ядра: 99,95% массы атома сосредоточено в
- 33. Движение α-частицы происходит по гиперболе: Угол рассеяния равен углу между асимптотами гиперболы m – масса α-частицы,
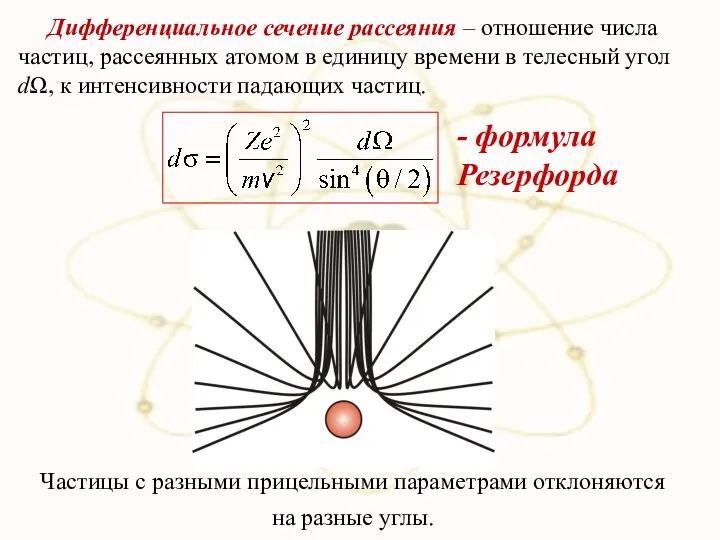
- 34. Дифференциальное сечение рассеяния – отношение числа частиц, рассеянных атомом в единицу времени в телесный угол dΩ,
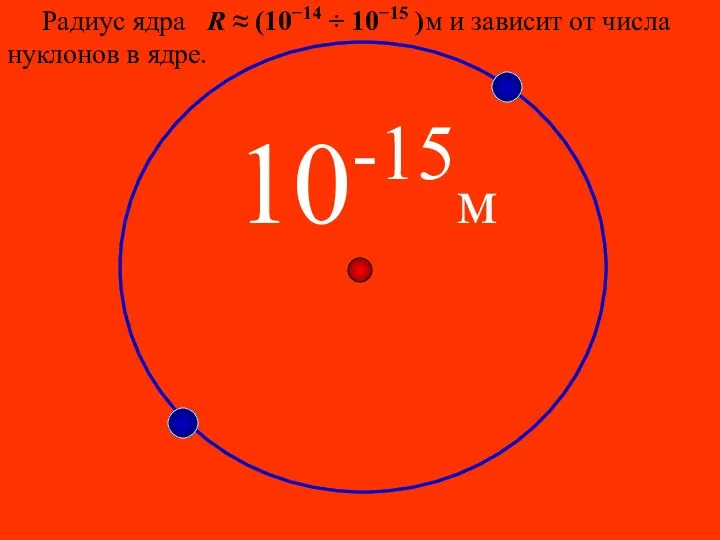
- 35. 10-15м Радиус ядра R ≈ (10−14 ÷ 10−15 )м и зависит от числа нуклонов в ядре.
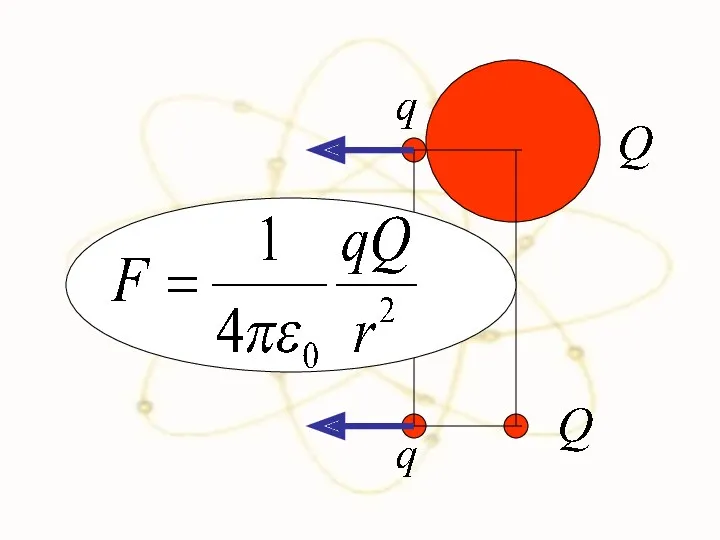
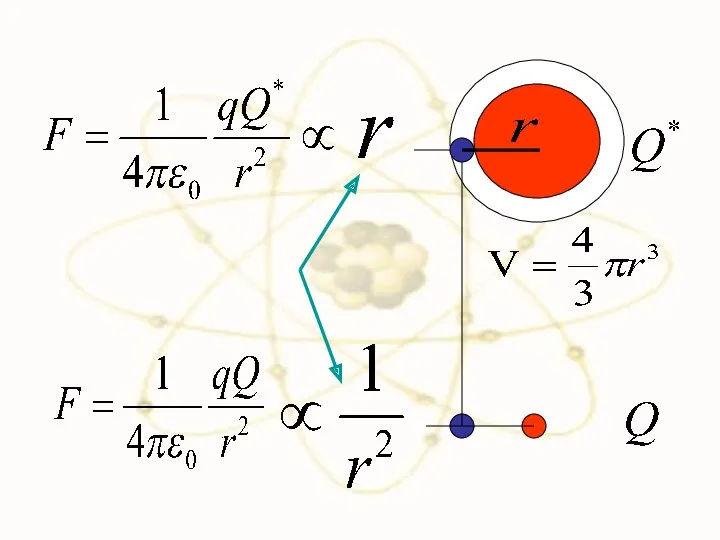
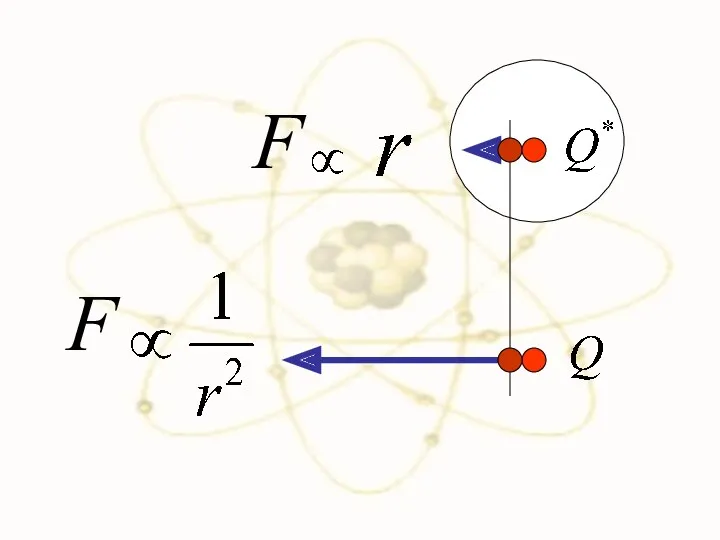
- 36. Сравним силы взаимодействия двух положительно заряженных частиц в разных моделях
- 39. F F
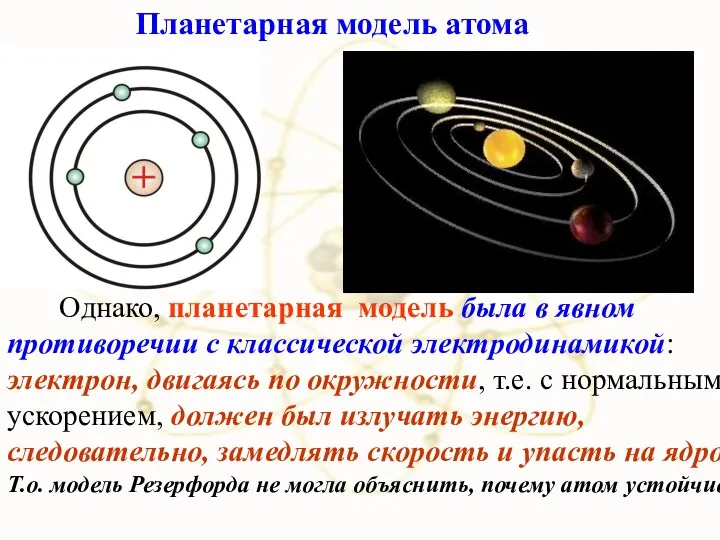
- 41. Однако, планетарная модель была в явном противоречии с классической электродинамикой: электрон, двигаясь по окружности, т.е. с
- 42. Планетарная модель атома противоречит электродинамике Максвелла!!!
- 43. Согласно теории Максвелла, ускоренно движущийся заряд излучает электромагнитные волны.
- 44. При движении по окружности имеется центростремительное ускорение. Поэтому электрон должен терять энергию на электромагнитное излучение и
- 45. Попыткой спасения планетарной модели атома стали постулаты Н. Бора
- 46. х 1.3. Элементарная теория Бора. БОР Нильс Хендрик Давид (1885–1962) – Выдающийся датский физик-теоретик, один из
- 47. 1. Атом следует описывать как «пирамиду» стационарных энергетических состояний. Пребывая в одном из стационарных состояний, атом
- 48. 2. При переходах между стационарными состояниями атом поглощает или излучает квант энергии. При поглощении энергии атом
- 49. Еn Em > En Поглощение энергии
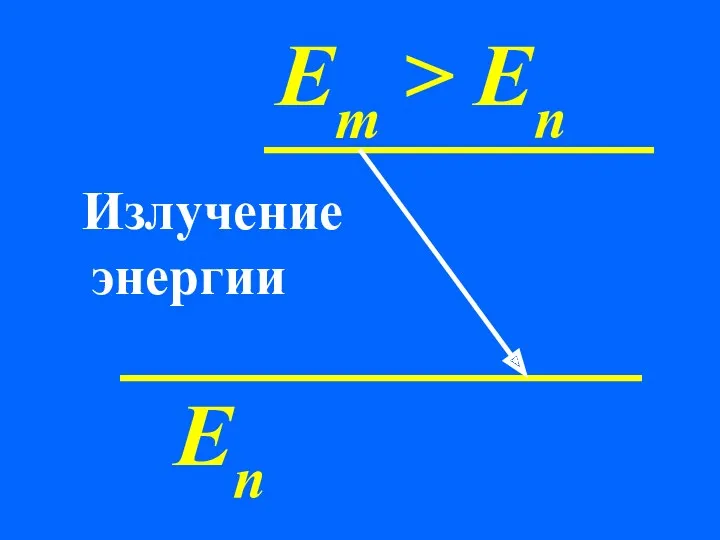
- 50. Еn Em > En Излучение энергии
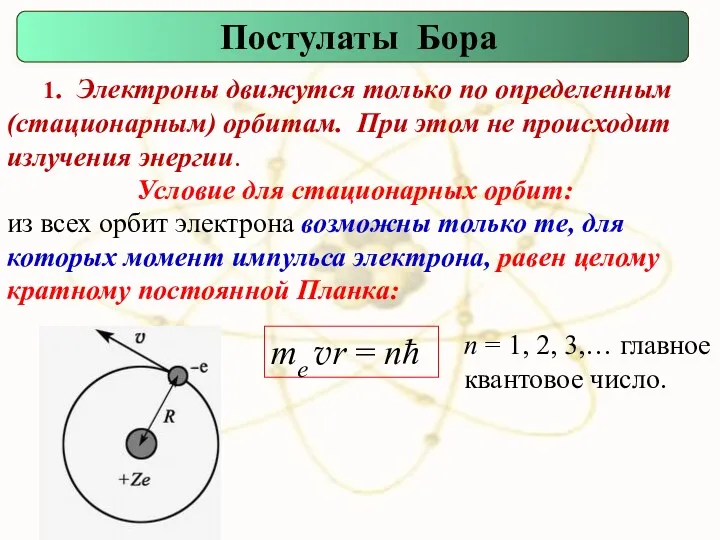
- 51. 1. Электроны движутся только по определенным (стационарным) орбитам. При этом не происходит излучения энергии. Постулаты Бора
- 52. 2. Излучение или поглощение энергии в виде кванта энергии hν происходит лишь при переходе электрона из
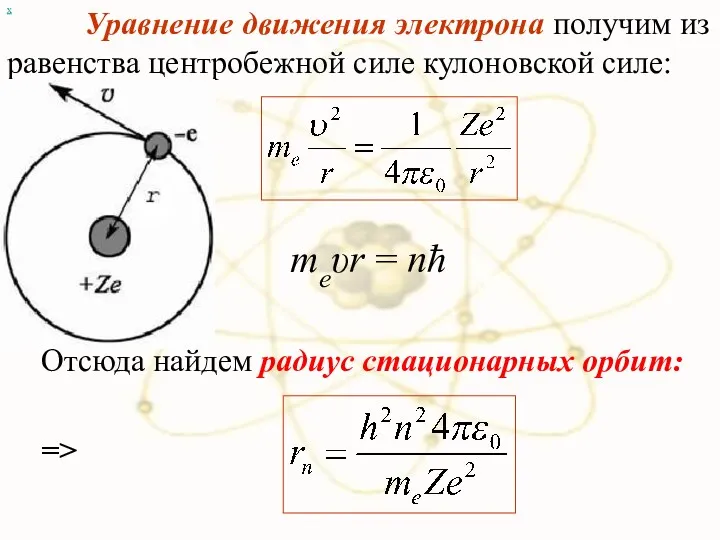
- 53. х Уравнение движения электрона получим из равенства центробежной силе кулоновской силе: => Отсюда найдем радиус стационарных
- 54. Радиус первой орбиты водородного атома называют Боровским радиусом: При n =1, Z = 1 для водорода
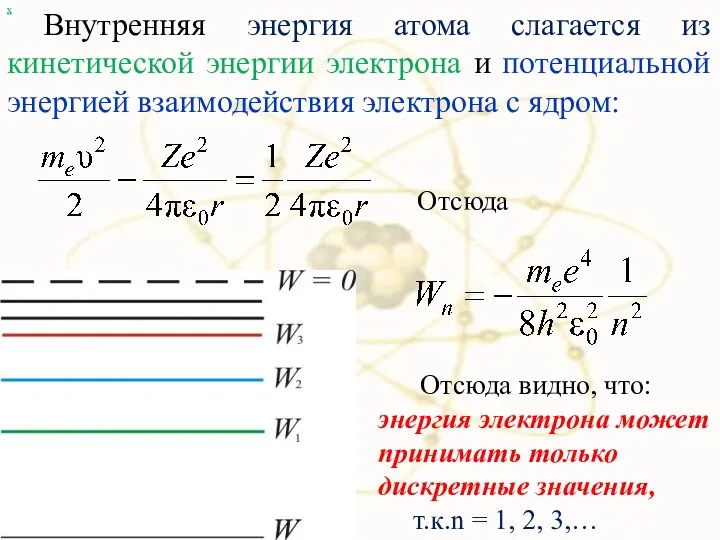
- 55. Внутренняя энергия атома слагается из кинетической энергии электрона и потенциальной энергией взаимодействия электрона с ядром: х
- 56. х Видимая область Инфракрасная обл. Ультрафиолетовая обл.
- 57. При переходе электрона в атоме водорода из состояния n в состояние k излучается фотон с энергией
- 58. Серьезным успехом теории Бора явилось: вычисление постоянной Ридберга для водородоподобных систем и объяснение структуры их линейчатых
- 59. 400 500 600 n 2 3 4 6 , нм
- 61. Бор теоретически вычислил отношение массы протона к массе электрона mp/me = 1847, это находится в соответствии
- 62. х Однако наряду с успехами в теории Бора с самого начала обнаружились существенные недостатки. Главнейшее –
- 63. х Стало ясно, что теория Бора является лишь переходным этапом на пути создания более общей и
- 64. Дальнейшее развитие квантовой механики привело к отказу от механической картины движения электрона в поле ядра.
- 65. х 1.4. Опыт Франка и Герца. Существование дискретных энергетических уровней атома и доказательство правильности теории Бора
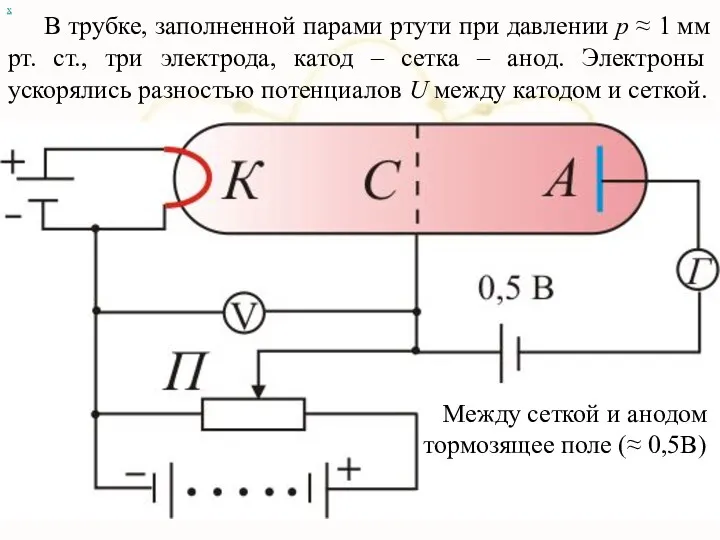
- 66. В трубке, заполненной парами ртути при давлении р ≈ 1 мм рт. ст., три электрода, катод
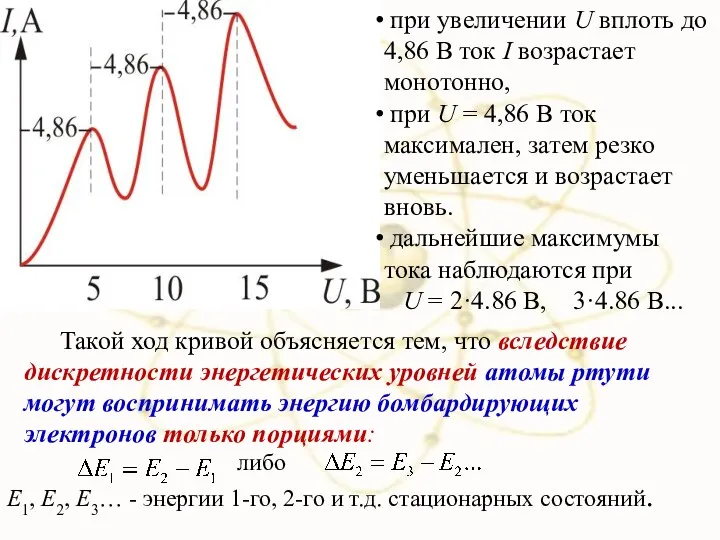
- 67. х Зависимость тока через гальванометр (Г) от разности потенциалов между катодом и сеткой (U): U =
- 68. Такой ход кривой объясняется тем, что вследствие дискретности энергетических уровней атомы ртути могут воспринимать энергию бомбардирующих
- 69. При U энергия электронов меньше ΔЕ1; соударения между электронами и атомами ртути носят упругий характер. При
- 70. Атомы ртути, получившие при соударении с электронами энергию ΔЕ1 и перешедшие в возбужденное состояние, спустя время
- 72. Скачать презентацию














































 Презентация по теме Давление твердых тел
Презентация по теме Давление твердых тел Задачи по квантовой механике
Задачи по квантовой механике Холодильні машини
Холодильні машини Применение интерференции в технике
Применение интерференции в технике Презентация Радиация
Презентация Радиация Сила тяжести. Явление тяготения - презентация к уроку для 8 класса коррекционной школы для детей с ОВЗ
Сила тяжести. Явление тяготения - презентация к уроку для 8 класса коррекционной школы для детей с ОВЗ Действие произвольной возмущающей нагрузки
Действие произвольной возмущающей нагрузки Разработка алгоритмов диагностики электросистем легкового автомобиля
Разработка алгоритмов диагностики электросистем легкового автомобиля Рентгеновское излучение
Рентгеновское излучение Метод Годунова для численного моделирования газодинамических течений
Метод Годунова для численного моделирования газодинамических течений Статические свойства атомных ядер. Ядерные модели
Статические свойства атомных ядер. Ядерные модели Презентация по физике на тему В мире звуков
Презентация по физике на тему В мире звуков Философские проблемы науки и техники. Наука, ее сущность и особенности возникновения. (Лекции 1-2)
Философские проблемы науки и техники. Наука, ее сущность и особенности возникновения. (Лекции 1-2) Математические модели процессов тепломассообмена
Математические модели процессов тепломассообмена Принцип действия тепловых двигателей КПД. Урок № 35. 10 класс
Принцип действия тепловых двигателей КПД. Урок № 35. 10 класс Внеклассное мероприятие Физика вокруг нас.
Внеклассное мероприятие Физика вокруг нас. Движение заряженных частиц в магнитном поле
Движение заряженных частиц в магнитном поле Кипение. Влажность воздуха. Способы определения влажности воздуха
Кипение. Влажность воздуха. Способы определения влажности воздуха Жұдырықшалы механизмдерді жіктеу
Жұдырықшалы механизмдерді жіктеу Превращение энергии. (Окружающий мир, 3 класс)
Превращение энергии. (Окружающий мир, 3 класс) Устройство тормозной системы автомобиля
Устройство тормозной системы автомобиля Подготовка к ЕГЭ и ГИА по физике (вариант 1, задания 13-32)
Подготовка к ЕГЭ и ГИА по физике (вариант 1, задания 13-32) Рентгеновские аппараты. Цифровые рентгенодиагностические комплексы. (Лекция 10)
Рентгеновские аппараты. Цифровые рентгенодиагностические комплексы. (Лекция 10) Элементы ядерной физики
Элементы ядерной физики Давление. Урок повторения и обобщения. 7 класс
Давление. Урок повторения и обобщения. 7 класс физика в сказках
физика в сказках Исследовательское проектирование прибрежных волноэнергетических систем
Исследовательское проектирование прибрежных волноэнергетических систем Неделя физики: Физика в мультфильмах
Неделя физики: Физика в мультфильмах