Содержание
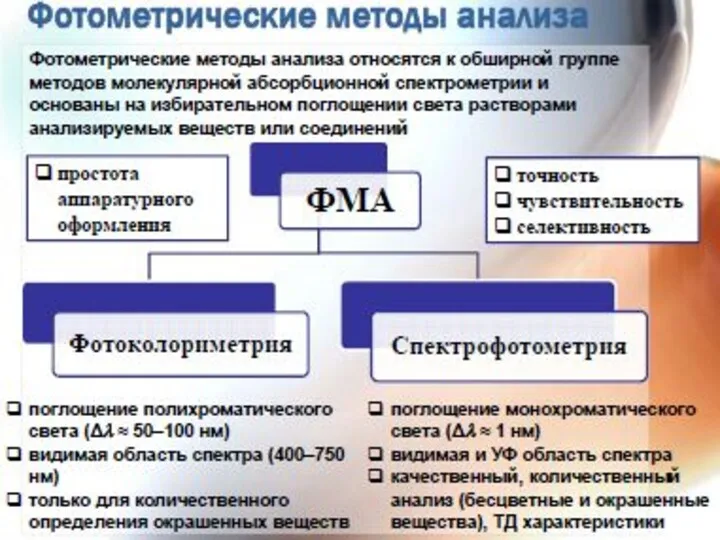
- 4. Методы абсорбционного оптического анализа Атомно- абсорбционный (фотометрия пламени, ААС) Молекулярный абсорбционный (поглощения света молекулами / ионами
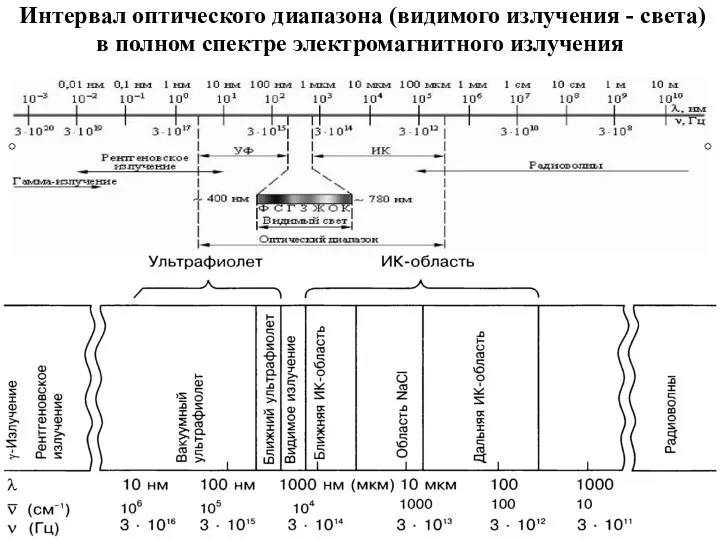
- 8. Интервал оптического диапазона (видимого излучения - света) в полном спектре электромагнитного излучения
- 9. Диапазоны оптического излучения
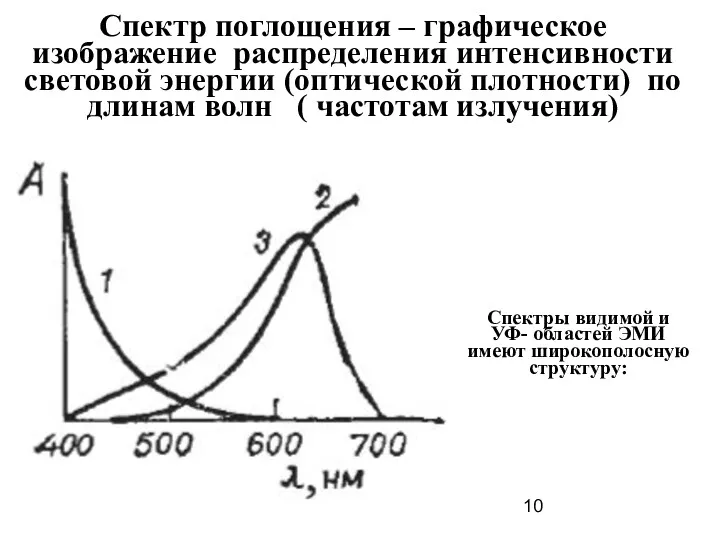
- 10. Спектр поглощения – графическое изображение распределения интенсивности световой энергии (оптической плотности) по длинам волн ( частотам
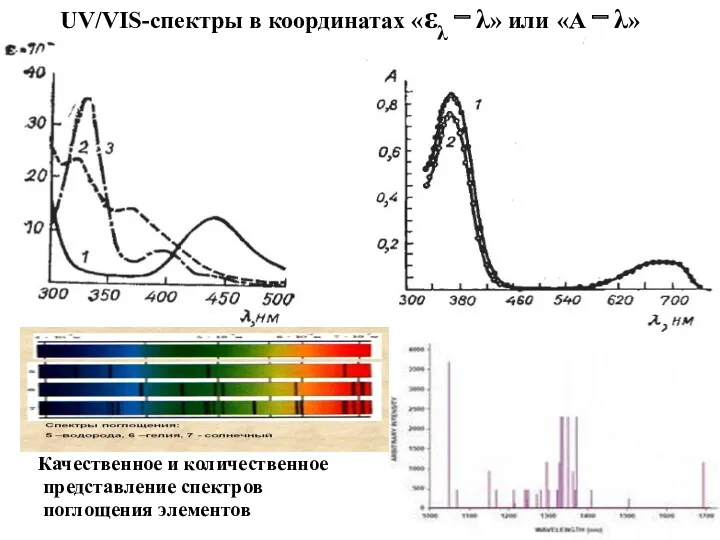
- 11. UV/VIS-спектры в координатах «ελ − λ» или «А − λ» Качественное и количественное представление спектров поглощения
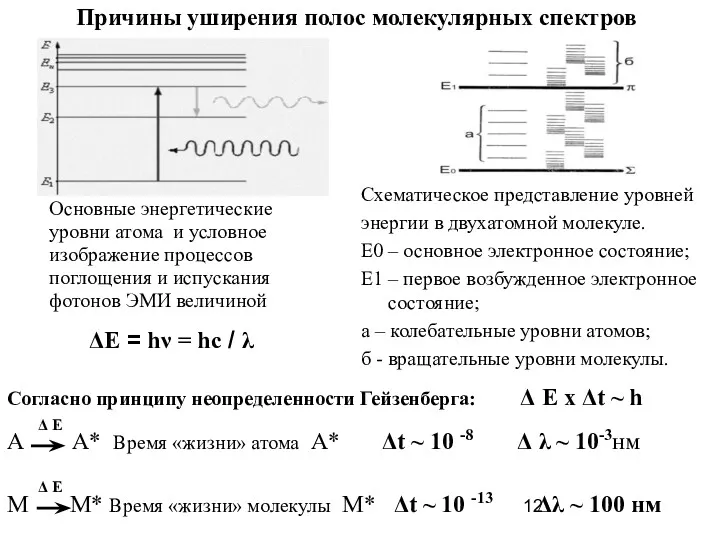
- 12. Согласно принципу неопределенности Гейзенберга: Δ E x Δt ~ h А А* Время «жизни» атома А*
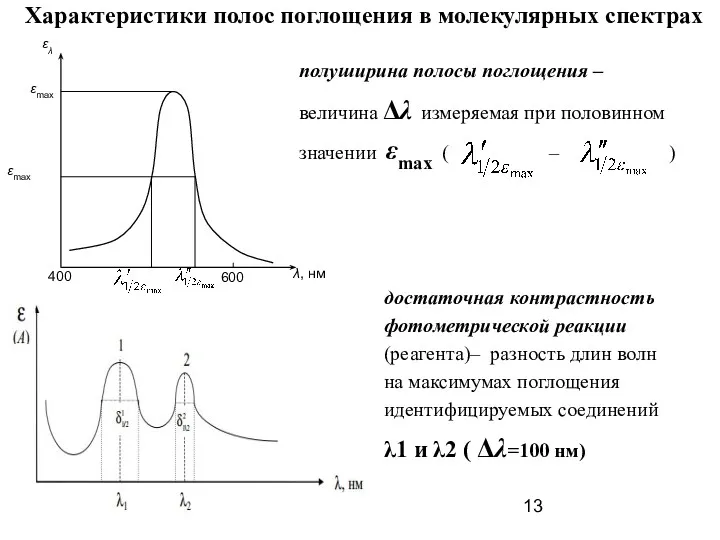
- 13. Характеристики полос поглощения в молекулярных спектрах достаточная контрастность фотометрической реакции (реагента)– разность длин волн на максимумах
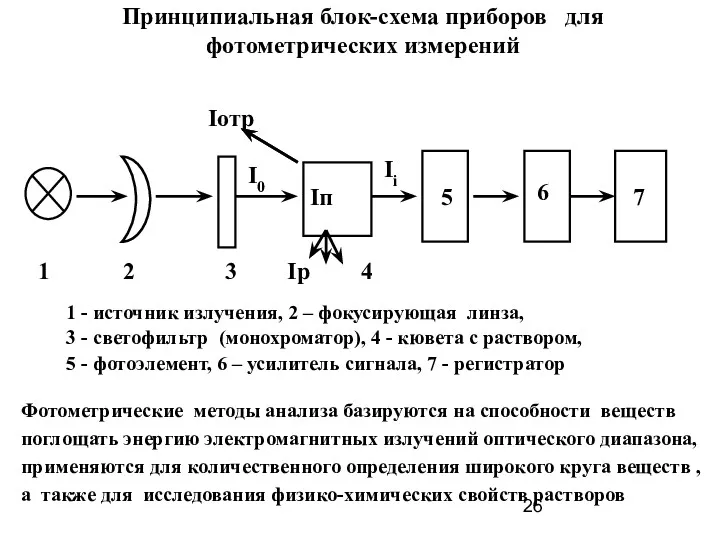
- 26. Принципиальная блок-схема приборов для фотометрических измерений 1 - источник излучения, 2 – фокусирующая линза, 3 -
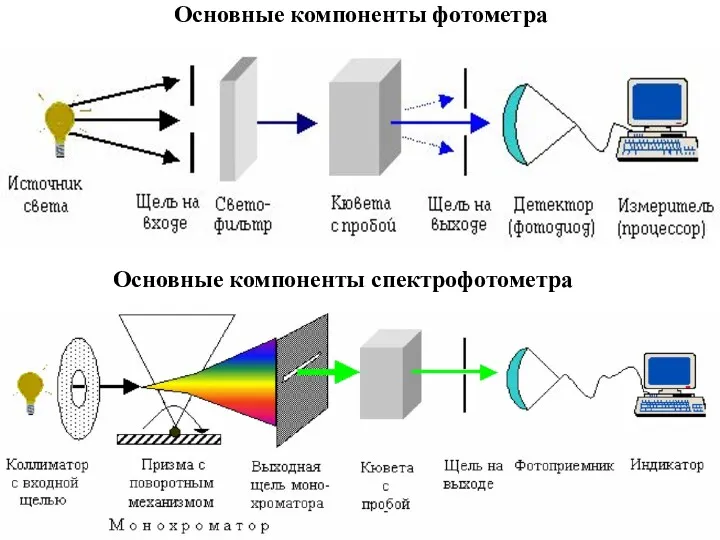
- 27. Основные компоненты фотометра Основные компоненты спектрофотометра
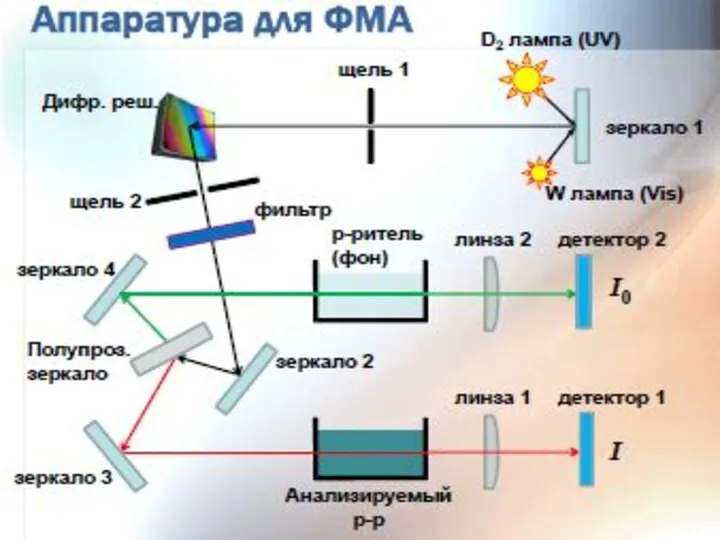
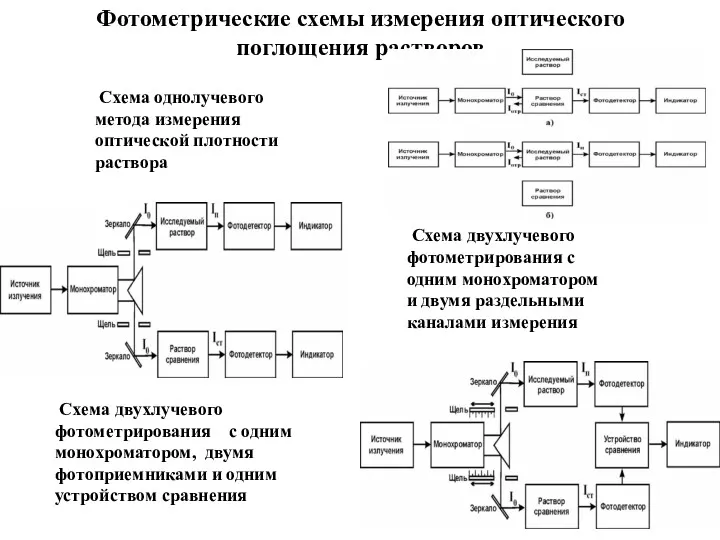
- 29. Фотометрические схемы измерения оптического поглощения растворов Схема однолучевого метода измерения оптической плотности раствора Схема двухлучевого фотометрирования
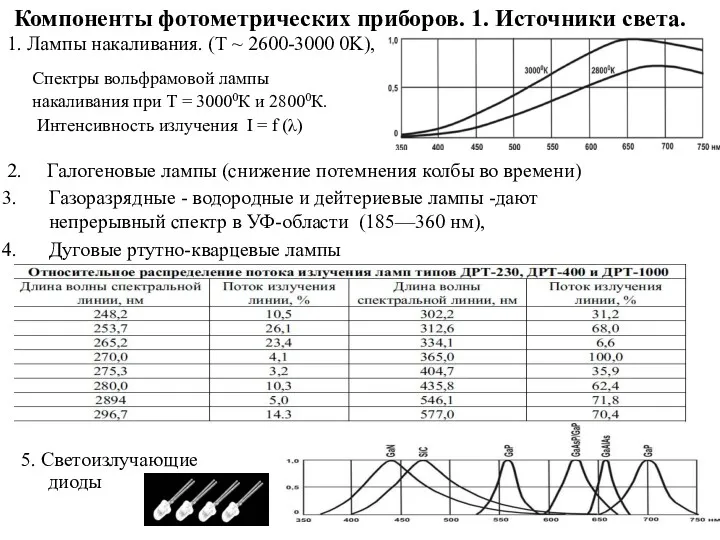
- 30. Компоненты фотометрических приборов. 1. Источники света. 1. Лампы накаливания. (T ~ 2600-3000 0K), Спектры вольфрамовой лампы
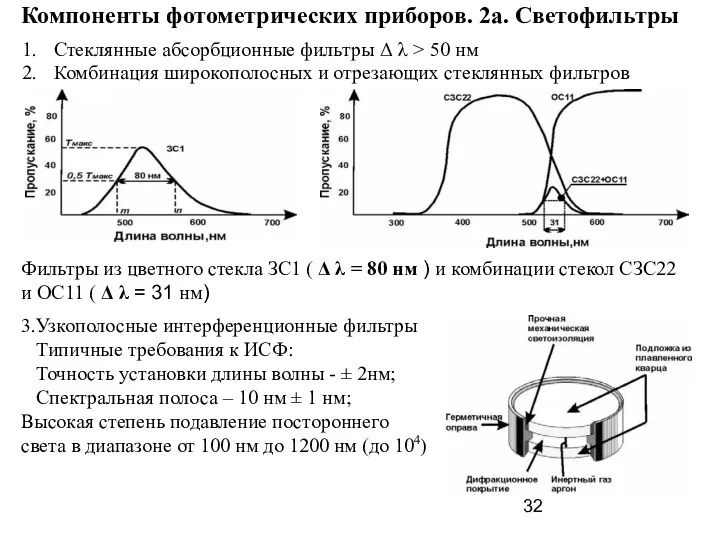
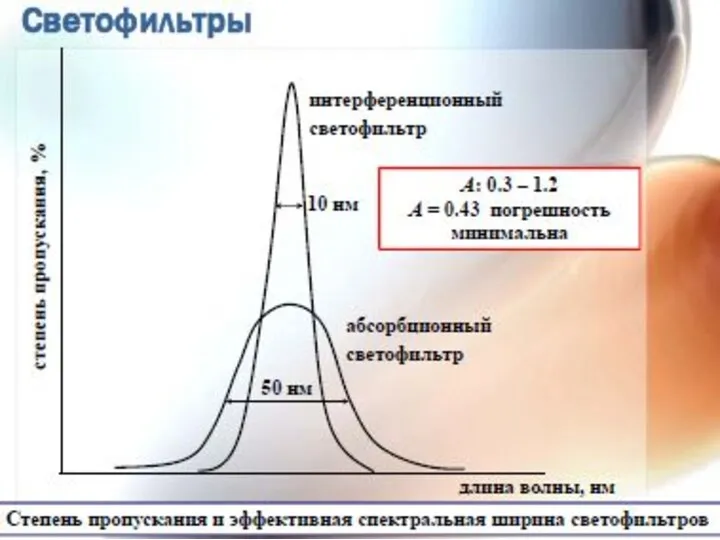
- 32. Стеклянные абсорбционные фильтры Δ λ > 50 нм Комбинация широкополосных и отрезающих стеклянных фильтров Компоненты фотометрических
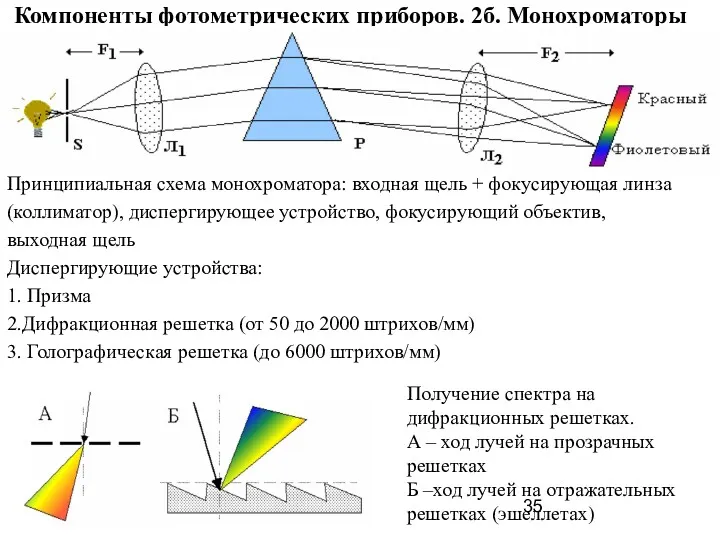
- 35. авщзвшвзшап Компоненты фотометрических приборов. 2б. Монохроматоры Принципиальная схема монохроматора: входная щель + фокусирующая линза (коллиматор), диспергирующее
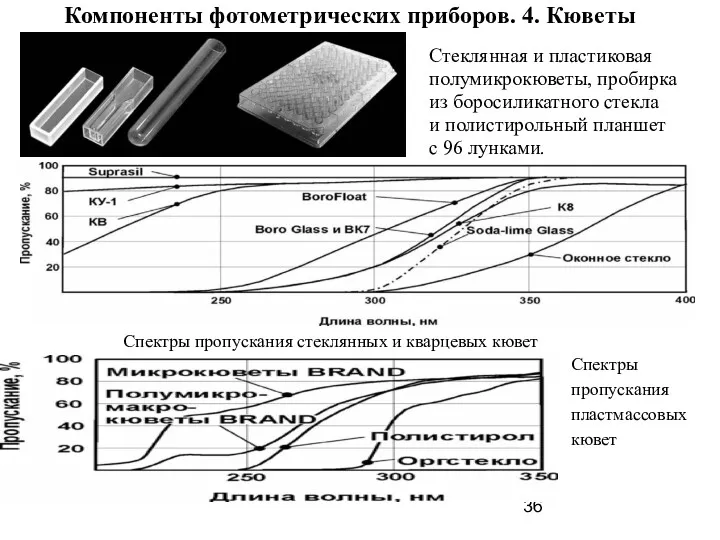
- 36. Стеклянная и пластиковая полумикрокюветы, пробирка из боросиликатного стекла и полистирольный планшет с 96 лунками. Компоненты фотометрических
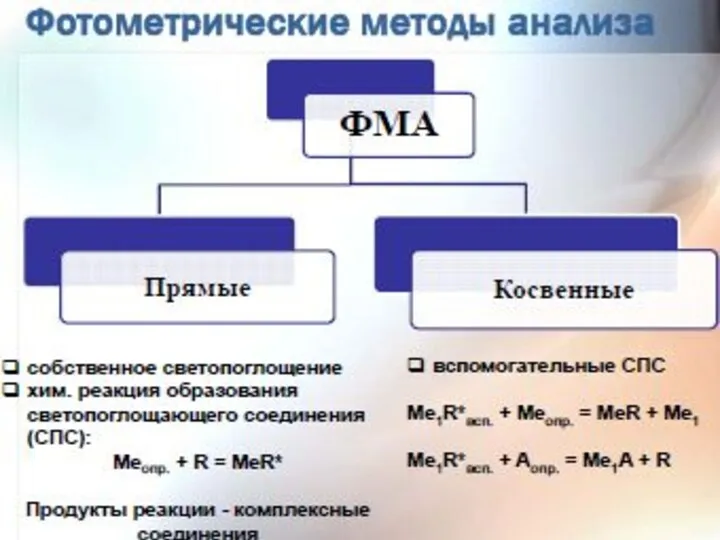
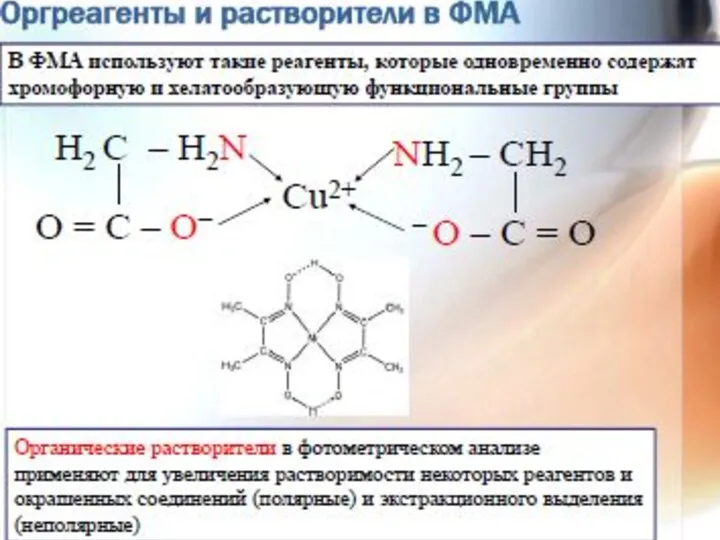
- 37. Методики фотометрических измерений Прямые фотометрические измерения - соединения, обладающие собственным поглощением соединения металлов , образующие светопоглощающие
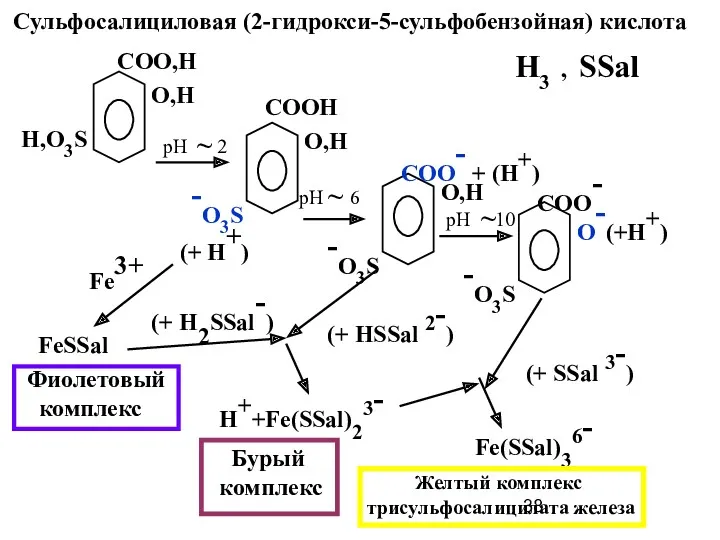
- 38. Сульфосалициловая (2-гидрокси-5-сульфобензойная) кислота СОО,Н Н,О3S О,Н -О3S (+ Н+) СООН О,Н рН ~ 6 -О3S СОО-
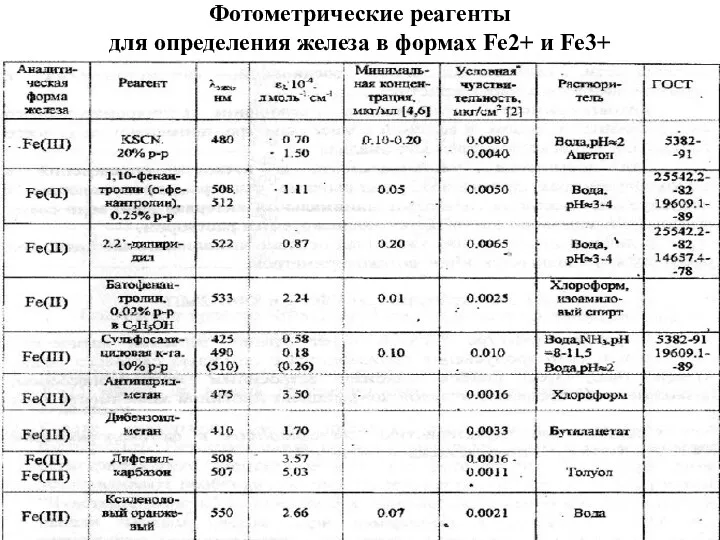
- 39. Фотометрические реагенты для определения железа в формах Fe2+ и Fe3+
- 43. Скачать презентацию















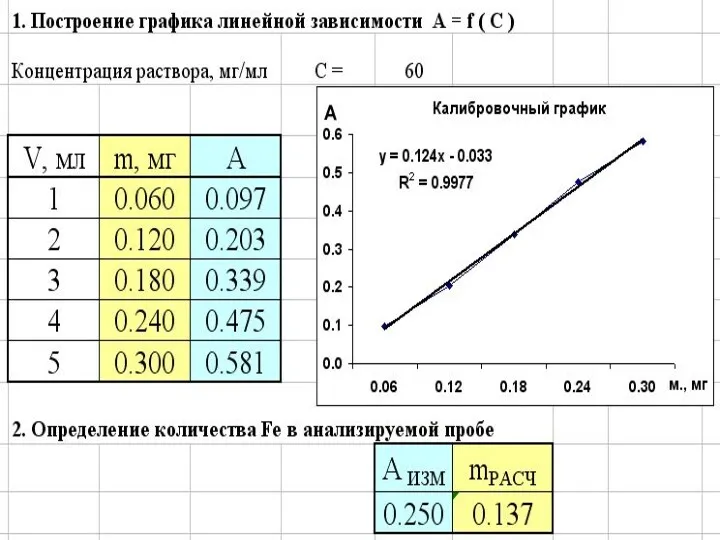
 Закон сохранения и превращения механической энергии
Закон сохранения и превращения механической энергии Тектоника плит
Тектоника плит Электрический ток. Действия электрического тока
Электрический ток. Действия электрического тока Инфракрасная Фурье - спектроскопия
Инфракрасная Фурье - спектроскопия Рулевое управление. Назначение и основные части рулевого управления
Рулевое управление. Назначение и основные части рулевого управления Методическая разработка урока Диффузия 7 класс, презентация
Методическая разработка урока Диффузия 7 класс, презентация Радіоактивні перетворення
Радіоактивні перетворення Электролиз
Электролиз Основные понятия сопромата. Лекция 1
Основные понятия сопромата. Лекция 1 Средства механизации строительства
Средства механизации строительства Тепловое излучение. Фотон. Внешний фотоэффект. Лекция № 5
Тепловое излучение. Фотон. Внешний фотоэффект. Лекция № 5 Поршневые кольца
Поршневые кольца Экспериментальные методы исследования частиц
Экспериментальные методы исследования частиц Спектр атома водорода. (Лекция 7а)
Спектр атома водорода. (Лекция 7а) Презентация к уроку Количество теплоты, удельная теплоёмкость
Презентация к уроку Количество теплоты, удельная теплоёмкость 175678a84a142c1939e5ca3e409e1bc1
175678a84a142c1939e5ca3e409e1bc1 ТО и ремонт системы питания двигателя автомобиля УРАЛ-NEXT
ТО и ремонт системы питания двигателя автомобиля УРАЛ-NEXT Математическое моделирование и численное исследование актуальных проблем физики плазмы
Математическое моделирование и численное исследование актуальных проблем физики плазмы Ремонт и хранение бронетанкового вооружения и техники. Возможные неисправности трансмиссии. (Занятие 6)
Ремонт и хранение бронетанкового вооружения и техники. Возможные неисправности трансмиссии. (Занятие 6) Основные понятия об усталости металлов. Предел выносливости
Основные понятия об усталости металлов. Предел выносливости Радиоактивность. Урок физики 11 класс
Радиоактивность. Урок физики 11 класс Физический вечер 8кл
Физический вечер 8кл Перемещения при изгибе
Перемещения при изгибе Сила трения
Сила трения Формирование ключевых компетенций при решении творческих задач на уроках физики
Формирование ключевых компетенций при решении творческих задач на уроках физики Расчёт статически неопределимой рамы методом перемещений
Расчёт статически неопределимой рамы методом перемещений Элементы квантовой механики и физики атомов, молекул, твердых тел. Лекция № 3
Элементы квантовой механики и физики атомов, молекул, твердых тел. Лекция № 3 Оптические волокна
Оптические волокна