Содержание
- 2. Цель урока: расширить знания о процессе растворения и растворах.
- 3. Задачи: Познакомить с растворением, как с физико-химическим процессом. Дать классификацию растворов по признаку растворимости. Сформировать понятия:
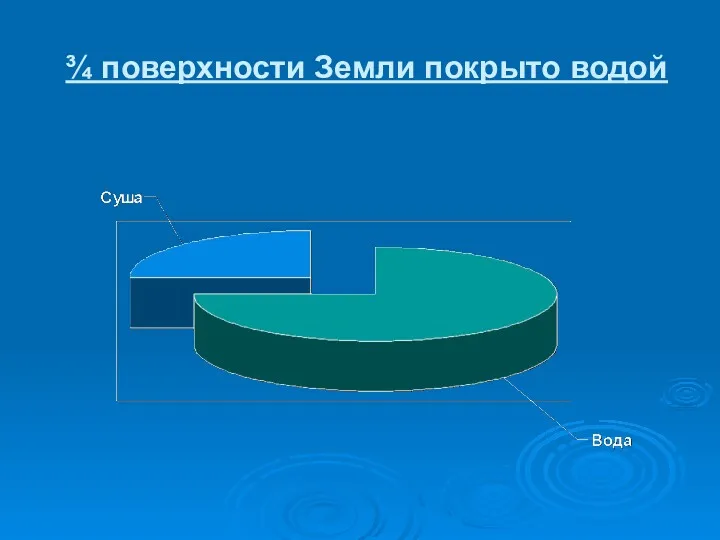
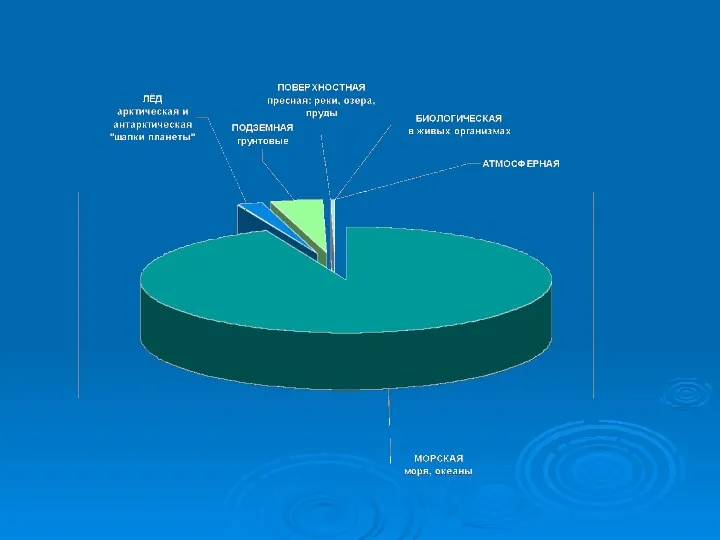
- 4. ¾ поверхности Земли покрыто водой
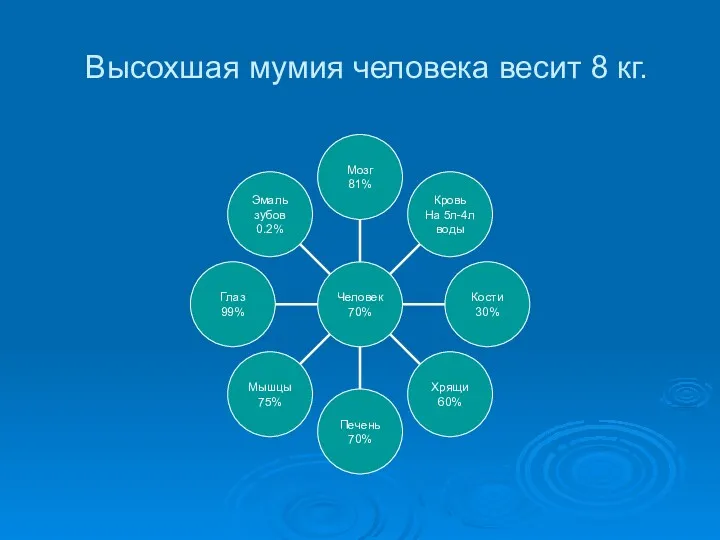
- 6. Высохшая мумия человека весит 8 кг.
- 8. Растворение Физический процесс – результат диффузии веществ Химический процесс –взаимодействие вещества с водой и образование гидратов
- 9. Растворимость - - Способность вещества образовывать с другими веществами (растворителями) однородные системы – растворы
- 10. Факторы влияющие на растворимость веществ 1 группа: природа растворенного вещества 2 группа: природа растворителя 3 группа:
- 11. Природа растворенного вещества Вещества хорошо растворимые (в 100г H2O больше 1г вещества) нерастворимые (в 100г H2O
- 12. Зависимость растворимости веществ от природы растворителя Растворение медного купороса в воде Растворение медного купороса в спирте
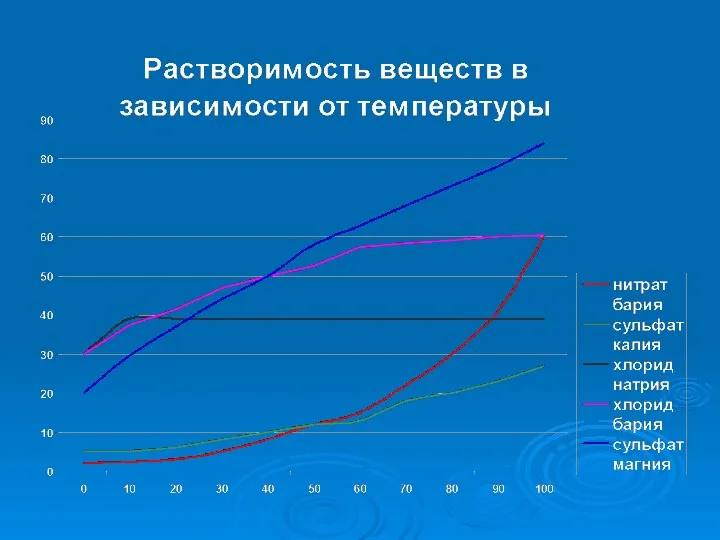
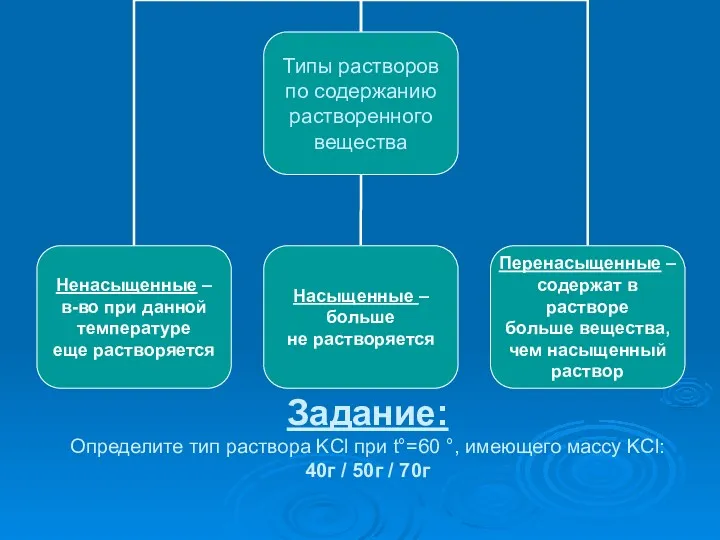
- 14. Задание: Определите тип раствора KCl при t°=60 °, имеющего массу KCl: 40г / 50г / 70г
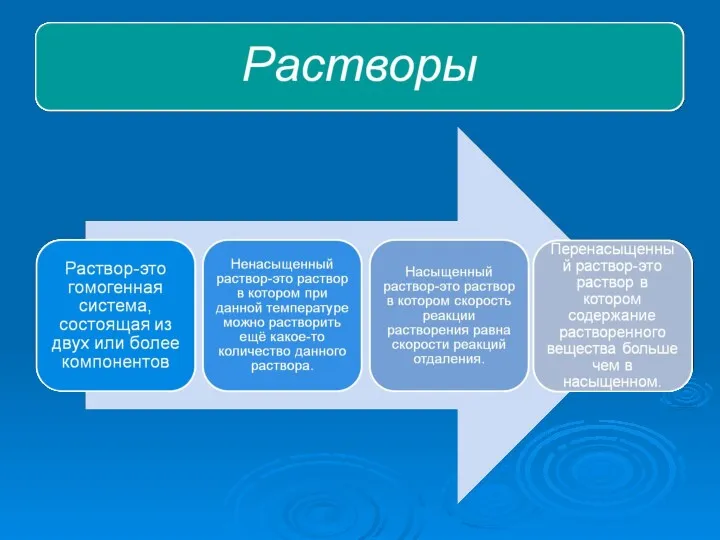
- 15. Классификация растворов по признаку растворимости Ненасыщенный раствор: при данной температуре находится меньше растворяемого вещества, чем в
- 16. Применение растворов в промышленности
- 17. Применение растворов в сельском хозяйстве
- 18. Применение растворов в быту и медицине
- 19. УСТНЫЙ ОПРОС: Что такое раствор? Из чего он состоит? Дайте определение растворимости. Перечислите признаки химического взаимодействия
- 20. Ответьте на вопросы : 1. От чего не зависит растворимость твердых веществ? А) от природы растворителя
- 22. Скачать презентацию













 Турнир Юных Физиков 2015
Турнир Юных Физиков 2015 Резка тонколистового металла и проволоки
Резка тонколистового металла и проволоки Механические колебания и волны. Акустика
Механические колебания и волны. Акустика Композиты - древний материал будущего
Композиты - древний материал будущего Плавание тел в жидкости
Плавание тел в жидкости Фрезерные станки. (Тема 6)
Фрезерные станки. (Тема 6) Трудности расчета турбулентных потоков (неустойчивость процессов)
Трудности расчета турбулентных потоков (неустойчивость процессов) Мыльные пузыри. Учебный проект по физике
Мыльные пузыри. Учебный проект по физике Способы соединения жил кабелей
Способы соединения жил кабелей Линзы. Ход лучей в линзах.
Линзы. Ход лучей в линзах. Дифференциал
Дифференциал Инженерно-авиационное обеспечение безопасности полётов. Тема 12
Инженерно-авиационное обеспечение безопасности полётов. Тема 12 Способ установки фаркопа для легковых автомобилей категории М1 и его сертификация
Способ установки фаркопа для легковых автомобилей категории М1 и его сертификация Предмет физики и её связь с другими науками
Предмет физики и её связь с другими науками Расчет потенциалов простейших электростатических полей
Расчет потенциалов простейших электростатических полей Итоги работы опытной путевой машинной станции № 103 Московской дирекции по ремонту пути
Итоги работы опытной путевой машинной станции № 103 Московской дирекции по ремонту пути Теплоизоляция домов
Теплоизоляция домов Jets in flight
Jets in flight 61f4bb8105f047b8922e06e3e916ed53
61f4bb8105f047b8922e06e3e916ed53 Тербелістер мен толқындар
Тербелістер мен толқындар Молекулярная физика. Тепловые явления. Уравнение состояния идеального газа. Газовые законы
Молекулярная физика. Тепловые явления. Уравнение состояния идеального газа. Газовые законы Урок-презентация по физике 8 класс на тему Молния
Урок-презентация по физике 8 класс на тему Молния Сборка электромагнита и испытание его действия. Лабораторная работа
Сборка электромагнита и испытание его действия. Лабораторная работа Методы электрофизической и электрохимической обработки поверхностей заготовок
Методы электрофизической и электрохимической обработки поверхностей заготовок В мире электричества.
В мире электричества. Инфракрасное, ультрафиолетовое и рентгеновское излучения. Их свойства и применение
Инфракрасное, ультрафиолетовое и рентгеновское излучения. Их свойства и применение История лампы накаливания
История лампы накаливания Электрические явления. Законы постоянного тока
Электрические явления. Законы постоянного тока