Содержание
- 2. Любая термодинамическая система стремиться уменьшить свою поверхностную энергию. Избыточная поверхностная энергия может уменьшиться за счет: уменьшения
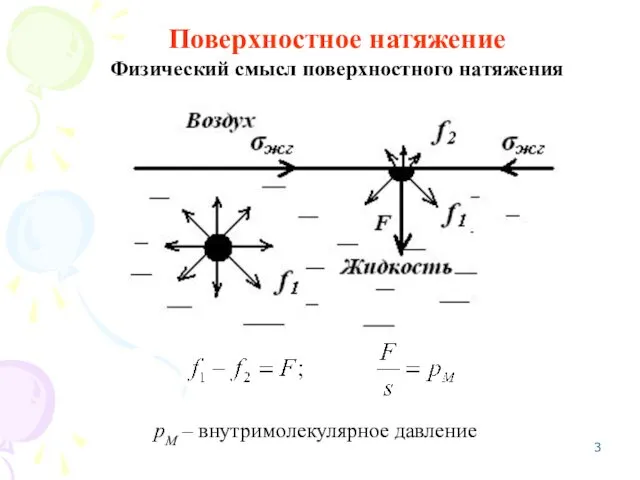
- 3. Поверхностное натяжение Физический смысл поверхностного натяжения рМ – внутримолекулярное давление
- 4. Энергетическое определение поверхностного натяжения Поверхностное натяжение (σ) – работа обратимого изотермического процесса, затраченная на образование единицы
- 5. Термодинамическое определение поверхностного натяжения При постоянных Т, р, ni, q имеем: Поверхностное натяжение - частная производная
- 6. Единицы измерения поверхностного натяжения Энергетическая единица измерения – Дж/м2, силовая – Н/м. Для воды при 293
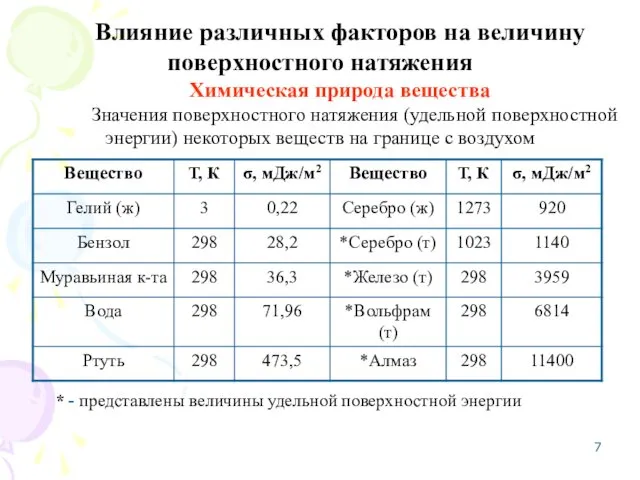
- 7. Влияние различных факторов на величину поверхностного натяжения Химическая природа вещества Значения поверхностного натяжения (удельной поверхностной энергии)
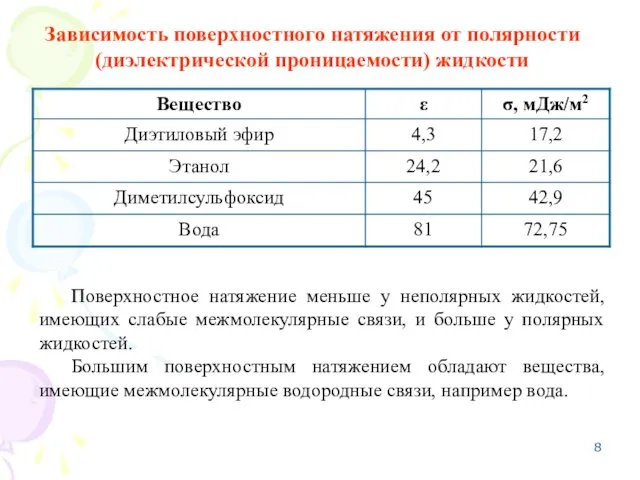
- 8. Зависимость поверхностного натяжения от полярности (диэлектрической проницаемости) жидкости Поверхностное натяжение меньше у неполярных жидкостей, имеющих слабые
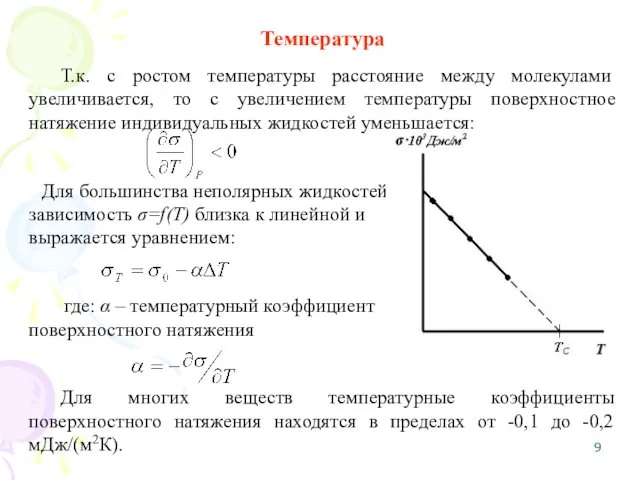
- 9. Температура Т.к. с ростом температуры расстояние между молекулами увеличивается, то с увеличением температуры поверхностное натяжение индивидуальных
- 10. Природа граничащих фаз Поверхностное натяжение на границе двух жидкостей зависит от их химической природы (полярности). Межфазное
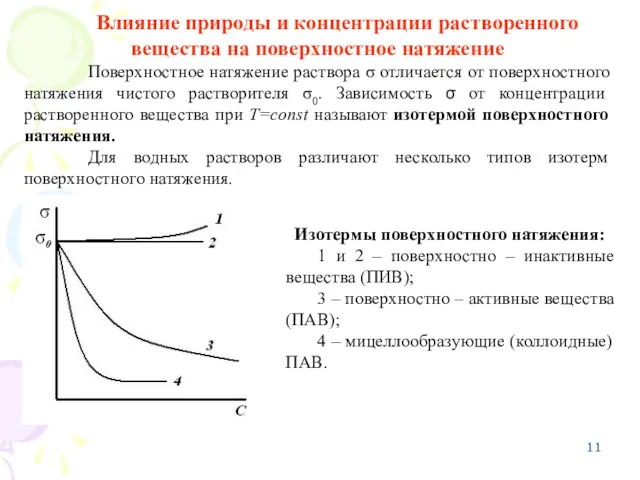
- 11. Влияние природы и концентрации растворенного вещества на поверхностное натяжение Поверхностное натяжение раствора σ отличается от поверхностного
- 12. Межмолекулярные и межфазные взаимодействия
- 13. Когезия Когезия – притяжение атомов или молекул внутри отдельной фазы, обусловленное межмолекулярными и межатомными взаимодействиями различной
- 14. Адгезия Адгезия – взаимодействие между разнородными конденсированными телами при их молекулярном контакте. Причина адгезии – молекулярное
- 15. Растекание одной жидкости по поверхности другой Правило Гаркинса - растекание одной жидкости по поверхности другой происходит,
- 16. Смачивание Смачивание (адгезия жидкости) – взаимодействие жидкости с твердым или другим жидким телом при наличии одновременного
- 17. Анализ уравнения Юнга 1. Если σТГ> σТЖ, то cos θ > 0, θ 2. Если σТГ
- 18. Правило: лучше смачивает поверхность та жидкость, которая ближе по полярности к смачиваемому материалу. По виду избирательного
- 19. Связь краевого угла смачивания с работой адгезии WA= σТГ+ σЖГ – σТЖ уравнение Дюпре. Отсюда: σ
- 20. Влияние шероховатости на смачивание Поверхность реальных твердых тел шероховатая: Sш > Sгл смачивание (cos θ >
- 21. Флотация Флотация - метод обогащения полезных ископаемых, основанное на их различной смачиваемости (этим методом обогащается около
- 22. Особенности искривленной поверхности раздела фаз
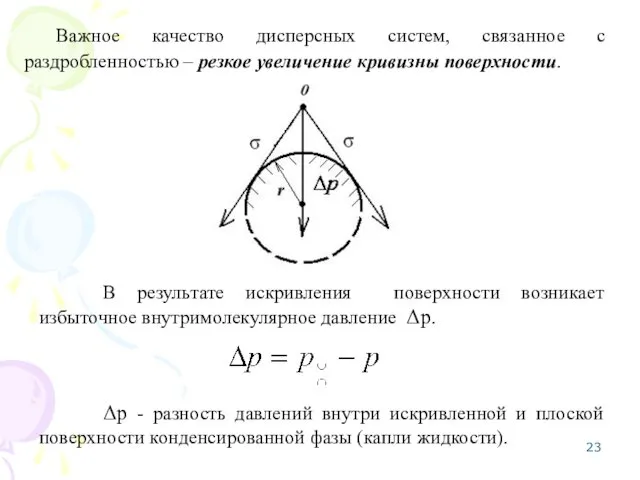
- 23. Важное качество дисперсных систем, связанное с раздробленностью – резкое увеличение кривизны поверхности. В результате искривления поверхности
- 24. Уравнение Лапласа (вывод) В результате искривления поверхности совершается работа δW, которая приводит к изменению объема тела
- 25. Для сферических частиц: Для частиц цилиндрической формы: Для частиц произвольной формы: уравнения Лапласа
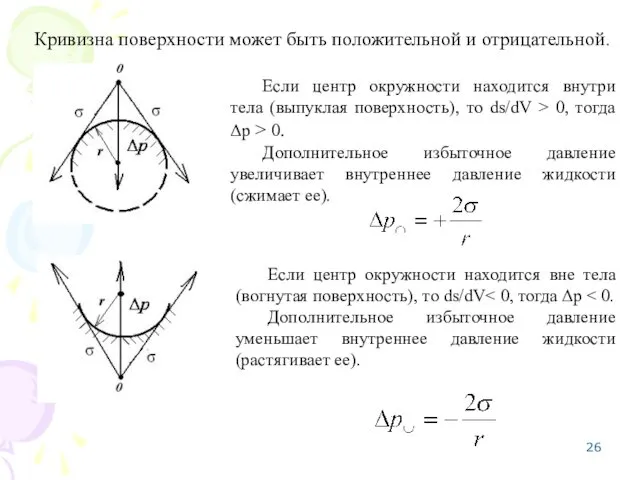
- 26. Кривизна поверхности может быть положительной и отрицательной. Если центр окружности находится внутри тела (выпуклая поверхность), то
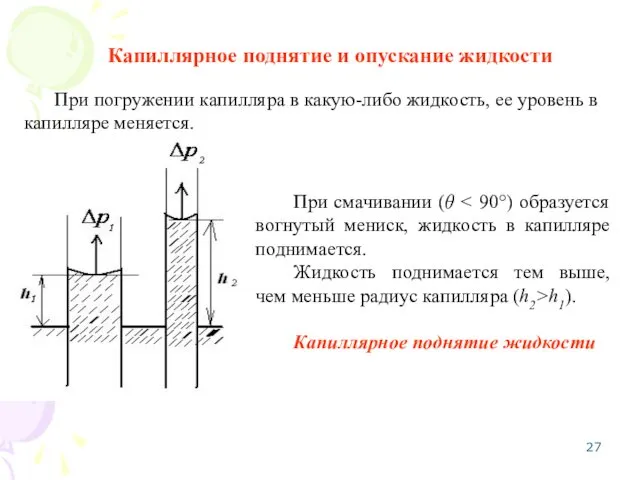
- 27. Капиллярное поднятие и опускание жидкости При смачивании (θ Жидкость поднимается тем выше, чем меньше радиус капилляра
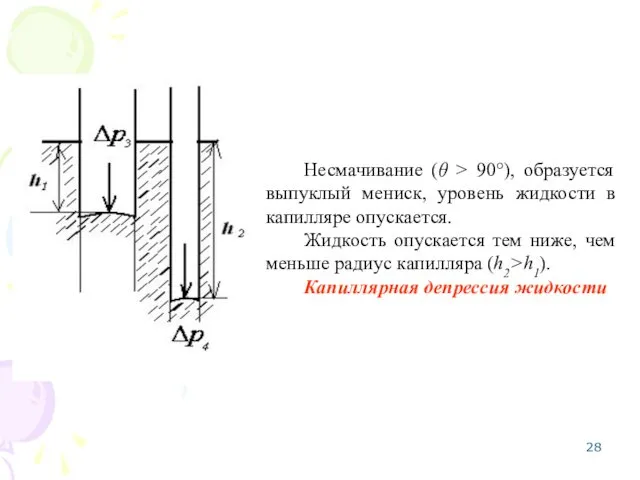
- 28. Несмачивание (θ > 90°), образуется выпуклый мениск, уровень жидкости в капилляре опускается. Жидкость опускается тем ниже,
- 29. При равновесии избыточное лапласовское давление равно гидростатическому давлению столба жидкости высотой h: , отсюда Высоту капиллярного
- 30. Капиллярным поднятием жидкостей объясняется ряд известных процессов и явлений: поднятие грунтовых вод в почвах обеспечивает существование
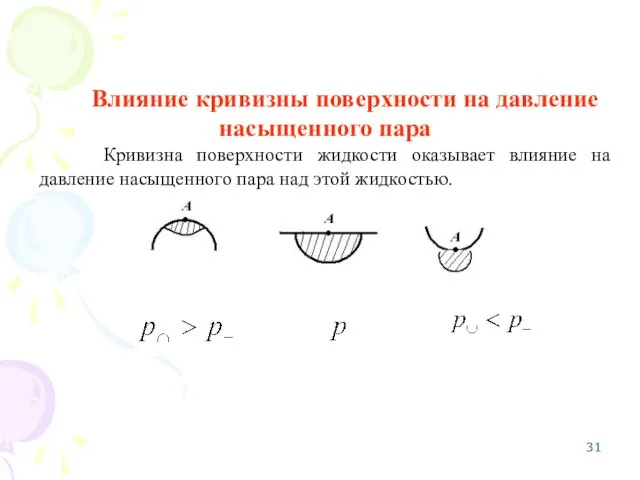
- 31. Влияние кривизны поверхности на давление насыщенного пара Кривизна поверхности жидкости оказывает влияние на давление насыщенного пара
- 32. Уравнения Томсона – Кельвина (вывод) Приращение энергии Гиббса в результате искривления поверхности: При T=const для индивидуального
- 33. С другой стороны в процессе испарения (Т=const) в случае искривленной поверхности: Или в интегральной форме: Приравняем
- 34. Для сферической поверхности: Аналогично, для цилиндрической поверхности: Уравнения Томсона – Кельвина
- 35. Капиллярная конденсация При отрицательной кривизне (вогнутая поверхность), давление насыщенного пара будет меньше чем над плоской: С
- 36. Изотермическая перегонка При положительной кривизне (выпуклая поверхность) давление насыщенного пара будет больше, чем над плоской поверхностью:
- 37. Влияние дисперсности (кривизны поверхности) на различные физико-химические процессы 1. Влияние дисперсности на реакционную способность веществ Реакционная
- 38. 2. Связь дисперсности с константой равновесия Степень дисперсности вещества влияет на равновесие химической реакции. Изменение энергии
- 39. 3. Влияние дисперсности на температуру фазовых переходов С изменением дисперсности меняется температура фазового перехода веществ. При
- 40. Заменим: на Тогда получим: где: ΔТ - изменение температуры при фазовом переходе при диспергировании. Из уравнения
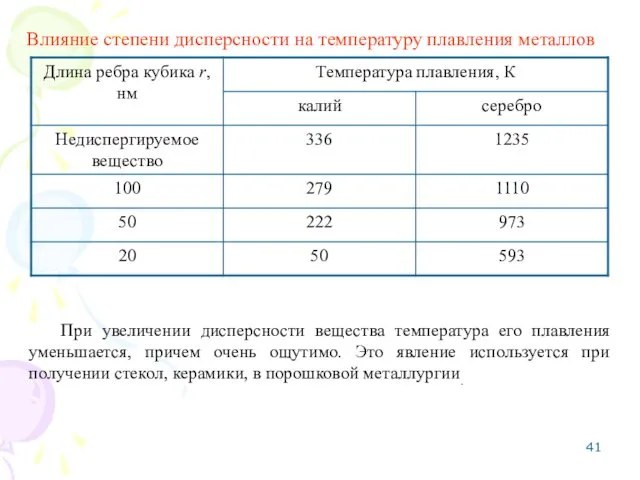
- 41. Влияние степени дисперсности на температуру плавления металлов При увеличении дисперсности вещества температура его плавления уменьшается, причем
- 42. Методы определения поверхностного натяжения Методы бывают: динамические и статические. Метод наибольшего давления пузырька газа (метод Ребиндера)
- 43. Сталагмометрический метод (метод счета капель) При вытекании жидкости из капилляра сталагмометра вес образующейся капли в момент
- 45. Скачать презентацию































 Сварочные тележки
Сварочные тележки Учебно-методическое пособие Тесты по физике 11 класс
Учебно-методическое пособие Тесты по физике 11 класс Кипение. Влажность воздуха. Способы определения влажности воздуха
Кипение. Влажность воздуха. Способы определения влажности воздуха Простой механизм. Двигатель
Простой механизм. Двигатель Качество электроэнергии
Качество электроэнергии Тербелістер мен толқындар
Тербелістер мен толқындар Урок по физике 8 класс. Обобщение материала по теме: Изменения агрегатных состояний вещества
Урок по физике 8 класс. Обобщение материала по теме: Изменения агрегатных состояний вещества Условные графические обозначения на принципиальных электрических схемах
Условные графические обозначения на принципиальных электрических схемах Рост наноструктур и микроскопия. Методы выращивания наноструктур
Рост наноструктур и микроскопия. Методы выращивания наноструктур презентация Виды теплообмена
презентация Виды теплообмена Электрическая проводимость металлов
Электрическая проводимость металлов Робот-исследователь, способный измерять некоторые физические факторы среды
Робот-исследователь, способный измерять некоторые физические факторы среды Типы приводов
Типы приводов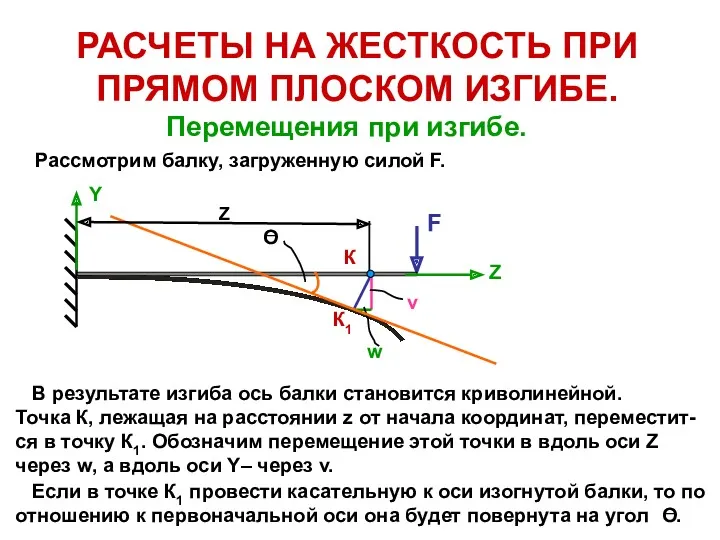 Расчеты на жесткость при прямом плоском изгибе. Перемещения при изгибе
Расчеты на жесткость при прямом плоском изгибе. Перемещения при изгибе Гидростатическое давление. Билет 20. Получение формулы для расчета давления жидкости
Гидростатическое давление. Билет 20. Получение формулы для расчета давления жидкости Моделирование электрофизических свойств gaas методом монте-карло
Моделирование электрофизических свойств gaas методом монте-карло Урок узагальнення та систематизації знань з теми Теплові явища. Розв’язування задач. 8 клас
Урок узагальнення та систематизації знань з теми Теплові явища. Розв’язування задач. 8 клас Основные законы электростатики
Основные законы электростатики Физический диктант (Ядерная физика 9 класс)
Физический диктант (Ядерная физика 9 класс) Использование комплекта Я сдам ЕГЭ для подготовки к экзамену по физике
Использование комплекта Я сдам ЕГЭ для подготовки к экзамену по физике Презентация к уроку в 7 классе по теме Масса тела.Измерение массы тела с помощью весов
Презентация к уроку в 7 классе по теме Масса тела.Измерение массы тела с помощью весов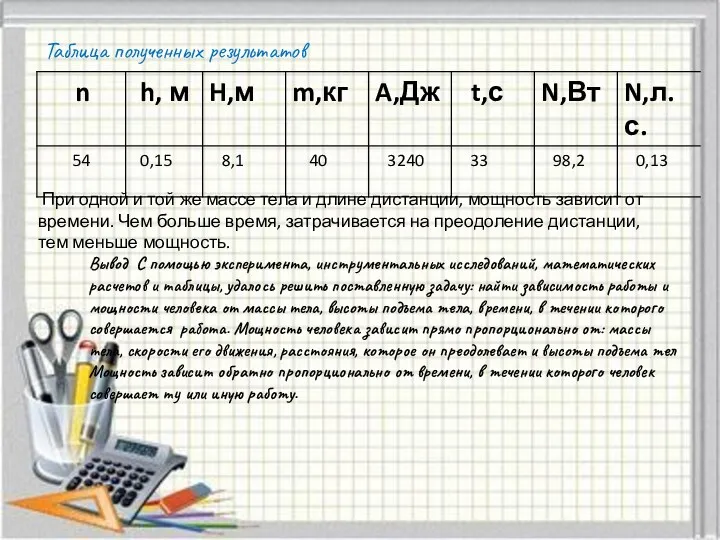 Явление диффузии в жидкостях
Явление диффузии в жидкостях Тұрақты электр тоғы
Тұрақты электр тоғы Исполнительные механизмы и регулирующие органы
Исполнительные механизмы и регулирующие органы Тиск. Результат тиску твердого тіла
Тиск. Результат тиску твердого тіла Топологические изоляторы и смежные вопросы
Топологические изоляторы и смежные вопросы Синтез нанокомпозитных материалов на основе субоксида кремния и наноструктур благородных металлов
Синтез нанокомпозитных материалов на основе субоксида кремния и наноструктур благородных металлов Эксперимент. Что такое эксперимент?
Эксперимент. Что такое эксперимент?