Содержание
- 2. Явления, свидетельствующие о сложной структуре атома. Слово «атом» означает «неделимый». В течение длительного времени атом считался
- 3. Модель атома Томсона В 1903г. Английский физик Джозеф Джон Томсон предложил одну из первых моделей строения
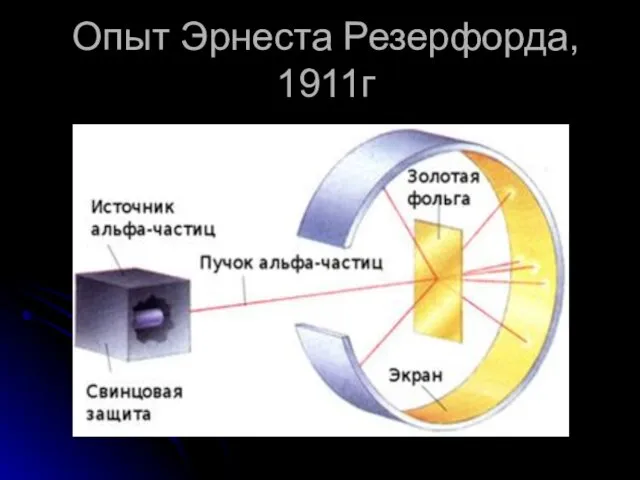
- 4. Опыт Э. Резерфорда по рассеянию альфа – частиц В1911г. Английский ученый Э.Резерфорд провел ряд опытов по
- 5. Опыт Эрнеста Резерфорда, 1911г
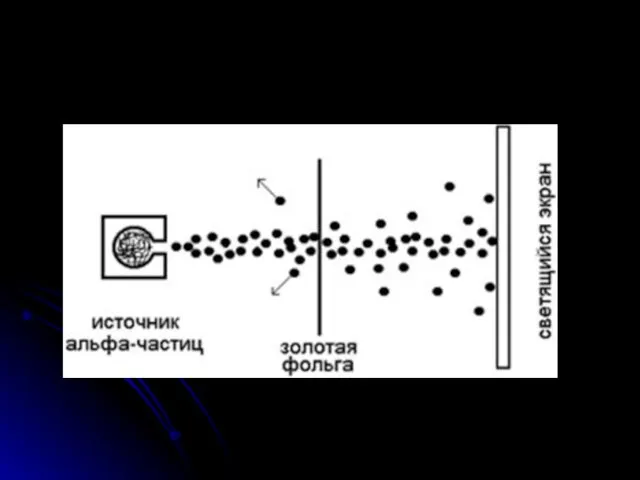
- 7. Результаты опытов Большинство альфа-частиц прошли через тонкую фольгу, почти не изменив своего направления. Небольшое количество альфа-
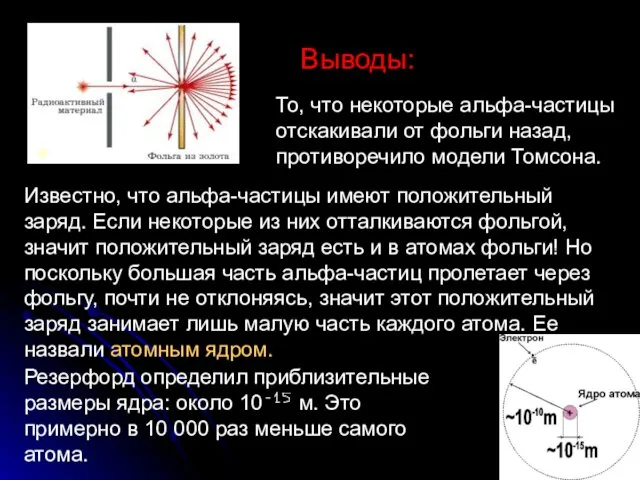
- 8. Выводы: То, что некоторые альфа-частицы отскакивали от фольги назад, противоречило модели Томсона. Известно, что альфа-частицы имеют
- 9. Ядерная (планетарная) модель атома Резерфода Атом имеет в центре ядро, размеры которого во много раз меньше
- 10. Объяснение результатов опыта Резерфорда на основе ядерной модели атома. Так как большую часть атома составляет пустота,
- 11. Планетарная модель строения атома
- 12. Лирическое отступление Вы никогда не думали, что может быть «космос внутри нас»? …а человек в основном
- 13. Чего не сумел объяснить Резерфорд Резерфорд доказал, что электроны обращаются вокруг ядра по круговым орбитам. Но
- 14. Первый постулат Бора Выход из создавшегося противоречия между теоретическими расчетами и практикой был найден в 1913г.
- 15. Нильс Бор ( 1885 – 1962 ) Нильс Бор - датский физик. Создал теорию атома, в
- 16. Второй постулат Бора Электрон может переходить с одной стационарной орбиты на другую. При переходе из стационарного
- 17. Модель атома водорода по Бору. Свои постулаты Бор применил для построения теории простейшей атомной системы –
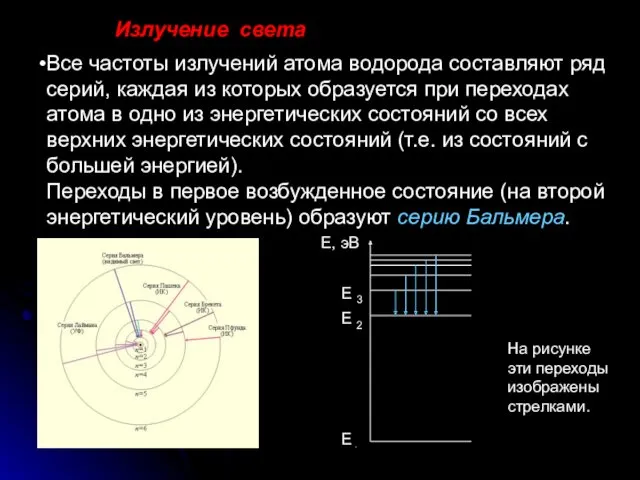
- 18. Все частоты излучений атома водорода составляют ряд серий, каждая из которых образуется при переходах атома в
- 19. Поглощение света Поглощение света – процесс, обратный излучению. Атом, излучая свет, переходит из низших энергетических состояний
- 20. Трудности теории Бора Теория Бора не была логически последовательной. На ее основе не удалось построить количественную
- 21. Значение теории Бора Теория Бора – это первая квантовая теория строения атома, которая послужила толчком к
- 23. 1. Свойства ядерных сил Сил, действующие между нуклонами в ядре. 1) очень велики; 2) короткодействующие (имеют
- 24. 2. Радиоактивность 1) 1896 г. Анри Беккерель, самопроизвольное испускание лучей солями урана. Мария Склодовская – Кюри
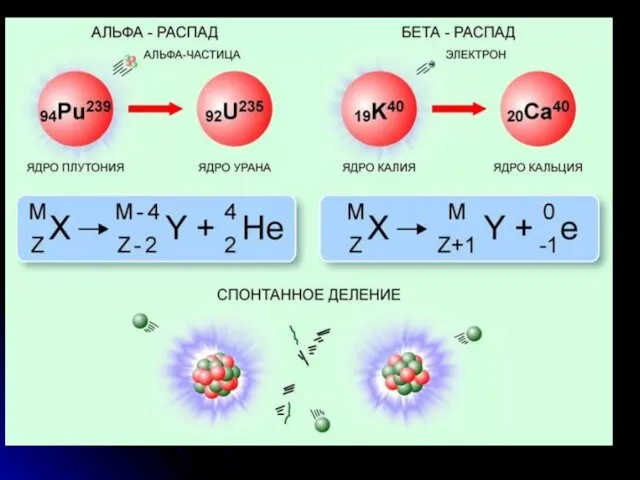
- 25. 3. Радиоактивные превращения 1) α-распад. α-частица – ядро атома гелия 24Не. Правило смещения: Элемент смещается на
- 27. Закон сохранения массового числа и заряда Сумма массовых чисел до распада, равна сумме массовых чисел после
- 28. Закон радиоактивного распада 1) Период полураспада – промежуток времени, в течение которого распадается половина начального числа
- 30. Скачать презентацию






















 Сложение сил. Равнодействующая сил.
Сложение сил. Равнодействующая сил. Поверхностное натяжение. Смачивание. Капиллярные явления
Поверхностное натяжение. Смачивание. Капиллярные явления Электр өрісіндегі диэлектриктер
Электр өрісіндегі диэлектриктер Высота, тембр и громкость звука
Высота, тембр и громкость звука Жарықтың изотропты ортада таралуы
Жарықтың изотропты ортада таралуы Виды теплопередачи. Примеры теплопередачи в природе и технике
Виды теплопередачи. Примеры теплопередачи в природе и технике Кинематический анализ механизмов
Кинематический анализ механизмов Занятие № 1 Методы повышения эффективности усвоения понятийпри изучении темы:Кинематика
Занятие № 1 Методы повышения эффективности усвоения понятийпри изучении темы:Кинематика Мощность. 7 класс
Мощность. 7 класс Анализ, диагностика, техническое обслуживание и ремонт комплексной системы управления двигателем (КСАУ-Д) Lada Priora
Анализ, диагностика, техническое обслуживание и ремонт комплексной системы управления двигателем (КСАУ-Д) Lada Priora Экологические проблемы работы АЭС
Экологические проблемы работы АЭС Метод проектов на уроках физики
Метод проектов на уроках физики Тепловые явления. Обобщающий урок (8 класс)
Тепловые явления. Обобщающий урок (8 класс) Аккумулятор. Применение аккумуляторов в жизни
Аккумулятор. Применение аккумуляторов в жизни Виготовлення наглядового стенду з будови, технічного обслуговування та ремонту коробки змінних передач автомобіля ВАЗ-2101
Виготовлення наглядового стенду з будови, технічного обслуговування та ремонту коробки змінних передач автомобіля ВАЗ-2101 Введение в кинематику
Введение в кинематику Оптимальная обработка сигналов с использованием согласованных фильтров. Тема 4: Часть 5
Оптимальная обработка сигналов с использованием согласованных фильтров. Тема 4: Часть 5 Плотность тела. Билет 4
Плотность тела. Билет 4 Электротехника и электроника
Электротехника и электроника Зубчатые передачи
Зубчатые передачи Конвекция. Ламинарный тепловой погранслой при вынужденном движении жидкости вдоль плоской поверхности. (Тема 2. Лекции 8,9)
Конвекция. Ламинарный тепловой погранслой при вынужденном движении жидкости вдоль плоской поверхности. (Тема 2. Лекции 8,9) Основы кинематики. 9 класс
Основы кинематики. 9 класс Электричество. Работа электрического тока
Электричество. Работа электрического тока Устройство и принципы работы жидкостного и металлического манометров
Устройство и принципы работы жидкостного и металлического манометров Простой механизм
Простой механизм дополнение к уроку физики Испарение- вопросы почемучки
дополнение к уроку физики Испарение- вопросы почемучки Вводный урок 7 класс
Вводный урок 7 класс Полевые транзисторы FET (field-effect transistor). Устройство, принципы работы полевых транзисторов различных типов
Полевые транзисторы FET (field-effect transistor). Устройство, принципы работы полевых транзисторов различных типов