Содержание
- 2. Открытие радиоактивности А.А.Беккерель был потомственным физиком. Его дед, Антуан Сезар Беккерель изучал термоэлектричество и флуоресценцию. Его
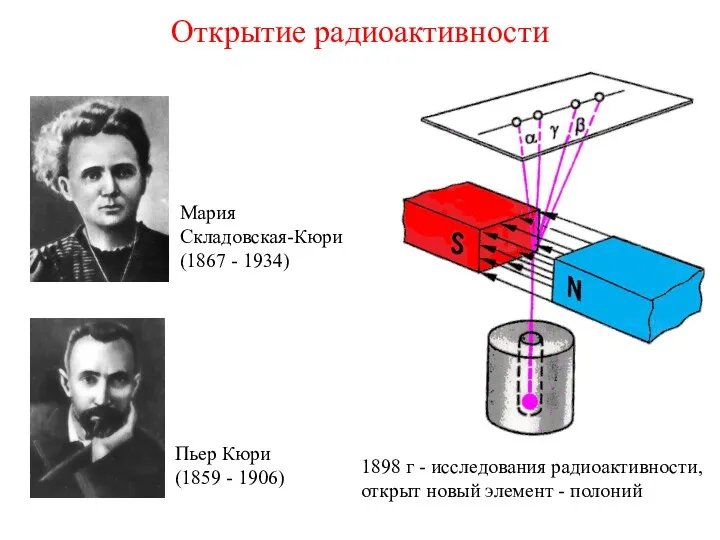
- 3. Открытие радиоактивности 1898 г - исследования радиоактивности, открыт новый элемент - полоний
- 4. Модели атома. 6.2.
- 5. Модель атома Томсона
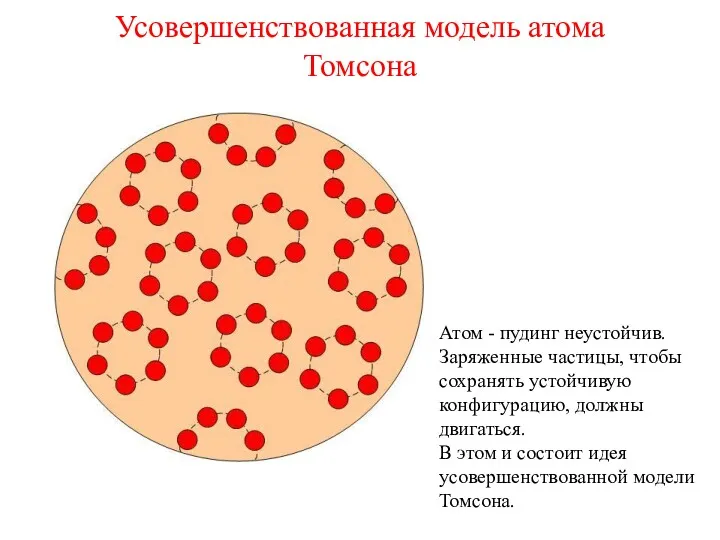
- 6. Усовершенствованная модель атома Томсона Атом - пудинг неустойчив. Заряженные частицы, чтобы сохранять устойчивую конфигурацию, должны двигаться.
- 7. Модель атома Нагаоке Следующий шаг - «сатурноподобная» модель Нагаоке. Здесь электроны - кольца вокруг положительно заряженного
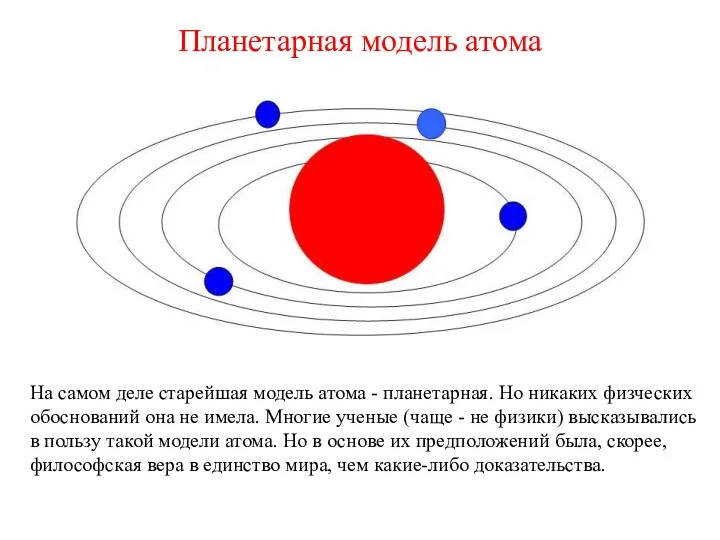
- 8. Планетарная модель атома На самом деле старейшая модель атома - планетарная. Но никаких физческих обоснований она
- 9. Быть может, эти электроны - миры, где пять материков, Свершенья, тайны, войны, троны и память сорока
- 10. Опыты Резерфорда по рассеянию α-частиц. 6.3.
- 11. Эрнест Резерфорд Родился в Новой Зеландии. Сын фермера-скотовода. С 1895 г. работал в Кавендишской лаборатории. Был
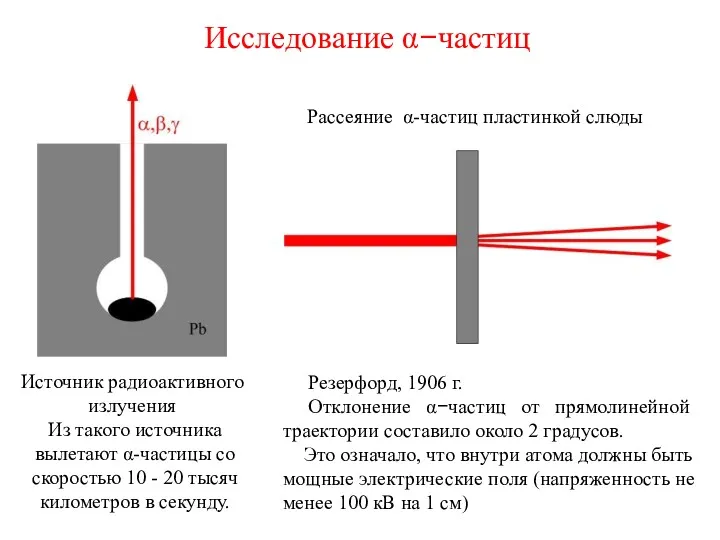
- 12. Исследование α−частиц Из такого источника вылетают α-частицы со скоростью 10 - 20 тысяч километров в секунду.
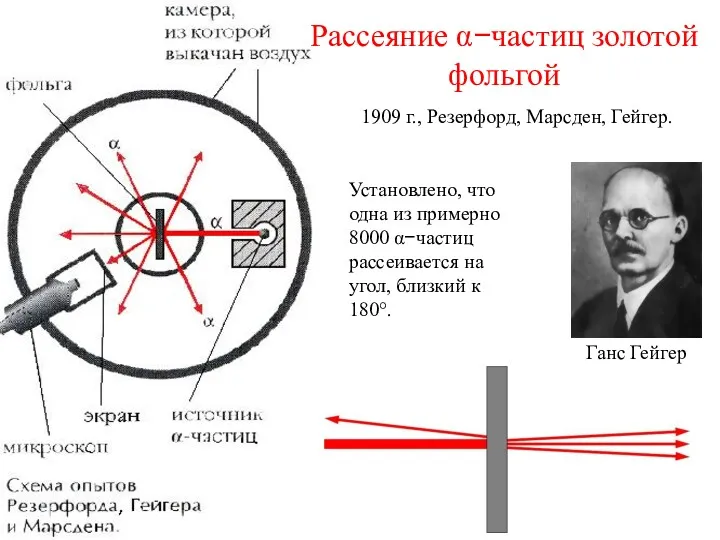
- 13. Рассеяние α−частиц золотой фольгой 1909 г., Резерфорд, Марсден, Гейгер. Установлено, что одна из примерно 8000 α−частиц
- 14. Рассеяние α−частиц золотой фольгой Резерфорд писал: “Это столь же невероятно, как если бы вы выстрелили 15-дюймовым
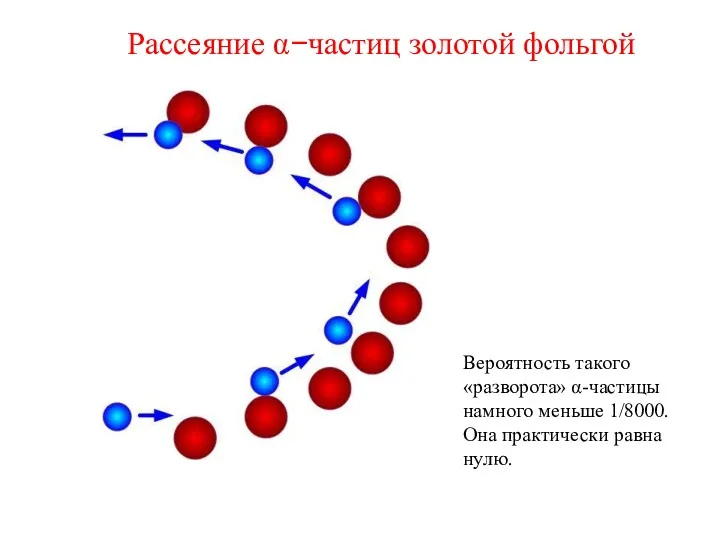
- 15. Рассеяние α−частиц золотой фольгой Вероятность такого «разворота» α-частицы намного меньше 1/8000. Она практически равна нулю.
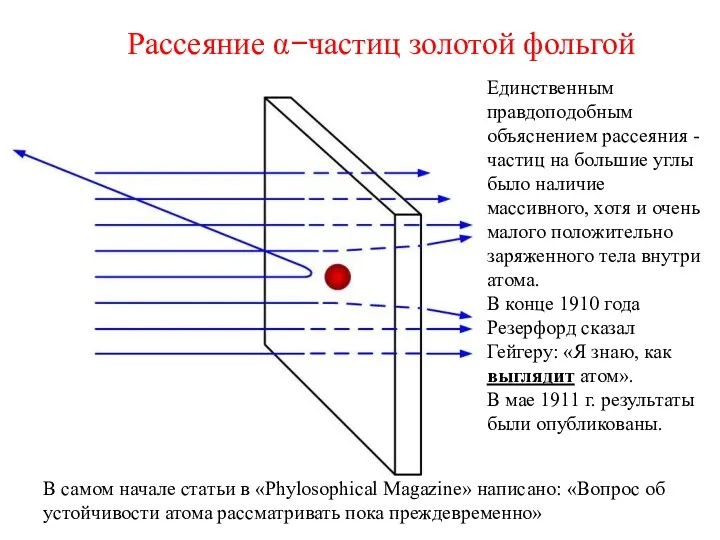
- 16. Рассеяние α−частиц золотой фольгой Единственным правдоподобным объяснением рассеяния -частиц на большие углы было наличие массивного, хотя
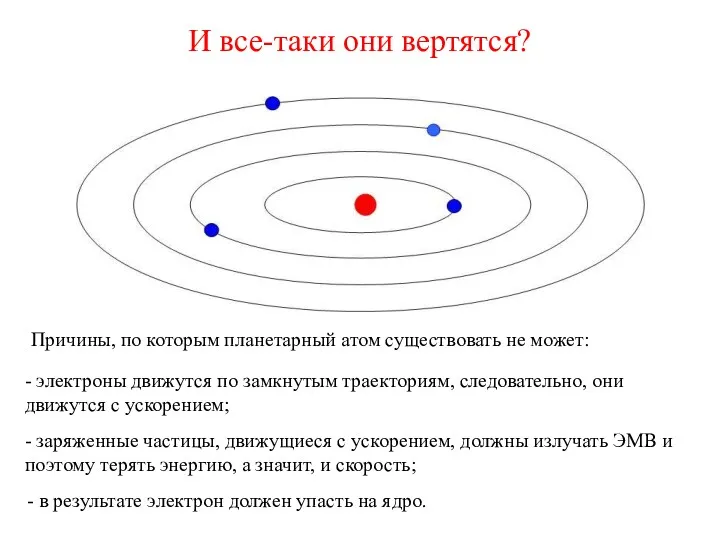
- 17. И все-таки они вертятся? Причины, по которым планетарный атом существовать не может: - электроны движутся по
- 18. Правило квантования Бора - Зоммерфельда. 6.4.
- 19. Что общего у атома и квантов? 1. Для того, чтобы объяснить, как может существовать планетарный атом
- 20. Правило квантования Бора - Зоммерфельда Согласно Планку излучение света происходит порциями – квантами, энергия которых равна
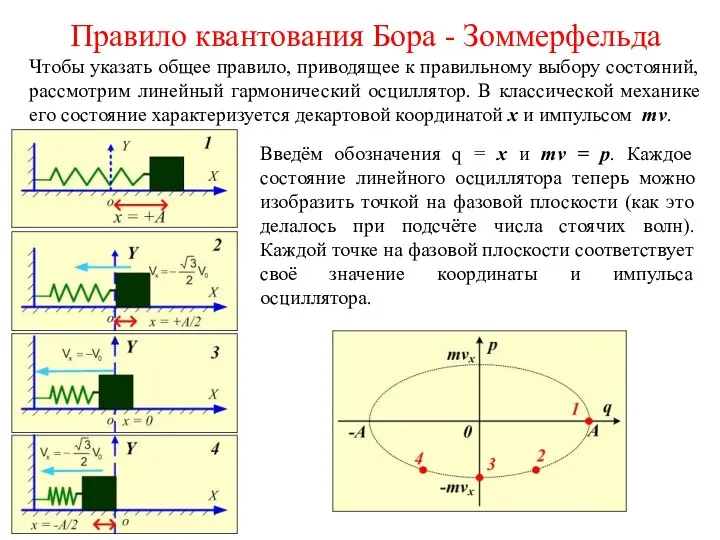
- 21. Правило квантования Бора - Зоммерфельда Чтобы указать общее правило, приводящее к правильному выбору состояний, рассмотрим линейный
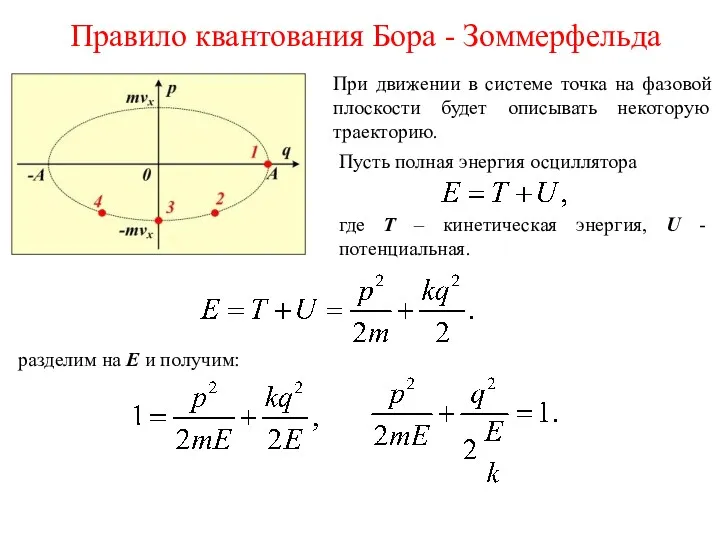
- 22. При движении в системе точка на фазовой плоскости будет описывать некоторую траекторию. Правило квантования Бора -
- 23. Правило квантования Бора - Зоммерфельда В координатах (p, q) это уравнение эллипса с полуосями Фазовая траектория
- 24. Исходя из предположения Планка о том, что энергия колебаний квантуется, то есть Здесь T – период
- 25. Правило квантования Бора - Зоммерфельда В процессе колебаний линейного осциллятора точка на фазовой плоскости будет описывать
- 26. Правило квантования Бора - Зоммерфельда Применим теперь правило квантования, выведенное для линейного осциллятора к движению электрона
- 27. Правило квантования Бора - Зоммерфельда Отсюда следует «правило квантования» круговых орбит: из всех возможных согласно классической
- 28. Боровская теория атома водорода. 6.5.
- 29. Боровская теория водородоподобного атома Электрон движется вокруг ядра по круговой орбите. На него действует кулоновская сила
- 30. где V - скорость электрона, R - радиус орбиты. здесь Z - заряд ядра. Запишем второй
- 31. Учтем, что согласно предположению Бора из всех возможных согласно классической механике орбит реализуются только те, у
- 32. Боровская теория водородоподобного атома Итак, энергия электрона в водородоподобном атоме может принимать ряд дискретных значений При
- 33. Радиус орбиты произвольного состояния с любым номером n удобно выражать через радиус первой бороской орбиты: Боровская
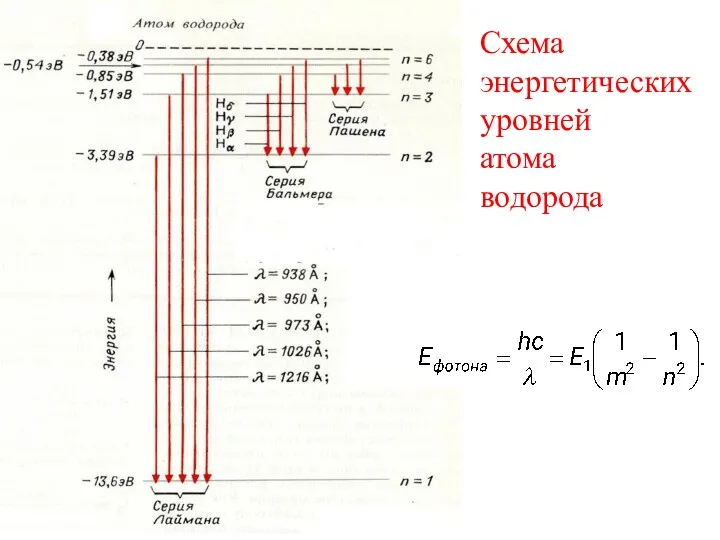
- 34. Схема энергетических уровней атома водорода
- 35. Постулаты Бора 1. Атом может находиться только в дискретных устойчивых состояниях, характеризуемых определенными дискретными значениями энергии.
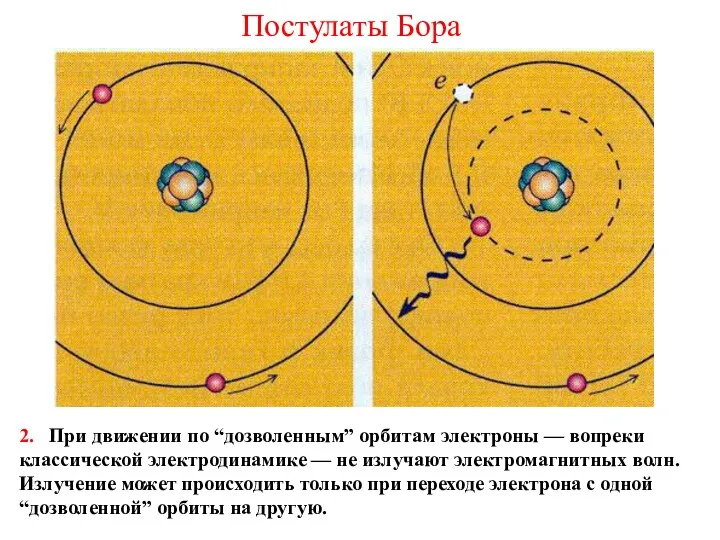
- 36. Постулаты Бора 2. При движении по “дозволенным” орбитам электроны — вопреки классической электродинамике — не излучают
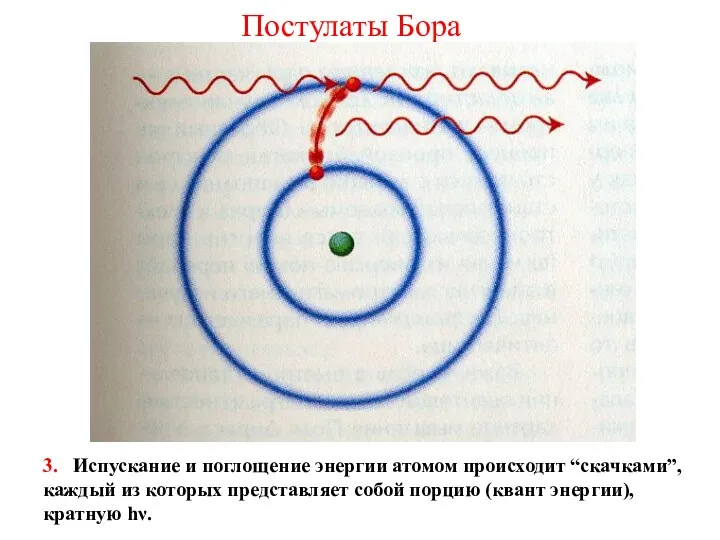
- 37. Постулаты Бора 3. Испускание и поглощение энергии атомом происходит “скачками”, каждый из которых представляет собой порцию
- 38. При поглощении энергии атомом электрон переходит с внутренней орбиты на внешнюю, более далекую от ядра. При
- 39. Экспериментальные подтверждения боровской теории атома водорода. 6.6.
- 40. Оптические спектры испускания атомов
- 41. Применение спектрального анализа
- 42. Как проверить? Формула Ридберга - обобщение формулы Бальмера: Согласно теории Бора Для водорда s = 1,
- 43. Схема энергетических уровней атома водорода
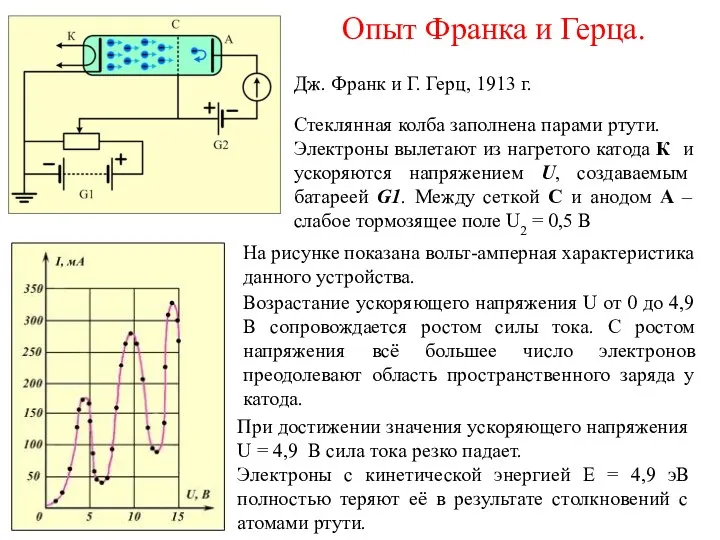
- 44. Опыт Франка и Герца. Дж. Франк и Г. Герц, 1913 г. Стеклянная колба заполнена парами ртути.
- 46. Скачать презентацию





























 Система впрыска топлива
Система впрыска топлива Задача силового анализа действующих на механизм
Задача силового анализа действующих на механизм Основные понятия теории тепломассообмена
Основные понятия теории тепломассообмена Электрический ток через контакт полупроводников p и n типов
Электрический ток через контакт полупроводников p и n типов Строительная физика. Несиловые воздействия окружающей среды на ограждающие конструкци
Строительная физика. Несиловые воздействия окружающей среды на ограждающие конструкци Простая Гаусс пушка
Простая Гаусс пушка Управляемость и проходимость автомобиля. Характеристика и показатели траекторной управляемости
Управляемость и проходимость автомобиля. Характеристика и показатели траекторной управляемости Передачи. Ременные, цепные, фрикционные передачи
Передачи. Ременные, цепные, фрикционные передачи Газовые законы
Газовые законы Презентация Лабораторная работа №2 Измерение размеров малых тел 7 класс
Презентация Лабораторная работа №2 Измерение размеров малых тел 7 класс Электрохимия. Физико –химические свойства ионных систем. (Лекция 13)
Электрохимия. Физико –химические свойства ионных систем. (Лекция 13) Влияние громкости звука на здоровье человека
Влияние громкости звука на здоровье человека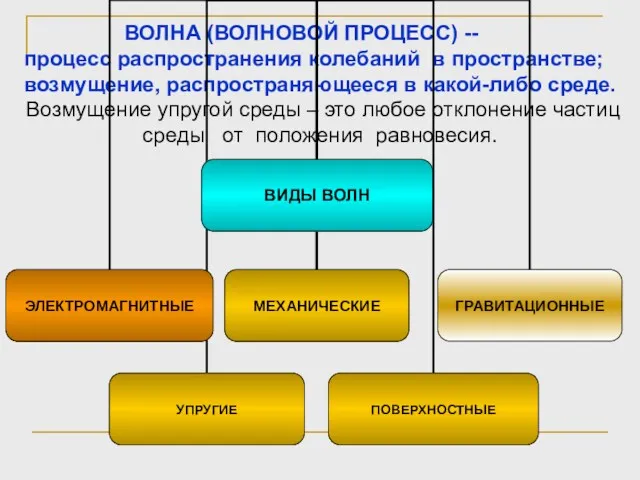 Волна (волновой процесс)
Волна (волновой процесс) Кинематика. Перемещение, путь, скорость, траектория
Кинематика. Перемещение, путь, скорость, траектория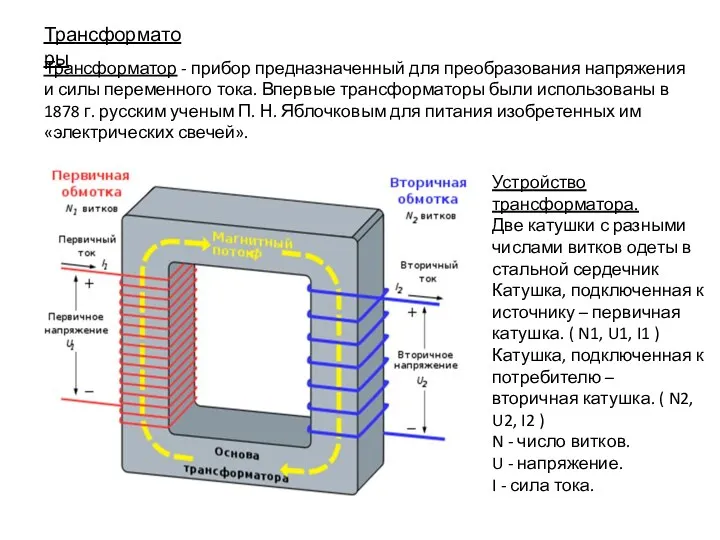 Трансформаторы
Трансформаторы презентация к уроку физики 11 класс
презентация к уроку физики 11 класс Особенности конструирования газоразрядных лазеров
Особенности конструирования газоразрядных лазеров Синусоидалы ток тізбектері. Синусоидалы ток және оны сипаттайтын параметрлер
Синусоидалы ток тізбектері. Синусоидалы ток және оны сипаттайтын параметрлер Атомная физика. Атомное ядро
Атомная физика. Атомное ядро Фізичні й хімічні явища у природі
Фізичні й хімічні явища у природі Теплова дія струму. Закон Джоуля – Ленца. Урок 58
Теплова дія струму. Закон Джоуля – Ленца. Урок 58 Гидродинамика. Поток жидкости и его основные понятия
Гидродинамика. Поток жидкости и его основные понятия Что такое воздух?
Что такое воздух? Переменный ток. (Лекция 29)
Переменный ток. (Лекция 29) Кинетическая и потенциальная энергии
Кинетическая и потенциальная энергии Оптическая модель упругого рассеяния
Оптическая модель упругого рассеяния Инженерные конструкции
Инженерные конструкции Основные термины и понятия в области диагностирования
Основные термины и понятия в области диагностирования