Содержание
- 2. ФИЗИКО –ХИМИЧЕСКИЕ СВОЙСТВА ИОННЫХ СИСТЕМ РОЛЬ ЭЛЕКТРОХИМИЧЕСКИХ МЕТОДОВ В ФАРМАЦИИ КЛАССИФИКАЦИЯ РАСТВОРОВ ЭЛЕКТРОЛИТОВ ТЕРМОДИНАМИЧЕСКАЯ КОНСТАНТА ИОНИЗАЦИИ
- 3. ЭЛЕКТРОХИМИЯ- ЭТО РАЗДЕЛ ФИЗХИМИИ, В КОТОРОМ ИЗУЧАЮТ ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ИОННЫХ СИСТЕМ, А ТАКЖЕ ПРОЦЕССЫ И ЯВЛЕНИЯ
- 4. Преимущества электрохимических методов анализа и разделения перед классическими химическими методами: -избирательность , -высокая чувствительнось, -экспрессность, -объективность,
- 5. Все растворы делятся на электролиты и неэлектролиты. Электролитами называются вещества, растворы или расплавы которых проводят электрический
- 6. Различают следующие виды электролитов: бинарные, тернарные и квартернарные : а)бинарные–это электролиты, которые при диссоциации распадаются на
- 7. В 1805 году литовский ученый Ф.Х.Гроттус впервые указал на то, что частицы растворенных веществ состоят из
- 8. Наряду с блестящими достижениями, теории Аррениуса присущи существенные недостатки, на которые указал Д.И.Менделеев. Недостатки теории Аррениуса
- 9. Современная теория водных растворов электролитов. В кристаллах электролитов противоположно заряженные частицы связаны между собой сильным электростатическим
- 10. Теория электролитической диссоциации Аррениуса, дополненная положениями Менделеева и Каблукова, применима только для растворов слабых электролитов, т.е.
- 11. Равновесие диссоциации воды сильно сдвинуто влево. Константа равновесия запишится: Кр воды= Сн+Сон-/ Своды Концентрация ионов водорода
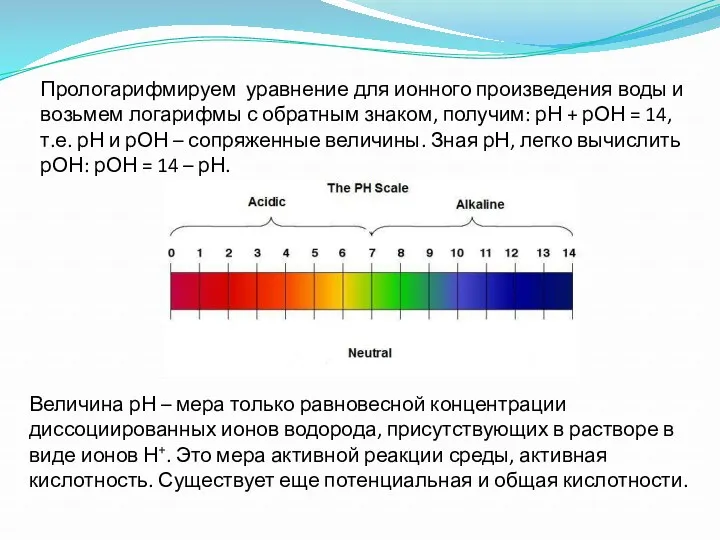
- 12. Прологарифмируем уравнение для ионного произведения воды и возьмем логарифмы с обратным знаком, получим: рН + рОН
- 13. Сильные электролиты В растворах сильных электролитов и концентрированных растворах электролитов любой силы необходимо учитывать взаимодействие между
- 14. Константу диссоциации, определяемую через активности, называют термодинамической или истинной: Кд.=a+ a-/ aм В реакции диссоциации изменение
- 15. Теория сильных электролитов Tеория сильных электролитов учитывает совокупность взаимодействия каждого данного иона со всеми остальными ионами
- 16. Чтобы сравнивать между собой ионные атмосферы в различных растворах, вводят понятие об условном радиусе ионной атмосферы:
- 17. ВЕСЬ ИЗБЫТОЧНЫЙ ЗАРЯД ИОННОЙ АТМОСФЕРЫ РАВЕН И ПРОТИВОПОЛОЖЕН ПО ЗНАКУ ЗАРЯДУ ЦЕНТРАЛЬНОГО ИОНА. ЭНЕРГИЯ ИОННОЙ АТМОСФЕРЫ:
- 18. ИЗУЧАЯ ЗАВИСИМОСТЬ КОЭФФИЦИЕНТОВ АКТИВНОСТИ ОТ СОСТАВА РАСТВОРА, ЛЬЮИС И ЕГО СОТРУДНИК РЕНДАЛЛ, УСТАНОВИЛИ: ИОННАЯ СИЛА РАСТВОРА
- 19. Сами авторы усовершенствовали свою теорию и расширили рамки ее применения: учли размеры ионов и не кулоновские
- 20. Проводники ІІ рода – это вещества, в которых ток переносится ионами. Относят: твердые соли, растворы электролитов,
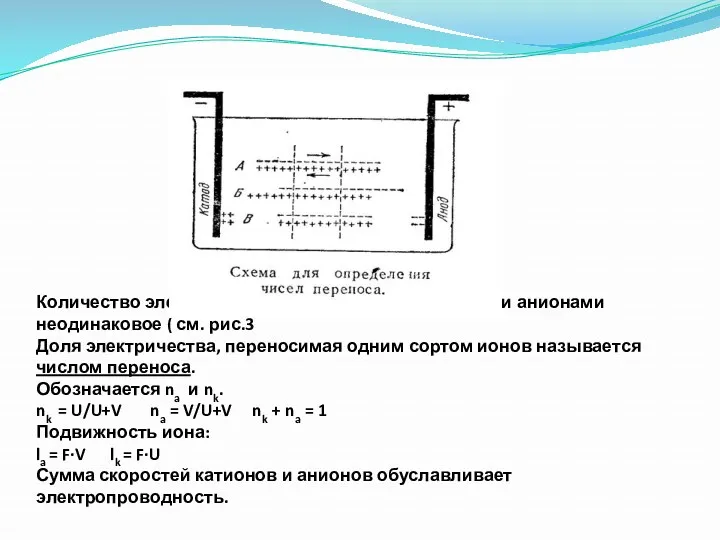
- 21. Количество электричества переносимое катионами и анионами неодинаковое ( см. рис.3 Доля электричества, переносимая одним сортом ионов
- 22. Электропроводность – это способность веществ проводить электрический ток под действием внешнего электрического поля. L - величина,
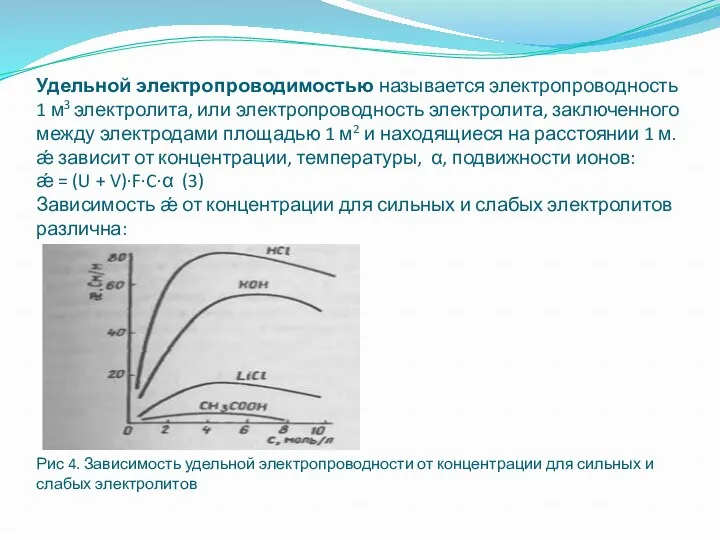
- 23. Удельной электропроводимостью называется электропроводность 1 м3 электролита, или электропроводность электролита, заключенного между электродами площадью 1 м2
- 24. Для сильных электролитов: вначале при повышении концентрации растет количество частиц, приносящих электричество, удельная электропрводность возрастает. После
- 25. По этому ввели понятие «эквивалентная электропроводность» - которая равна электрической проводимости объема электролита, содержащего моль/экв растворенного
- 26. Рис 5. Зависимость эквивалентной электропроводности от концентрации для сильных электролитов (1), для слабых электролитов (2) Для
- 27. Рис 6. Зависимость эквивалентной электропроводности от разведения для сильного (KCl) и слабого (CH3COOH) электролитов Если в
- 28. Электропроводность неводных растворов В практической деятельности провизор часто сталкивается с неводными растворами. Неводные растворы электролитов обладают
- 29. Рис 7. Полулогарифмическая зависимость эквивалентной электропроводности от концентрации в неводных растворителях Позже В.К.Семенченко показал, что в
- 30. Механизм действия природы растворителя на эквивалентную электропроводность объясняется природой связей, т.е. строением: Если вещество в «чистом»
- 31. При увеличении концентрации равновесие сместится в сторону недиссоциированных молекул. Это снижает λ (объясняется минимумом на графике).
- 32. Лекция2 Электрохимия КОНДУКТОМЕТРИЯ. ЭЛЕКТРОДНЫЕ ПРОЦЕССЫ.
- 33. КОНДУКТОМЕТРИЯ. ЭЛЕКТРОДНЫЕ ПРОЦЕССЫ. ПЛАН: 1. Кондуктометрия. Практическое применение кондуктометрических методов анализа. 2. Особенности электрохимических реакций. 3.Механизм
- 34. Кондуктометрия – это метод определения заданной величины по электропроводности. Кондуктометрия позволяет решить ряд задач: 1. Определение
- 35. Постоянную сосуда определяют по стандартному электролиту: Ксосуда = æстандарт∙ Rcтандарт Рис. 8. Принципиальная схема моста Кольрауша
- 36. Сопротивление стандартного и исследуемого электролитов определяют с помощью моста Кольрауша (см. рис.8). Нуль инструментом является осциллограф,
- 37. Релаксационный – связан с ионной атмосферой. Под действием электрического поля центральный ион выходит из центра ионной
- 38. 3. Определение растворимости трудно растворимых электролитов. Количественная характеристика плохо растворимых электролитов – произведение растворимости: Пр =
- 39. Рассмотрим наиболее типичные примеры: Титрование сильной кислоты сильным основанием. При титровании сильной кислоты щелочью идет реакция
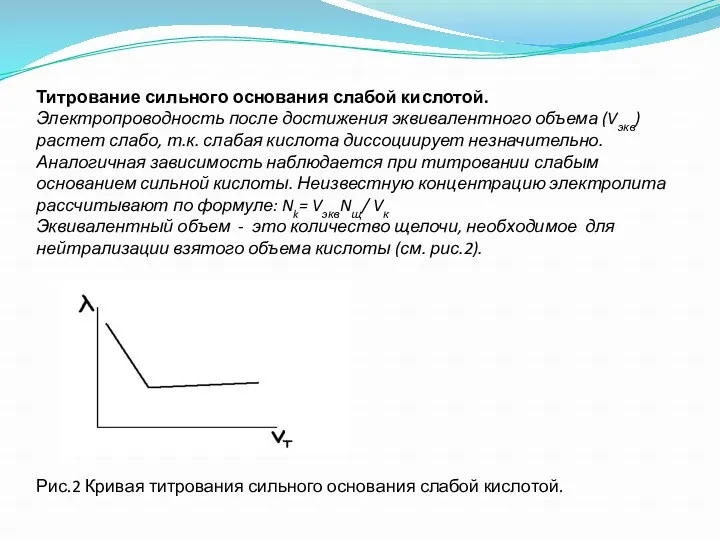
- 40. Титрование сильного основания слабой кислотой. Электропроводность после достижения эквивалентного объема (Vэкв) растет слабо, т.к. слабая кислота
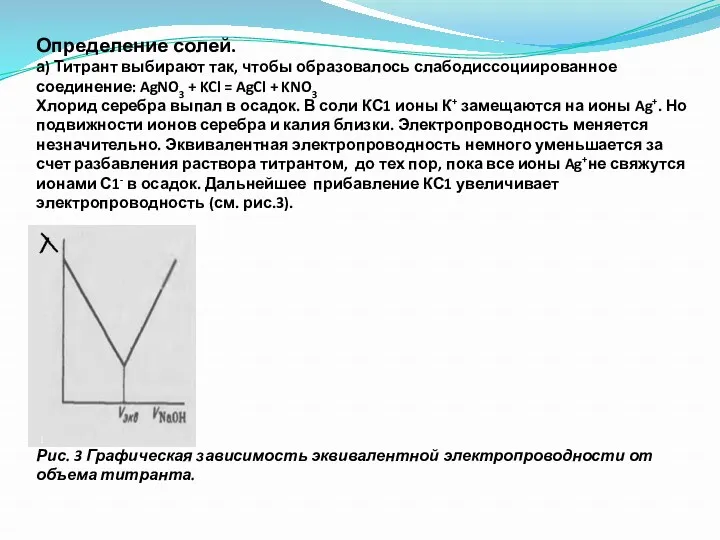
- 41. Определение солей. а) Титрант выбирают так, чтобы образовалось слабодиссоциированное соединение: AgNO3 + KCl = AgCl +
- 42. б) Оба продукта реакции мало растворимы: MgSO4+Ba(OH)2 = Mg(OH)2 + BaSO4 осадок осадок В начале электропроводность
- 43. Особенности электрохимических реакций В электрохимии реакции служат источником получения электрической энергии или, наоборот протекает за счет
- 44. В 1800 г. Вольта установил контактный потенциал, который возникает на границе 2-х металлов за счет разной
- 45. Каждый ион гидратирован. Кристаллическая решетка металла состоит из положительно заряженных ионов, находящихся в углах и электронного
- 46. Возникающее электростатическое притяжения между ионами, перешедшими в раствор, и противоположено заряженной пластинкой металла препятствует дальнейшему течению
- 47. Способность выделять ионы в раствор для каждого металла своя, специфическая. Нет двух металлов и одинаковой такой
- 48. Электрический ток в этой гальванической цепи возникает в результате реакции восстановления ионов меди цинком: Zn +
- 49. При наличии системы двух электродов, находящихся соответственно в растворах своих солей, между ними возникает ЭДС, равна
- 50. Уравнение Нернста для ЭДС гальванического элемента и электродного потенциала. Если рассматривать работу гальванического элемента как процесс
- 51. Для обратимо протекающей реакции можно записать: Для окислительно-восстановительного процесса в элементе Якоби – Даниэля: Zn +
- 52. Изобарно – изотермический потенциал будет определяться выражением: А ЭДС гальванического элемента будет равна:
- 53. Обозначим: Тогда поставив Е0 в выражение , получим уравнение Нернста для ЭДС гальванического элемента: Из которого
- 54. Для электродных потенциалов уравнение Нернста записывается следующим образом: - для электрода обратимого с катионами - для
- 56. Скачать презентацию
















































 Теплообмен излучением между телами, разделённой прозрачной средой. Коэффициент облучённости. Теплообмен между телами
Теплообмен излучением между телами, разделённой прозрачной средой. Коэффициент облучённости. Теплообмен между телами Критерии работоспособности твэлов, формулировка критерия, расчётноэкспериментальное обоснование. (Лекция 19-21. Тема 9)
Критерии работоспособности твэлов, формулировка критерия, расчётноэкспериментальное обоснование. (Лекция 19-21. Тема 9) Человеческий глаз. Автор Максимова Наталья Сергеевна
Человеческий глаз. Автор Максимова Наталья Сергеевна Система смазки двигателя танка Т-72. Тема 6. Занятие 1
Система смазки двигателя танка Т-72. Тема 6. Занятие 1 Повторение темы Электростатика
Повторение темы Электростатика Действительный цикл. Газообмен ДВС
Действительный цикл. Газообмен ДВС Основы молекулярно-кинетической теории. Масса молекул. Количество вещества
Основы молекулярно-кинетической теории. Масса молекул. Количество вещества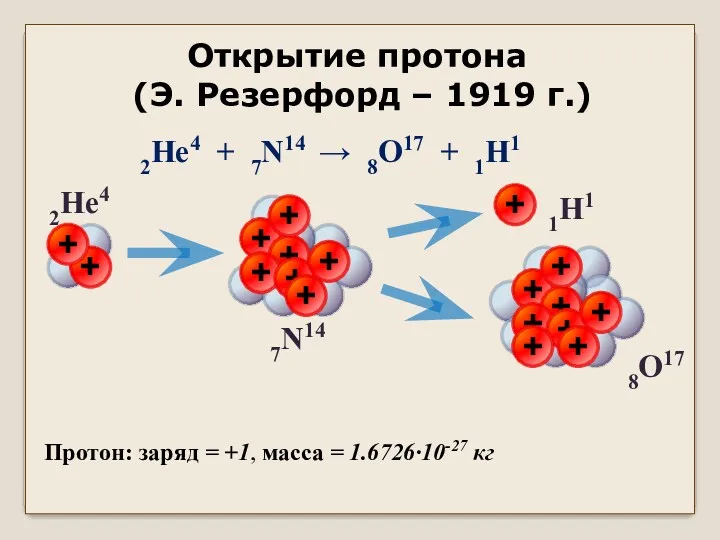 Открытие протона (Э. Резерфорд – 1919 г.)
Открытие протона (Э. Резерфорд – 1919 г.) Т-130 Бульдозері
Т-130 Бульдозері Оптика. Закон отражения света
Оптика. Закон отражения света Презентация к уроку в 5 классе по теме Дефекты зрения и оптические иллюзии
Презентация к уроку в 5 классе по теме Дефекты зрения и оптические иллюзии Презентация Испарение и конденсация
Презентация Испарение и конденсация Последовательное и параллельное соединение проводников
Последовательное и параллельное соединение проводников Значение освоения космоса
Значение освоения космоса Работа и мощность электрического тока. 8 класс
Работа и мощность электрического тока. 8 класс Делимость электрического заряда
Делимость электрического заряда Внеклассное мероприятие по физике Классная физика для любознательных Диск
Внеклассное мероприятие по физике Классная физика для любознательных Диск Строение атомов
Строение атомов Электрический ток в электролитах
Электрический ток в электролитах Выталкивающая сила. Урок физики в 7 классе
Выталкивающая сила. Урок физики в 7 классе Исследование термодинамических процессов водяного пара. Смеси идеальных газов. Влажный воздух. (Занятие 5)
Исследование термодинамических процессов водяного пара. Смеси идеальных газов. Влажный воздух. (Занятие 5) Об открытии закона Архимеда.
Об открытии закона Архимеда. Лекция 8. Магнитоэлектрические приборы
Лекция 8. Магнитоэлектрические приборы Свисты-волны ОНЧ диапазона (1-30 кГц) в магнитосфере
Свисты-волны ОНЧ диапазона (1-30 кГц) в магнитосфере §9. Сложное движение точки
§9. Сложное движение точки Презентация по теме Электрическое поле и его свойства
Презентация по теме Электрическое поле и его свойства Плавание судов
Плавание судов Закон Ома для участка цепи
Закон Ома для участка цепи