Содержание
- 2. Применение стабильных изотопов в геологии Выяснение предыстории химического элемента в месторождении, которую не представляется возможным восстановить
- 3. Главные стабильные изотопы в геологии Главной задачей изучения геохимии изотопов является установление условий фракционирования (разделения) изотопов,
- 4. Общие характеристики фракционирования Главная причина разделения стабильных изотопов в природных процессах – это разница в их
- 5. 1) Физико-химические процессы 1.1 Реакции изотопного обмена при подвижных равновесных процессах 1.2. Абсорбция и катионный обмен
- 6. 2) Биогенные процессы 2.1 Фотосинтез 2.2 Жизнедеятельность бактерий
- 7. Параметры, характеризующие фракционирование Изотопные отношения. Например: 32S / 34S = 22,22; 34S / 32S = 0,045.
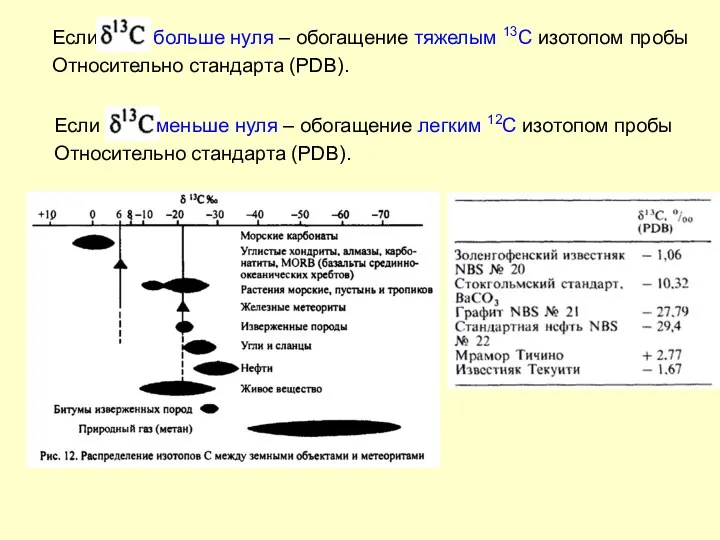
- 8. Если больше нуля – обогащение тяжелым 13С изотопом пробы Относительно стандарта (PDB). Если меньше нуля –
- 10. Скачать презентацию






 Знаки вторичной переработки
Знаки вторичной переработки Азот и фосфор
Азот и фосфор Химические свойства полимеров
Химические свойства полимеров Фотохимический смог и химизм его образования
Фотохимический смог и химизм его образования Соли
Соли Волшебные кристалы
Волшебные кристалы Химические свойства металлов
Химические свойства металлов Общая характеристика неметаллов
Общая характеристика неметаллов Механизм и закономерности кристаллизации металлов
Механизм и закономерности кристаллизации металлов Тіршілік гетерофункционалды қосылыстар
Тіршілік гетерофункционалды қосылыстар Средние породы. Типичный андезитовый вулкан
Средние породы. Типичный андезитовый вулкан Химический состав прямогонных бензинов
Химический состав прямогонных бензинов Коррозия металлов
Коррозия металлов Синтетические каучуки: хлоропреновый каучук
Синтетические каучуки: хлоропреновый каучук Круговорот углерода в природе
Круговорот углерода в природе Химические свойства неорганических соединений
Химические свойства неорганических соединений Термодинамика. 1 закон термодинамики
Термодинамика. 1 закон термодинамики Особливості горіння дисперсних систем
Особливості горіння дисперсних систем Пластмассы
Пластмассы Химические свойства металлов
Химические свойства металлов Кислород
Кислород Диаграмма состояния Железо – Углерод. Материаловедение. Лекция 2
Диаграмма состояния Железо – Углерод. Материаловедение. Лекция 2 Білки (протеїни)
Білки (протеїни) Олимпиадные задачи муниципального этапа по химии
Олимпиадные задачи муниципального этапа по химии Ауыл шаруашылығындағы пестицидтер
Ауыл шаруашылығындағы пестицидтер Относительная атомная масса
Относительная атомная масса Углерод. Аллотропные модификации углерода
Углерод. Аллотропные модификации углерода Виды химической связи
Виды химической связи