Слайд 2

Изучать мы, начинаем, неметаллы и их соединения.
В природе, несомненно, их велико
значение.
Водород, азот и фосфор, кислород и углерод.
Круг в природе, в организмах. Так идет за годом год.
Баланс природе не нарушишь, они вреда не принесут
Во многом примененье они всегда себе найдут.
Слайд 3
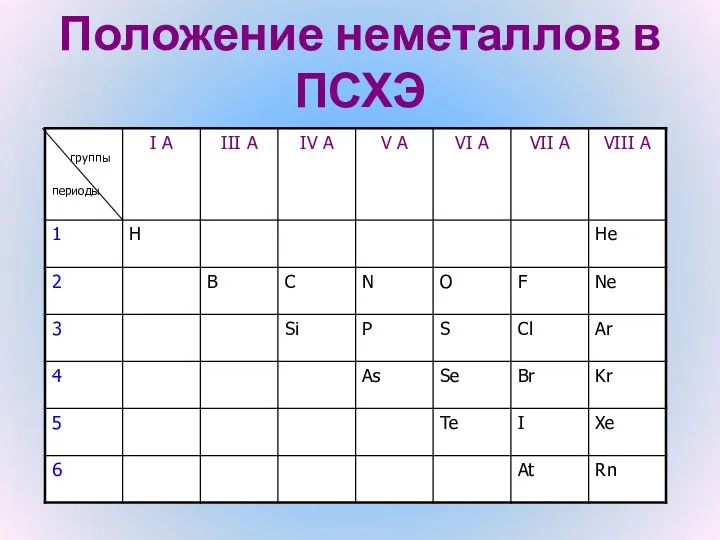
Положение неметаллов в ПСХЭ
Слайд 4

Особенности атомного
строения неметаллов:
Небольшой атомный радиус
На внешнем уровне 4-8 электронов
Слайд 5

Электроотрицательность
– это способность атомов химического элемента притягивать к себе общие электронные
пары
H Si P C S Br Cl N O F
у с и л е н и е ЭО
Слайд 6

Агрегатное состояние
Газы
Жидкие
Твердые
Br2
I2, P4, C,
Si, B, S8
Слайд 7

Цветовая палитра:
Красно-бурый Фиолетовый
Красный
фосфор
Красный
Бром
Пары йода
Желто-зеленый
Хлор
Желтый
Сера
Графит
Черный
Слайд 8

Температура плавления
3 8000 С – у графита
- 2100 С - азота
Слайд 9

Аллотропия – способность атомов одного химического элемента образовывать несколько простых веществ,
различных по своим свойствам
Слайд 10

Аллотропные изменения углерода
Слайд 11

Аллотропные изменения кислорода
О - кислород
Кислород
Озон
Слайд 12

Химические свойства
Ярко выражены окислительные свойства
В меньшей степени восстановительные (с более электроотрицательными
элементами)











 Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії
Загальна характеристика неметалічних елементів. Неметали як прості речовини. Явище алотропії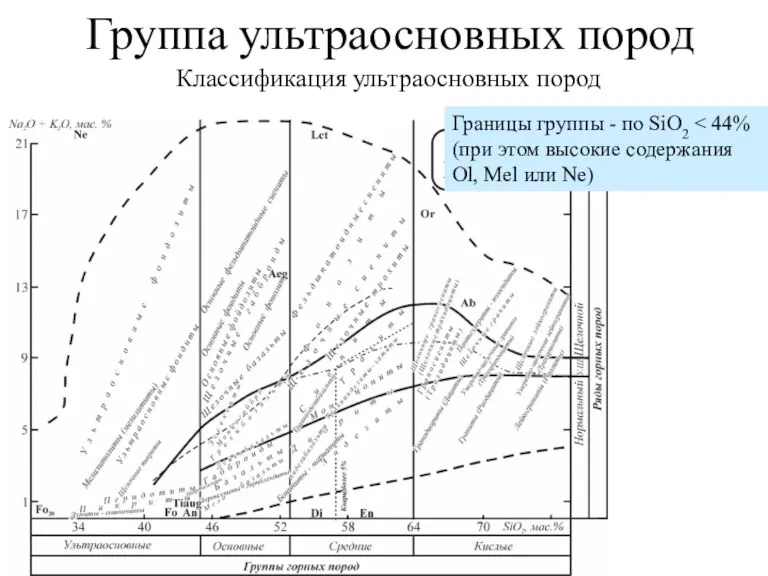 Группа ультраосновных пород
Группа ультраосновных пород Аммиак
Аммиак Физические и химические свойства алмаза. Алмазная промышленность в России
Физические и химические свойства алмаза. Алмазная промышленность в России Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Карбонильные соединения. Альдегиды
Карбонильные соединения. Альдегиды Уральские самоцветы
Уральские самоцветы Амфотерные органические и неорганические соединения
Амфотерные органические и неорганические соединения Гибридизация. Формы электронных облаков
Гибридизация. Формы электронных облаков Классификация химических реакций
Классификация химических реакций Общая характеристика халькогенов. Кислород
Общая характеристика халькогенов. Кислород Electrochemistry. Oxidation-reduction equilibrium in water solutions
Electrochemistry. Oxidation-reduction equilibrium in water solutions Задачи на вывод формулы органических веществ
Задачи на вывод формулы органических веществ Степень окисления. Определение степени окисления в соединениях
Степень окисления. Определение степени окисления в соединениях кл.химия 24.01
кл.химия 24.01 Химические свойства получение и применение солей
Химические свойства получение и применение солей Массовая и объемная доли компонентов смеси (раствора)
Массовая и объемная доли компонентов смеси (раствора) Введение в количественный анализ
Введение в количественный анализ Хімічна кінетика
Хімічна кінетика Различные теории кислот и оснований
Различные теории кислот и оснований Кристалдардың ішкі құрылымы
Кристалдардың ішкі құрылымы Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.)
Алканы. (Предельные углеводороды. Парафины. Насыщенные углеводороды.) Оксиды. Классификация. Номенклатура. Свойства оксидов. Получение. Применение
Оксиды. Классификация. Номенклатура. Свойства оксидов. Получение. Применение Галогены. История открытия галогенов
Галогены. История открытия галогенов Introduction in bioorganic chemistry. Isomerism and structure of organic compounds
Introduction in bioorganic chemistry. Isomerism and structure of organic compounds Щелочные породы среднего состава
Щелочные породы среднего состава Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность
Процессы дыхания, брожения, обмена веществ, фотосинтеза, нервная деятельность Назначение установки Пенекс
Назначение установки Пенекс