Содержание
- 2. ПРЕДМЕТ ФИЗИЧЕСКОЙ ХИМИИ Физическая химия – наука, которая изучает взаимосвязи химических процессов и физических явлений, которые
- 3. ОБЪЕКТЫ ИЗУЧЕНИЯ ФИЗИЧЕСКОЙ ХИМИИ Объектами изучения физической химии являются любые системы, в которых могут протекать химические
- 4. СОДЕРЖАНИЕ КУРСА Химическая термодинамика Учение о растворах Электрохимия Химическая кинетика
- 5. 2. Химическая термодинамика 2.1. Основные понятия Термодинамика – наука, изучающая взаимные переходы различных форм энергии. Термодинамика
- 6. 2. Химическая термодинамика 2.1. Основные понятия Особенность термодинамики: она не рассматривает «внутренний мир» термодинамической системы, механизм
- 7. 2. Химическая термодинамика 2.1. Основные понятия Объект изучения термодинамики – термодинамические системы. Системы бывают: открытые, закрытые
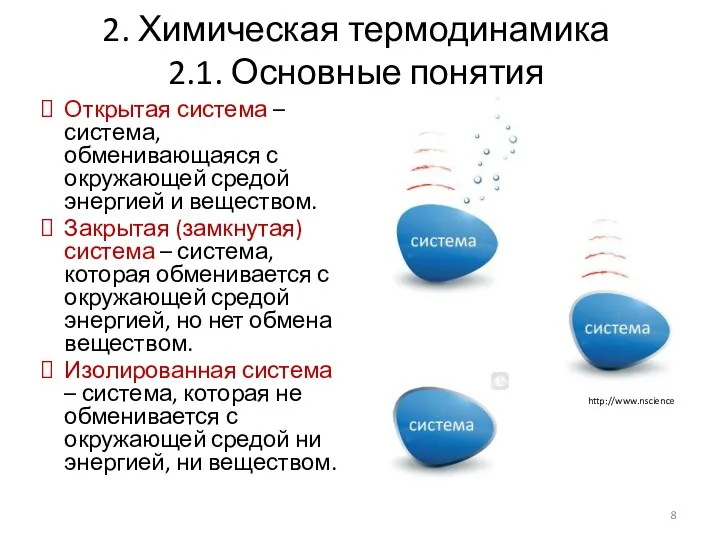
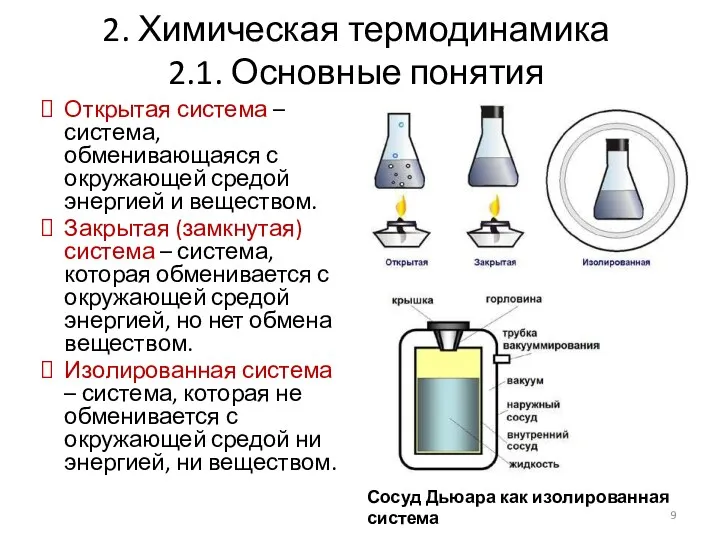
- 8. 2. Химическая термодинамика 2.1. Основные понятия Открытая система – система, обменивающаяся с окружающей средой энергией и
- 9. 2. Химическая термодинамика 2.1. Основные понятия Открытая система – система, обменивающаяся с окружающей средой энергией и
- 10. 2. Химическая термодинамика 2.1. Основные понятия Гомогенная система — однородная система, состоящая из одной фазы, химический
- 11. 2. Химическая термодинамика 2.1. Основные понятия Простая система – система, состоящая из одного вещества. Например: вода
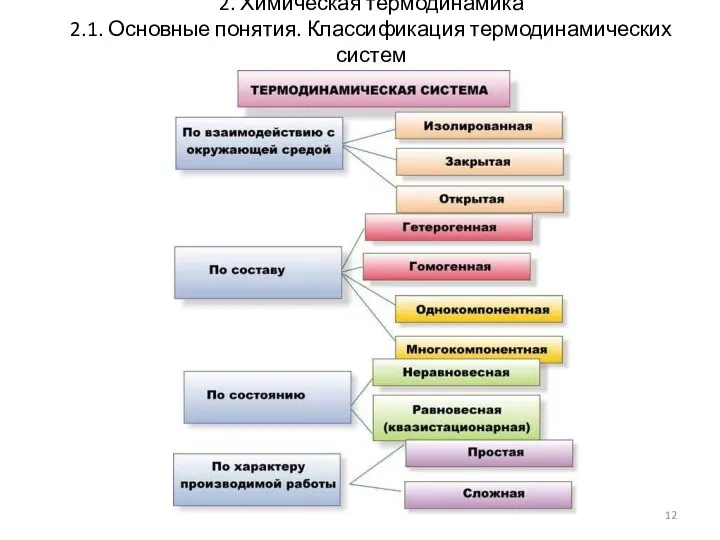
- 12. 2. Химическая термодинамика 2.1. Основные понятия. Классификация термодинамических систем
- 13. 2. Химическая термодинамика 2.1. Основные понятия. Параметры Состояние системы характеризуется совокупностью всех её физических и химических
- 14. 2. Химическая термодинамика 2.1. Основные понятия. Параметры Термодинамические параметры (параметры состояния) или свойства: Внешние параметры; определяются
- 15. 2. Химическая термодинамика 2.1. Основные понятия. Состояния Состояния термодинамических систем: Равновесное Неравновесное (неустойчивое, лабильное) Стационарное
- 16. 2. Химическая термодинамика 2.1. Основные понятия. Состояния Равновесное состояние – такое состояние системы, при котором её
- 17. 2. Химическая термодинамика 2.1. Основные понятия. Состояния Стационарное состояние - такое состояние системы, при котором её
- 18. 2. Химическая термодинамика 2.1. Основные понятия. Состояния Неравновесное состояние – состояние , при котором хотя бы
- 19. 2. Химическая термодинамика 2.1. Основные понятия. Состояния Параметры состояния (термодинамические переменные) – макроскопические величины, которые можно
- 20. 2. Химическая термодинамика 2.1. Основные понятия. Процессы Изменение хотя бы одного из термодинамических параметров изменяет состояние
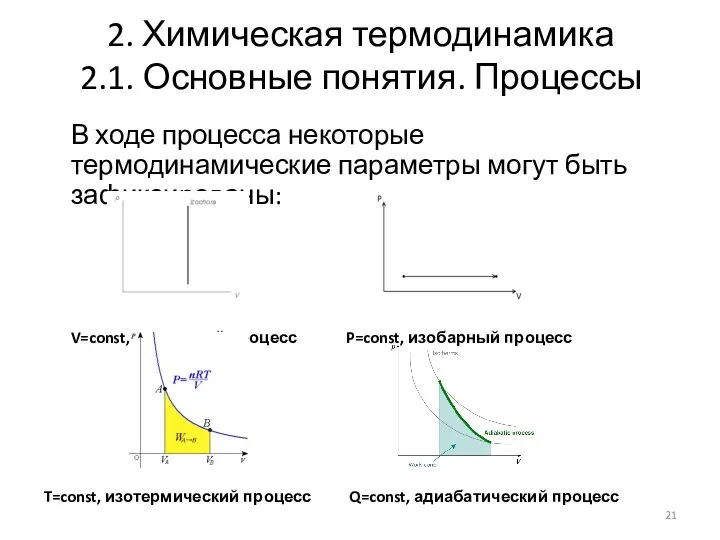
- 21. 2. Химическая термодинамика 2.1. Основные понятия. Процессы В ходе процесса некоторые термодинамические параметры могут быть зафиксированы:
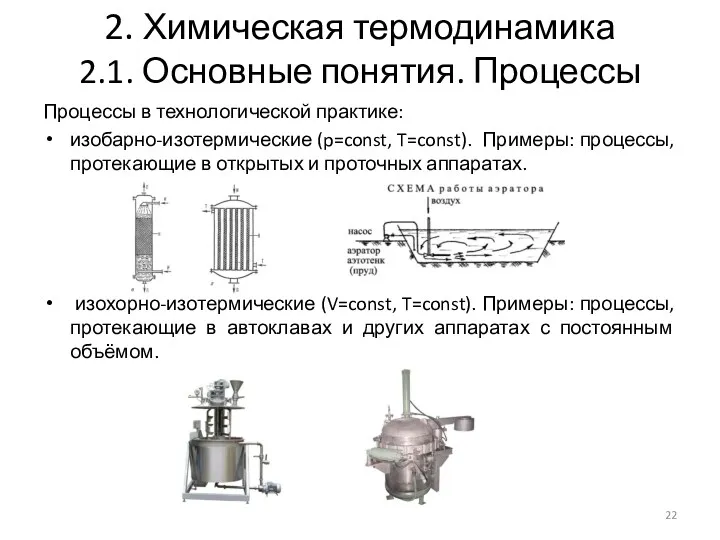
- 22. 2. Химическая термодинамика 2.1. Основные понятия. Процессы Процессы в технологической практике: изобарно-изотермические (p=const, T=const). Примеры: процессы,
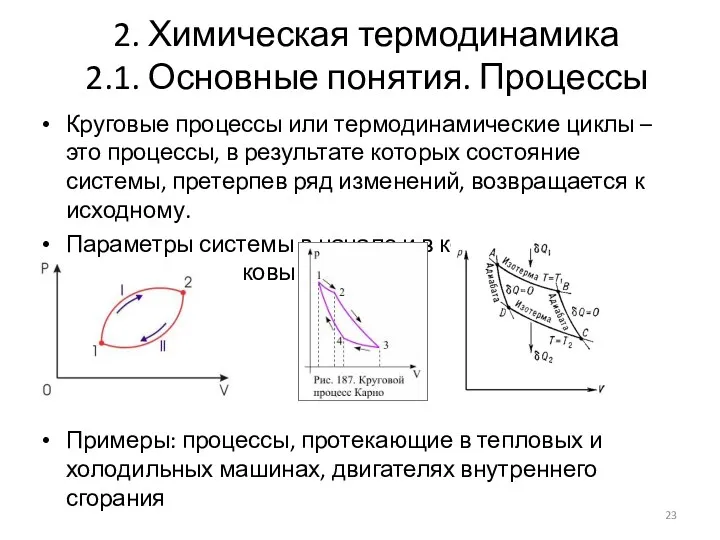
- 23. 2. Химическая термодинамика 2.1. Основные понятия. Процессы Круговые процессы или термодинамические циклы – это процессы, в
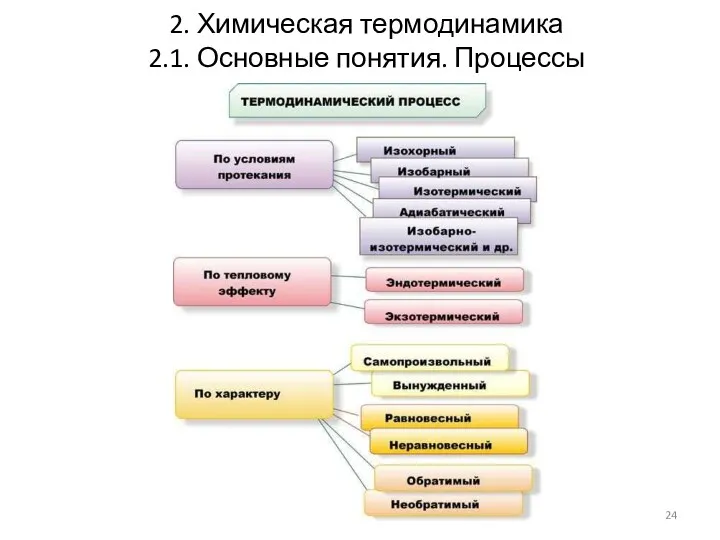
- 24. 2. Химическая термодинамика 2.1. Основные понятия. Процессы
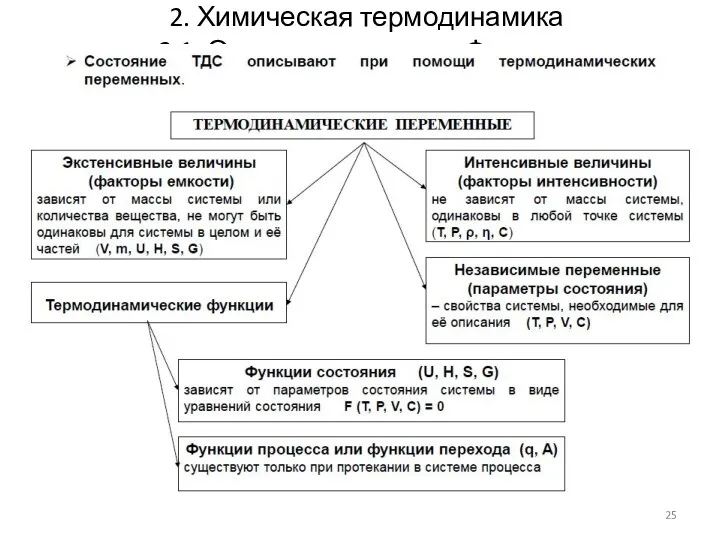
- 25. 2. Химическая термодинамика 2.1. Основные понятия. Функции
- 26. 2. Химическая термодинамика 2.1. Основные понятия. Функции Термодинамические функции: Функции состояния (термодинамические потенциалы) – величины, значение
- 27. 2. Химическая термодинамика 2.1. Основные понятия Внутренняя энергия – полная энергия системы, складывается из кинетической энергии
- 28. 2. Химическая термодинамика 2.1. Основные понятия. Функции
- 29. 2. Химическая термодинамика 2.1. Основные понятия
- 30. 2. Химическая термодинамика 2.1. Основные понятия Термодинамика основывается на двух постулатах (исходных положениях) и трех законах.
- 31. 2. Химическая термодинамика 2.1. Основные понятия Основной постулат термодинамики (первое исходное положение): Любая изолированная система с
- 32. 2. Химическая термодинамика 2.1. Основные понятия Нулевой закон термодинамики (второе исходное положение): Если система А находится
- 33. 2. Химическая термодинамика 2.2. Уравнение состояния Уравнение состояния идеального газа Уравнение Менделеева — Клапейрона или где
- 34. 2. Химическая термодинамика 2.2. Уравнение состояния Уравнения состояния реального газа Уравнение Ван-дер Ваальса Уравнение Бертло Уравнение
- 35. 2. Химическая термодинамика 2.2. Уравнение состояния Это уравнение учитывает отклонение свойств реальных газов от идеальных в
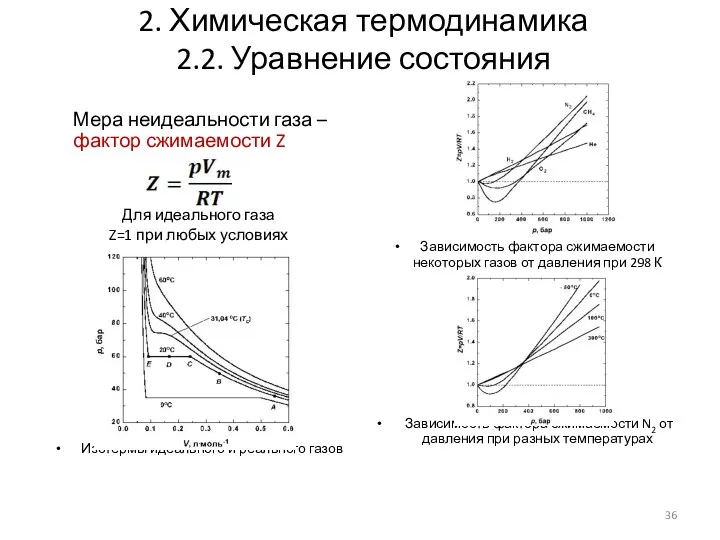
- 36. 2. Химическая термодинамика 2.2. Уравнение состояния Мера неидеальности газа – фактор сжимаемости Z Для идеального газа
- 37. 2. Химическая термодинамика 2.3. Первый закон термодинамики Закон сохранения и превращения энергии для термодинамической системы Изменение
- 38. 2. Химическая термодинамика 2.3. Первый закон термодинамики Для изолированной системы (Q = W = 0)
- 40. 2. Химическая термодинамика 2.3. Первый закон термодинамики Для открытой системы - “химическая работа”, работа переноса вещества
- 41. 2. Химическая термодинамика 2.3. Первый закон термодинамики Невозможно существование вечного двигателя 1-го рода, который совершал бы
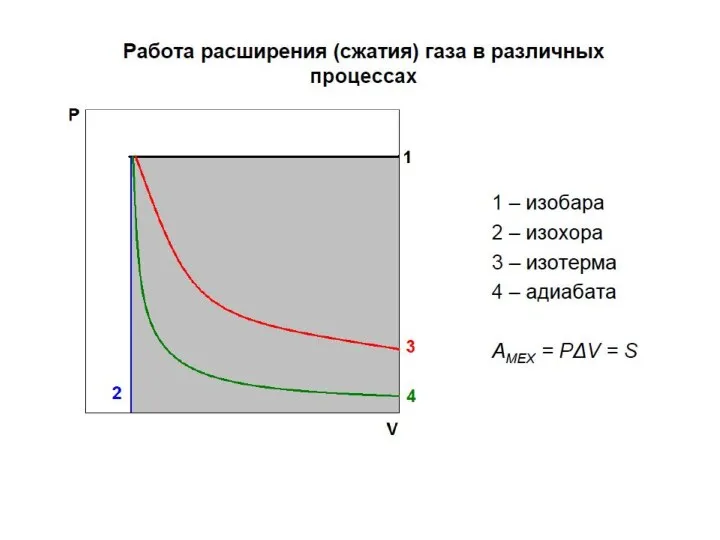
- 42. 2. Химическая термодинамика 2.3. Первый закон термодинамики Работа W – это упорядоченная форма передачи энергии от
- 43. 2. Химическая термодинамика 2.4. Термохимия 2.4.1 Тепловые эффекты реакций Химические реакции сопровождаются либо выделением, либо поглощением
- 44. 2. Химическая термодинамика 2.4. Термохимия Тепловым эффектом химической реакции называется количество теплоты, которое выделяется или поглощается
- 45. 2. Химическая термодинамика 2.4. Термохимия Физико-химические процессы протекают при постоянном объеме (V=const) или постоянном давлении (p=const)
- 46. 2. Химическая термодинамика 2.4. Термохимия Для реакций с участием идеальных газов, протекающих при p=const и T=const
- 47. 2. Химическая термодинамика 2.4. Термохимия Тепловые эффекты зависят от природы реагирующих веществ, агрегатного состояния исходных и
- 48. 2. Химическая термодинамика 2.4. Термохимия стандартная энтальпия/теплота реакции при температуре Т (энтальпия реакции между веществами), кДж
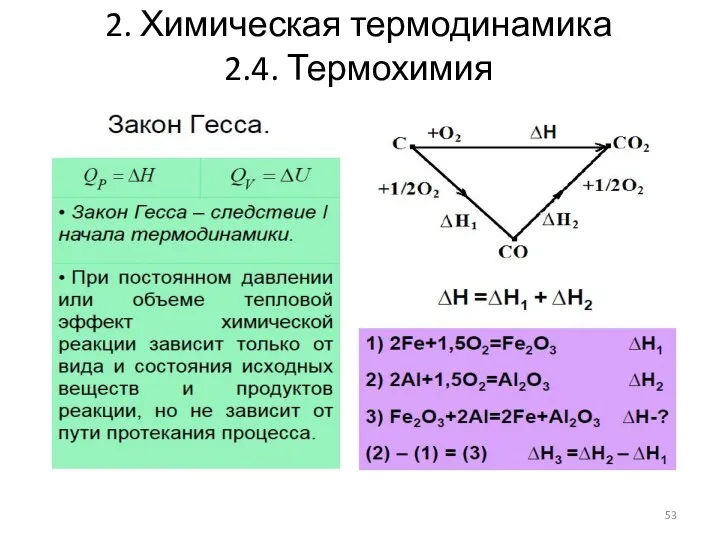
- 49. 2. Химическая термодинамика 2.4. Термохимия 2.4.2. Закон Гесса (1840 г.) Тепловой эффект химической реакции при постоянном
- 50. 2. Химическая термодинамика 2.4. Термохимия Термохимическое уравнение - уравнение химической реакции, в котором приведен тепловой эффект.
- 51. 2. Химическая термодинамика 2.4. Термохимия Экзотермическая реакция – сопровождается выделением теплоты При Т, р=const и W=0
- 52. 2. Химическая термодинамика 2.4. Термохимия Определение теплового эффекта реакций по закону Гесса Метод составления термохимических схем
- 53. 2. Химическая термодинамика 2.4. Термохимия
- 54. 2. Химическая термодинамика 2.4. Термохимия Следствия из закона Гесса: Следствие 1. Стандартная энтальпия химической реакции (тепловой
- 56. Определение теплового эффекта реакции по стандартной теплоте образования веществ
- 58. Определение теплового эффекта реакции по стандартной теплоте сгорания веществ
- 61. 2. Химическая термодинамика 2.4. Термохимия Зная тепловой эффект образования химического соединения в одном агрегатном состоянии, можно
- 62. 2. Химическая термодинамика 2.4. Термохимия Иногда при вычислении теплот образования, теплот сгорания и теплот химических реакций
- 63. 2. Химическая термодинамика 2.4. Термохимия 2.4.3. Калориметрия Калориметрия (лат. calor — тепло и metro — измеряю)
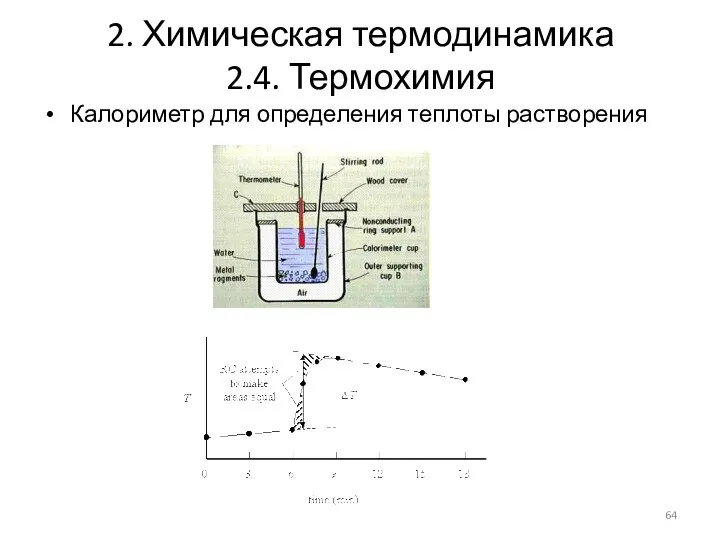
- 64. 2. Химическая термодинамика 2.4. Термохимия Калориметр для определения теплоты растворения
- 65. 2. Химическая термодинамика 2.4. Термохимия Калориметрическая бомба http://www.esru.strath.ac.uk/EandE/Web_sites/06-07/Biodiesel/Experiment/bombcalorimeter.gif
- 66. 2. Химическая термодинамика 2.4. Термохимия 2.4.4. Закон Лавуазье–Лапласа Является следствием закона сохранения энергии. Тепловой эффект прямой
- 67. 2. Химическая термодинамика 2.5. Теплоемкость Теплоемкость – количество теплоты, поглощенное телом при нагревании на один градус
- 68. 2. Химическая термодинамика 2.5. Теплоемкость У газов различают: изохорную теплоемкость – теплоемкость при постоянном объеме Изобарную
- 69. 2. Химическая термодинамика 2.5. Теплоемкость Средняя теплоемкость Истинная теплоемкость Связь между истинной и средней теплоемкостями
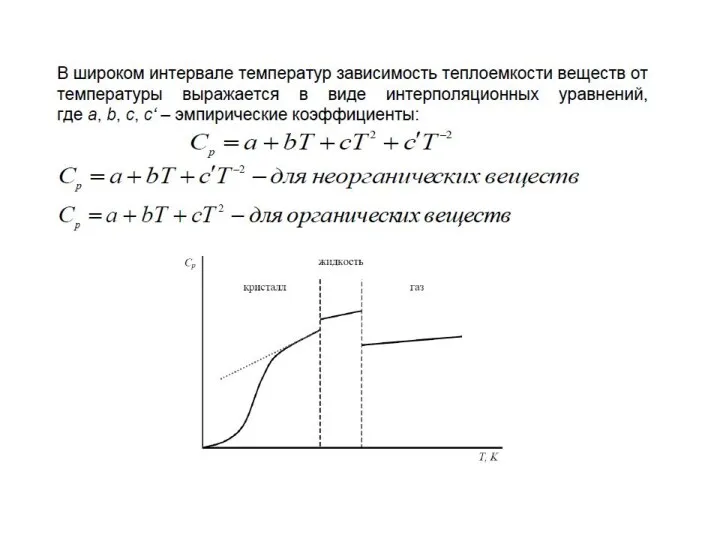
- 70. 2. Химическая термодинамика 2.4. Теплоемкость Зависимость теплоемкости от температуры: Теплоемкость – экспериментально измеряемая экстенсивная величина Значения
- 71. Изменение теплоемкости веществ в ходе реакции
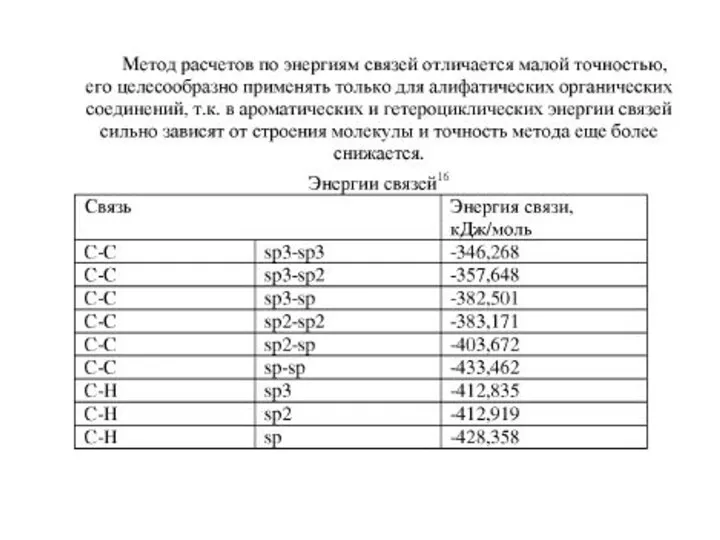
- 73. Способы расчета теплоемкости Правило Дюлонга-Пти: Теплоемкость cv твердых соединений приблизительно равна сумме атомных теплоемкостей (т.е. является
- 74. 2. Химическая термодинамика 2.4. Теплоемкость Теплоемкость смесей (газовых, растворов, суспензий, эмульсий и пр.) при отсутствии химического
- 75. 2. Химическая термодинамика 2.4. Теплоемкость Зная теплоёмкость, можно рассчитать теплоту:
- 76. 2. Химическая термодинамика 2.5. Термохимия Уравнение (закон) Кирхгофа Тепловой эффект реакции зависит от температуры. Большинство термохимических
- 77. 2. Химическая термодинамика 2.5. Термохимия Закон Кирхгофа: Температурный коэффициент теплового эффекта реакции равен разности суммарных мольных
- 78. 2. Химическая термодинамика 2.5. Термохимия Для изобарных процессов (р=const):
- 79. 2. Химическая термодинамика 2.5. Термохимия Для изохорных процессов (V=const):
- 80. 2. Химическая термодинамика 2.5. Термохимия С помощью уравнения Кирхгофа можно вычислить приращение энтальпии ∆H при любой
- 81. 2. Химическая термодинамика 2.5. Термохимия Если теплоемкость во время процесса не меняется, то тепловой эффект процесса
- 82. Зависимость теплового эффекта реакции от температуры Если пренебречь изменением теплоемкостей исходных веществ и продуктов реакции в
- 83. Зависимость теплового эффекта реакции от температуры
- 84. Зависимость теплового эффекта реакции от температуры Если необходимо учесть изменение теплоемкости с температурой, следует воспользоваться уравнениями
- 85. Зависимость теплового эффекта реакции от температуры
- 87. Скачать презентацию






































































 Лекция 5. Коллигативные свойства растворов
Лекция 5. Коллигативные свойства растворов становление органической химии
становление органической химии Полимерные материалы
Полимерные материалы Природные (натуральные) полимеры. Композиционные материалы
Природные (натуральные) полимеры. Композиционные материалы ВКР: Изучение золей на основе железа и марганца, полученных методом химической конденсации
ВКР: Изучение золей на основе железа и марганца, полученных методом химической конденсации Возобновляемое сырье органической химии
Возобновляемое сырье органической химии Растворы и растворители
Растворы и растворители Поляризация электродов
Поляризация электродов Алкены (олефины). Лекция 3
Алкены (олефины). Лекция 3 Электроотрицательность химических элементов
Электроотрицательность химических элементов Алюминий и бор
Алюминий и бор Карбон қышқылдары
Карбон қышқылдары Атыраудағы химиялық өндіріс кәсіп орындары
Атыраудағы химиялық өндіріс кәсіп орындары Формальдегід. Будова та шкідливість
Формальдегід. Будова та шкідливість Изучение состава чая
Изучение состава чая Особенности строения твердых тел
Особенности строения твердых тел Галогенопохідні ароматичних вуглеводнів
Галогенопохідні ароматичних вуглеводнів Амины. Физические и химические свойства
Амины. Физические и химические свойства Массовая доля вещества в растворе. Урок химии. 8 класс
Массовая доля вещества в растворе. Урок химии. 8 класс Каучук. История открытия
Каучук. История открытия Types of chemical bonds in crystals
Types of chemical bonds in crystals Степень окисления. Подготовка к контрольной работе
Степень окисления. Подготовка к контрольной работе Химические свойства металлов
Химические свойства металлов Углеводы (сахариды)
Углеводы (сахариды) Изменения, происходящие с липидами в процессах технологической переработки сырья и параметры, характеризующие их
Изменения, происходящие с липидами в процессах технологической переработки сырья и параметры, характеризующие их Basis Sets and Pseudopotentials
Basis Sets and Pseudopotentials Ізомерія. Структурна ізомерія
Ізомерія. Структурна ізомерія Бор шикізатын қышқылдық ыдырату
Бор шикізатын қышқылдық ыдырату