Содержание
- 2. АЛКЕНЫ (олефины) CnH2n Углеводороды, содержащие двойную углерод-углеродную связь
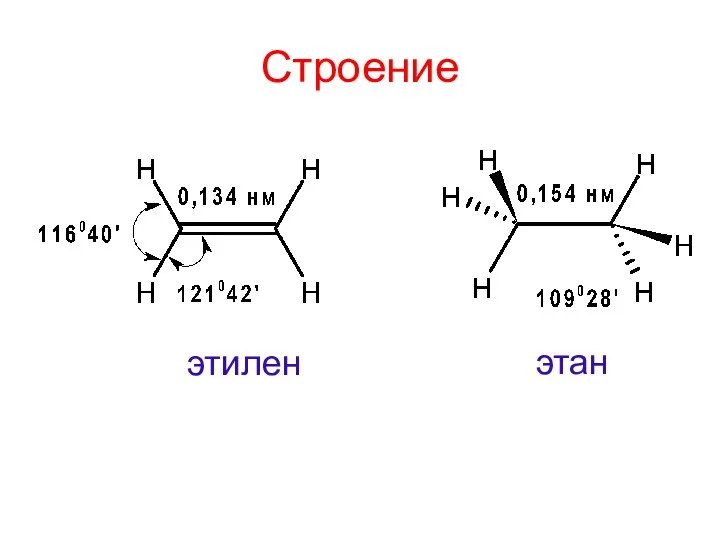
- 3. Строение этилен этан
- 4. Строение этилена
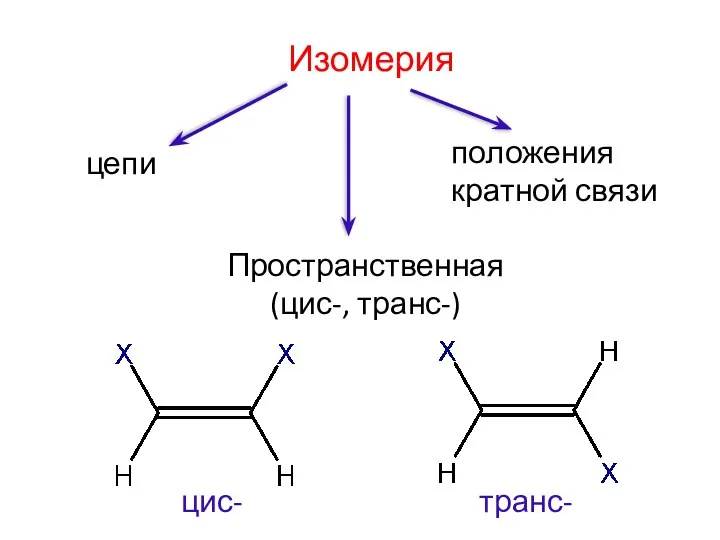
- 5. Изомерия цепи положения кратной связи Пространственная (цис-, транс-) цис- транс-
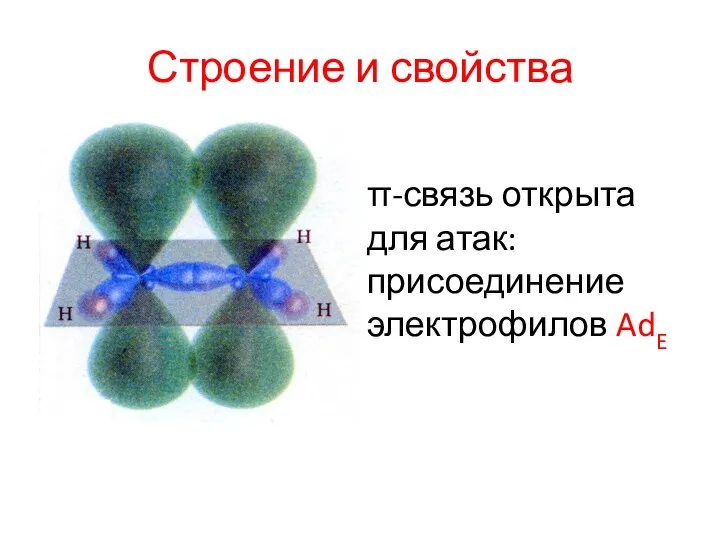
- 6. Строение и свойства π-связь открыта для атак: присоединение электрофилов AdE
- 7. Алкены Кратная связь Реакции присоединения Механизм электрофильный AdE
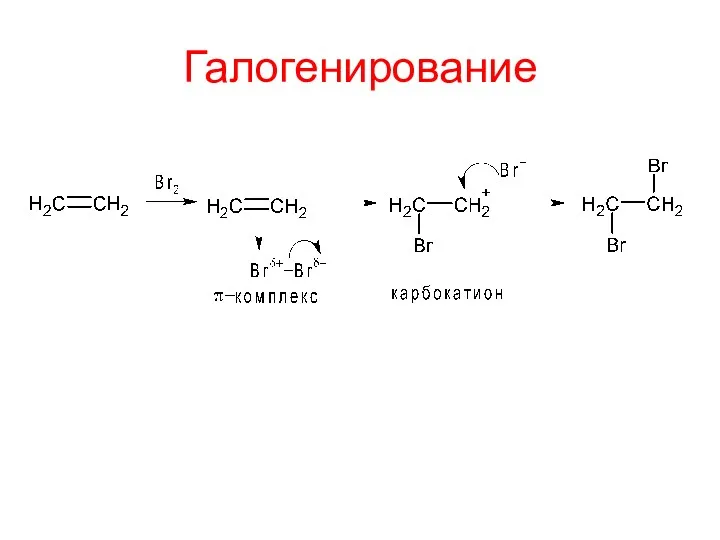
- 8. Галогенирование
- 9. Гидрогалогенирование Правило Марковникова: при реакциях алкенов с Н-Х (Х = ОН, Br, Cl) водород присоединяется к
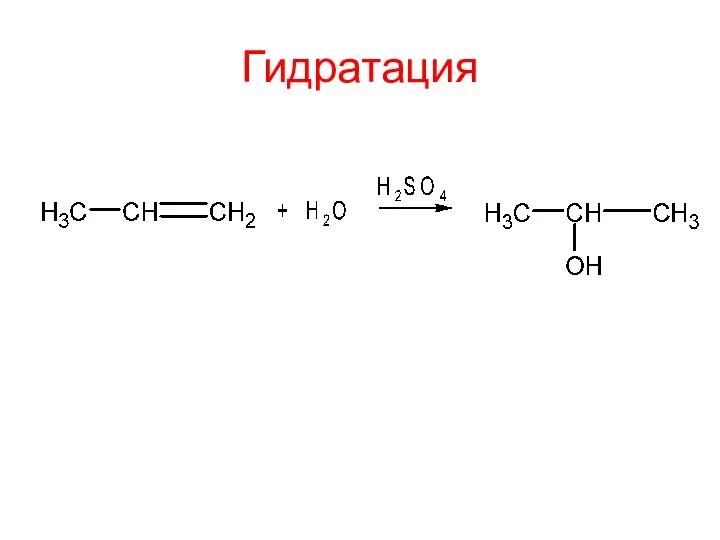
- 10. Гидратация
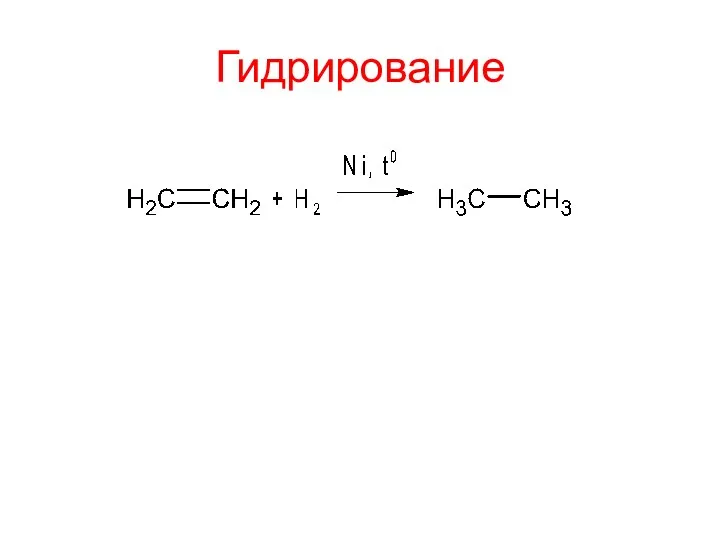
- 11. Гидрирование
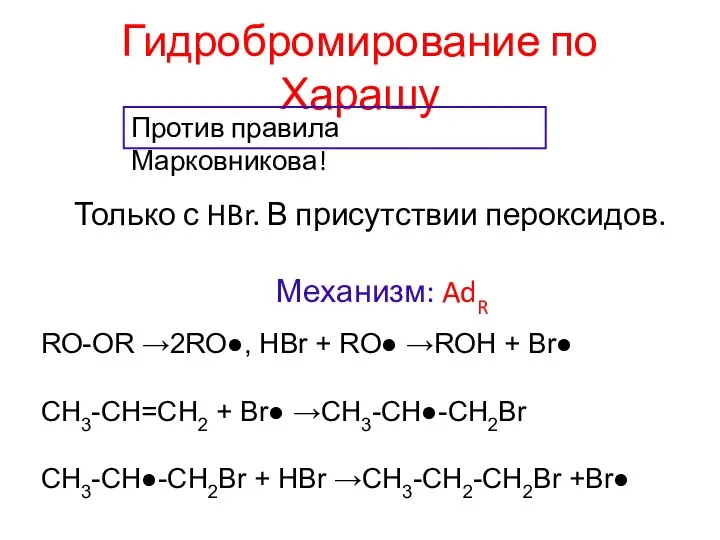
- 12. Гидробромирование по Харашу Только с HBr. В присутствии пероксидов. Механизм: AdR RO-OR →2RO●, HBr + RO●
- 13. Полимеризация (радикальная реакция) СН2=СН2 → -(СН2-СН2)-n n = 100-1000 Пероксиды, р = 100 МПа и t
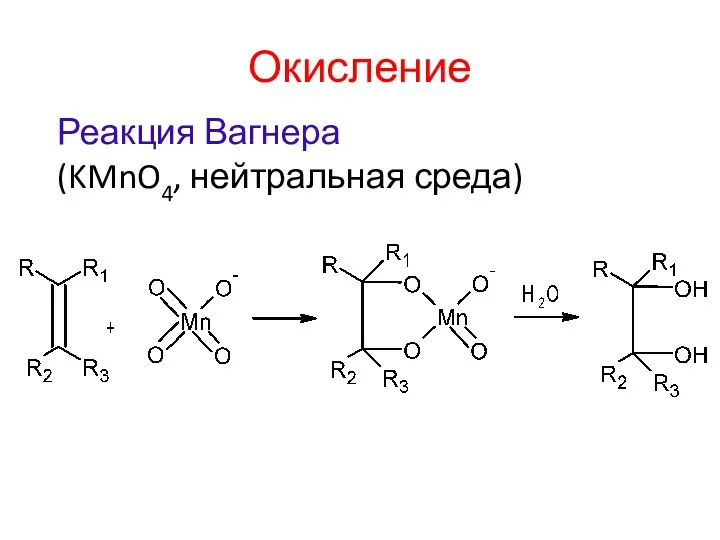
- 14. Окисление Реакция Вагнера (KMnO4, нейтральная среда)
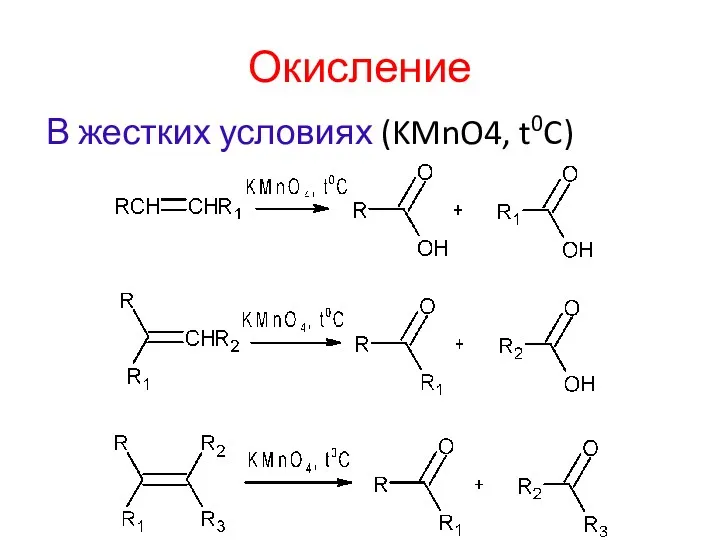
- 15. Окисление В жестких условиях (KMnO4, t0C)
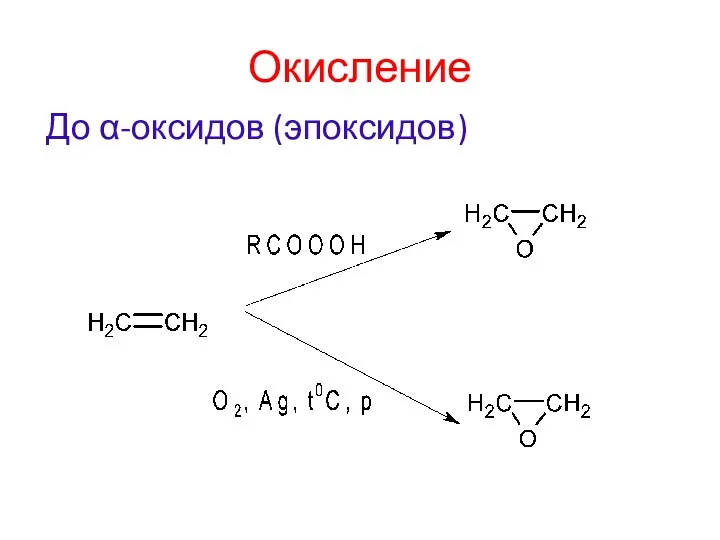
- 16. Окисление До α-оксидов (эпоксидов)
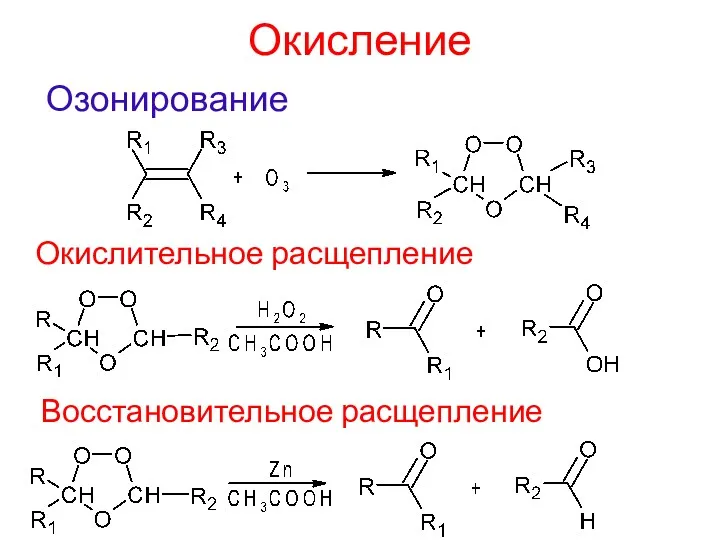
- 17. Окисление Озонирование Окислительное расщепление Восстановительное расщепление
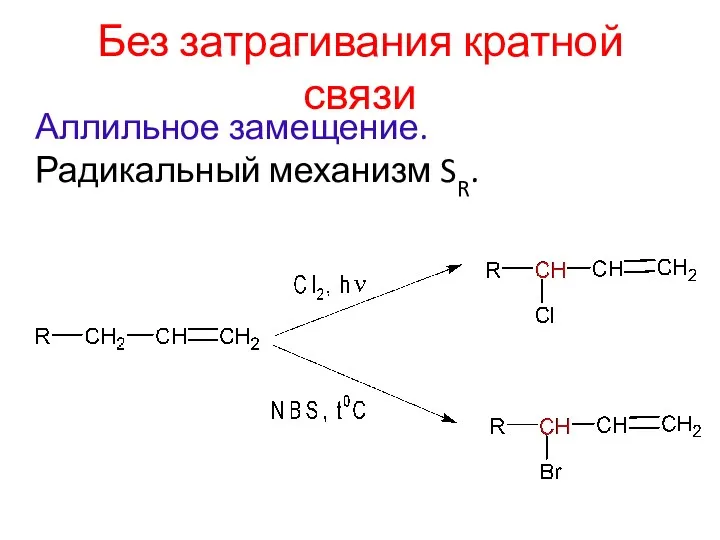
- 18. Без затрагивания кратной связи Аллильное замещение. Радикальный механизм SR.
- 19. Получение алкенов В промышленности Крекинг алканов Дегидрирование алканов (t°, кат.) CnH2n+2→ CnH2n + Н2 3) Гидрирование
- 21. Скачать презентацию





 Висбрекинг (перспективный процесс ТК)
Висбрекинг (перспективный процесс ТК) Изотопная геохимия
Изотопная геохимия Сплавы и коррозия металлов
Сплавы и коррозия металлов Поверхневі явища в дисперсних системах. Поверхнева енергія
Поверхневі явища в дисперсних системах. Поверхнева енергія Строение, реакционные способности и методы синтеза алкадиенов
Строение, реакционные способности и методы синтеза алкадиенов Титриметрический метод анализа
Титриметрический метод анализа Соляная кислота (HCI)
Соляная кислота (HCI) Кількість речовини. Моль - одиниця кількості речовини. Число Авогадро
Кількість речовини. Моль - одиниця кількості речовини. Число Авогадро The nobel prize in chemistry 2020
The nobel prize in chemistry 2020 Автомобильные бензины
Автомобильные бензины Алкени і алкіни
Алкени і алкіни Расчеты по химическим уравнениям. Алгоритм решения расчетных задач
Расчеты по химическим уравнениям. Алгоритм решения расчетных задач Акарицидтер. Тетразиндер. Бензи-латтар. Сульфоқышқыл туындылары. Хина-золиндер . Пирозолдар. Пиридазипондар
Акарицидтер. Тетразиндер. Бензи-латтар. Сульфоқышқыл туындылары. Хина-золиндер . Пирозолдар. Пиридазипондар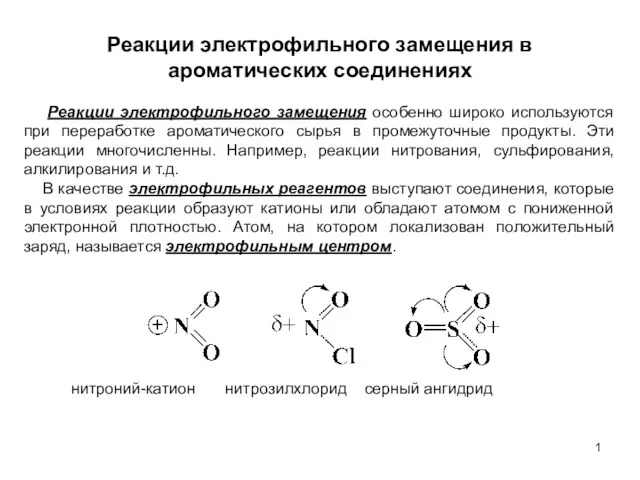 Реакции электрофильного замещения в ароматических соединениях. (Лекция 6)
Реакции электрофильного замещения в ароматических соединениях. (Лекция 6) Ионное произведение воды. Понятие о рН раствора
Ионное произведение воды. Понятие о рН раствора Органическая химия
Органическая химия Масса и формулы (8 класс)
Масса и формулы (8 класс) Органическая химия. Альдегиды и кетоны
Органическая химия. Альдегиды и кетоны Общая и неорганическая химия
Общая и неорганическая химия Диэлектрофорез: движение клеток или частиц в неоднородном переменном электрическом поле
Диэлектрофорез: движение клеток или частиц в неоднородном переменном электрическом поле Неорганические вяжущие вещества. (Лекция 6)
Неорганические вяжущие вещества. (Лекция 6) Современные методы образования амидной связи с использованием ацилгалогенидов, ангидридов, активированных эфиров и их аналогов
Современные методы образования амидной связи с использованием ацилгалогенидов, ангидридов, активированных эфиров и их аналогов Кристаллы и их свойства. Понятие о симметрии кристаллов и элементах симметрии. Сингония
Кристаллы и их свойства. Понятие о симметрии кристаллов и элементах симметрии. Сингония Полимеры. Мономер
Полимеры. Мономер Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості (10 клас)
Альдегіди. Карбонові кислоти. Одержання. Фізичні та хімічні властивості (10 клас) Термопластические полимеры
Термопластические полимеры Новое направление в бизнесе компании – катализаторы синтеза метанола
Новое направление в бизнесе компании – катализаторы синтеза метанола История открытия кислорода
История открытия кислорода