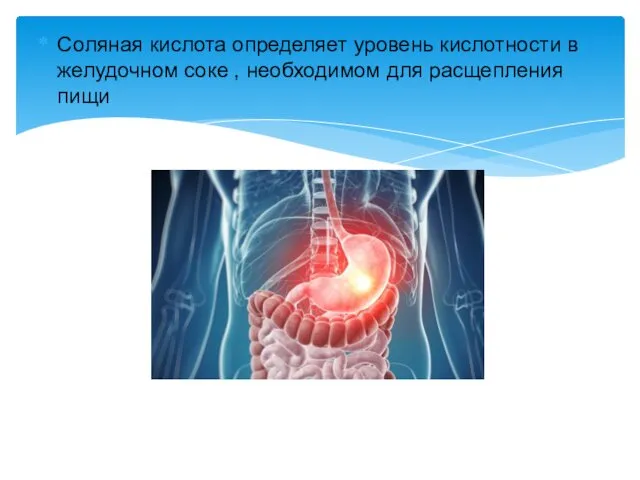
На вид раствор бесцветный. Выдает его запах. Он кислый, удушливый. Аромат
резкий и, скорее, характеризуется, как вонь.
Растворяя хлороводород в воде, можно получить даже 40% раствор соляной кислоты с плотностью 1,19 г/см3. Однако имеющаяся в продаже концентрированная соляная кислота содержит около 0,37 массовых долей, или около 37% хлороводорода. Плотность данного раствора составляет примерно 1,19 г/см3. При разбавлении кислоты плотность ее раствора уменьшается.
Концентрированная соляная кислота является бесценным раствором, сильно дымящая во влажном воздухе, обладающая резким запахом вследствие выделения хлороводорода.
Физические свойства









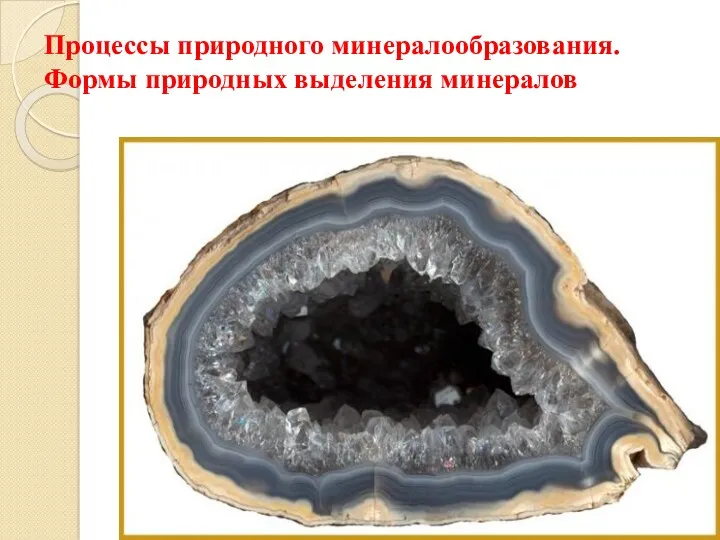 Процессы природного минералообразования. Формы природных выделений минералов
Процессы природного минералообразования. Формы природных выделений минералов Химический элемент титан
Химический элемент титан Химическая термодинамика
Химическая термодинамика Обзор электродных процессов
Обзор электродных процессов Азотсодержащие органические соединения
Азотсодержащие органические соединения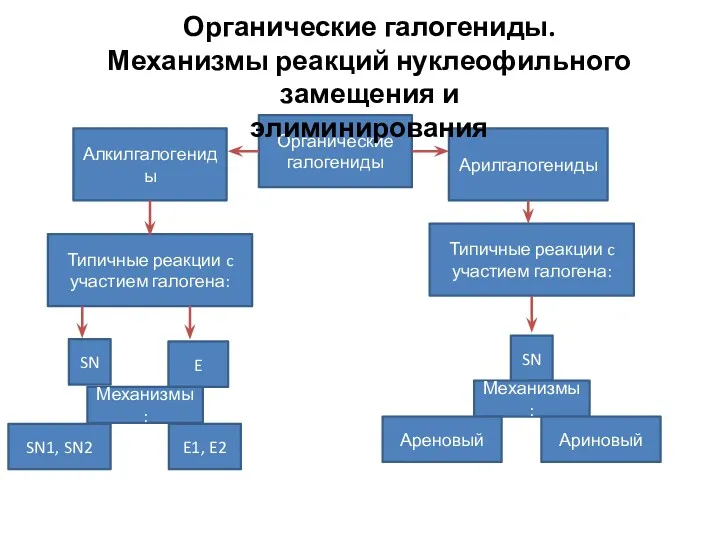
 Никель – тяжелый металл
Никель – тяжелый металл Хром. Строение атома
Хром. Строение атома ЕГЭ по химии. Решение задач 27, 28, 29
ЕГЭ по химии. Решение задач 27, 28, 29 Технология производства бутилкаучука
Технология производства бутилкаучука Катализ кислотами и основаниями. Лекция 3
Катализ кислотами и основаниями. Лекция 3 Силикатное производство
Силикатное производство серная кислота и ее соли 9 класс
серная кислота и ее соли 9 класс Химическая кинетика
Химическая кинетика Арены - ароматические соединения
Арены - ароматические соединения Электролиз растворов. Применение вытеснительного ряда металлов для прогнозирования продуктов электролиза
Электролиз растворов. Применение вытеснительного ряда металлов для прогнозирования продуктов электролиза Склад та властивості основних класів неорганічних сполук
Склад та властивості основних класів неорганічних сполук Воздух, которым мы дышим
Воздух, которым мы дышим Жуғыш заттардың адам өміріндегі маңызы
Жуғыш заттардың адам өміріндегі маңызы Строение и свойства атомов в свете квантовомеханической теории. Периодический закон – основа основ химии
Строение и свойства атомов в свете квантовомеханической теории. Периодический закон – основа основ химии Измерение и оценка химического фактора. Лекция 9
Измерение и оценка химического фактора. Лекция 9 Коррозия металлов
Коррозия металлов Неметаллы. Общая характеристика неметаллов
Неметаллы. Общая характеристика неметаллов Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю
Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю Периодическая система Д. И. Менделеева
Периодическая система Д. И. Менделеева Кислород. Открытие кислорода
Кислород. Открытие кислорода Lipid metabolism
Lipid metabolism Алканы: физические и химические свойства, получение
Алканы: физические и химические свойства, получение