Исследование термодинамических процессов водяного пара. Смеси идеальных газов. Влажный воздух. (Занятие 5) презентация
Содержание
- 2. Уравнение Ван-дер-Ваальса (1873): Уравнение состояния реальных газов
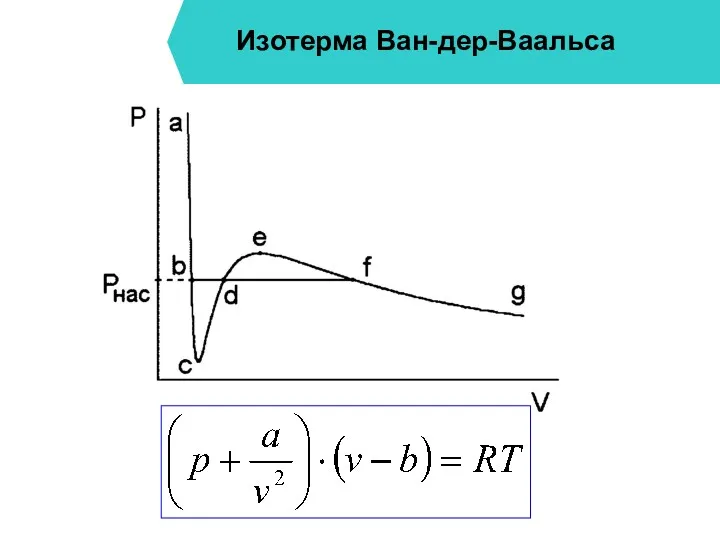
- 3. Изотерма Ван-дер-Ваальса
- 4. Изотерма Ван-дер-Ваальса
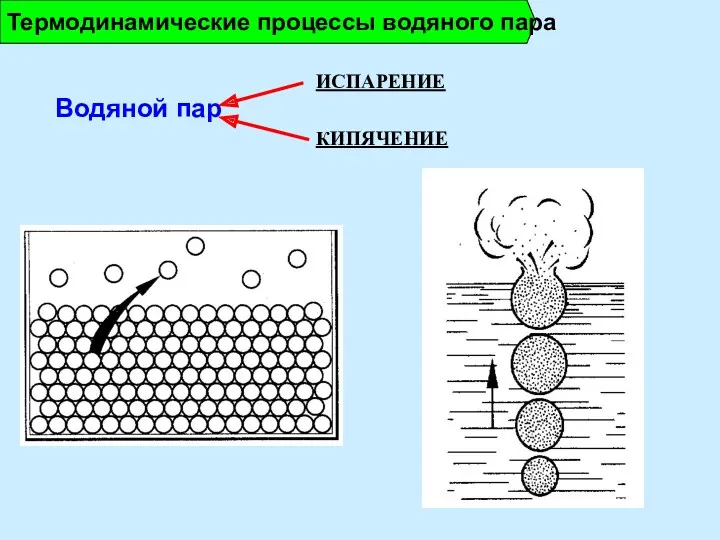
- 5. Водяной пар Термодинамические процессы водяного пара ИСПАРЕНИЕ КИПЯЧЕНИЕ
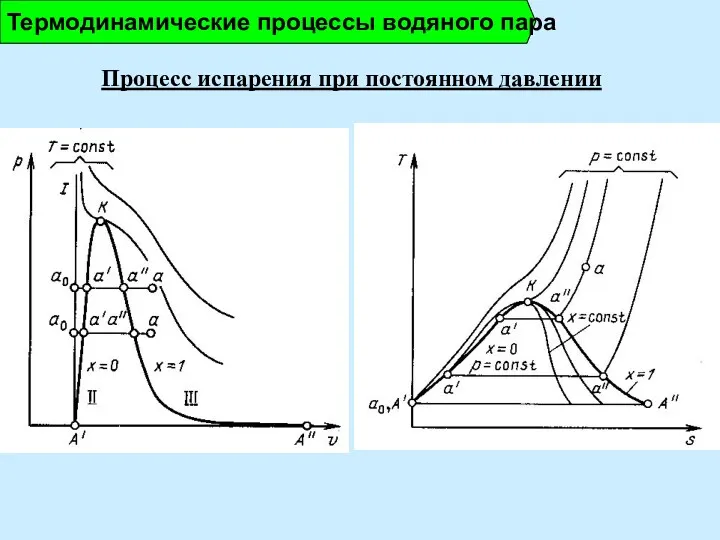
- 6. Термодинамические процессы водяного пара Процесс испарения при постоянном давлении
- 7. Параметры водяного пара Насыщенный – пар, находящийся в термическом и динамическом равновесии с жидкостью из которой
- 8. Параметры водяного пара Насыщенный – пар, находящийся в термическом и динамическом равновесии с жидкостью из которой
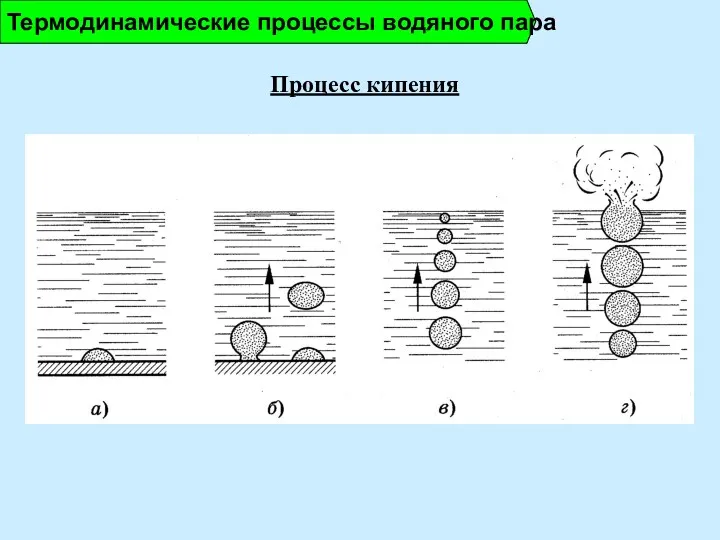
- 9. Термодинамические процессы водяного пара Процесс кипения
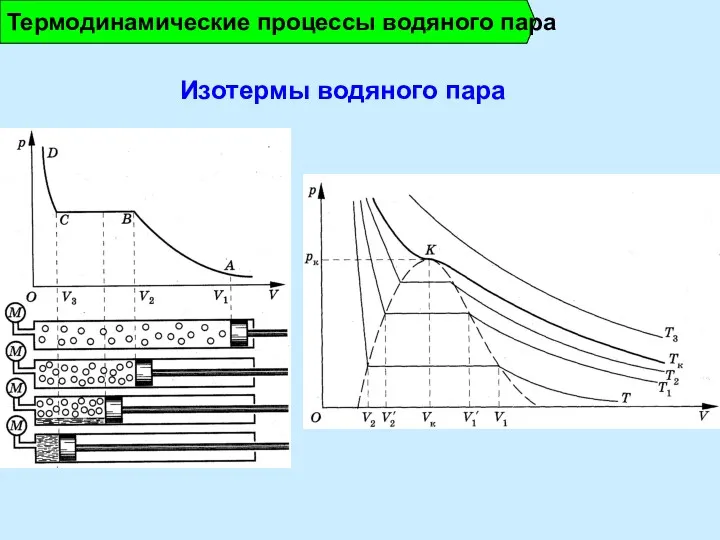
- 10. Изотермы водяного пара Термодинамические процессы водяного пара
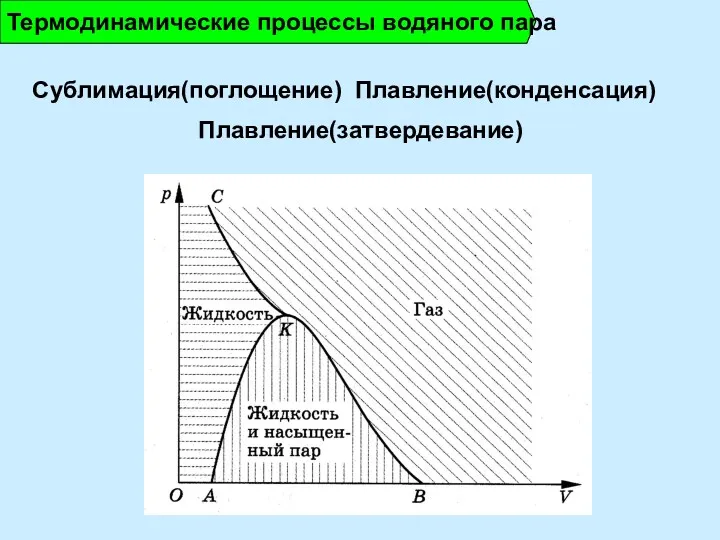
- 11. Сублимация(поглощение) Плавление(конденсация) Плавление(затвердевание) Термодинамические процессы водяного пара
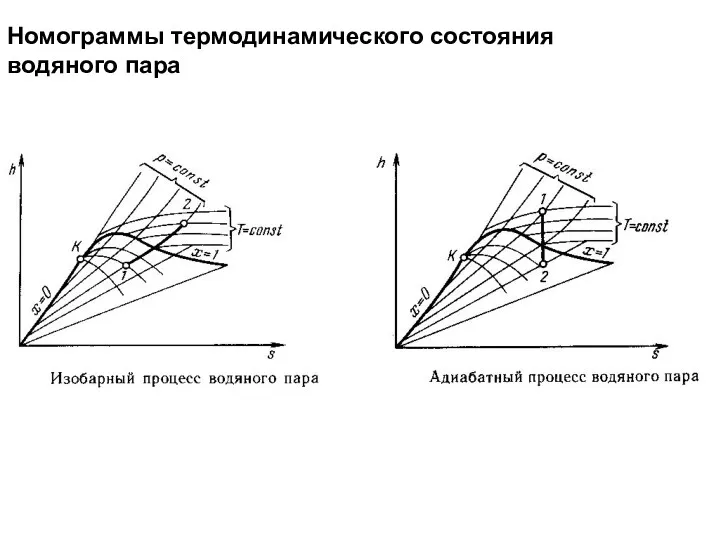
- 12. Номограммы термодинамического состояния водяного пара
- 13. Смеси идеальных газов Газовая смесь – механическая смесь отдельных компонентов различных газов, химически не реагирующих между
- 14. Смеси идеальных газов . 3. Каждый из газов, входящих в смесь, подчиняется своему уравнению состояния. 4.
- 15. Смеси идеальных газов Закон Дальтона - давление смеси газов, химически не взаимодействующих друг с другом, равно
- 16. Смеси идеальных газов Для каждого компонента смеси уравнение состояния следует записывать так: Массовая доля Объемная доля
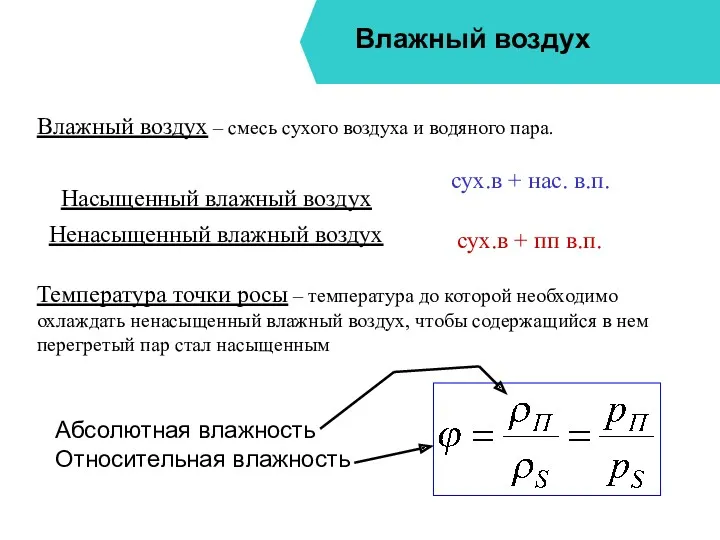
- 17. Влажный воздух Влажный воздух – смесь сухого воздуха и водяного пара. сух.в + нас. в.п. Температура
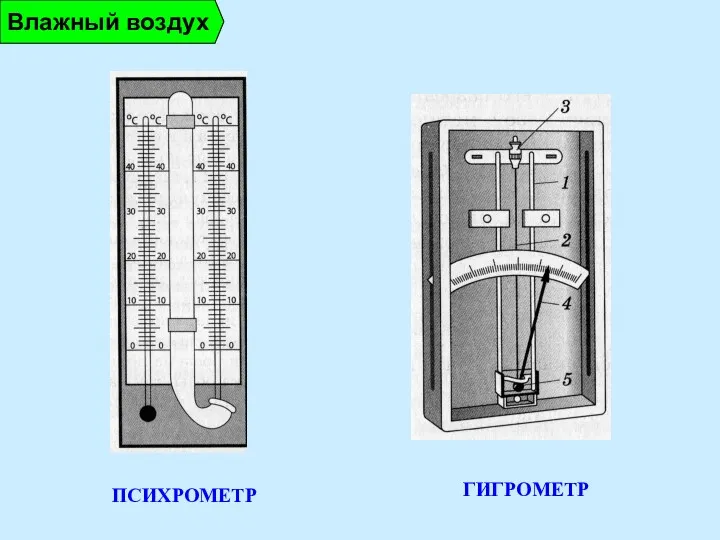
- 18. Влажный воздух ПСИХРОМЕТР ГИГРОМЕТР
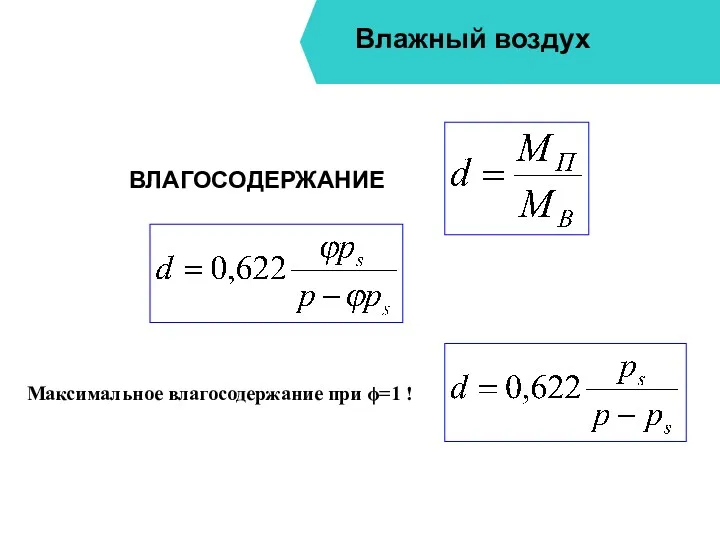
- 19. Влажный воздух ВЛАГОСОДЕРЖАНИЕ Максимальное влагосодержание при ϕ=1 !
- 20. Влажный воздух Теплоемкость и энтальпия При теплоемкости сухого воздуха 1 кДж/(кг·К) и водяного пара 2 кДж/(кг·К)
- 22. Скачать презентацию









 Постоянный электрический ток
Постоянный электрический ток Электромагнетизм. Уравнения Максвелла. Лекция 4
Электромагнетизм. Уравнения Максвелла. Лекция 4 Электромагнитное поле. Электромагнитные волны
Электромагнитное поле. Электромагнитные волны Лабораторная работа по физике в 11 классе Наблюдение линейчатого и сплошного спектров
Лабораторная работа по физике в 11 классе Наблюдение линейчатого и сплошного спектров Датчики. Датчики крутящего момента. Датчики уровня
Датчики. Датчики крутящего момента. Датчики уровня Процедура разборки КПП Wet 8DCT (D8LF1)
Процедура разборки КПП Wet 8DCT (D8LF1) Unusual modes pf transport
Unusual modes pf transport Техническая термодинамика. Второй закон термодинамики. (Лекция 3)
Техническая термодинамика. Второй закон термодинамики. (Лекция 3) Простые механизмы. Работа. Мощность. Энергия
Простые механизмы. Работа. Мощность. Энергия Способы восстановления деталей
Способы восстановления деталей Магнитное поле. 11 класс
Магнитное поле. 11 класс Физические явления
Физические явления Электростатика. Электризация. Заряд. Взаимодействие зарядов. Закон Кулона
Электростатика. Электризация. Заряд. Взаимодействие зарядов. Закон Кулона Волновые процессы. Эффект Допплера. (Лекция 1)
Волновые процессы. Эффект Допплера. (Лекция 1) Электростатика. Тема 1. Электростатическое поле в вакууме
Электростатика. Тема 1. Электростатическое поле в вакууме Урок № 36 2 Промывочные жидкости
Урок № 36 2 Промывочные жидкости Линзы. Понятие о линзе
Линзы. Понятие о линзе Закони збереження в механіці
Закони збереження в механіці Электромагнитная индукция. Энергия магнитного поля. Лекция №11
Электромагнитная индукция. Энергия магнитного поля. Лекция №11 Модель атома. Опыт Резерфорда. Постулаты Бора
Модель атома. Опыт Резерфорда. Постулаты Бора Гидродинамика
Гидродинамика Охлаждение, нагревание тел конечных размеров. Нагрев параллелепипеда
Охлаждение, нагревание тел конечных размеров. Нагрев параллелепипеда Анализ сигналов
Анализ сигналов Физико – химические характеристики электротехнических материалов
Физико – химические характеристики электротехнических материалов Коробка скоростей
Коробка скоростей Электроразведка. Электромагнитные зондирования
Электроразведка. Электромагнитные зондирования Лекция 15. Тема: Закон Био-Савара - Лапласа
Лекция 15. Тема: Закон Био-Савара - Лапласа Предыстория радиотехники. Лекция 1
Предыстория радиотехники. Лекция 1