Содержание
- 2. Для газов удобно пользоваться молярной тепло-емкостью Сμ − количество теплоты необходимое для нагревания 1 моля газа
- 3. Если газ нагревать при постоян-ном объёме, то всё подводимое тепло идёт на нагревание газа, то есть
- 4. Итак, подводимое тепло и теплоёмкость зависят от того, каким путём осуществляется передача тепла. Следовательно Q и
- 5. В общем случае (22.13) так как U может зависеть не только от температуры. Но в случае
- 6. Для произвольной массы идеального газа: (22.16) При изобарическом процессе кроме увеличения внутренней энергии происходит совершение работы
- 7. Подставим полученный результат в уравнение (22.18) Сp = СV + R (22.19) это уравнение Майера для
- 8. 3. Теплоёмкости одноатомных и многоатомных газов Напомню, что в одном моле содержится NА = 6,02⋅1023 молекул.
- 9. Внутренняя энергия произвольного количества газа: (22.24) Её изменение: (22.25) Теплоёмкости одноатомных газов СV и СР: (22.26)
- 10. Учитывая физический смысл R для изобаричес-ких процессов можно записать: dQP = dUμ + RdT (для одного
- 11. Тогда и из этого следует, что (22.30) Кроме того Подставив в выражение для внутренней энергии: а
- 12. Теплоемкости многоатомных газов Однако опыты с азотом и кислородом и другими двухатомными газами дали А для
- 13. Ранее было введено понятие числа степеней свободы — числа независимых переменных (координат), полностью определяющих положение системы
- 14. Трехатомная (рис. 22.3, в) и многоатомная нелинейные молекулы имеют шесть степеней свободы — три поступательных и
- 15. вращательного движений), но и потенциальная энергия, причем средние значения кинетической и потенциальной энергий одинаковы. Таким образом,
- 16. 4. Закон о равномерном распределении энергии по степеням свободы Итак, средняя энергия приходящаяся на одну степень
- 17. Но на среднюю кинетическую энергию молекулы, имеющей i-степеней свободы приходится (22.35) Это и есть закон Больцмана
- 18. В общем случае, для молярной массы газа (22.36) (22.37) (22.38) Для произвольного количества газов: (22.39) (22.40)
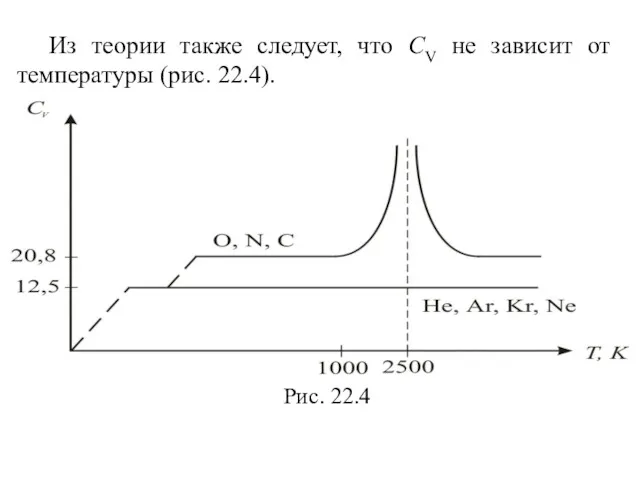
- 19. Из теории также следует, что СV не зависит от температуры (рис. 22.4).
- 20. Для одноатомных газов это выполняется в очень широких пределах, а для двухатомных газов только в интервале
- 21. Одна колебательная степень свободы несёт так как при этом есть и кинетическая и потенциальная энергия, то
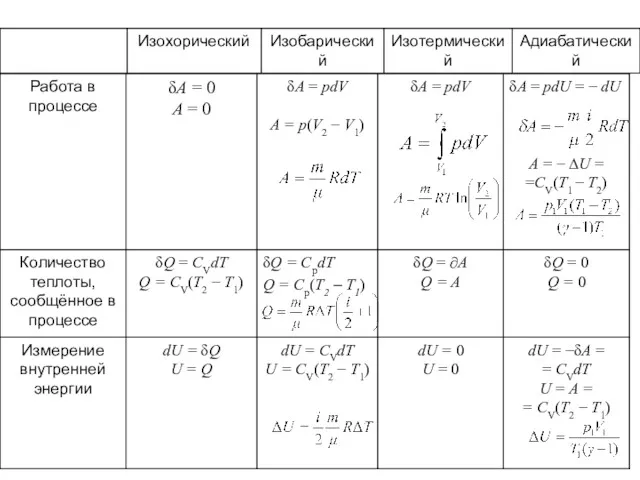
- 22. 5. Применение первого начала термодинамики к изопроцессам идеальных газов В таблице (22.1) приводятся сводные данные о
- 23. - удельная теплоемкость; - молярная теплоемкость; Ср= СV + R - уравнение Майера; - показатель адиабаты
- 26. Здесь уместно рассмотреть еще и политропный процесс – такой процесс, при котором изменяются все основные параметры
- 27. С помощью этого показателя можно легко описать любой изопроцесс: 1. Изобарный процесс р = const, n
- 29. Скачать презентацию
























 Ректификация үдерісі
Ректификация үдерісі Ремонт колёсных пар и буксовых узлов
Ремонт колёсных пар и буксовых узлов AdvPh mirrors
AdvPh mirrors Сопротивление материалов
Сопротивление материалов Блез Паскаль — французский математик, механик, физик, литератор и философ
Блез Паскаль — французский математик, механик, физик, литератор и философ Изоляторы ЛЭП. Линейные изоляторы
Изоляторы ЛЭП. Линейные изоляторы 1. Строение атома
1. Строение атома Магнитные материалы. Магнитное поле в веществе
Магнитные материалы. Магнитное поле в веществе Передача давления жидкостями и газами. Закон Паскаля
Передача давления жидкостями и газами. Закон Паскаля Покорение Силы
Покорение Силы Требования к заданиям с развернутым ответом в ЕГЭ по физике
Требования к заданиям с развернутым ответом в ЕГЭ по физике Электромагнитное излучение на границе раздела сред и в структурированном веществе. Оптическая микроскопия ближнего поля
Электромагнитное излучение на границе раздела сред и в структурированном веществе. Оптическая микроскопия ближнего поля Газовые законы
Газовые законы Физика и познание мира
Физика и познание мира Ременные передачи
Ременные передачи Свет и цвета тел
Свет и цвета тел Урок по физике в 8 классе на тему Влажность воздуха
Урок по физике в 8 классе на тему Влажность воздуха Голография
Голография Магнитопорошковая дефектоскопия сварных швов
Магнитопорошковая дефектоскопия сварных швов R,C,L в цепи переменного тока
R,C,L в цепи переменного тока Magnetismo, Fluidos e Perispírito
Magnetismo, Fluidos e Perispírito Решение задач по ядерной физике
Решение задач по ядерной физике Сопротивление материалов. Основные требования к деталям и конструкциям и виды расчетов
Сопротивление материалов. Основные требования к деталям и конструкциям и виды расчетов Отопитель и климатическая установка в современных автомобилях
Отопитель и климатическая установка в современных автомобилях Импульс тела. Закон сохранения
Импульс тела. Закон сохранения Гармонические колебания и их характеристики
Гармонические колебания и их характеристики Основы электродинамики
Основы электродинамики Трёхфазные цепи
Трёхфазные цепи