Типы оптических спектров. Поглощение и испускание света атомами. Происхождение линейчатых спектров презентация
Содержание
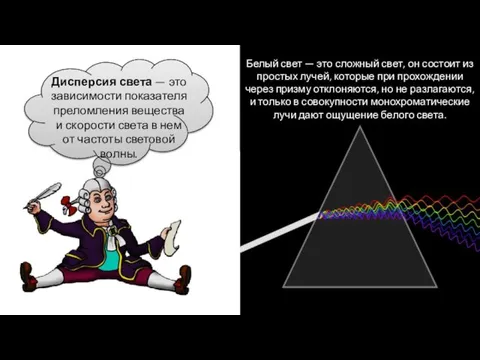
- 2. Белый свет — это сложный свет, он состоит из простых лучей, которые при прохождении через призму
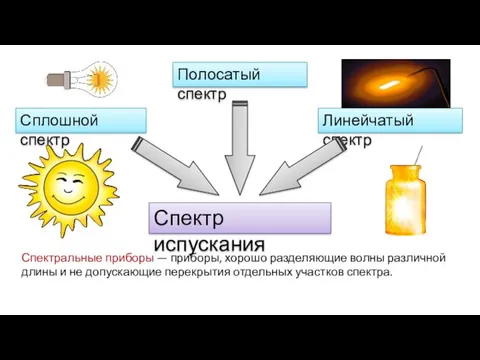
- 3. Спектральные приборы — приборы, хорошо разделяющие волны различ-ной длины и не допускающие перек-рытия отдельных участков спектра.
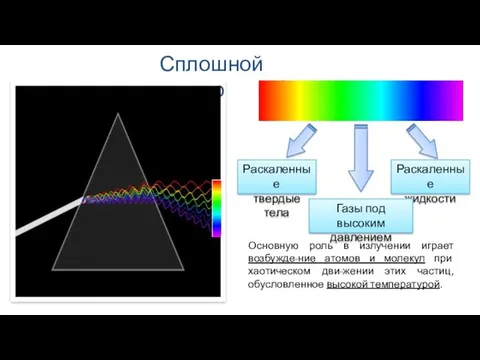
- 4. Сплошной спектр Раскаленные твердые тела Раскаленные жидкости Газы под высоким давлением Основную роль в излучении играет
- 5. Линейчатый спектр спектр, состоящий из отдельных резко очерченных цветных линий, отделенных друг от друга широкими темными
- 6. Полосатый спектр состоит из отдельных полос, разделенных темными промежутками. Каждая полоса представляет собой совокупность большого числа
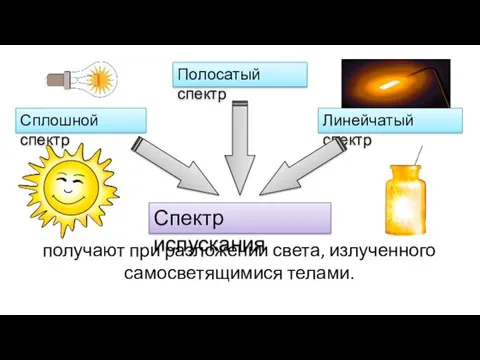
- 7. Спектр испускания Сплошной спектр Линейчатый спектр Полосатый спектр получают при разложении света, излученного самосветящимися телами.
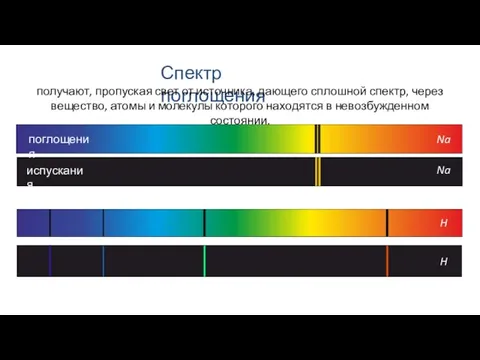
- 8. Спектр поглощения получают, пропуская свет от источника, дающего сплошной спектр, через вещество, атомы и молекулы которого
- 9. Густав Роберт Кирхгоф 12. 03. 1824 — 17. 10. 1887 1859 год Закон обратимости спектральных линий:
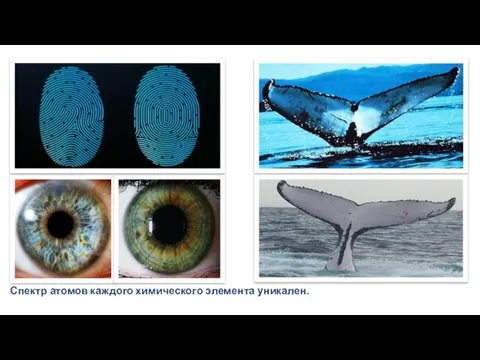
- 10. Спектр атомов каждого химического элемента уникален.
- 11. Г. Кирхгоф В. Бунзен 1859 год Спектральный анализ — это ме-тод исследования химического состава различных веществ
- 12. Эмиссионный анализ: 1. Каждый элемент имеет свой спектр, который не зависит от способов воз-буждения. 2. Интенсивность
- 13. Применение спектрального анализа металлургия машиностроение Атомная промышленность геология археология криминалистика
- 14. Как объяснить, почему атомы каждого химиче-ского элемента имеют свой строго индивидуаль-ный набор спектральных линий? Почему совпадают
- 15. Нильс Хенрик Давид Бор 7. 10. 1885 — 18. 11. 1962 Постулат стационарных состояний: атомная система
- 16. Состояние атома, в котором все элек-троны находятся на стационарных орбитах с наименьшей возможной энергией, называется основным.
- 17. Спектр испускания Сплошной спектр Линейчатый спектр Полосатый спектр Спектральные приборы — приборы, хорошо разделяющие волны различной
- 19. Скачать презентацию










 Свойства воды
Свойства воды Решение задач по теме Законы Ньютона
Решение задач по теме Законы Ньютона Рабочий режим насоса и его регулирование. (Лекция 7)
Рабочий режим насоса и его регулирование. (Лекция 7) Какое движение называют механическим?
Какое движение называют механическим? Молекулярно-кинетическая теория вещества
Молекулярно-кинетическая теория вещества Презентация Задачи по физике. 7 класс.(Г. Остер)
Презентация Задачи по физике. 7 класс.(Г. Остер) Стартовая презентация к проекту Зрение и компьютер
Стартовая презентация к проекту Зрение и компьютер Водородная бомба
Водородная бомба Презентация по теме: Механические колебания
Презентация по теме: Механические колебания Замедление нейтронов. Уравнение переноса
Замедление нейтронов. Уравнение переноса Основные уравнения электростатики в вакууме. (Лекция 2)
Основные уравнения электростатики в вакууме. (Лекция 2) Исследовательская работа учащихся .
Исследовательская работа учащихся . Повторительно-обобщающий урок по теме Движение и взаимодействие тел (7 класс)
Повторительно-обобщающий урок по теме Движение и взаимодействие тел (7 класс) Презентация к Научно-исследовательской работе Физика и ВОВ
Презентация к Научно-исследовательской работе Физика и ВОВ Аккумуляторные батареи. Назначение аккумуляторных батарей и их основные характеристики
Аккумуляторные батареи. Назначение аккумуляторных батарей и их основные характеристики Магнитное поле Земли
Магнитное поле Земли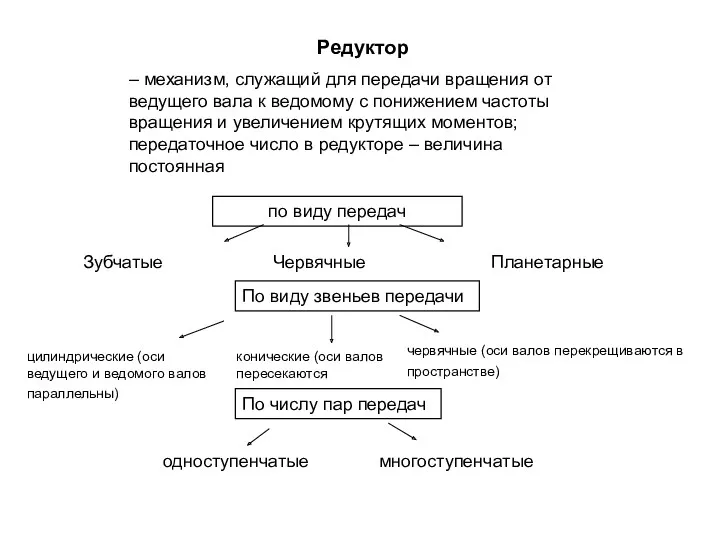 Редукторы по виду передач, по виду звеньев передачи, по числу пар передач
Редукторы по виду передач, по виду звеньев передачи, по числу пар передач Происхождение элементов
Происхождение элементов Способы изменения внутренней энергии
Способы изменения внутренней энергии Вес тела. Сила тяжести. Динамометр
Вес тела. Сила тяжести. Динамометр Презентация к уроку Виды сил. Равнодействующая сила. Правила сложения сил для 7 класса
Презентация к уроку Виды сил. Равнодействующая сила. Правила сложения сил для 7 класса Природа света. Световые волны. Законы отражения и преломления. Интерференция. Дифракция
Природа света. Световые волны. Законы отражения и преломления. Интерференция. Дифракция Интегрированный урок физика- математика Применение производной при решении физических задач
Интегрированный урок физика- математика Применение производной при решении физических задач Изотопы. Радиоактивные превращения атомных ядер
Изотопы. Радиоактивные превращения атомных ядер Адсорбция үдерісі
Адсорбция үдерісі Растяжение и сжатие
Растяжение и сжатие Устройство колесных пар
Устройство колесных пар История патефона
История патефона