Содержание
- 2. Макроскопические параметры – это…: Масса, давление, объем, температура давление, объем, температура
- 3. Состояние газа данной массы характеризуется тремя макроскопическими параметрами: давлением– р, объемом – V и температурой –
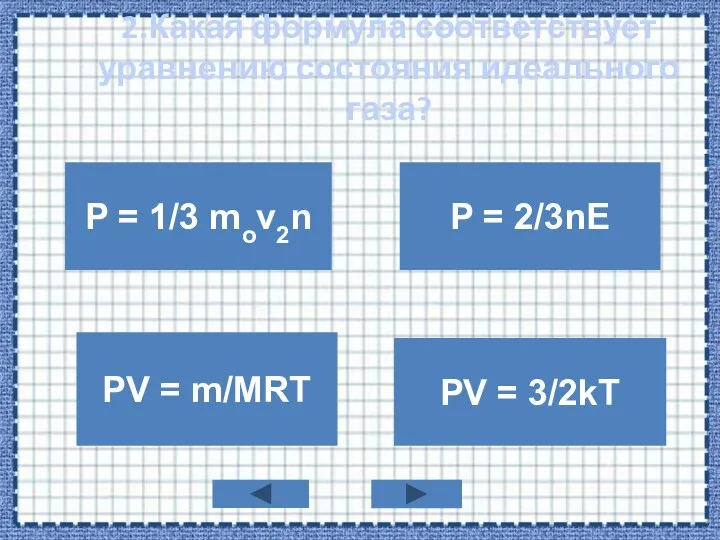
- 4. 2.Какая формула соответствует уравнению состояния идеального газа? P = 1/3 mov2n PV = m/MRT P =
- 5. Ответ неверен! Повтори теорию!
- 6. Молодец! Можешь приступать к следующему вопросу
- 7. Ответ неверен! Повтори теорию!
- 8. Уравнение, связывающее все три макроскопических параметра р, V и T, характеризующие состояние достаточно разряженного газа данной
- 9. Молодец! Можешь приступать к следующему вопросу
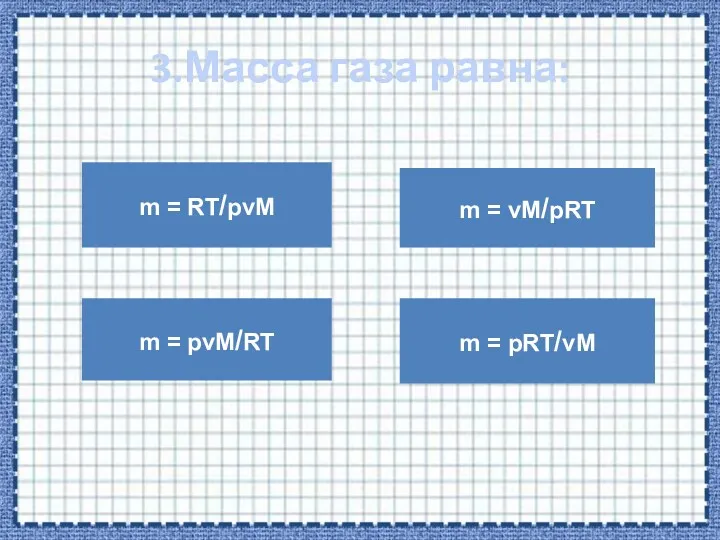
- 10. 3.Масса газа равна: m = RT/pvM m = pvM/RT m = vM/pRT m = pRT/vM
- 11. Молодец! Можешь приступать к следующему вопросу
- 12. Ответ неверен! Повтори теорию!
- 13. pv = m/MRT Чтобы выразить неизвестную величину из уравнения Менделеева – Клапейрона, умножь левую и правую
- 14. Универсальная газовая постоянная численно равна…: 6,022 *10 23 моль-1 1,38 * 10 – 23Дж/К 8,31 Дж/
- 15. Ответ неверен! Повтори теорию!
- 16. Молодец! Можешь приступать к следующему вопросу
- 17. Произведение постоянной Больцмана к и постоянной Авогадро Na называют универсальной газовой постоянной и обозначают буквой R
- 18. Процесс изменения состояния системы макроскопических тел (термодинамической системы) при постоянной температуре называется… изобарный изохорный изотермический
- 19. pv = const Согласно уравнению состояния газа в любом состоянии с неизменной температурой произведение давления газа
- 20. Молодец! Можешь приступать к следующему вопросу
- 21. Ответ неверен! Повтори теорию!
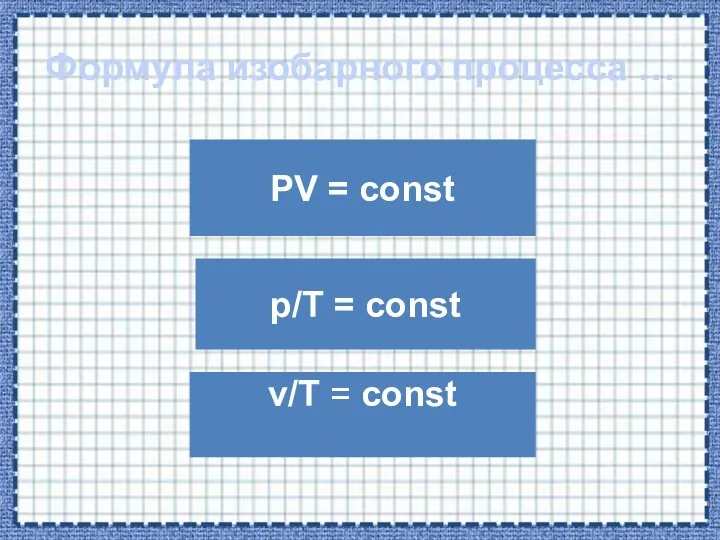
- 22. Формула изобарного процесса … PV = const v/T = const p/T = const
- 23. Ответ неверен! Повтори теорию!
- 24. Молодец! Можешь приступать к следующему вопросу
- 25. P = const Для данной массы газа отношение объема к температуре постоянно, если давление газа не
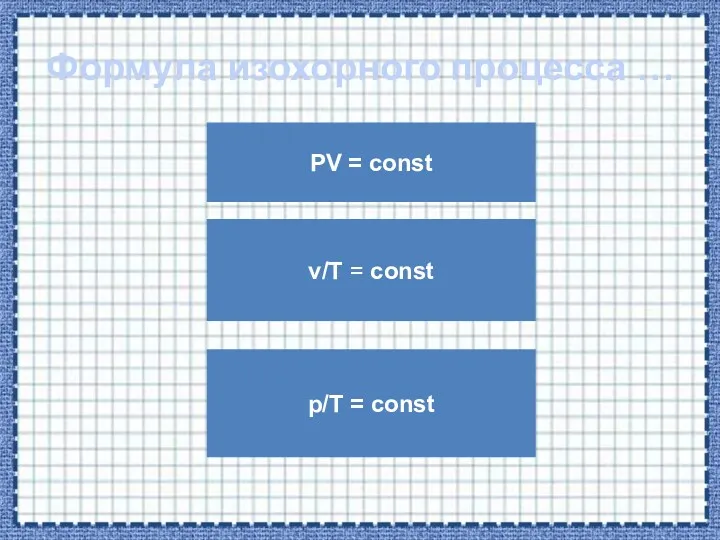
- 26. Формула изохорного процесса … PV = const p/T = const v/T = const
- 27. Ответ неверен! Повтори теорию!
- 28. Молодец! Можешь приступать к следующему вопросу
- 29. p/T = const Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным. Газовый закон Шарля.
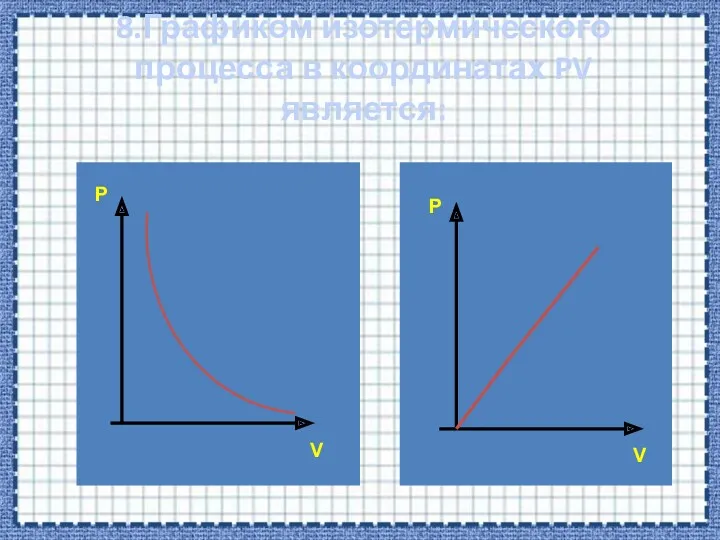
- 30. 8.Графиком изотермического процесса в координатах PV является: P P V V
- 31. Молодец! Можешь приступать к следующему вопросу
- 32. Ответ неверен! Повтори теорию!
- 33. Р V Зависимость между давлением и объемом в изотермическом процессе обратно пропорциональная. Графиком в координатах PV
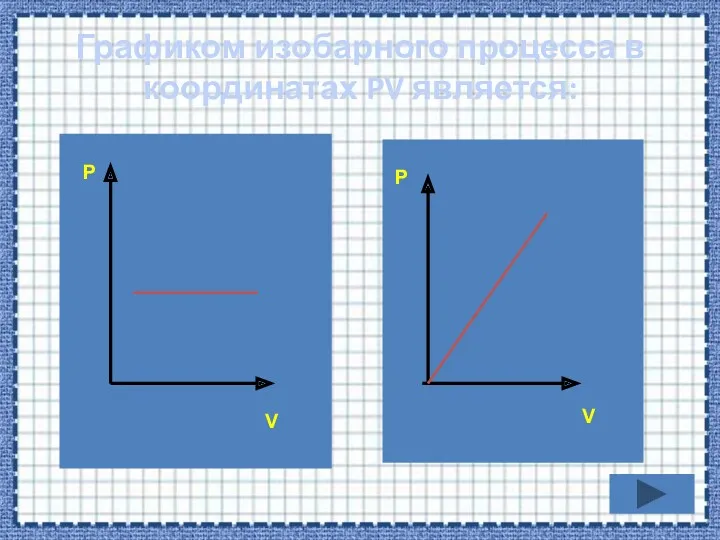
- 34. Графиком изобарного процесса в координатах PV является: P V P V
- 35. Молодец! Можешь приступать к следующему вопросу
- 36. Ответ неверен! Повтори теорию!
- 37. Если процесс изобарный давление постоянно, в координатах PV график прямая линия параллельная оси объема. Р V
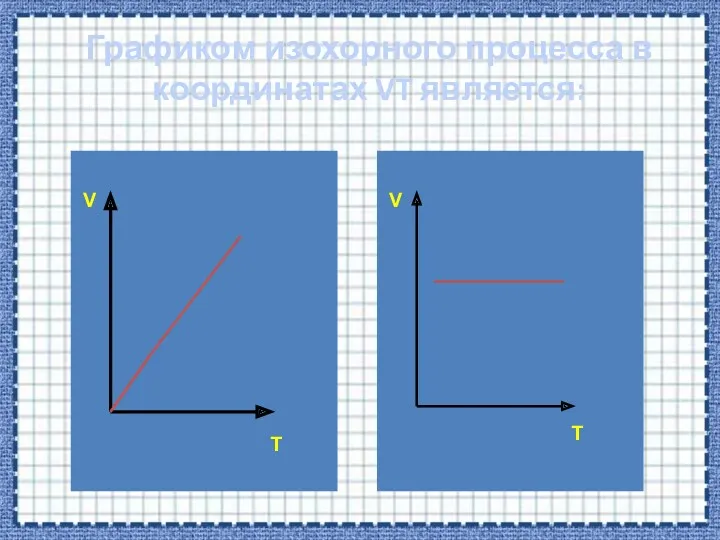
- 38. Графиком изохорного процесса в координатах VT является: V V T T
- 39. Молодец! Можешь приступать к следующему вопросу
- 40. Ответ неверен! Повтори теорию!
- 41. V T Если процесс изохорный объем постоянный, в координатах VT график - прямая линия параллельная оси
- 42. Реши задачу: В сосуде вместимостью 500 см3 содержится 0,89 г водорода при температуре 170С. Определите давление
- 43. Молодец! Задача решена правильно! Решим еще!
- 44. Ответ неверен! Проанализируй правильное решение задачи
- 45. Дано: V=500см3 =500*10-6м3 m = 0,89г = 0,89 *10-3кг T = 2900К R = 8,31 Дж/моль
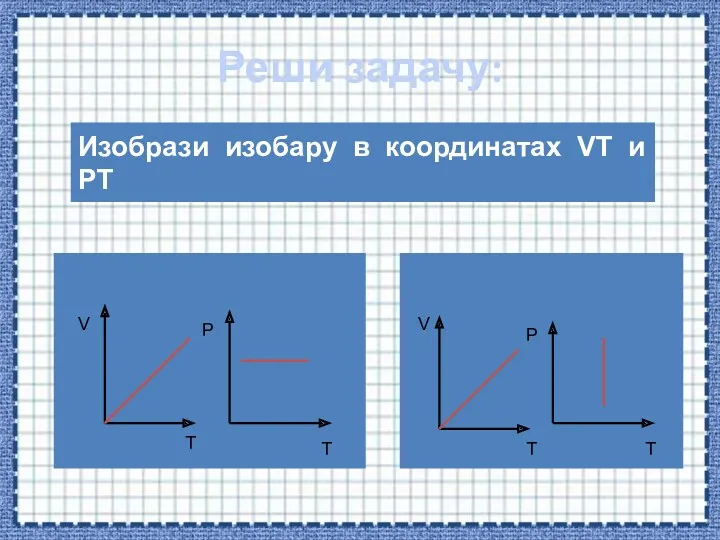
- 46. Реши задачу: Изобрази изобару в координатах VT и PT V T P T V T P
- 47. Поздравляю! Ты знаешь данную тему
- 49. Скачать презентацию




































 Кипение. Удельная теплота парообразования и конденсации.
Кипение. Удельная теплота парообразования и конденсации. Презентация к уроку физики в 7 классе по теме Давление. Единицы давления. Способы увеличения и уменьшения давления
Презентация к уроку физики в 7 классе по теме Давление. Единицы давления. Способы увеличения и уменьшения давления Виды ламп освещения
Виды ламп освещения ДЕЯТЕЛЬНОСТНЫЙ ПОДХОД В ПРЕПОДАВАНИИ ФИЗИКИ Диск
ДЕЯТЕЛЬНОСТНЫЙ ПОДХОД В ПРЕПОДАВАНИИ ФИЗИКИ Диск Фізичні методи дослідження хімічних сполук
Фізичні методи дослідження хімічних сполук Электротехника. Методы расчёта электрических цепей. (лекция 4)
Электротехника. Методы расчёта электрических цепей. (лекция 4) Работа и мощность электрического тока. 8 класс
Работа и мощность электрического тока. 8 класс Сұйықтардың беттік керілуі
Сұйықтардың беттік керілуі Кинематика точки (Лекция 1, кафедра теоретической механики )
Кинематика точки (Лекция 1, кафедра теоретической механики ) Механические колебания и волны. Звук
Механические колебания и волны. Звук Конденсатор - устройство, предназначенное для накопления заряда и энергии электрического поля
Конденсатор - устройство, предназначенное для накопления заряда и энергии электрического поля Электромагнит
Электромагнит Измерение работы силы трения, расчет погрешностей косвенных измерений
Измерение работы силы трения, расчет погрешностей косвенных измерений Люминесцентный анализ
Люминесцентный анализ Анализ рабочих процессов и их влияние на формирование эксплуатационных свойств автомобиля
Анализ рабочих процессов и их влияние на формирование эксплуатационных свойств автомобиля Постоянные магниты
Постоянные магниты Електричний струм у газах. Самостійний і несамостійний газові розряди. Плазма
Електричний струм у газах. Самостійний і несамостійний газові розряди. Плазма Арматура и ее свойства. Робот для вязки арматуры (9 класс)
Арматура и ее свойства. Робот для вязки арматуры (9 класс) Плоское движение твёрдого тела
Плоское движение твёрдого тела Основные термодинамические процессы идеального газа
Основные термодинамические процессы идеального газа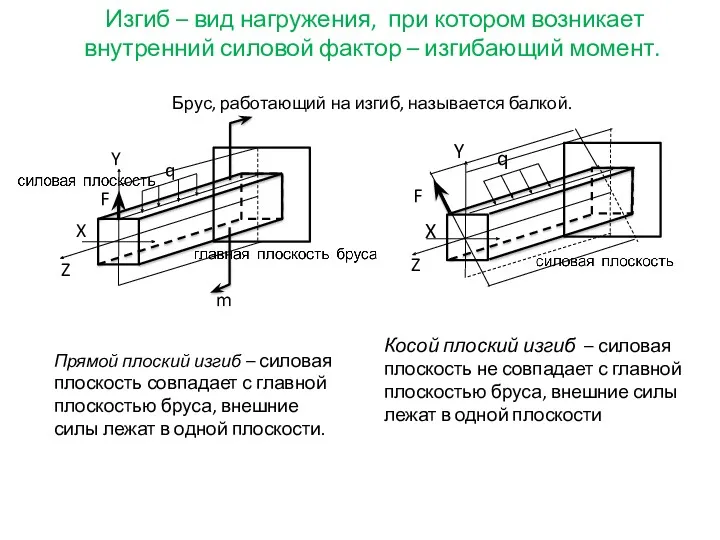 Изгиб бруса. Виды изгибов
Изгиб бруса. Виды изгибов Задачи на закон Ома
Задачи на закон Ома Axles and shafts
Axles and shafts Кинематический и силовой расчет привода
Кинематический и силовой расчет привода Основні способи отримання низьких та наднизьких температур
Основні способи отримання низьких та наднизьких температур Радиолокация и ее техническое применение
Радиолокация и ее техническое применение Тепломассообмен. Основы теории массообмена. (Лекция 16)
Тепломассообмен. Основы теории массообмена. (Лекция 16) Звук - физическое явление
Звук - физическое явление