Содержание
- 3. План Cпецифика доклинических испытаний Этические нормы проведения экспериментов на животных Концепция трех «R» Этико-правовое регулирование доклинических
- 4. «Чем полнее будет проделан опыт на животных, тем менее часто больным придется быть в положении опытного
- 5. Доклиническое исследование лекарственного средства – биологические, микробиологические, иммунологические, токсикологические, фармакологические, физические, химические и другие исследования лекарственного
- 6. Таким образом, целью доклинических исследований ЛС является получение научными методами оценок и доказательств их эффективности и
- 7. Доклинические исследования ЛС включают в себя следующие виды экспериментальных исследований: химические, физические, биологические, микробиологические, фармакологические, токсикологические
- 9. При токсикологических исследованиях устанавливают характер и выраженность возможного повреждающего воздействия препаратов на экспериментальных животных.
- 10. В токсикологических исследованиях выделяют три этапа: изучение острой токсичности вещества при однократном введении; определение хронической токсичности
- 11. В рамках этой проблемы можно выделить следующие точки зрения: своего рода антропоцентризм является ли человек высшей
- 12. В ХХ веке требование этичности стало обязательным условием проведения экспериментов на животных во всех странах мира
- 13. Этика экспериментов на животных Международный комитет по лабораторным животным в 1974 г. предложил следующее определение эксперимента
- 14. Эксперимент на животных необходим в случаях: когда изучаются популяции животных при проведении заключительных опытов по обработке
- 15. когда необходимо изучить отдельные результаты воздействия; когда органы и системы животного не могут быть изолированы; для
- 16. В начале 1985 г. Совет международных медицинских научных организаций (СММНО) опубликовал «Этический кодекс», который содержит «международные
- 17. Эксперименты на животных должны соответствовать строгим этическим нормам: цели одобрены обществом и этическим комитетом, основаны на
- 18. животные не используются в повторных экспериментах, которые превращают их жизнь в непрерывное страдание; умерщвление безболезненно; опыты
- 19. отказ от проведения эксперимента на живом организме, если ответ на научный вопрос может быть получен альтернативным
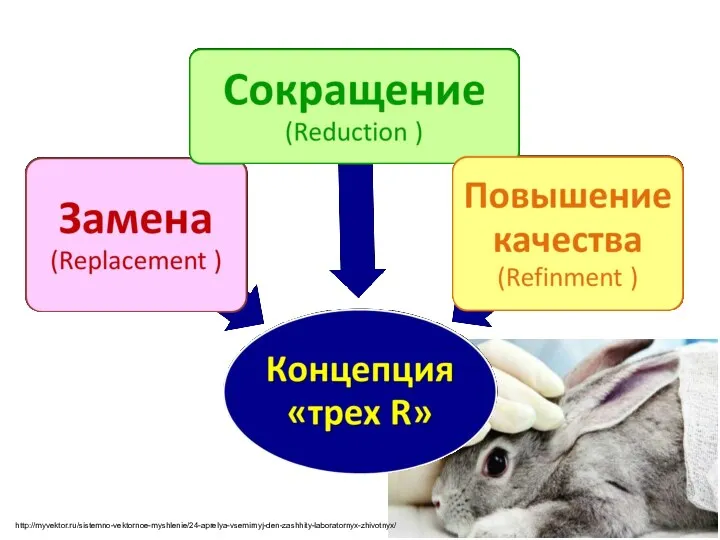
- 20. концепцией «трех R» У. Рассела и Р. Берча, описанной в их книге «Принципы гуманной экспериментальной техники»
- 21. http://myvektor.ru/sistemno-vektornoe-myshlenie/24-aprelya-vsemirnyj-den-zashhity-laboratornyx-zhivotnyx/
- 22. замена в опыте, когда это возможно, высокоорганизованных животных менее развитыми живыми объектами или применение альтернативных методов
- 23. достижение воспроизводимых результатов с использованием минимального количества животных; адекватный выбор лабораторных животных; оптимальное планирование https://infourok.ru/issledovatelskiy-proekt-na-temu-moy-domashniy-drug-krisa-407036.html Сокращение
- 24. улучшение условий содержания лабораторных животных и использования их в экспериментах, уменьшение дистресса животных во время экспериментов
- 25. В России доклинические исследования с использованием животных проводятся в соответствии с этическими и правовыми нормами использования
- 26. Этико-правовое регулирование доклинических испытаний в России Федеральный закон от 12.04.2010 N 61-ФЗ «Об обращении лекарственных средств»
- 27. Основы надлежащей лабораторной практики (GLP) Правила лабораторной практики устанавливают требования к: Организации ДИ, Планированию ДИ Проведению
- 28. Правила GLP содержат следующие разделы: Общие положения Проведение доклинического исследования лекарственного средства Система обеспечения качества доклинических
- 29. Согласно GLP ДИ проводятся в соответствии со следующими документами: план протокол первичные записи (записи в рабочих
- 30. В ПЛАНЕ ДИ излагаются схемы и график проведения ДИ (включая его этапы и части), описываются цели,
- 31. В протоколе ДИ фиксируются действия, связанные с выполнением процедур доклинического исследования, осуществляемые в соответствии с утвержденным
- 32. В отчет о результатах ДИ включаются: описание ДИ лекарственного средства, используемые методы исследования полученные результаты, статистический
- 33. Правила лабораторной практики (GLP) при использовании животных в доклинических исследованиях П. 23. Для экспериментальных исследований с
- 34. П. 33. Доклинические исследования проводятся на здоровых животных. Все процедуры, связанные с уходом за животными (кормление,
- 35. П. 58. В случае проведения экспериментальных исследований с использованием животных в отчете о результатах доклинического исследования
- 36. К альтернативным методам исследований относятся следующие: улучшенная система хранения и использования информации, а также обмен информацией
- 37. использование математических и компьютерных моделей; молекулярное моделирование и использование компьютерных графических средств; моделирование биохимических, физиологических, фармакологических,
- 38. использование низших организмов с ограниченной чувствительностью; использование позвоночных животных на ранних этапах их развития, предшествующих той
- 39. Стоит отметить, что результаты, полученные в процессе исследований на животных, не могут полностью гарантировать такого же
- 40. Правовую основу проведения КИ в России составляют Конституция РФ от 12.12.1993 ФЗ № 323 от 21.11.2011
- 41. Клинические испытания проводятся в соответствии с Национальным стандартом РФ «Надлежащая клиническая практика» Good Clinical Practice (GCP)
- 42. Надлежащая клиническая практика (GCP) представляет собой международный этический и научный стандарт планирования и проведения исследований с
- 43. Клинические исследования могут проводиться на базе одного исследовательского центра в одной стране (т.е. быть одноцентровыми), а
- 44. В большинстве исследований сравнивается два препарата, в некоторых исследованиях – три и более. Цель, задачи, дизайн,
- 45. Протокол – это своеобразная инструкция для врачей, проводящих исследование. Врачи-исследователи обязаны строго ему следовать, это служит
- 46. Правила опубликования результатов исследований Итоги исследований и экспериментов должны быть опубликованы в профессиональной литературе, иначе они
- 48. Скачать презентацию










































 Сестринский процесс при заболеваниях системы крови и кроветворных органов у детей
Сестринский процесс при заболеваниях системы крови и кроветворных органов у детей Стромалық-қантамырлық диспротеиноздар: мукоидті ісіну, фибриноидті ісіну, гиалиноз. Амилаидоз
Стромалық-қантамырлық диспротеиноздар: мукоидті ісіну, фибриноидті ісіну, гиалиноз. Амилаидоз № 2 Симптомдық артериальды гипертензия. № 3 вариант: Иценко-Кушинг синдромы кезіндегі
№ 2 Симптомдық артериальды гипертензия. № 3 вариант: Иценко-Кушинг синдромы кезіндегі Aspecte contemporane în diagnosticul şi tratamentul bronhopneumopatiei cronice obstructive
Aspecte contemporane în diagnosticul şi tratamentul bronhopneumopatiei cronice obstructive Ішкі сәулеленуден медициналық қорғану
Ішкі сәулеленуден медициналық қорғану Лучевые методы диагностики заболеваний органов дыхания
Лучевые методы диагностики заболеваний органов дыхания Методика адаптивного физического воспитания для обучающихся с задержкой психического развития
Методика адаптивного физического воспитания для обучающихся с задержкой психического развития Патогенные и условно патогенные микроорганизмы
Патогенные и условно патогенные микроорганизмы Острая печеночная недостаточность
Острая печеночная недостаточность Функциональные показатели деятельности сердца. Регуляция сердца
Функциональные показатели деятельности сердца. Регуляция сердца Илья Ильич Мечников
Илья Ильич Мечников Заболевания глотки, гортани и трахеи
Заболевания глотки, гортани и трахеи ҚР бала тұрғындарына амбулаторлық көмек көрсетуді ұйымдастыру. Ана және нәресте қлімін
ҚР бала тұрғындарына амбулаторлық көмек көрсетуді ұйымдастыру. Ана және нәресте қлімін Анемиясы бар балаларды
Анемиясы бар балаларды Этиловый спирт и его влияние на организм человека
Этиловый спирт и его влияние на организм человека Рахит. Классификация рахита
Рахит. Классификация рахита Планирование лечения
Планирование лечения Несеп жолдарының туа біткен аномалиялары
Несеп жолдарының туа біткен аномалиялары Неатложный помощь при судорожном и гипертермическом синдроме у детей
Неатложный помощь при судорожном и гипертермическом синдроме у детей Мероприятия по профилактике агрессивных действий у пациентов, страдающих психическими расстройствами
Мероприятия по профилактике агрессивных действий у пациентов, страдающих психическими расстройствами Электромагниттік терапия
Электромагниттік терапия Ферментные лекарственные средства
Ферментные лекарственные средства Диабетическая полинейропатия
Диабетическая полинейропатия Кровоснабжение головного мозга
Кровоснабжение головного мозга Токсикоз беременных (гестоз)
Токсикоз беременных (гестоз) Диагностика клинических синдромов в пульмонологии
Диагностика клинических синдромов в пульмонологии Симптомы, признаки и профилактика СПИДА
Симптомы, признаки и профилактика СПИДА Организация работы специализированных и линйных бригад скорой медицинской помощи
Организация работы специализированных и линйных бригад скорой медицинской помощи