Содержание
- 3. Новая иммунология – иммунология образраспознающих рецепторов ( К.А.Лебедев, И.Д.Понякина,2006 )
- 4. Чарльз Джаневей (1943—2003) Чарльз Дженуэй (1943-2003) и Руслан Меджитов
- 5. 1988 г. – C. Hashimoto, K. L. Hudson, K. V. Anderson
- 6. Определение понятия иммунной системы и иммунитета Иммунная система – совокупность органов и тканей, обеспечивающих иммунитет (клетки,
- 7. Виды иммунитета и главные функции Врожденный иммунитет Адаптивный иммунитет Защита организма от агрессии биологического происхождения:чужеродных и
- 8. Виды веществ, несущих признаки генетически чужеродной информации микроорганизмы (внутри- и внеклеточные): бактерии, вирусы, грибы, простейшие чужеродные
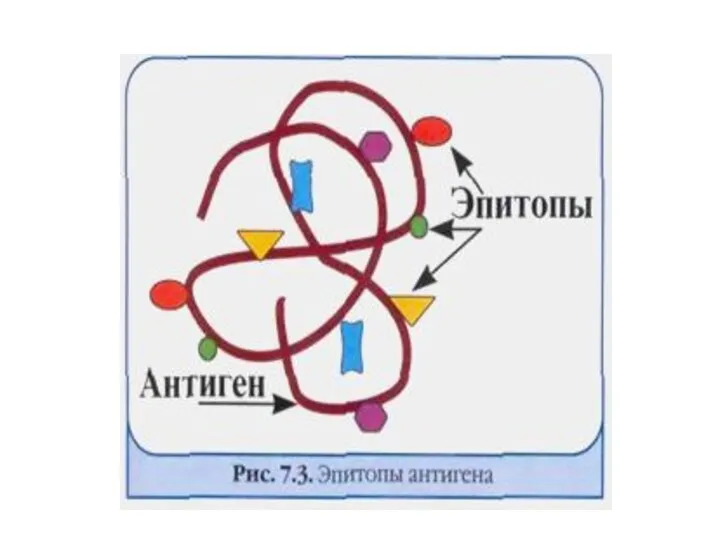
- 9. Определение понятия антиген, свойства антигенов Антиген – молекула, которую могут специфически распознавать элементы иммунной системы (антитела
- 10. ЭПИТОПЫ АНТИГЕНА
- 11. Виды антигенов По физико-химическим свойствам: растворимые (бактериальные токсины); корпускулярные (частицы вирусов, бактериальные клетки, пыльца растений, эритроциты)
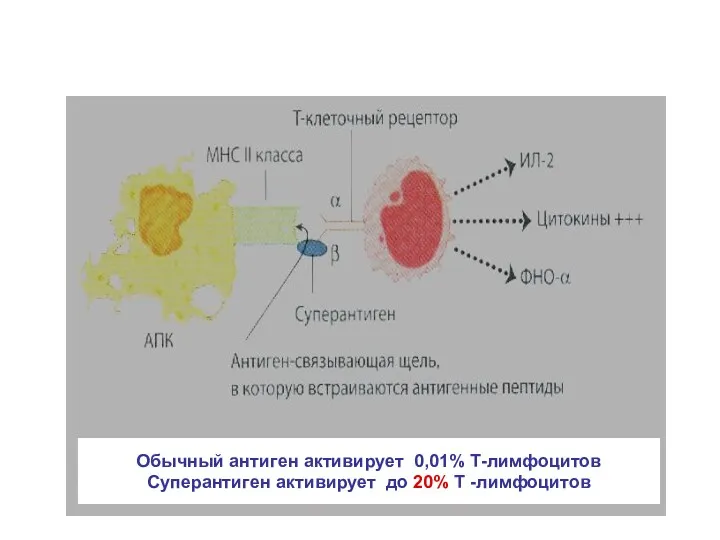
- 12. Обычный антиген активирует 0,01% Т-лимфоцитов Суперантиген активирует до 20% Т -лимфоцитов ПОСЛЕДСТВИЯ СТИМУЛЯЦИИ Т-ЛИМФОЦИТОВ СУПЕРАНТИГЕНОМ
- 13. Антитела Антитела – специфические гаммаглобулины (гликопротеиновые молекулы из семейства иммуноглобулинов - Ig), образующиеся под действием антигена
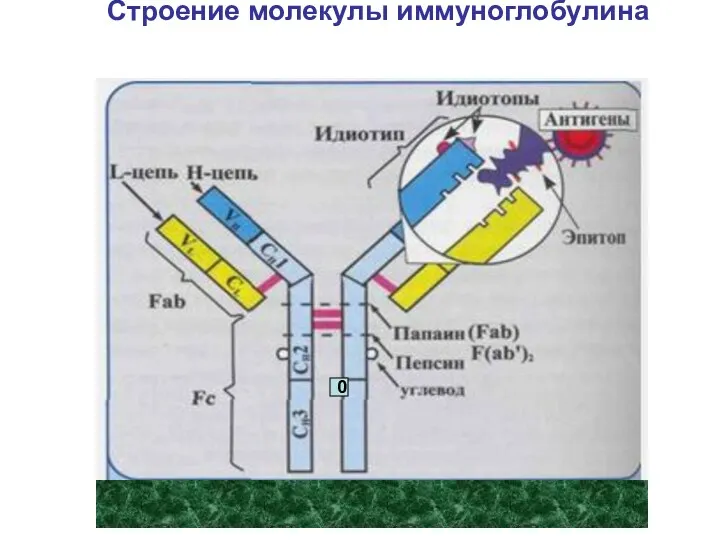
- 14. Строение молекулы иммуноглобулина G 0
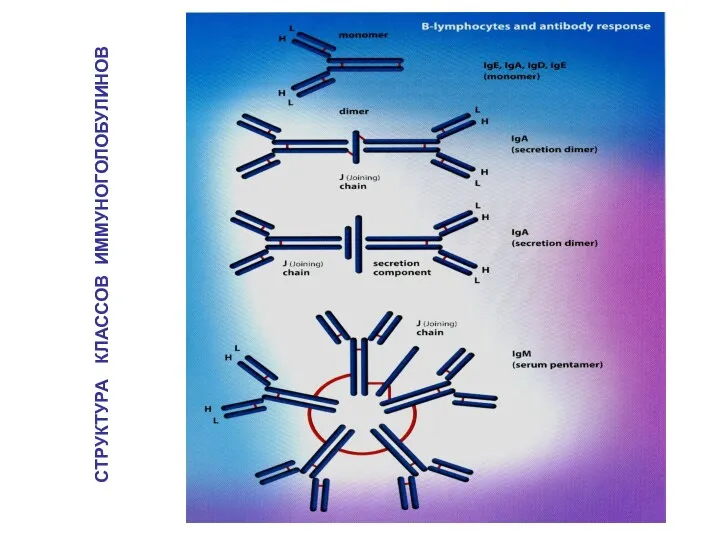
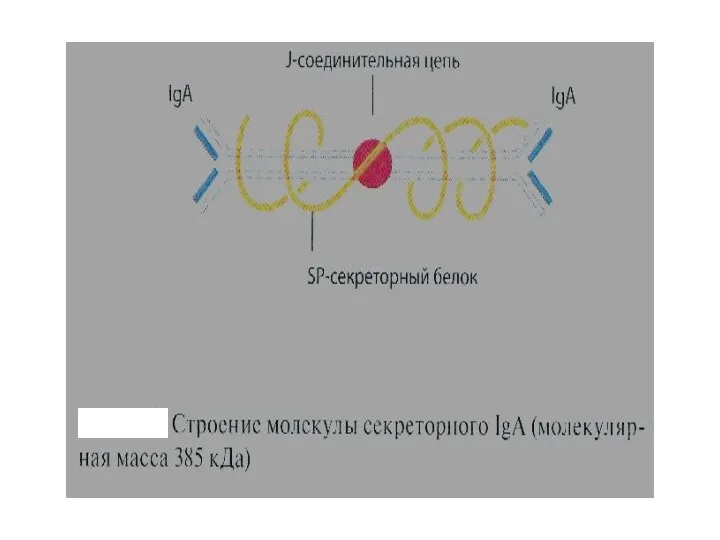
- 15. СТРУКТУРА КЛАССОВ ИММУНОГОЛОБУЛИНОВ
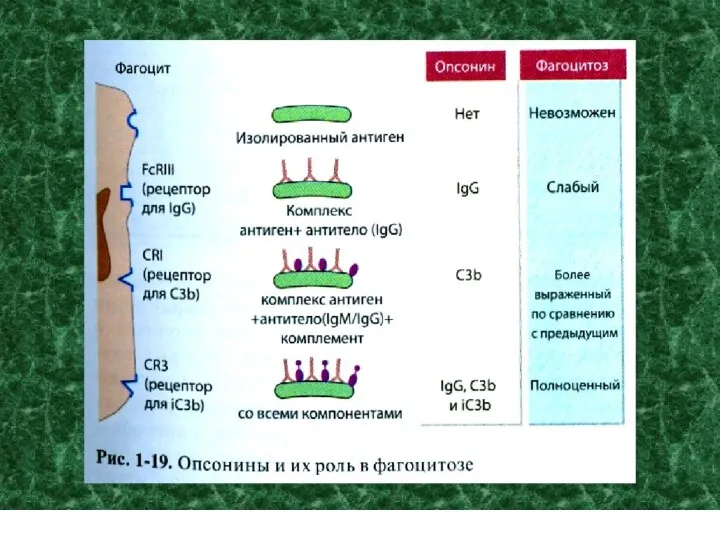
- 17. Функции антител Специфическое связывание АГ Fab-фрагментом АТ, образование иммунного комплекса (АГ+АТ) Связывание комплекса АГ-АТ с макрофагами
- 19. Структура иммунной системы Центральные органы (красный костный мозг, тимус). В них происходят процессы антигеннезависимой дифференцировки (созревания)
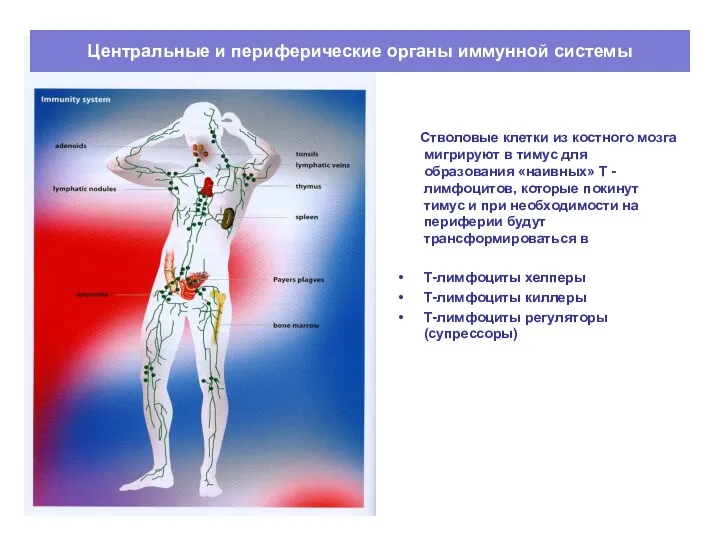
- 20. Центральные и периферические органы иммунной системы Стволовые клетки из костного мозга мигрируют в тимус для образования
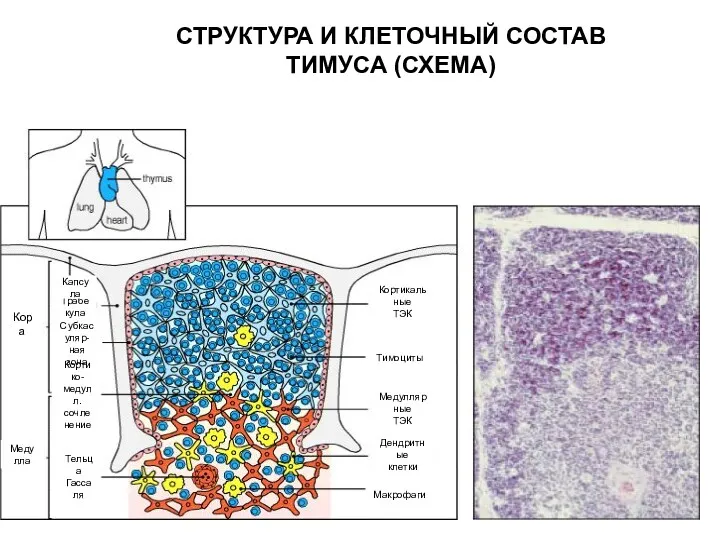
- 21. СТРУКТУРА И КЛЕТОЧНЫЙ СОСТАВ ТИМУСА (СХЕМА) Кора Медулла Тельца Гассаля Кортико- медулл. сочленение Субкасуляр- ная зона
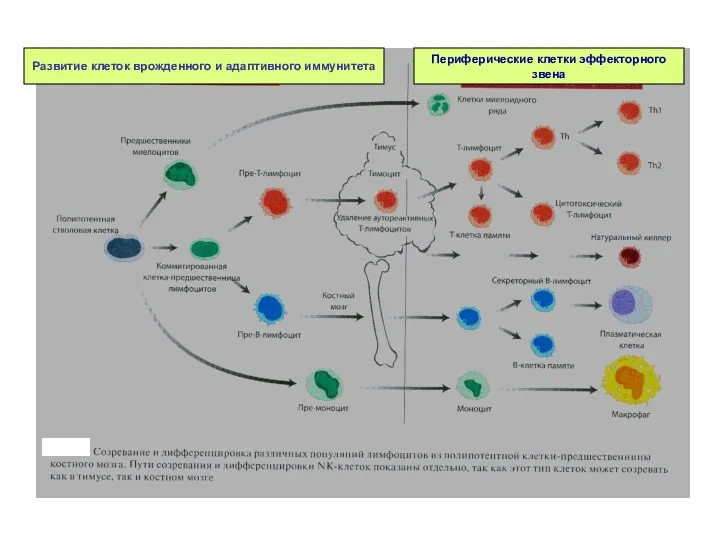
- 22. Развитие клеток врожденного и адаптивного иммунитета Периферические клетки эффекторного звена
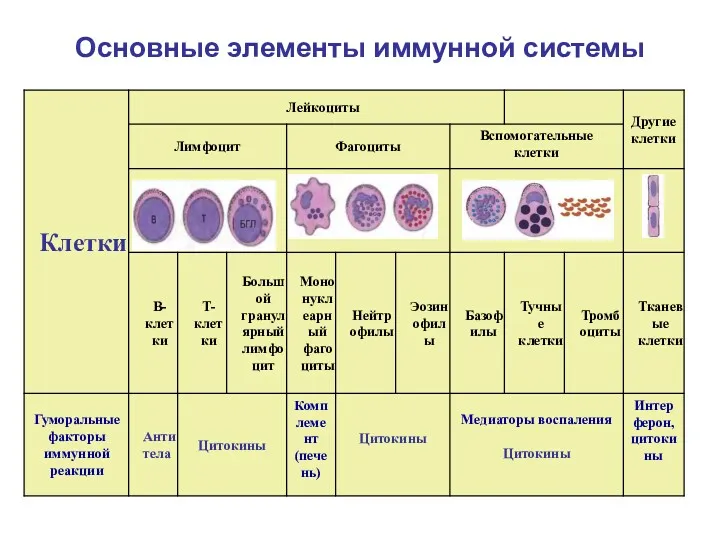
- 23. Основные элементы иммунной системы
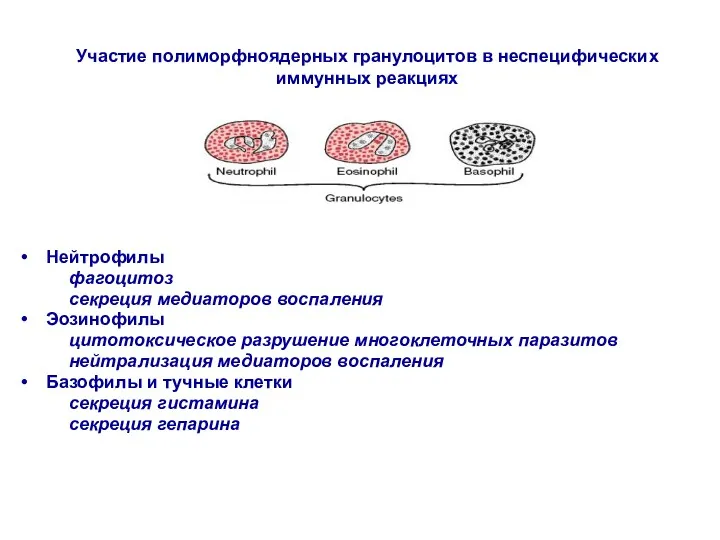
- 24. Нейтрофилы фагоцитоз секреция медиаторов воспаления Эозинофилы цитотоксическое разрушение многоклеточных паразитов нейтрализация медиаторов воспаления Базофилы и тучные
- 27. Свойства иммунной системы Высокая специфичность (лимфоциты с помощью антигенспецифических рецепторов распознают антигенные молекулы, различающиеся по 1-2
- 28. Основные понятия и термины, используемые при изучении физиологии иммунной системы СD (от англ. Cluster Differentiation) –
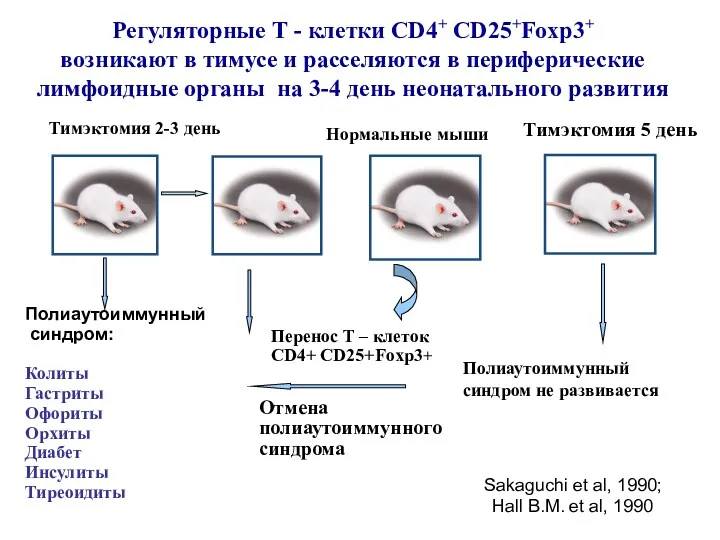
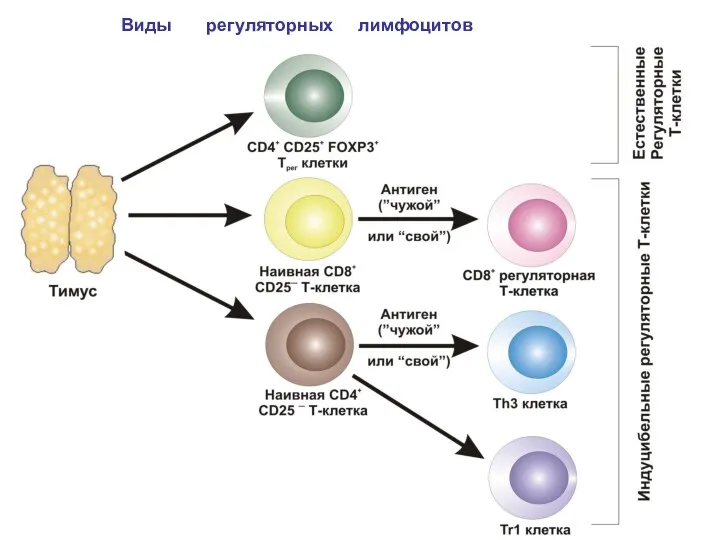
- 29. Регуляторные Т - клетки CD4+ CD25+Foxp3+ возникают в тимусе и расселяются в периферические лимфоидные органы на
- 30. Интервалы распределения фенотипов лимфоцитов условно здоровых доноров (n = 362) Тип клеток % ПК Абс.к-во кл/л
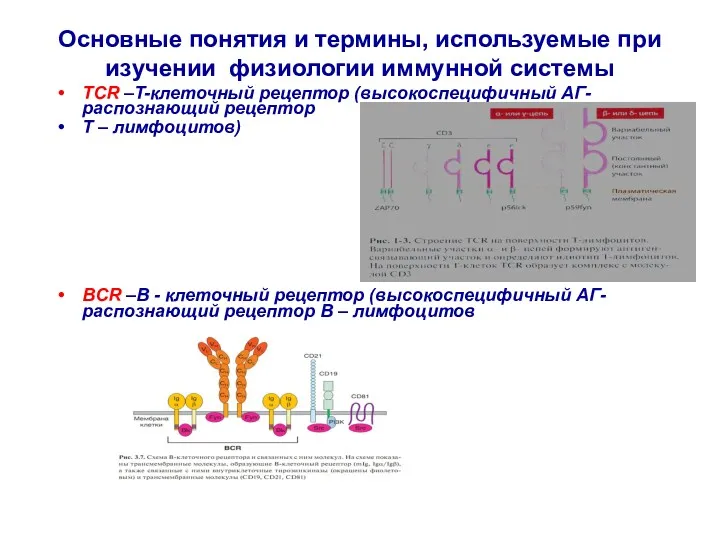
- 31. Основные понятия и термины, используемые при изучении физиологии иммунной системы TCR –T-клеточный рецептор (высокоспецифичный АГ-распознающий рецептор
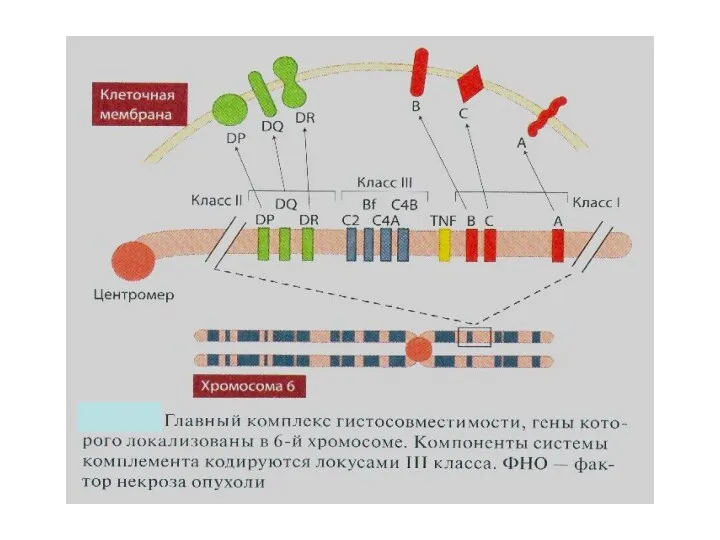
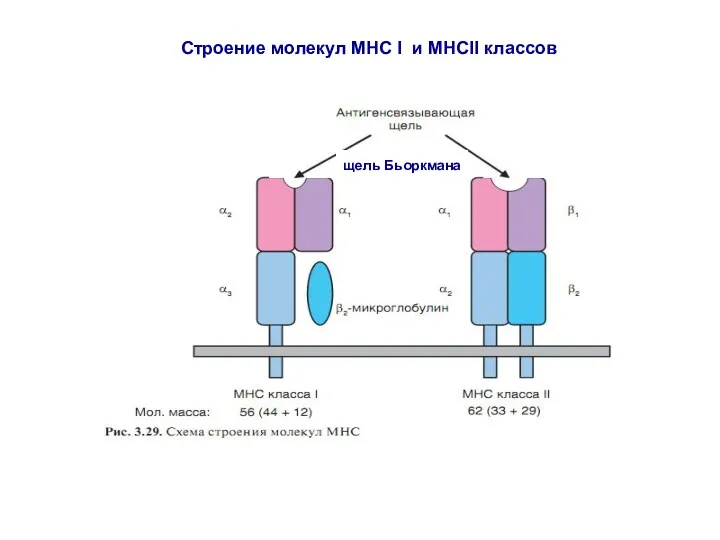
- 32. Основные понятия и термины, используемые при изучении физиологии иммунной системы МНС – главный комплекс гистосовместимости; у
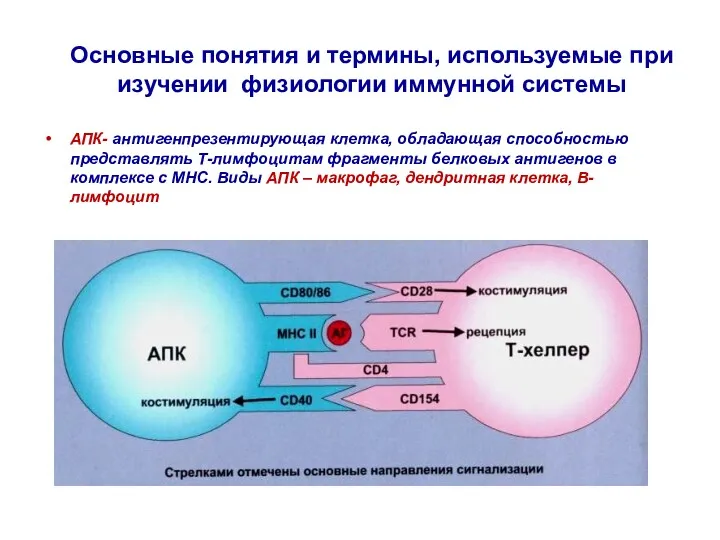
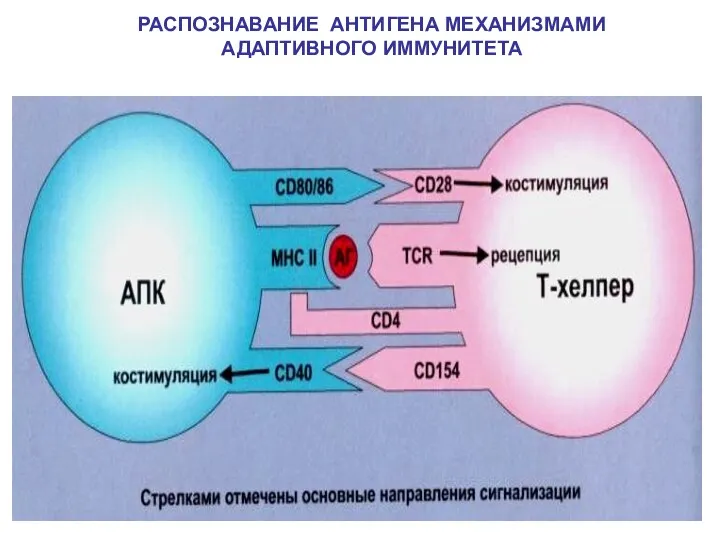
- 33. Основные понятия и термины, используемые при изучении физиологии иммунной системы АПК- антигенпрезентирующая клетка, обладающая способностью представлять
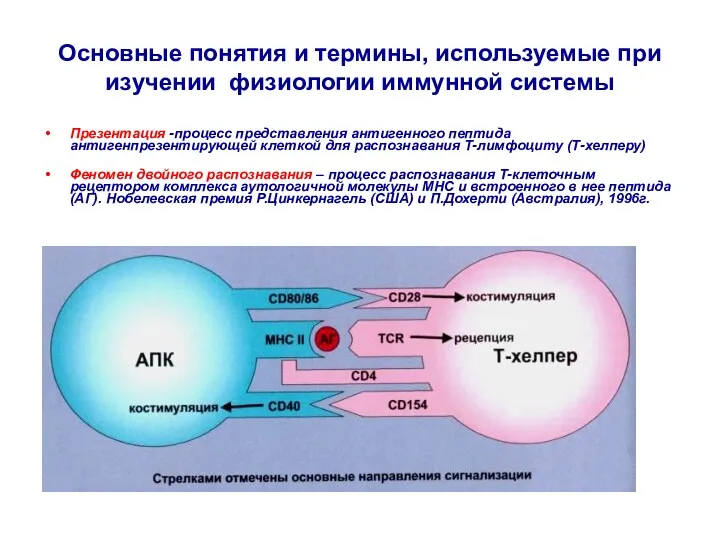
- 34. Основные понятия и термины, используемые при изучении физиологии иммунной системы Презентация -процесс представления антигенного пептида антигенпрезентирующей
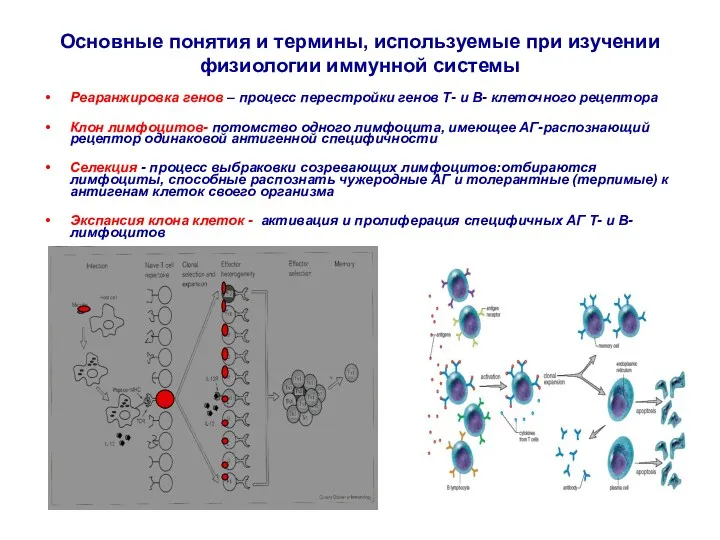
- 35. Основные понятия и термины, используемые при изучении физиологии иммунной системы Реаранжировка генов – процесс перестройки генов
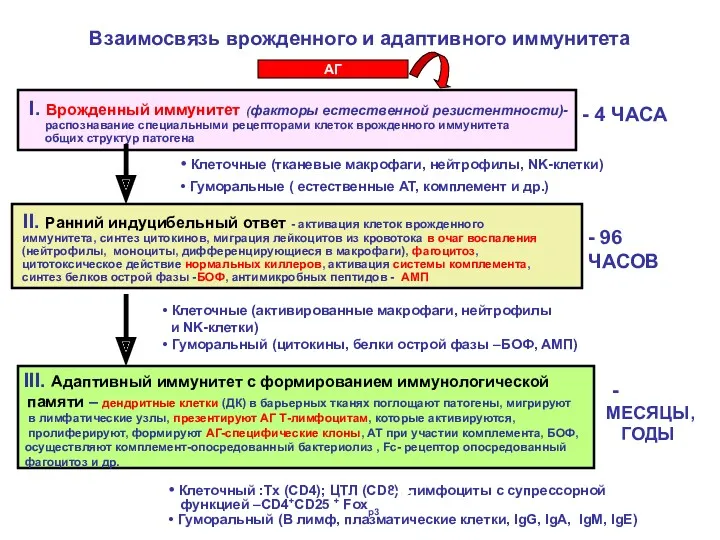
- 36. Взаимосвязь врожденного и адаптивного иммунитета I. Врожденный иммунитет (факторы естественной резистентности)- распознавание специальными рецепторами клеток врожденного
- 37. Понятие врожденного иммунитета Врожденный иммунитет ( от англ.innate or natural immunity)- наследственно закрепленная система защиты многоклеточных
- 38. Отличительтные свойства врожденного иммунитета Является главной системой (сенсором) распознавания «чужого» (например, заражения патогенами) и первой линией
- 39. Механизмы распознавания «своего» и «чужого» на начальных этапах врожденного иммунитета Цель распознавания – раннее установление различий
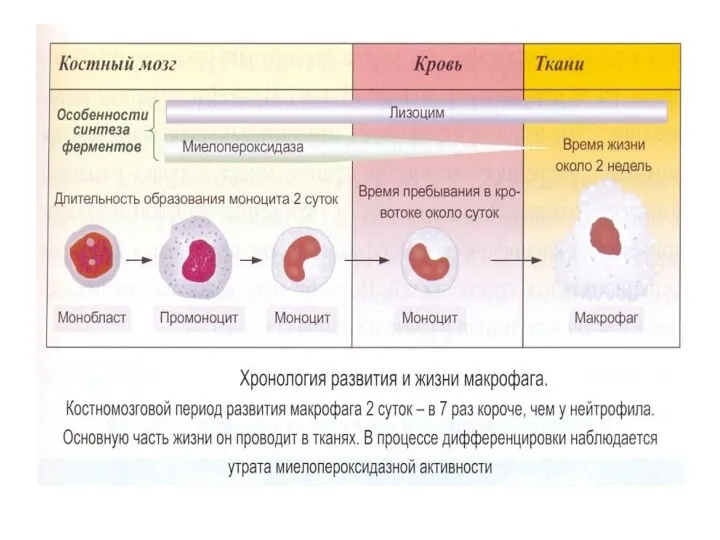
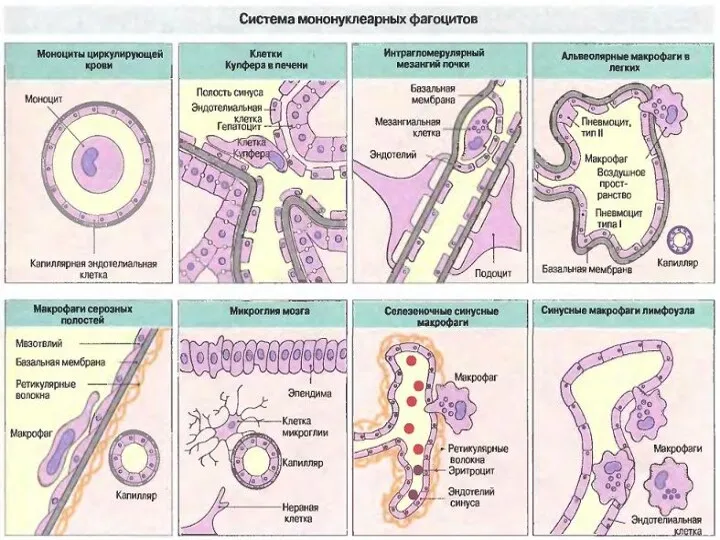
- 40. Эффекторы врожденного иммунитета (клетки, гуморальные факторы) Фагоцитирующие клетки ( нейтрофилы, моноциты, макрофаги ) Презентирующие антиген клетки
- 41. Эффекторные молекулы врожденного иммунитета Пептиды: Дефенсины беспозвоночных β-дефенсины α-дефенсины θ-дефенсины кателицидины (LL-37, протегрины, профенины) Белки: лизоцим
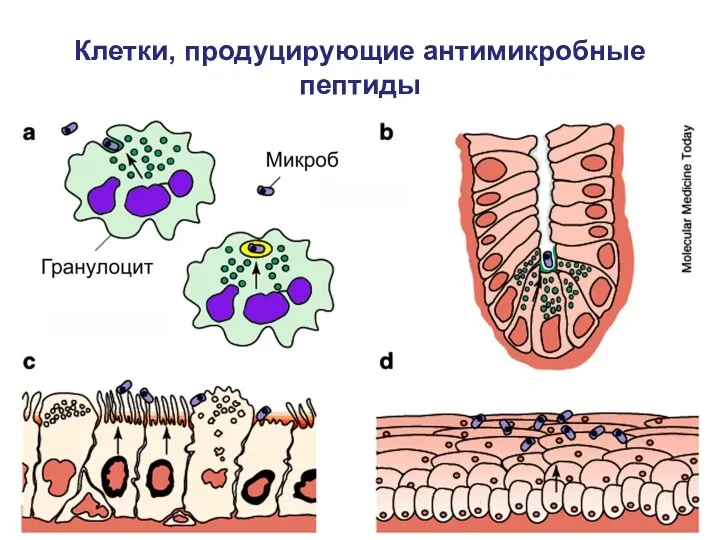
- 42. Клетки, продуцирующие антимикробные пептиды
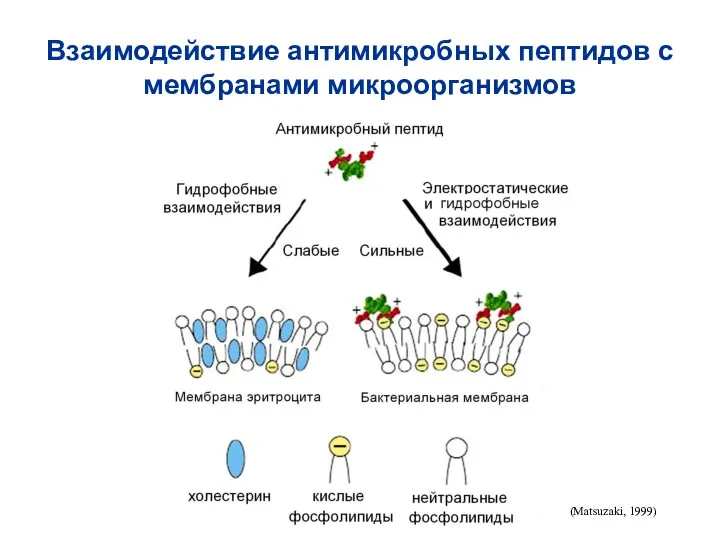
- 43. Взаимодействие антимикробных пептидов с мембранами микроорганизмов (Matsuzaki, 1999)
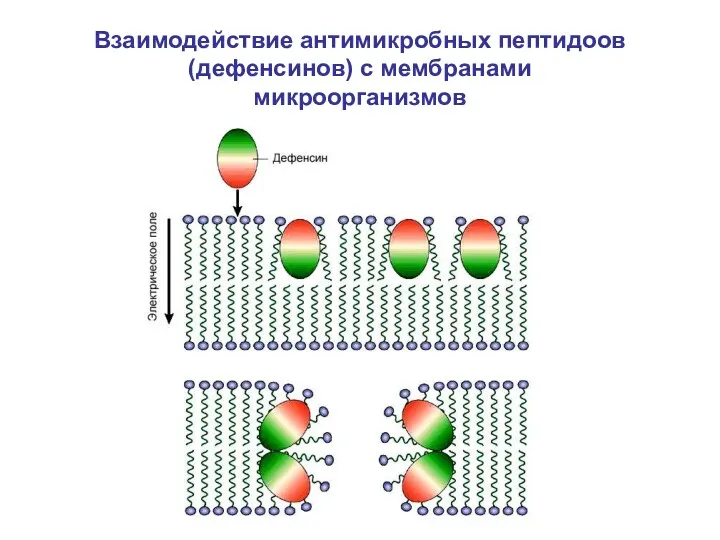
- 44. Взаимодействие антимикробных пептидоов (дефенсинов) с мембранами микроорганизмов
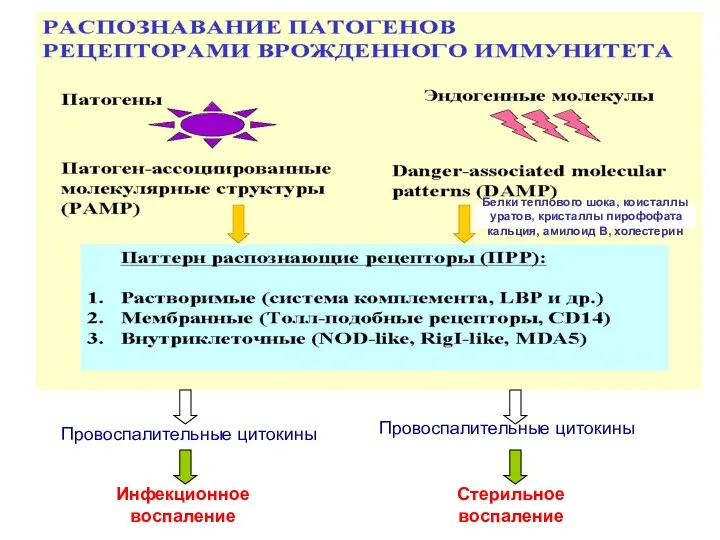
- 48. Провоспалительные цитокины Провоспалительные цитокины Инфекционное воспаление Стерильное воспаление Белки теплового шока, коисталлы уратов, кристаллы пирофофата кальция,
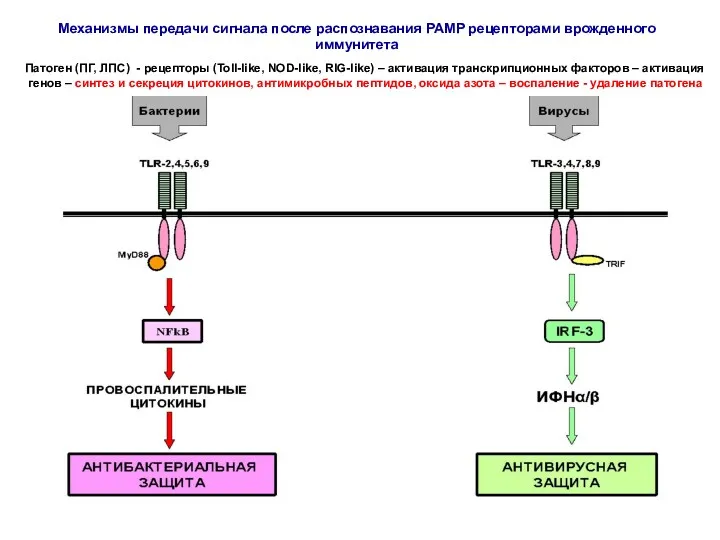
- 49. Патоген (ПГ, ЛПС) - рецепторы (Toll-like, NOD-like, RIG-like) – активация транскрипционных факторов – активация генов –
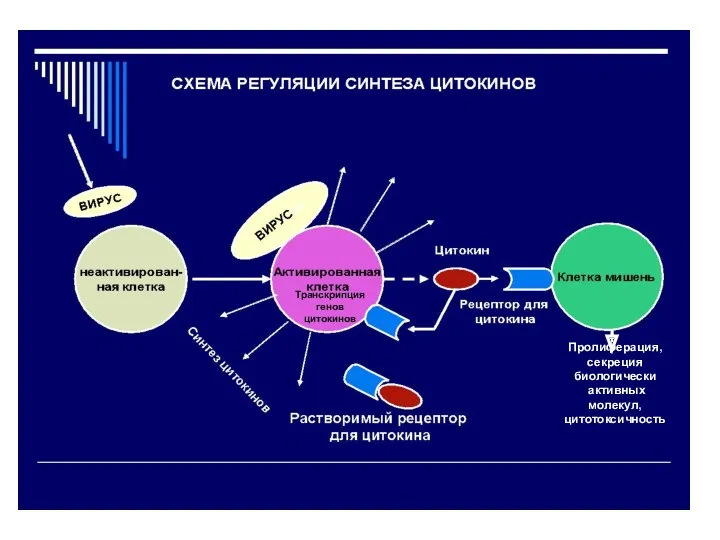
- 50. Цитокины – эндогенные полипептидные медиаторы межклеточного взаимодействия Cистема цитокинов объединяет: клетки-продуценты; растворимые цитокины и их антагонисты;
- 51. Транскрипция генов цитокинов Пролиферация, секреция биологически активных молекул, цитотоксичность
- 52. Классификация цитокинов по биологическим эффектам 1. Факторы роста и дифференцировки кроветворных клеток 2. Интерфероны 3. Интерлейкины
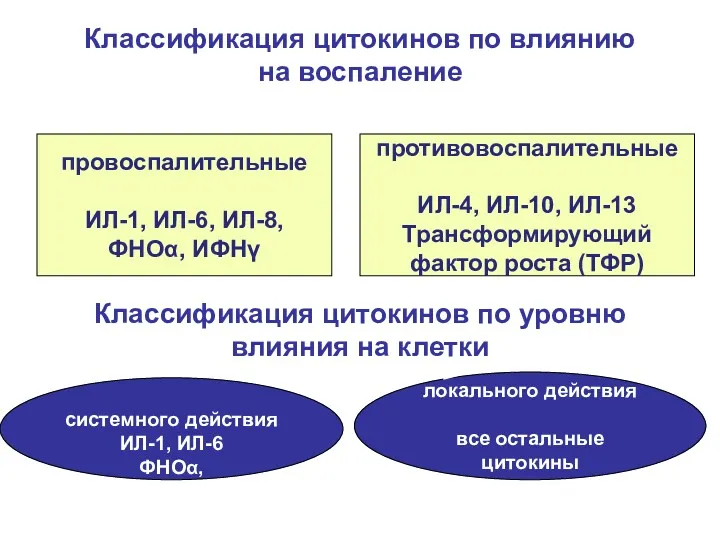
- 53. Классификация цитокинов по влиянию на воспаление провоспалительные ИЛ-1, ИЛ-6, ИЛ-8, ФНОα, ИФНγ противовоспалительные ИЛ-4, ИЛ-10, ИЛ-13
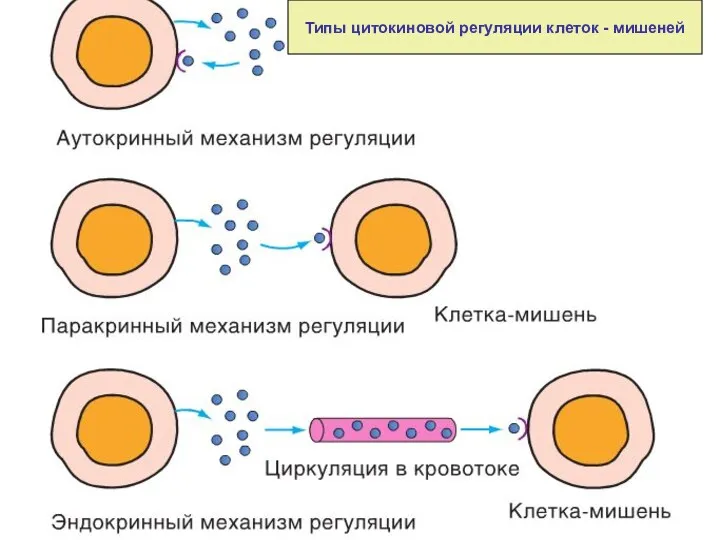
- 55. Типы цитокиновой регуляции клеток - мишеней
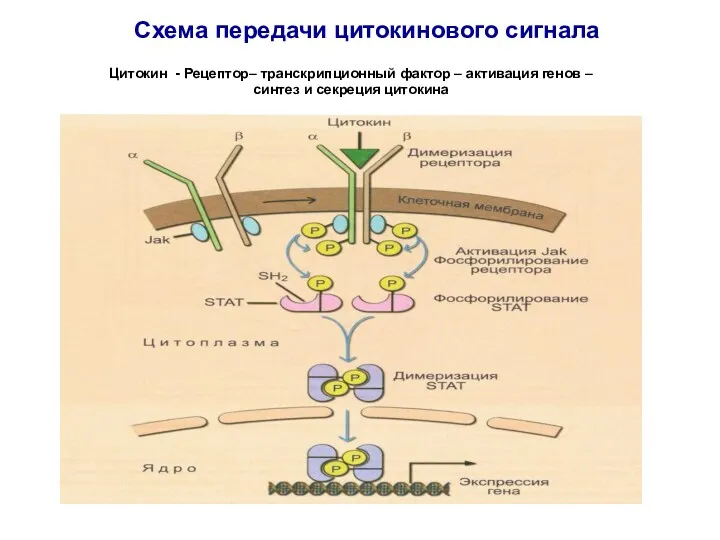
- 56. Схема передачи цитокинового сигнала Цитокин - Рецептор– транскрипционный фактор – активация генов – синтез и секреция
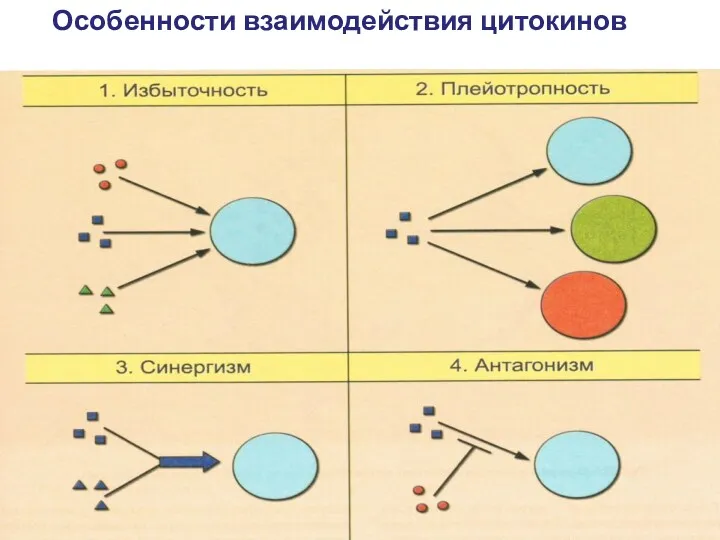
- 57. СВОЙСТВА ЦИТОКИНОВ Принадлежность к пептидам Сетевой принцип работы Индуцибельность Синтез de novo Избыточность Плейотропность действия Специфичность
- 58. Особенности взаимодействия цитокинов
- 60. ЦИТОКИНОВЫЙ ШТОРМ The term “cytokine storm” calls up vivid images of an immune system gone awry
- 61. Блокировка ФНО: лекарства* *Примерная стоимость курса лечения в Европе – 15 тыс Евро в год
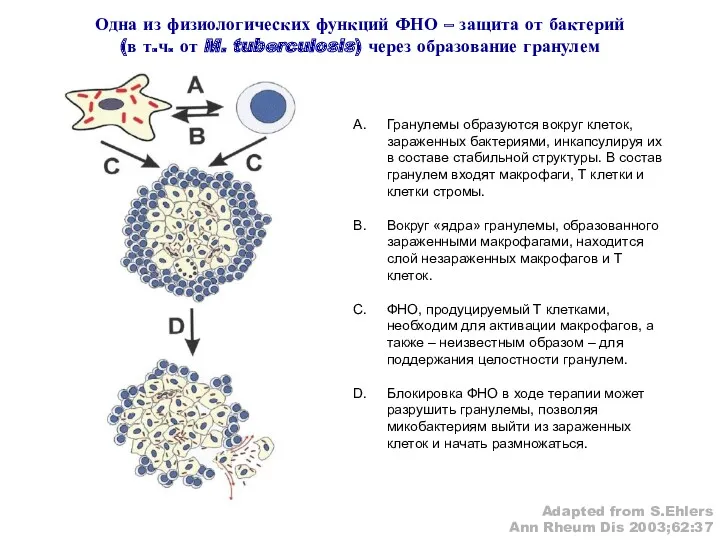
- 62. Гранулемы образуются вокруг клеток, зараженных бактериями, инкапсулируя их в составе стабильной структуры. В состав гранулем входят
- 63. Адаптивный иммунитет Эволюционно более поздний. Эффекторы адаптивного иммунитета: Т- и В-лимфоциты с их антигенраспознающими рецепторами (TCR
- 64. Механизмы распознавания «своего» и «чужого» адаптивным иммунитетом иммунитета Кто распознает ? – Т- и В-лимфоциты Что
- 66. Строение молекул МНС I и МНСII классов щель Бьоркмана
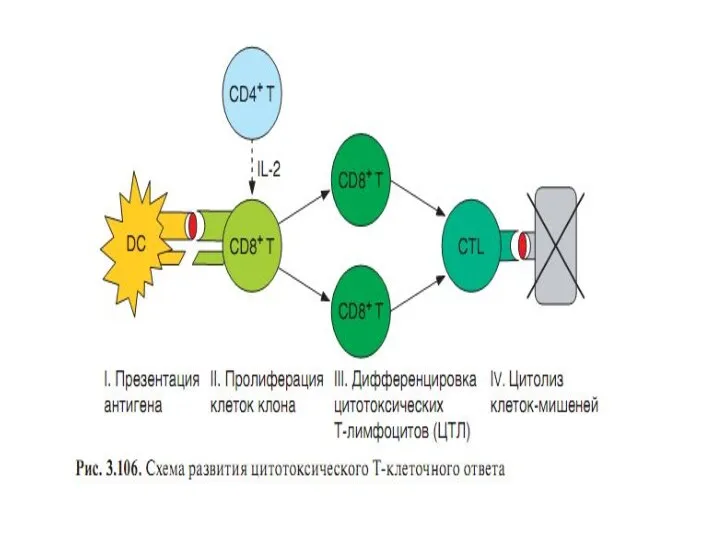
- 67. РАСПОЗНАВАНИЕ АНТИГЕНА МЕХАНИЗМАМИ АДАПТИВНОГО ИММУНИТЕТА
- 70. Иммунный ответ Иммунный ответ – специфическая реакция лимфоцитов на антиген, направленная на его элиминацию Фазы иммунного
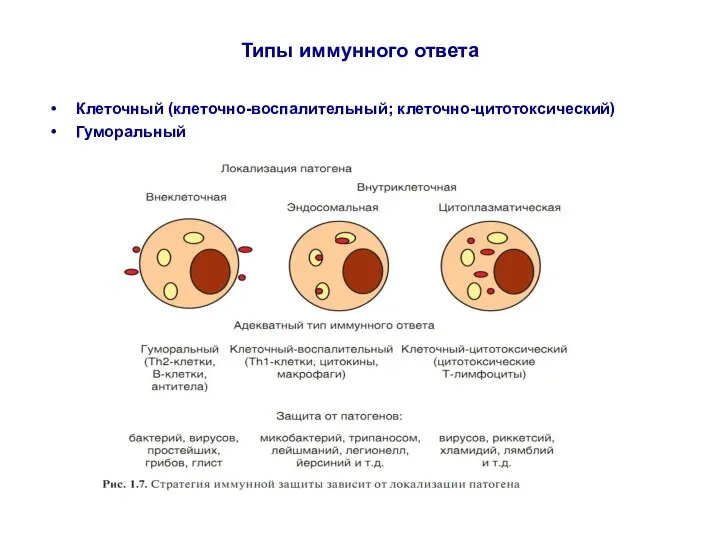
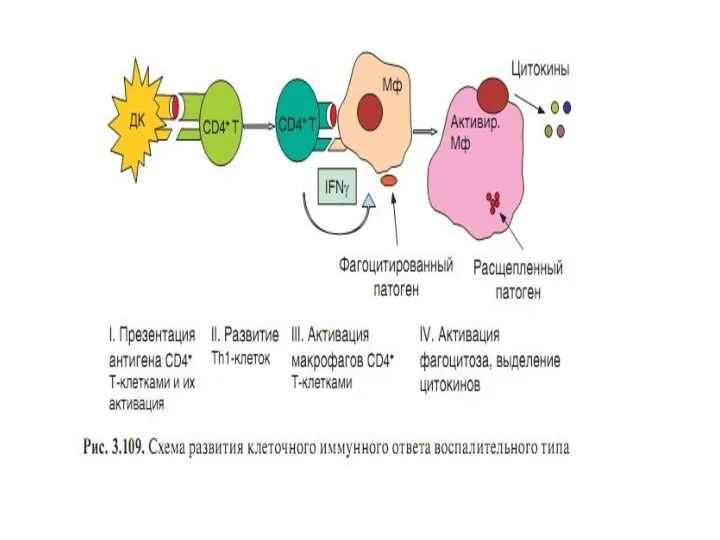
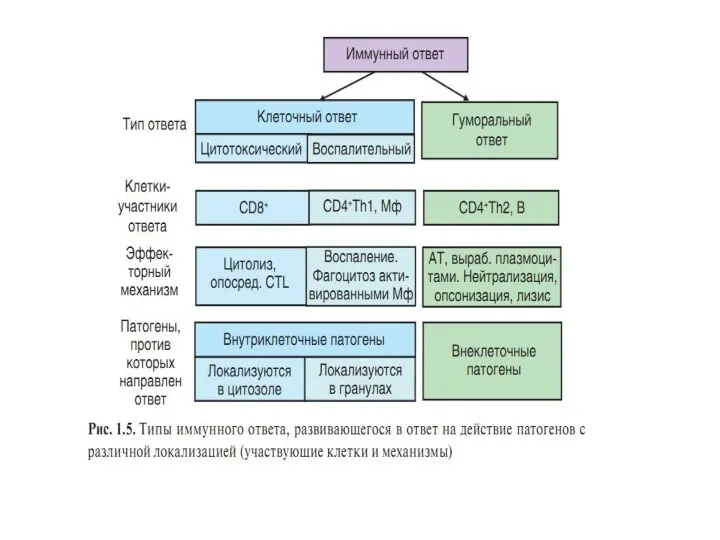
- 71. Типы иммунного ответа Клеточный (клеточно-воспалительный; клеточно-цитотоксический) Гуморальный
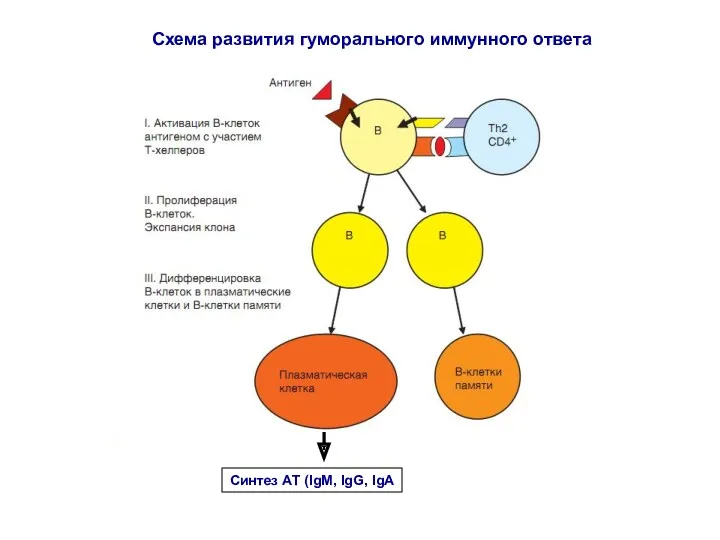
- 72. Cхема развития гуморального иммунного ответа Синтез АТ (IgM, IgG, IgA
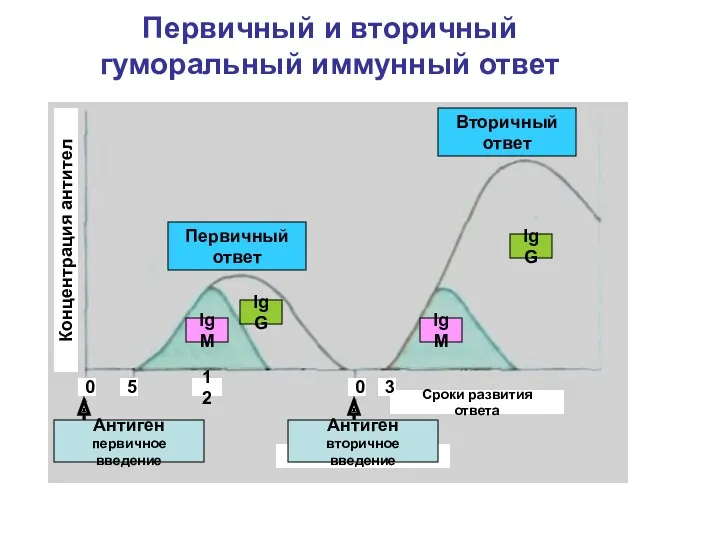
- 73. Первичный и вторичный гуморальный иммунный ответ Первичный ответ Вторичный ответ Антиген первичное введение Концентрация антител Ig
- 77. Виды регуляторных лимфоцитов
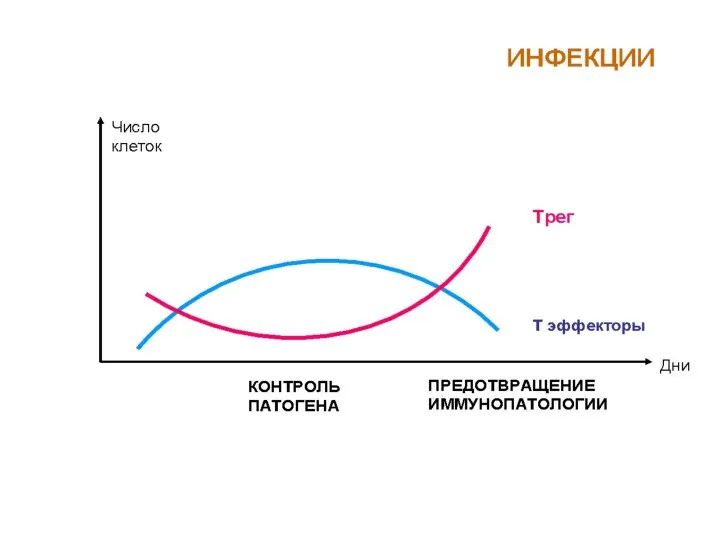
- 78. Основные характеристики Трег Постоянные маркеры СD25+ (альфа цепь рецептора ИЛ-2) Foxp3 (ядерный фактор транскрипции, связанный с
- 79. В презентации доклада использованы материалы лекции : С.А.Недоспасова (Институт Молекулярной Биологии им. В.А. Энгельгардта РАН Институт
- 80. Благодарю за внимание !
- 81. Типы иммунного ответа Факторы, определяющие тип ИО природа АГ локализация АГ по отношению к клетке способ
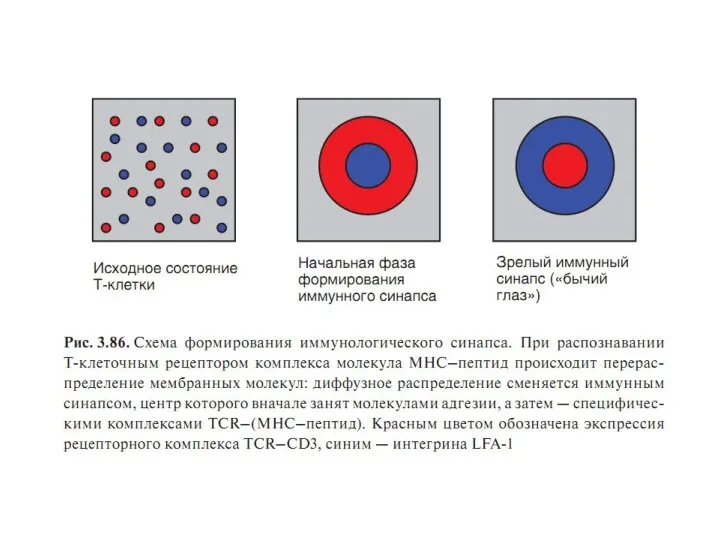
- 83. Иммунный синапс - структурированная (упорядоченная ) зона контакта между клетками, участвующими в реализации той или иной
- 84. Характеристика регуляторных Т-клеток В 1995 г. С. Сакагучи (S. Sakaguchi) и соавт. описали естественные регуляторные Т-
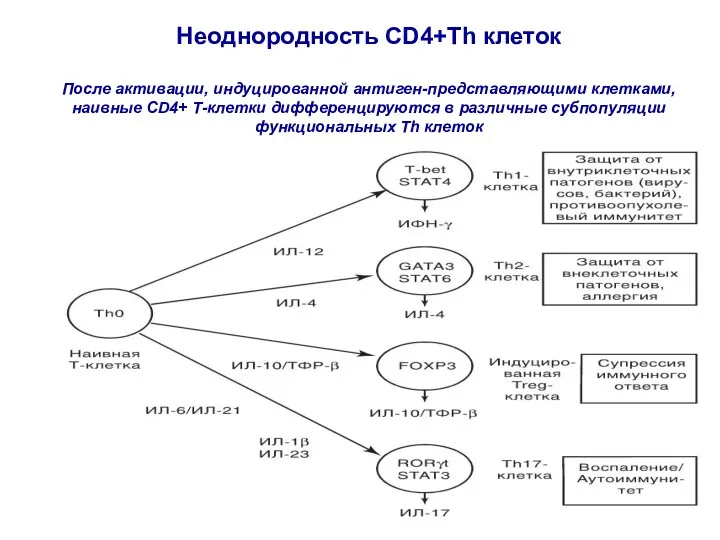
- 85. Неоднородность CD4+Th клеток После активации, индуцированной антиген-представляющими клетками, наивные CD4+ Т-клетки дифференцируются в различные субпопуляции функциональных
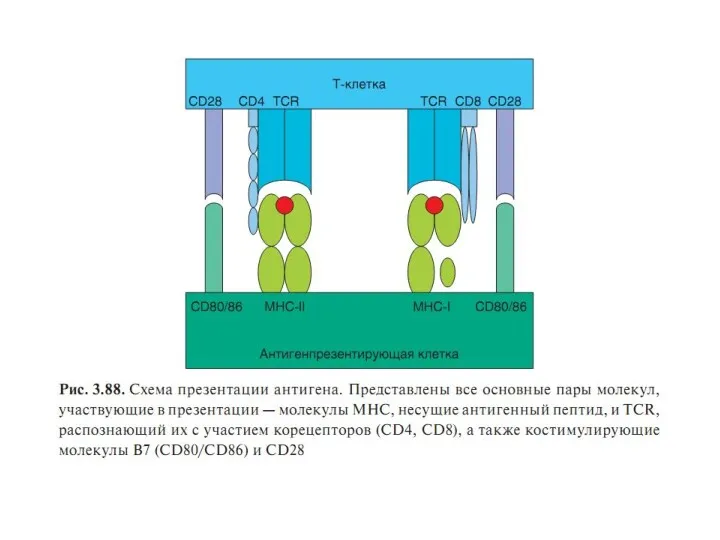
- 87. ЭТАПЫ ПРЕДСТАВЛЕНИЯ АГ Т-КЛЕТКАМ Ферментативная переработка экзогенных и эндогенных АГ до коротких пептидов Синтез молекул HLA
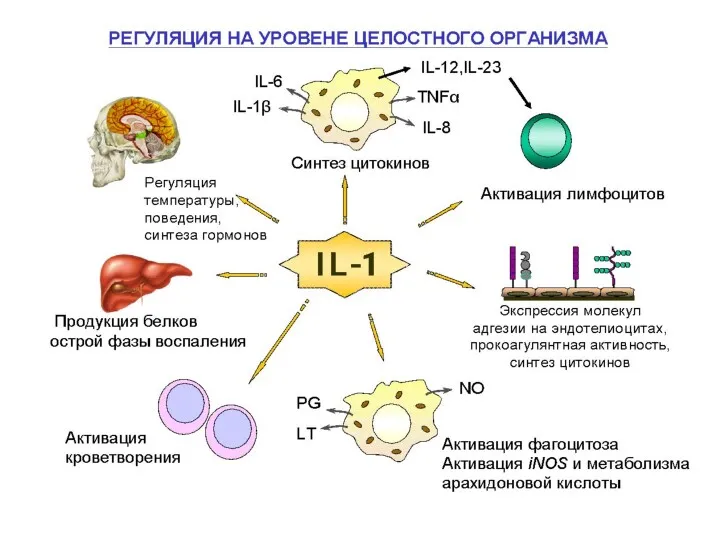
- 88. Ц И Т О К И Н Ы (от греч.CYTO – КЛЕТКА,KINOS-ДВИЖЕНИЕ)- низкомолекулярные белковые вещества, продуцируемые
- 89. Основные понятия и термины, используемые при изучении физиологии иммунной системы СD (от англ. Cluster Differentiation) –
- 90. Лекарственные препараты на основе генно-инженерных гуманизированных моноклональных антител МАТ против IgE человека – лечение тяжелых форм
- 92. Скачать презентацию








































 Hellp- синдромы, диагностикасы, емі
Hellp- синдромы, диагностикасы, емі Возбудители коклюша, паракоклюша, дифтерии, туберкулеза
Возбудители коклюша, паракоклюша, дифтерии, туберкулеза Лихорадки Эбола, Ласса, Марбург
Лихорадки Эбола, Ласса, Марбург Динамика роста и развития зубов у детей
Динамика роста и развития зубов у детей Повреждение груди
Повреждение груди Лёгочное сердце
Лёгочное сердце Эндометриоз. Актуальность проблемы
Эндометриоз. Актуальность проблемы Жүрек қарыншалары мен жүрекшелері гипертрофиясының визуальді диагностика әдістері
Жүрек қарыншалары мен жүрекшелері гипертрофиясының визуальді диагностика әдістері Кемеровская клиническая районная больница
Кемеровская клиническая районная больница Средства, влияющие на тонус и сократительную активность миометрия
Средства, влияющие на тонус и сократительную активность миометрия COVID-19. Профилактика
COVID-19. Профилактика Герпетические инфекции у детей
Герпетические инфекции у детей Анатомо-физиологические особенности формирования потребностей человека. (Лекция 1)
Анатомо-физиологические особенности формирования потребностей человека. (Лекция 1) Вакцинация. Правовые аспекты вакцинопрофилактики в РК
Вакцинация. Правовые аспекты вакцинопрофилактики в РК Оңтүстік қазақстан медицина академиясы
Оңтүстік қазақстан медицина академиясы Анестезиология. Ингаляционный наркоз
Анестезиология. Ингаляционный наркоз Ісік клеткасының дамуына әкелетін р53 ақуызының мутациясы
Ісік клеткасының дамуына әкелетін р53 ақуызының мутациясы Планирование семьи. Регулирование рождаемости. Бесплодный брак
Планирование семьи. Регулирование рождаемости. Бесплодный брак Патология водносолевого обмена состояния гипер- и гипогидрии отёки. Этиология и патогенез
Патология водносолевого обмена состояния гипер- и гипогидрии отёки. Этиология и патогенез Средства, действующие на ЦНС
Средства, действующие на ЦНС Ұзақ өмір сүрушілік, қартаю.Клиникалық және этикалық аспектілері. Ұзақ өмір сүрушілік феноменінің генетикалық механизмдері
Ұзақ өмір сүрушілік, қартаю.Клиникалық және этикалық аспектілері. Ұзақ өмір сүрушілік феноменінің генетикалық механизмдері Вегетативно-сосудистая дистония: проблемы диагностики и лечения
Вегетативно-сосудистая дистония: проблемы диагностики и лечения Ведение беременности и родов при тазовом предлежании плода
Ведение беременности и родов при тазовом предлежании плода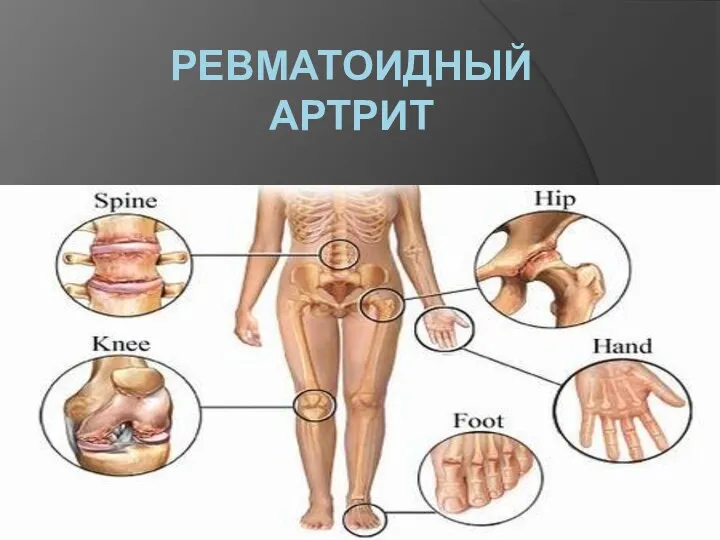 Ревматоидный артрит
Ревматоидный артрит Экстракорпоральная поддержка функции печени
Экстракорпоральная поддержка функции печени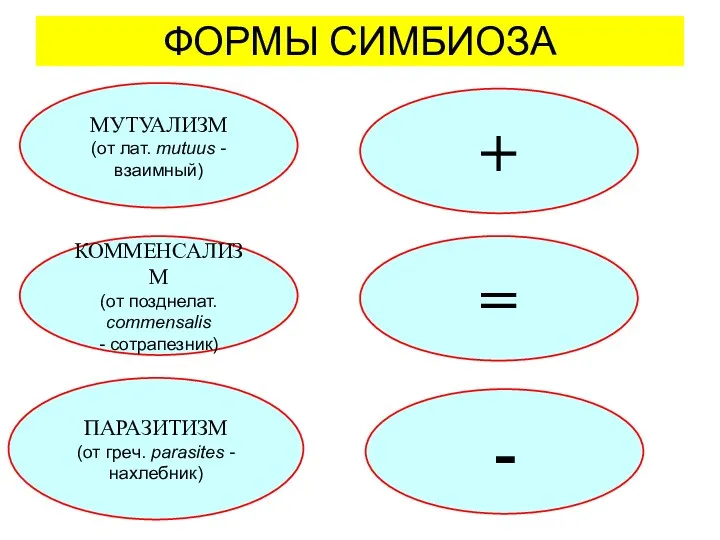 Протозоология. Формы симбиоза
Протозоология. Формы симбиоза Заболевания органов пищеварения. Профилактика и первая помощь
Заболевания органов пищеварения. Профилактика и первая помощь Острые респираторные вирусные инфекции
Острые респираторные вирусные инфекции