Содержание
- 2. наука о защите организма от операционной травмы и её последствий, контроле и управлении жизненно важными функциями
- 3. Общая анестезия искусственно вызванное обратимое торможение ЦНС, сопровождающееся утратой сознания, чувствительности, мышечного тонуса и некоторых видов
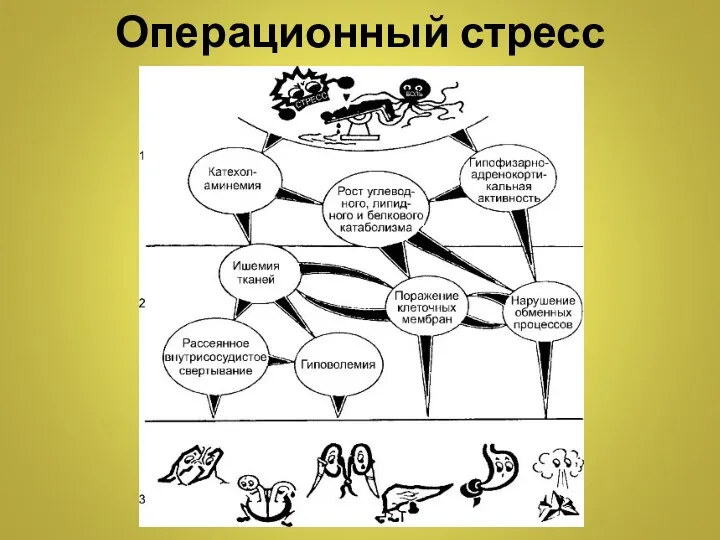
- 4. Операционный стресс
- 5. Этапы анестезиологического пособия: Подготовка: компенсация всех жизненноважных функций организма, коррекция гиповолемии, ацидоза, электролитных нарушений, нормотензия, нормотермия
- 6. Премедикация при плановом вмешательстве: Накануне операции, вечером: Снотворное из группы бензодиазепинов (феназепам)+ блокатор Н1-рецепторов гистамина (димедрол,
- 7. Премедикация при экстренном вмешательстве: На операционном столе: Наркотический анальгетик фентанил 0,01мкг/кг + реланиум (сибазон) 10 мг
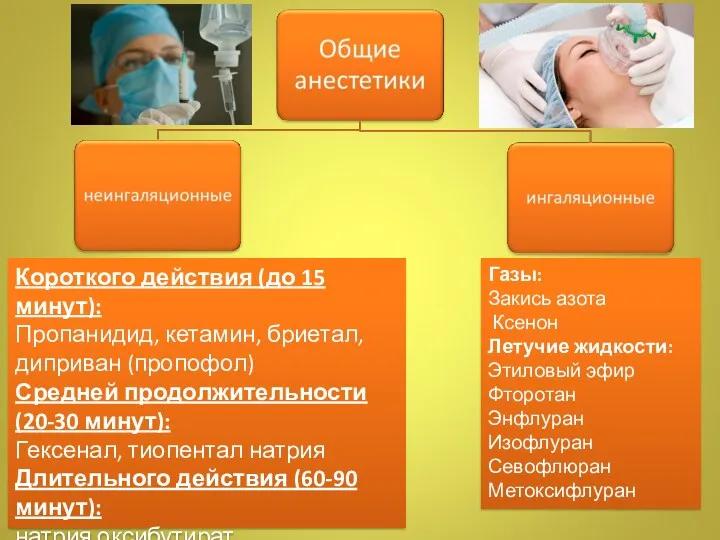
- 8. Виды наркозов: По способу доставки анестетика: Ингаляционный (масочный, эндотрахеальный, эндобронхиальный) Неингаляционный (внутривенный, внутримышечный) По количеству используемых
- 9. Теории наркоза 1. Коагуляционная теория Кюна (1864): анестетики вызывают своеобразное свёртывание внутриклеточного белка, что приводит к
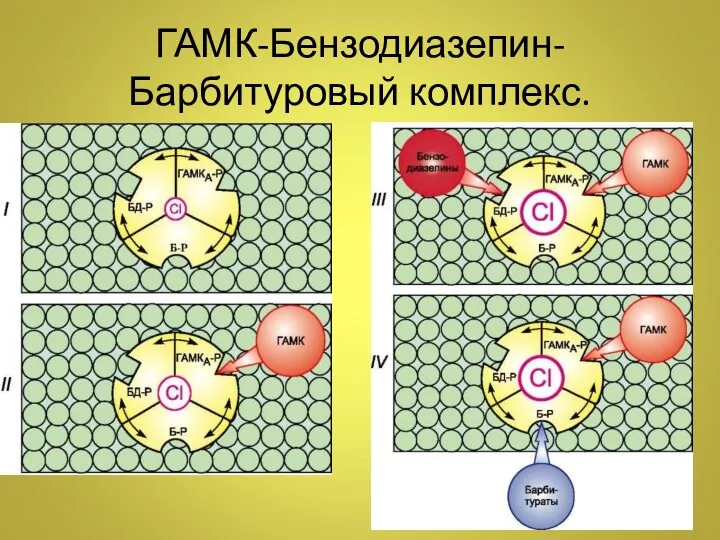
- 10. ГАМК-Бензодиазепин-Барбитуровый комплекс.
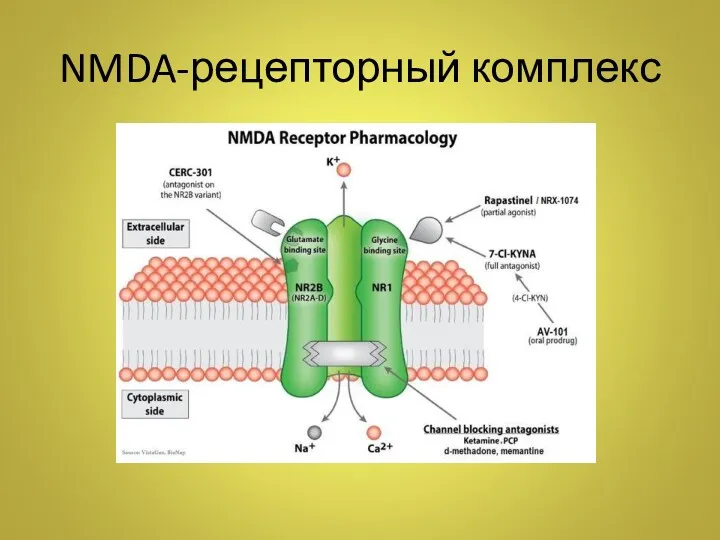
- 11. NMDA-рецепторный комплекс
- 13. Газы: Закись азота Ксенон Летучие жидкости: Этиловый эфир Фторотан Энфлуран Изофлуран Севофлюран Метоксифлуран Короткого действия (до
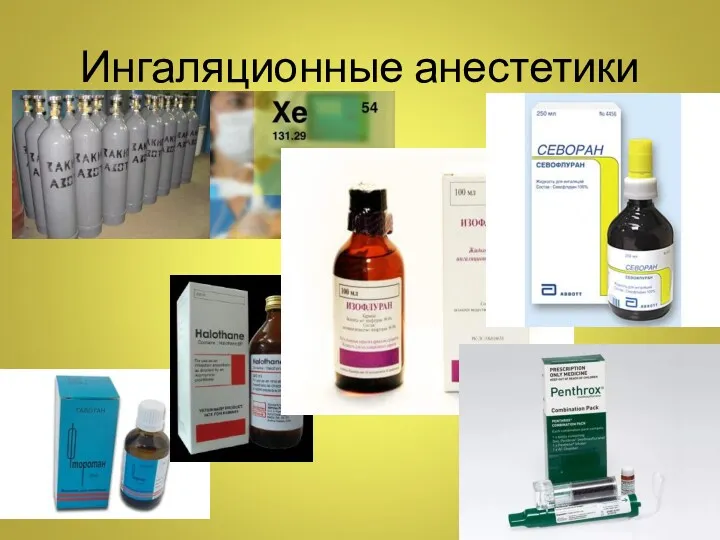
- 14. Ингаляционные анестетики
- 15. Минимальная альвеолярная концентрация МАК — это альвеолярная концентрация ингаляционного анестетика, которая предотвращает движение 50 % больных
- 16. Свойства современных ингаляционных анестетиков
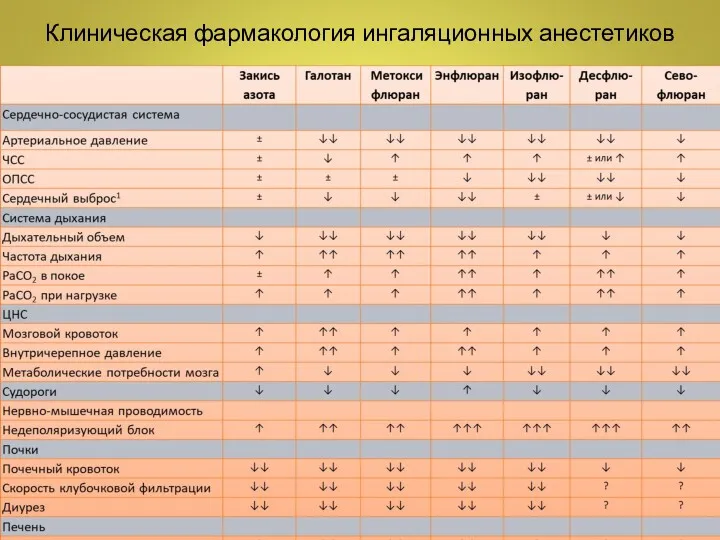
- 17. Клиническая фармакология ингаляционных анестетиков
- 18. Севофлюран раствор для ингаляционного наркоза, 250 мл Препарат предназначен для ингаляционного наркоза. Применение препарата для вводного
- 19. Ксенон Средство для ингаляционной анестезии. В соотношении с кислородом (60:40, 70:30, 80:20) оказывает миорелаксирующее, анальгезирующее и
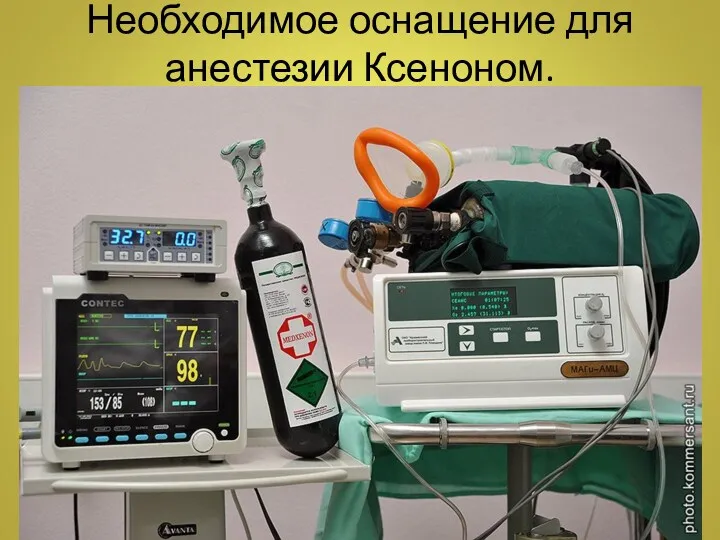
- 20. Необходимое оснащение для анестезии Ксеноном.
- 21. Неингаляционные анестетики Короткого действия (до 15 минут): Пропанидид, кетамин, бриетал, диприван (пропофол) Средней продолжительности (20-30 минут):
- 22. Пропофол (диприван) – 1% эмульсия для в/в введения. (1 мл - 10 мг) Индукция: 1-2,5 мг/кг
- 23. Сердечно-сосудистая система. Пропофол значительно уменьшает ОПСС, сократимость миокарда и преднагрузку, что приводит к значительному снижению артериального
- 24. Кетамин (кеталар, калипсол) 2, 5, 10% р-р, амп. Индукция: 1-2 мг/кг Основной наркоз: 0,6-2 мг/кг для
- 25. Кетамин (кеталар, калипсол) Вызывает аналгезию, амнезию и утрату сознания. Сердечно-сосудистая система. Резко отличаясь от всех остальных
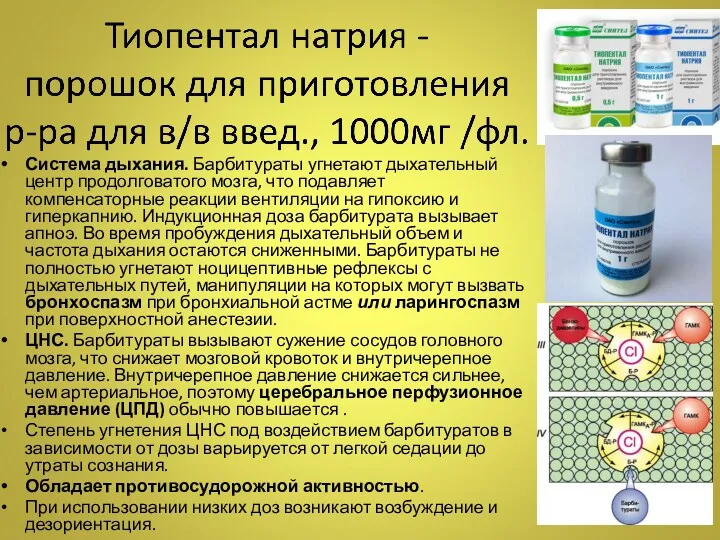
- 26. Тиопентал натрия - порошок для приготовления р-ра для в/в введ., 1000мг /фл. производные барбитуровой кислоты Индукция:
- 27. Система дыхания. Барбитураты угнетают дыхательный центр продолговатого мозга, что подавляет компенсаторные реакции вентиляции на гипоксию и
- 28. Оксибутират натрия (ГОМК, Оксибат-Na) – 20% р-р, амп. 5 мл. – 1000 мг. Взаимодействует с пре-
- 29. Основной наркоз: 50-200 мг/кг Неингаляционный наркоз (вводный и базисный, при малотравмирующих операциях, при оперативном родоразрешении, для
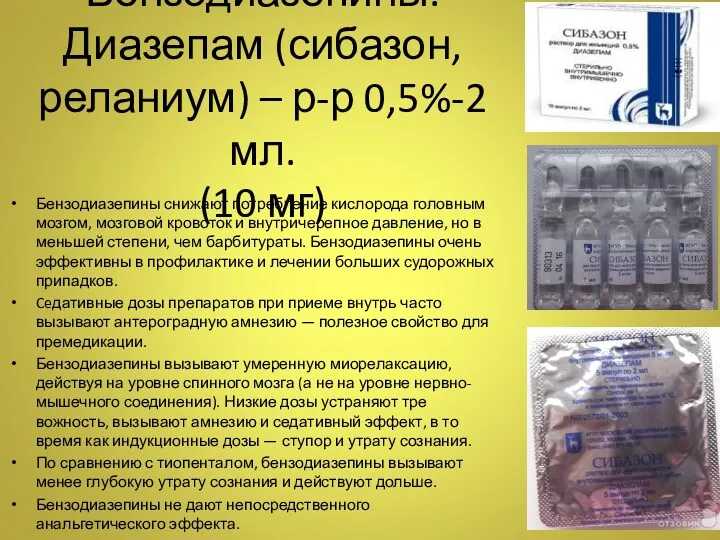
- 30. Бензодиазепины. Диазепам (сибазон, реланиум) – р-р 0,5%-2 мл. (10 мг) Бензодиазепины снижают потребление кислорода головным мозгом,
- 31. Сердечно-сосудистая система. Даже в индукционных дозах бензодиазепины практически не влияют на кровообращение. Незначительно снижаются артериальное давление,
- 32. Расчетные дозы бензодиазепинов.
- 33. Опиоиды Опиоиды вызывают незначительную седацию, но в клинике их применяют благодаря мощному анальгетическому эффекту. Фармакодинамические свойства
- 34. Классификация опиатных рецепторов
- 35. Дозы наркотических анальгетиков:
- 36. Миорелаксанты
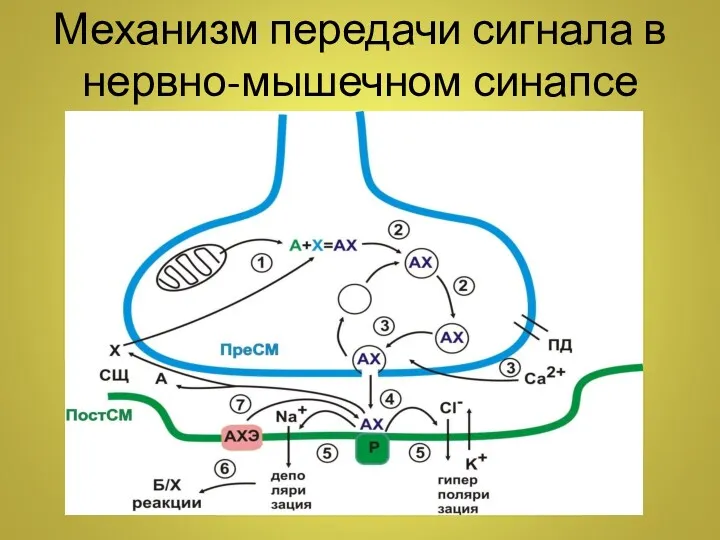
- 37. Механизм передачи сигнала в нервно-мышечном синапсе
- 38. Суксаметония хлорид (Листенон) Суксаметония иодид (Дитилин) 20мг/мл – 5 мл. Деполяризующие миорелаксанты действуют в 2 этапа.
- 39. Сукцинилхолин может приводить к заметному изменению частоты сердечных сокращений и повышению или понижению артериального давления. Это
- 40. Для интубации трахеи используют дозу 1 – 2 мг/кг. При этом интубация возможна через 1 мин.
- 41. Недеполяризующие миорелаксанты Недеполяризующие релаксанты действуют как конкурентные антагонисты ацетилхолина. Они экранируют н-холинорецепторы от взаимодействия с медиатором.
- 42. Пипекурония бромид (Ардуан, Веро-пипекуроний) Лиофилизат для приготовления раствора для внутривенного введения, 4 мг Рекомендуемые дозы для
- 43. Рокурония бромид (Эсмерон) – 10 мг/мл – 5 мл. Только в/в. При интубации, а также для
- 45. Скачать презентацию































 Биожүйелердің электрөткізгіштігі
Биожүйелердің электрөткізгіштігі Затяжной субфебрилитет в амбулаторно-поликлинической практике
Затяжной субфебрилитет в амбулаторно-поликлинической практике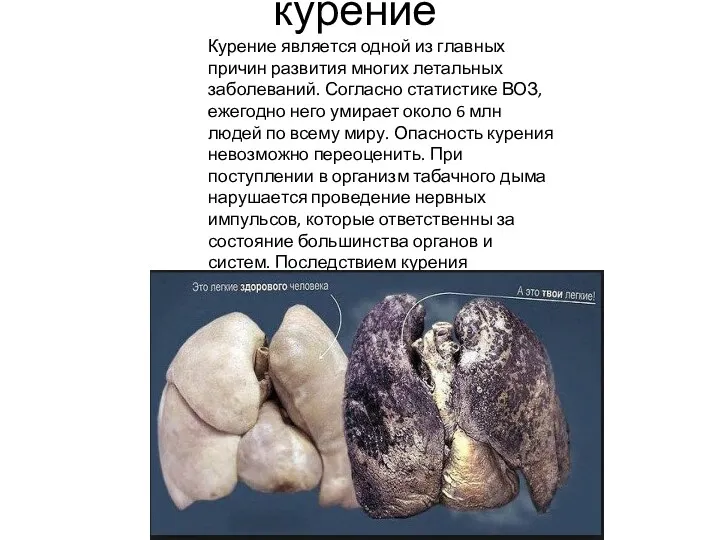 Вред курения, алкголя, наркотиков
Вред курения, алкголя, наркотиков Железодефицитная анемия у детей
Железодефицитная анемия у детей История хирургии. Асптика. Антисептика. (лекция 1)
История хирургии. Асптика. Антисептика. (лекция 1) Синдром поражения миокарда
Синдром поражения миокарда ЛФК при переломах верхних конечностей
ЛФК при переломах верхних конечностей Дәрігердің кәсіби деформациясы
Дәрігердің кәсіби деформациясы Жедел медициналық жәрдем беру Құрысу синдромы.Балалардағы ерекшеліктері.Жіті психоздар.Эпилепсия. Эпилептикалық статус
Жедел медициналық жәрдем беру Құрысу синдромы.Балалардағы ерекшеліктері.Жіті психоздар.Эпилепсия. Эпилептикалық статус Молекулярно-цитогенетическая диагностика острых лейкозов
Молекулярно-цитогенетическая диагностика острых лейкозов Группы крови. Переливание крови
Группы крови. Переливание крови Види і мета медичних оглядів на підприємстві
Види і мета медичних оглядів на підприємстві Жүкті әйелдерде жүктіліктің 16 аптасына дейін истмико-цервикальды жетіспеушілік кезінде акушерлік пессарий
Жүкті әйелдерде жүктіліктің 16 аптасына дейін истмико-цервикальды жетіспеушілік кезінде акушерлік пессарий Периодонтит. Часть 3
Периодонтит. Часть 3 Расщелина верхней губы и нёба
Расщелина верхней губы и нёба Ожоги глаз и их придатков
Ожоги глаз и их придатков Паренхиматозные дистрофии
Паренхиматозные дистрофии Профилактика инфекционных заболеваний
Профилактика инфекционных заболеваний Жедел коронарлы синдром
Жедел коронарлы синдром Пастереллёз животных
Пастереллёз животных Атопиялық дерматит
Атопиялық дерматит Противовирусные средства
Противовирусные средства Миокардит
Миокардит Ящур животных
Ящур животных Инфекционная безопасность. Профилактика внутрибольничной инфекции
Инфекционная безопасность. Профилактика внутрибольничной инфекции Миокард инфарктының қауіп топтарын анықтау және оның алдын алу тақырыбындағы диплом жұмысы
Миокард инфарктының қауіп топтарын анықтау және оның алдын алу тақырыбындағы диплом жұмысы Организация медицинской помощи детскому населению на территории городского округа Чехов
Организация медицинской помощи детскому населению на территории городского округа Чехов Программа государственных гарантий бесплатного оказания гражданам медицинской помощи
Программа государственных гарантий бесплатного оказания гражданам медицинской помощи