Содержание
- 2. Азотистый баланс – соотношение поступившего в организм азота (в виде азота аминокислот) и выведенного азота (в
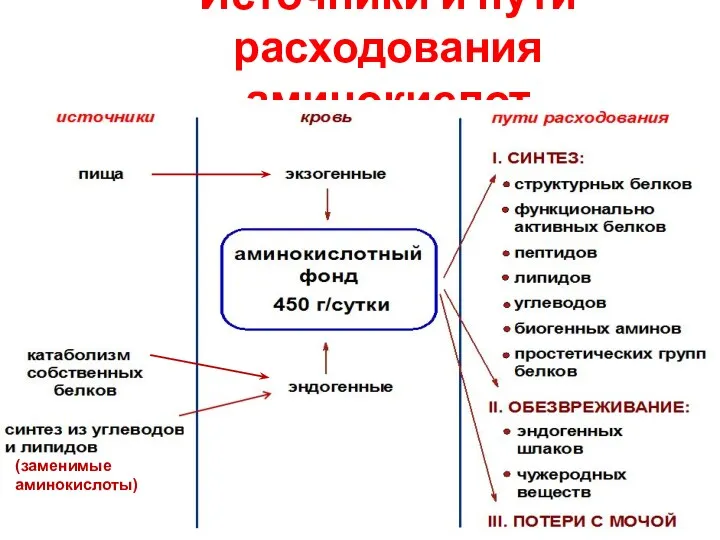
- 3. Источники и пути расходования аминокислот (заменимые аминокислоты)
- 4. Потребность в пищевых белках 23,2 г/сут – коэффициент Рубнера – «коэффициент изнашивания» (азотистый баланс отрицательный). 30-45
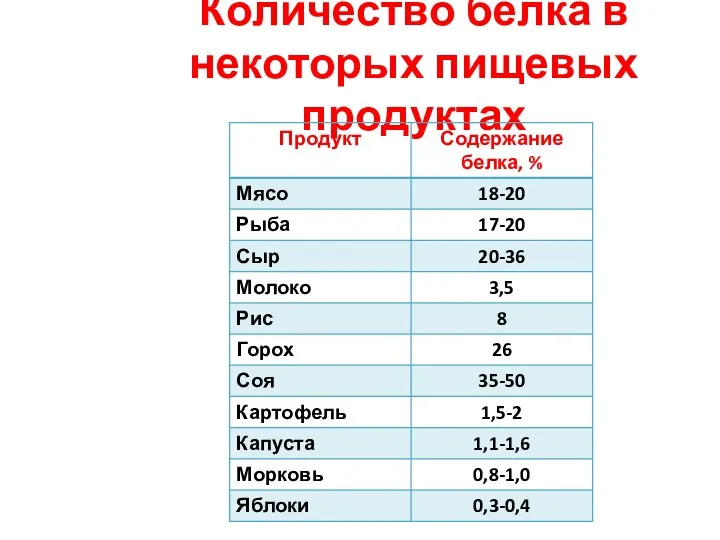
- 5. Количество белка в некоторых пищевых продуктах
- 6. Критерии полноценности пищевого белка Белок должен содержать все заменимые аминокислоты в соотношениях, близких к их соотношениям
- 7. Ферменты, переваривающие белки (гидролизующие пептидные связи), называются протеиназы (пептидазы, протеазы, протеолитические ферменты)
- 8. Катепсины – лизосомальные протеолитические ферменты (протеиназы), обеспечивающие распад тканевых (собственных) белков, рН оптимум их лежит в
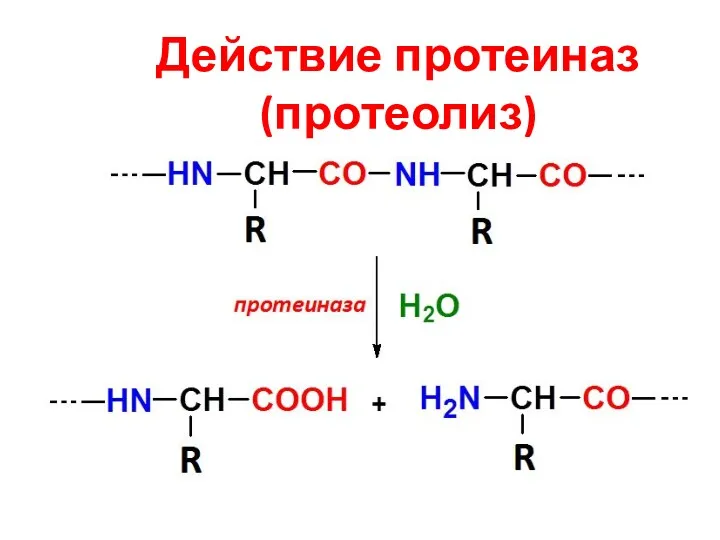
- 9. Действие протеиназ (протеолиз)
- 10. Протеиназы ЖКТ Эндопептидазы Пепсин; Реннин; Гастриксин; Трипсин; Химотрипсин; Эластаза. Экзопептидазы Карбоксипептидазы А и В; Аминопептидазы; Дипептидазы;
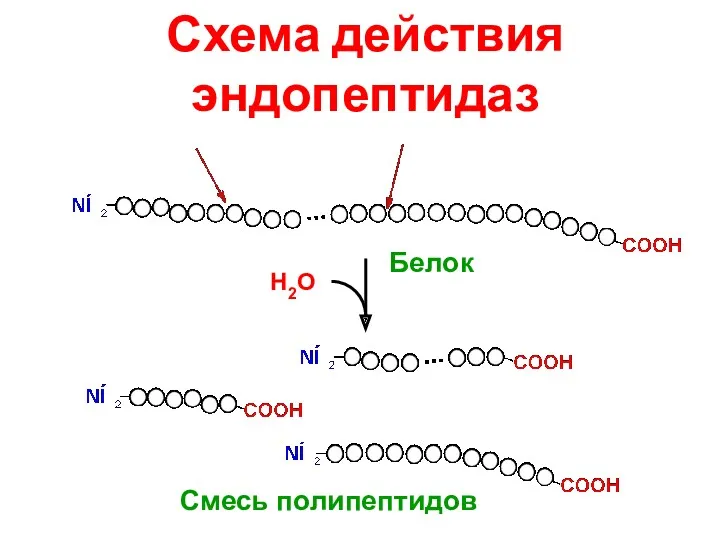
- 11. Схема действия эндопептидаз Н2О Смесь полипептидов Белок
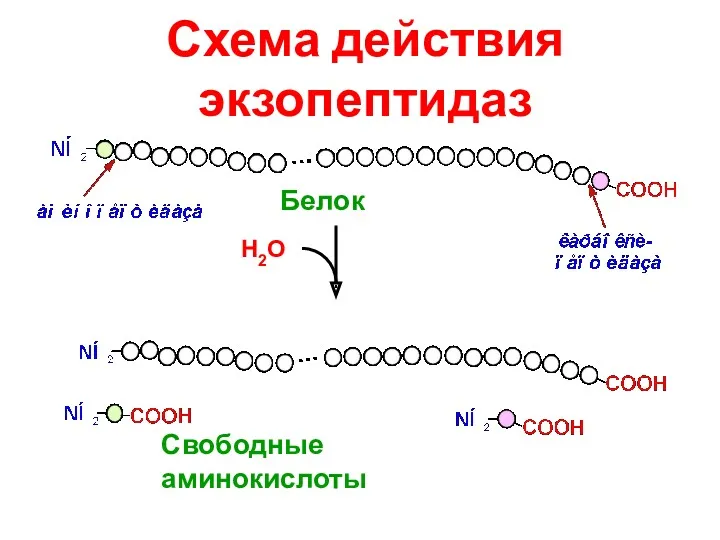
- 12. Схема действия экзопептидаз Н2О Свободные аминокислоты Белок
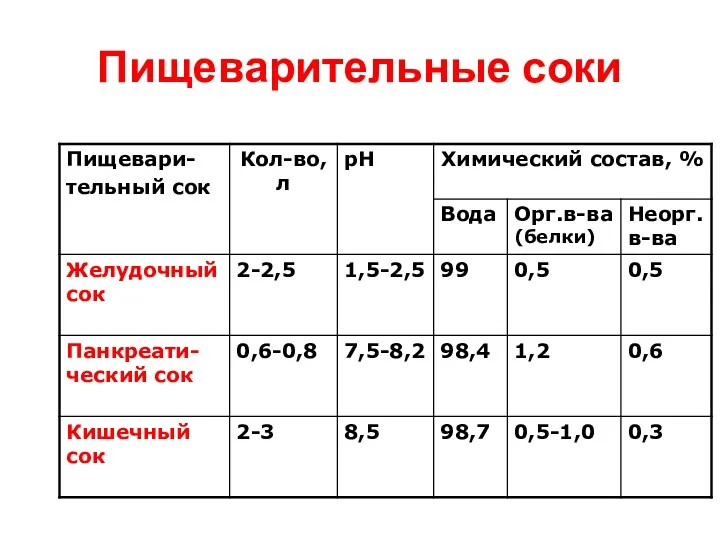
- 13. Пищеварительные соки
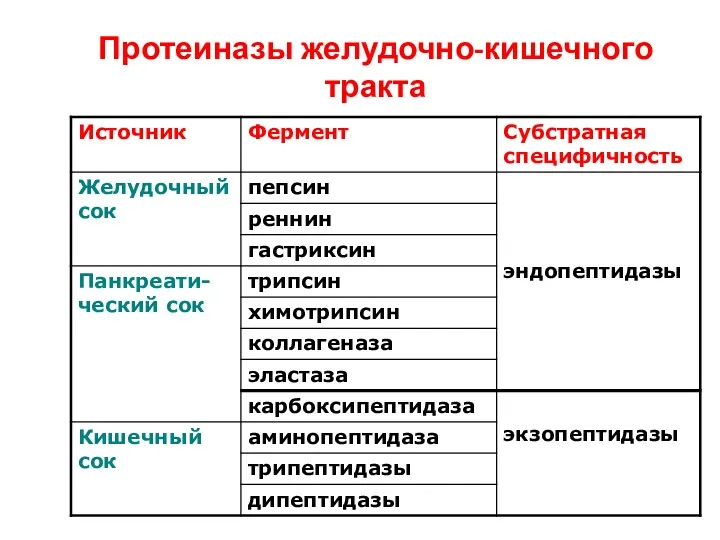
- 14. Протеиназы желудочно-кишечного тракта
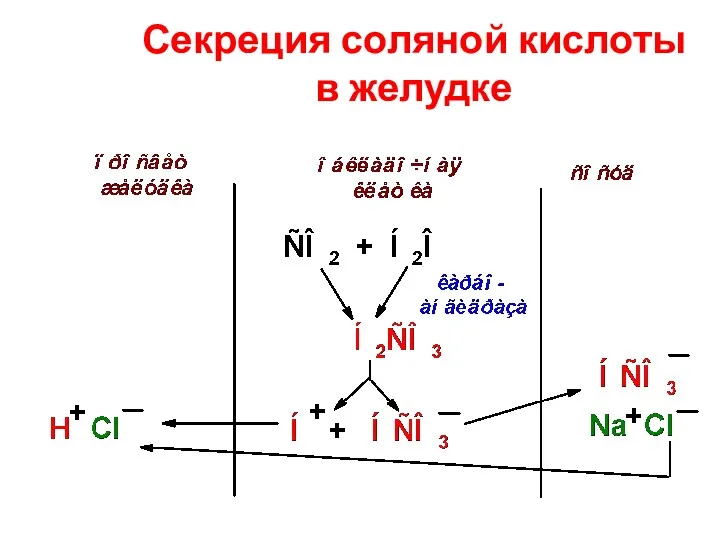
- 15. Секреция соляной кислоты в желудке
- 16. Функции соляной кислоты активация пепсиногена создание рН-оптимума для пепсина (1,5-2,5) бактерицидное действие денатурирует белки регулирует работу
- 17. Виды кислотности желудочного сока Общая кислотность (НСl + прочие кислые вещества – кислые соли, органические кислоты)
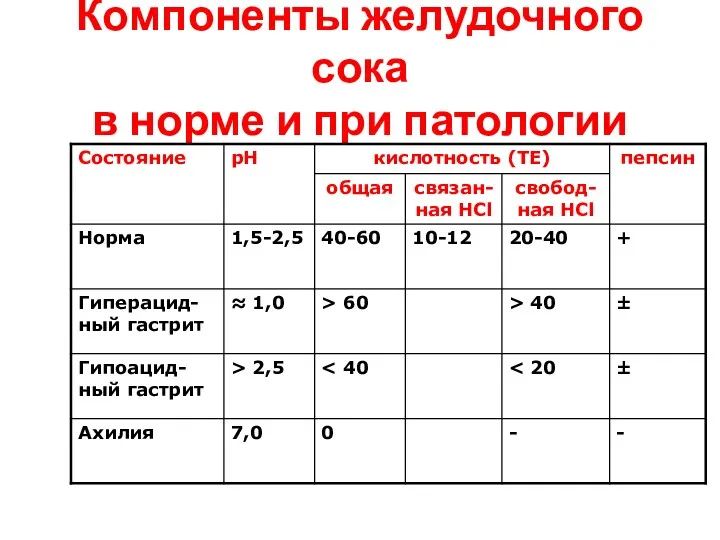
- 18. Компоненты желудочного сока в норме и при патологии
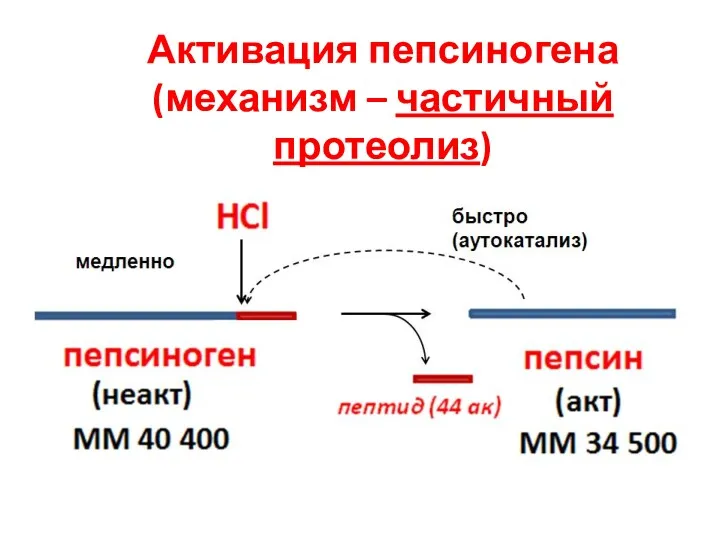
- 19. Активация пепсиногена (механизм – частичный протеолиз)
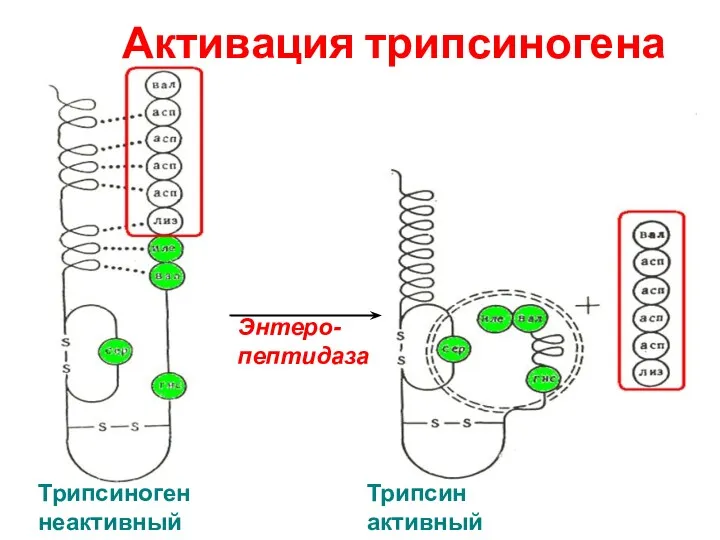
- 20. Активация трипсиногена Энтеро-пептидаза Трипсиноген неактивный Трипсин активный
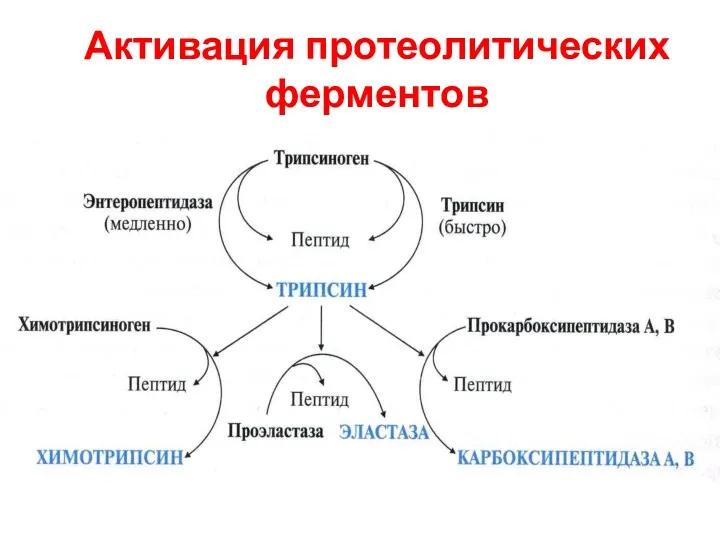
- 21. Активация протеолитических ферментов
- 22. Биологический смысл синтеза проферментов – защита тканей пищеварительных желёз от самопереваривания (аутолиза)
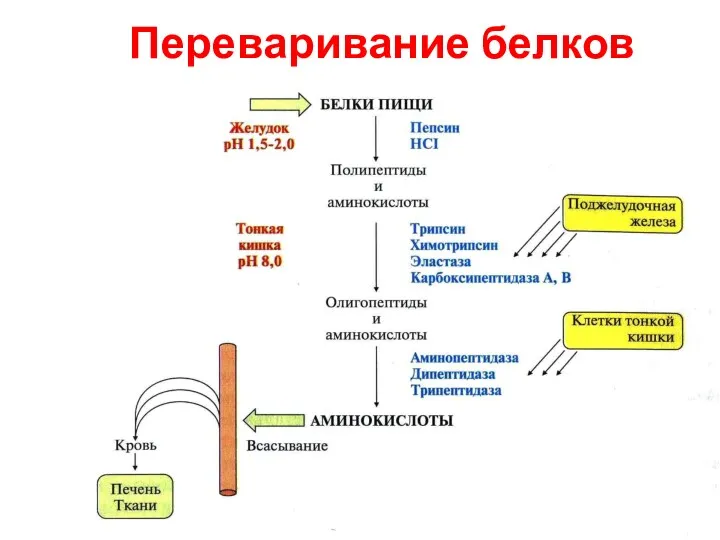
- 23. Переваривание белков
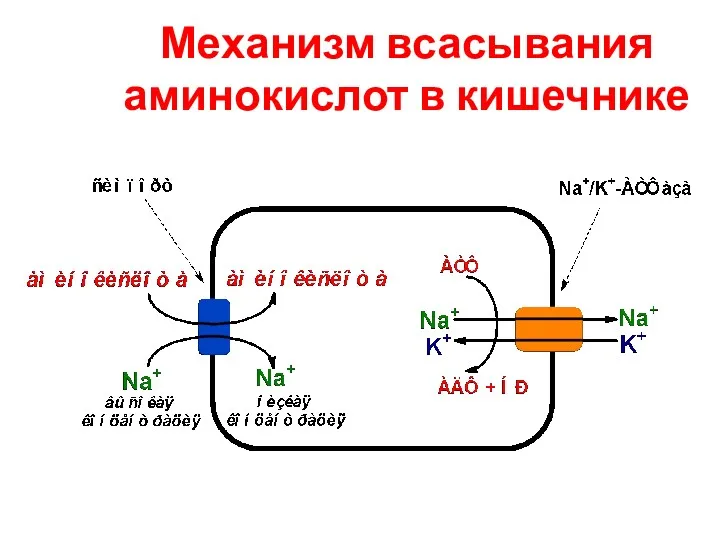
- 25. Механизм всасывания аминокислот в кишечнике
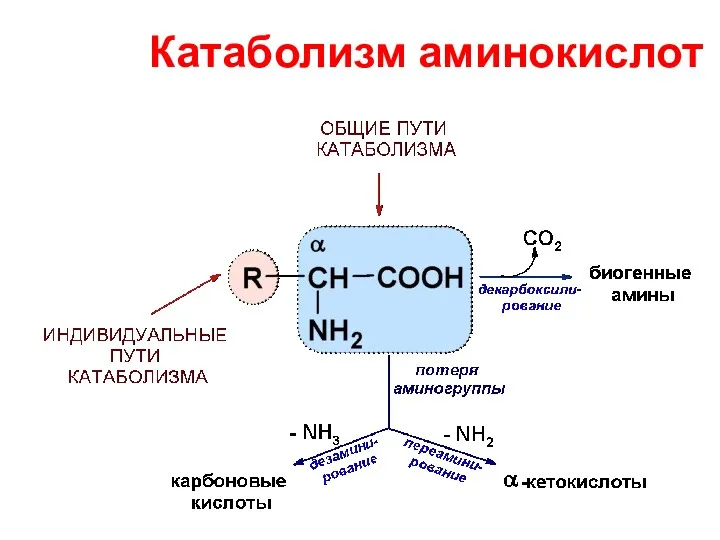
- 26. Катаболизм аминокислот
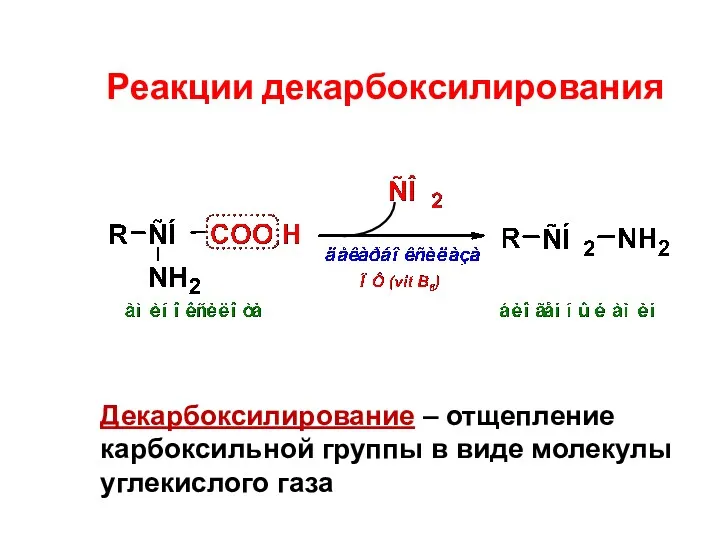
- 27. Реакции декарбоксилирования Декарбоксилирование – отщепление карбоксильной группы в виде молекулы углекислого газа
- 28. Биологическая роль реакций декарбоксилирования – образование биогенных аминов, которые могут быть: Гормонами Нейромедиаторами Входить в состав
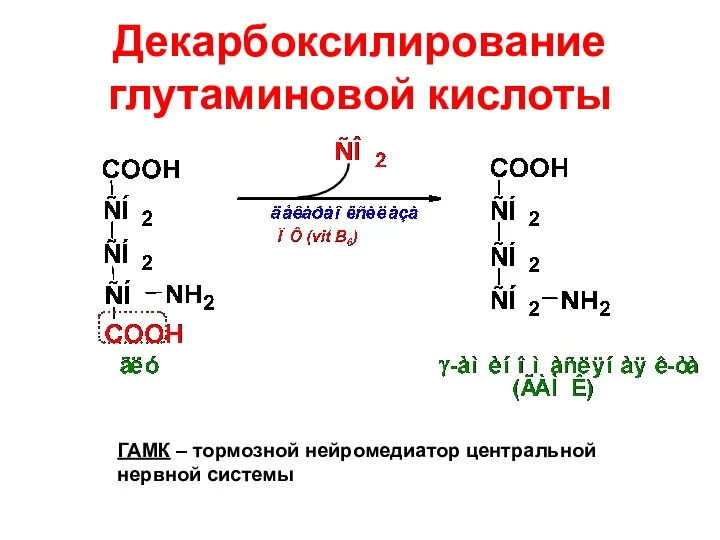
- 29. Декарбоксилирование глутаминовой кислоты ГАМК – тормозной нейромедиатор центральной нервной системы
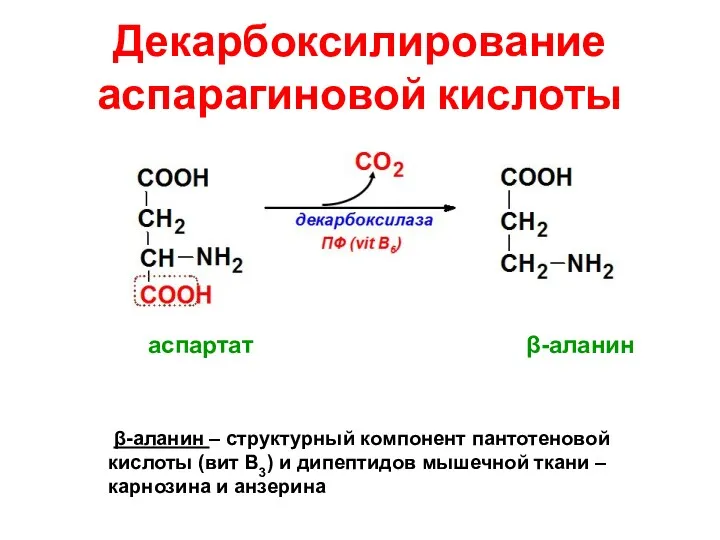
- 30. Декарбоксилирование аспарагиновой кислоты β-аланин – структурный компонент пантотеновой кислоты (вит В3) и дипептидов мышечной ткани –
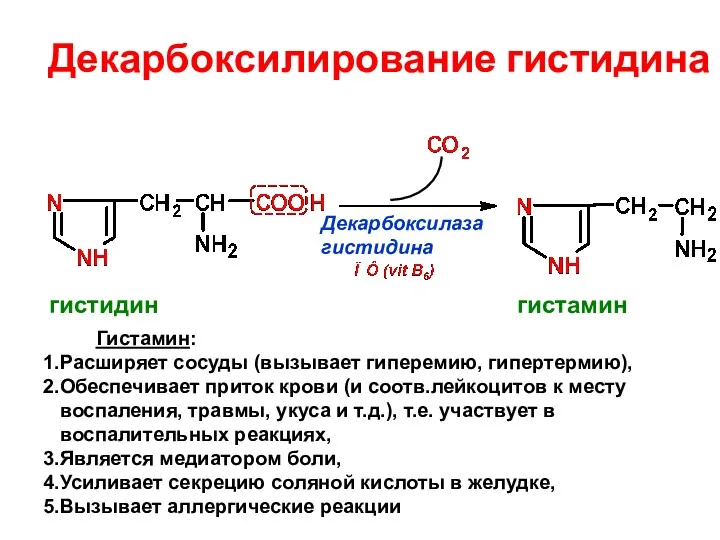
- 31. Декарбоксилирование гистидина Декарбоксилаза гистидина гистидин гистамин Гистамин: Расширяет сосуды (вызывает гиперемию, гипертермию), Обеспечивает приток крови (и
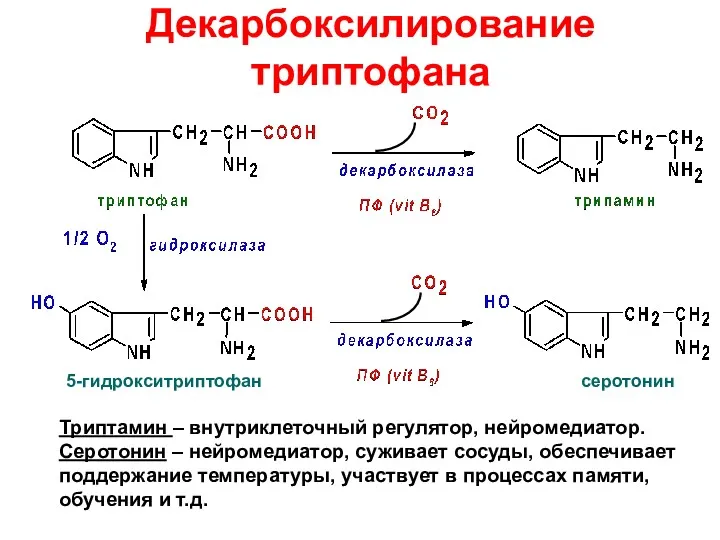
- 32. Декарбоксилирование триптофана 5-гидрокситриптофан серотонин Триптамин – внутриклеточный регулятор, нейромедиатор. Серотонин – нейромедиатор, суживает сосуды, обеспечивает поддержание
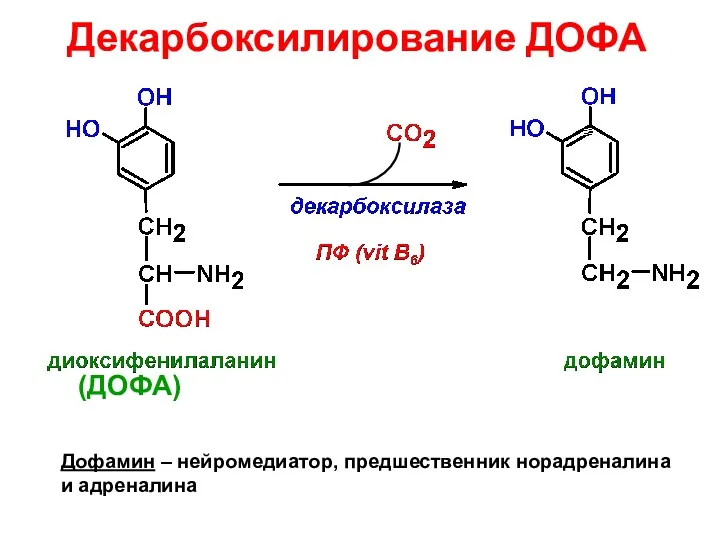
- 33. Декарбоксилирование ДОФА Дофамин – нейромедиатор, предшественник норадреналина и адреналина (ДОФА)
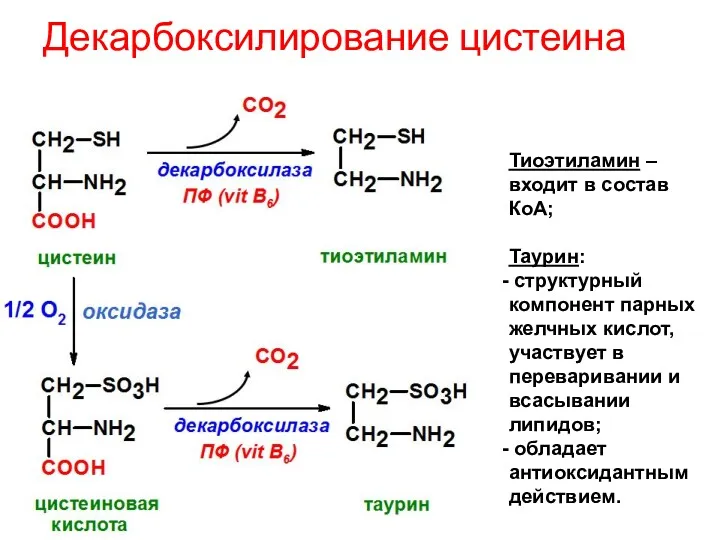
- 34. Декарбоксилирование цистеина Тиоэтиламин – входит в состав КоА; Таурин: структурный компонент парных желчных кислот, участвует в
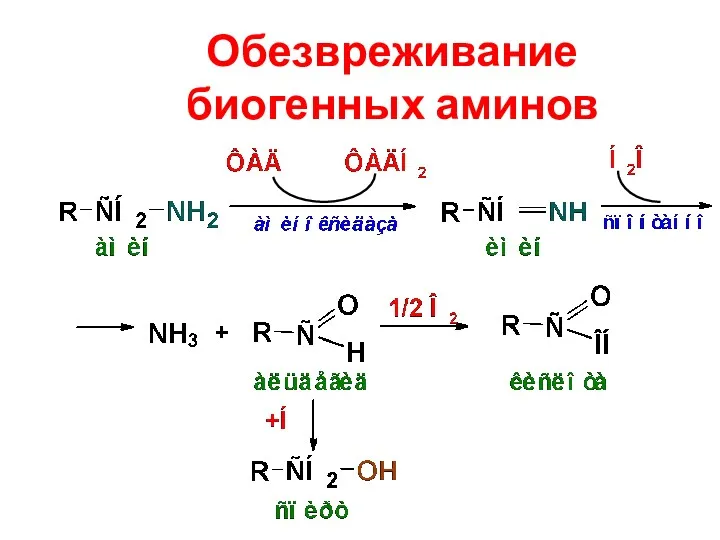
- 35. Обезвреживание биогенных аминов
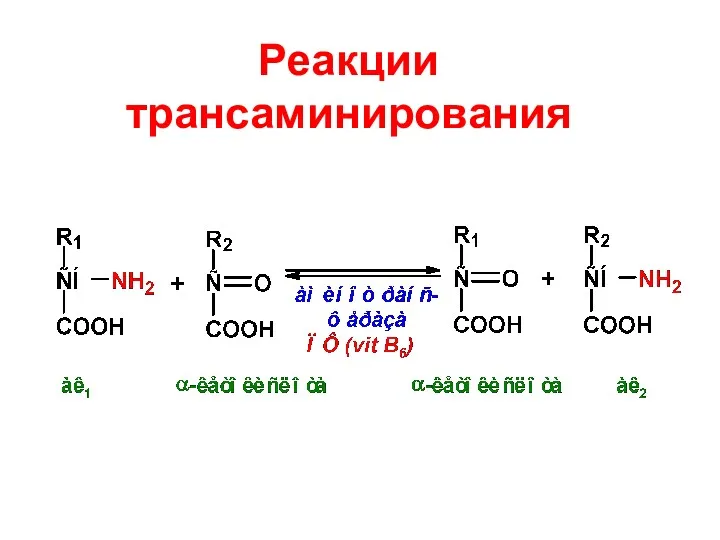
- 36. Реакции трансаминирования
- 37. Вещества, участвующие в трансаминировании: Аминокислоты – практически все, кроме треонина, лизина и пролина, но особенно активны
- 38. Роль пиридоксальфосфата в трансаминировании – является промежуточным переносчиком аминогруппы (первичным акцептором)
- 39. Биологическая роль трансаминирования Путь синтеза заменимых аминокислот Путь перераспределения азота без образования токсичного аммиака Путь пополнения
- 40. Реакции трансаминирования
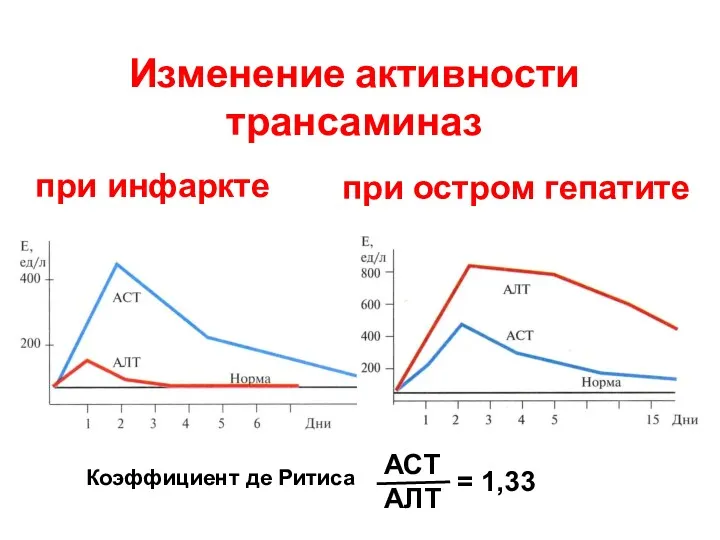
- 41. Изменение активности трансаминаз при инфаркте при остром гепатите Коэффициент де Ритиса АСТ АЛТ = 1,33
- 42. Типы реакций дезаминирования Восстановительное Гидролитическое Внутримолекулярное Окислительное Дезаминирование – отщепление аминогруппы в виде молекулы аммиака
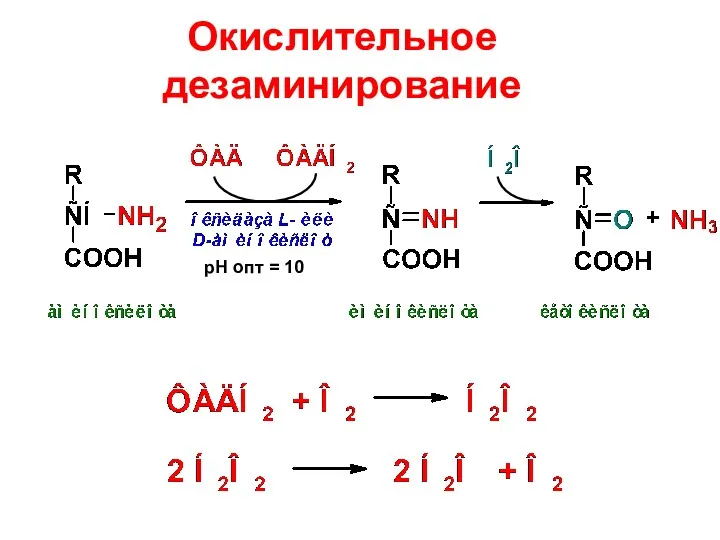
- 43. Окислительное дезаминирование рН опт = 10
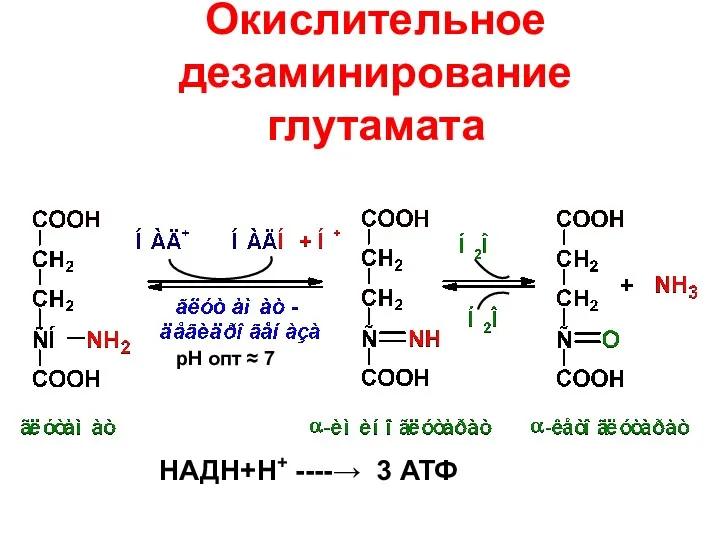
- 44. Окислительное дезаминирование глутамата НАДН+Н+ ----→ 3 АТФ рН опт ≈ 7
- 45. Отличия и роль процесса дезаминирования глутамата Глутаматдегидрогеназа активна при физиологических значениях рН; Глутаматдегидрогеназа обладает обратимостью действия
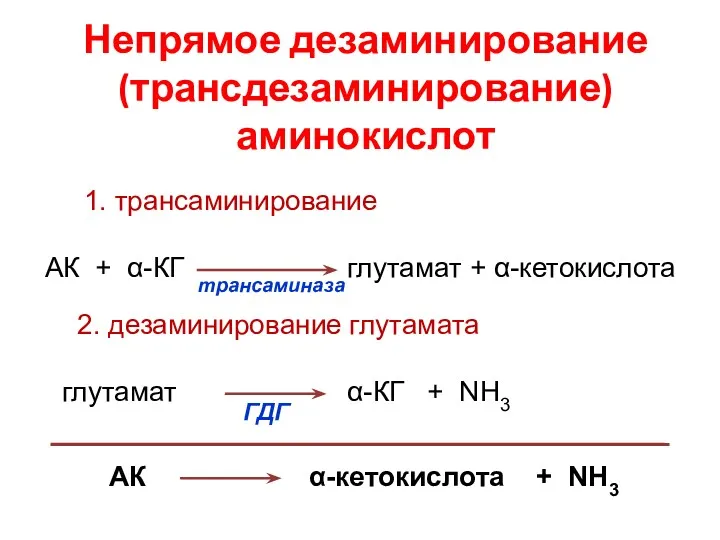
- 46. Непрямое дезаминирование (трансдезаминирование) аминокислот АК α-кетокислота + NH3 1. трансаминирование АК + α-КГ глутамат + α-кетокислота
- 48. Скачать презентацию
















 Денсаулық сақтаудағы бизнес жоспарлау
Денсаулық сақтаудағы бизнес жоспарлау Эмбриогенез, анатомо-физиологические особенности почек и мочевыделительной системы у детей
Эмбриогенез, анатомо-физиологические особенности почек и мочевыделительной системы у детей Анкерлі штифттер
Анкерлі штифттер диффузный токсический зоб. Гипотериоз
диффузный токсический зоб. Гипотериоз Алопеция
Алопеция Новые технологии в диагностике сахарного диабета
Новые технологии в диагностике сахарного диабета Биомеханика тела пациента и медицинского работника
Биомеханика тела пациента и медицинского работника Лекарственные растения и сырье, содержащие витамины
Лекарственные растения и сырье, содержащие витамины Медициналық заттарды стерилизациялау. Медициналық құралжабдықтарды стерилизация алды өңдеу
Медициналық заттарды стерилизациялау. Медициналық құралжабдықтарды стерилизация алды өңдеу Поражение нервной системы при заболеваниях сердечно-сосудистой системы
Поражение нервной системы при заболеваниях сердечно-сосудистой системы Острый аппендицит
Острый аппендицит Иммунитеттіѕ жасушалыќ жїйесі. Иммунологиялыќ тґзімділік (толеранттылыќ). Цитокиндер
Иммунитеттіѕ жасушалыќ жїйесі. Иммунологиялыќ тґзімділік (толеранттылыќ). Цитокиндер Іштен біткен жүрек ақаулары
Іштен біткен жүрек ақаулары Острый рассеянный энцефаломиелит
Острый рассеянный энцефаломиелит Влияние вредных факторов на репродуктивную систему человека
Влияние вредных факторов на репродуктивную систему человека Acute Lymphoblastic Leukemia ALL
Acute Lymphoblastic Leukemia ALL Диагностика гнойновоспалительных заболеваний и гемолитической болезни новорожденного
Диагностика гнойновоспалительных заболеваний и гемолитической болезни новорожденного Клинико-диагностические маркеры патологии сердечно-сосудистой системы
Клинико-диагностические маркеры патологии сердечно-сосудистой системы Гелиотерапия
Гелиотерапия Иммунология беременности. Изоантигенная несовместимость. Гемолитическая болезнь плода и новорожденного
Иммунология беременности. Изоантигенная несовместимость. Гемолитическая болезнь плода и новорожденного Мышцы человека - 2 часть
Мышцы человека - 2 часть ЭКГ (электро- кардиография)
ЭКГ (электро- кардиография) Выделительная система
Выделительная система Нейросенсорная тугоухость
Нейросенсорная тугоухость Средства, возбуждающие ЦНС
Средства, возбуждающие ЦНС ГЭРБ. Лос-Анжелесская классификация
ГЭРБ. Лос-Анжелесская классификация Основы психогенетики
Основы психогенетики Воспалительные заболевания женских половых органов
Воспалительные заболевания женских половых органов