Содержание
- 2. План: Введение; Фазы апаптоза; Регуляция апаптоза; Роль апаптоза в организме; Патология, обусловленная нарушениями апоптоза; Вывод; Список
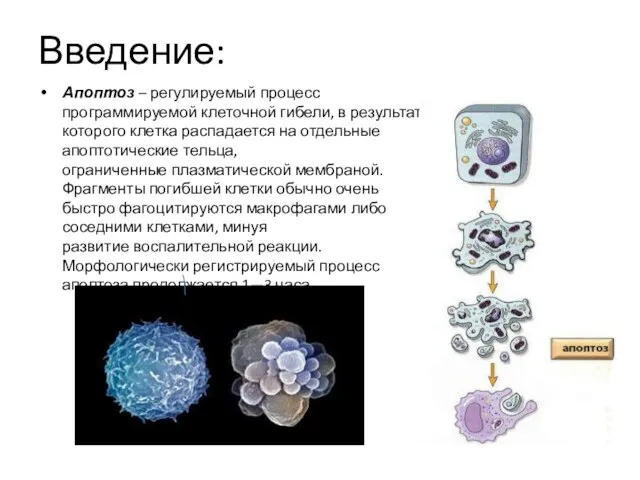
- 3. Введение: Апоптоз – регулируемый процесс программируемой клеточной гибели, в результате которого клетка распадается на отдельные апоптотические
- 4. Апоптоз Одной из основных функций апоптоза является уничтожение дефектных клеток. К тому же, апоптоз задействован в
- 5. Краткие исторические сведения: Термин «апоптоз» был впервые употреблён в 1972 году в работе британских учёных —
- 6. Интерес учёных связан с возможностью применения знаний о программируемой клеточной смерти в медицине при лечении онкологических,
- 7. В организме среднестатистического взрослого человека в результате апоптоза погибает ежедневно порядка 50—70 миллиардов клеток. Для среднестатистического
- 8. Апоптоз условно разделить на три фазы: Сигнальная (индукторная) Эффекторная Деградационная (фаза экзекуции или деструкции)
- 9. Сигнальная фаза Инициация апоптоза может происходить посредством внешних или внутриклеточных факторов. Например, в результате гипоксии, гипероксии,
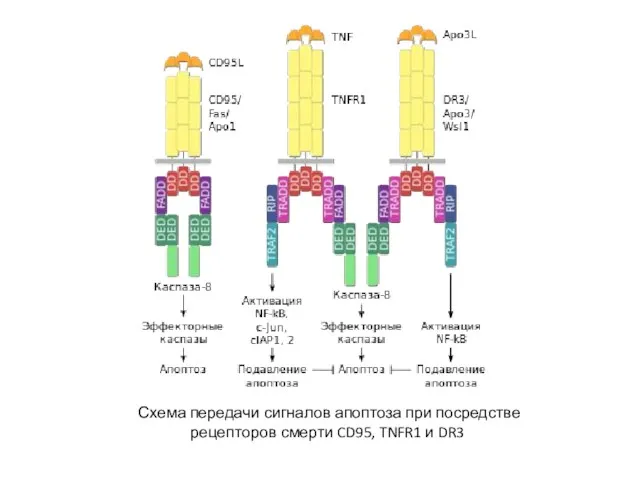
- 10. Схема передачи сигналов апоптоза при посредстве рецепторов смерти CD95, TNFR1 и DR3
- 11. Митохондриальный сигнальный путь Большинство форм апоптоза у позвоночных реализуется по митохондриальному пути. Митохондриальный сигнальный путь апоптоза
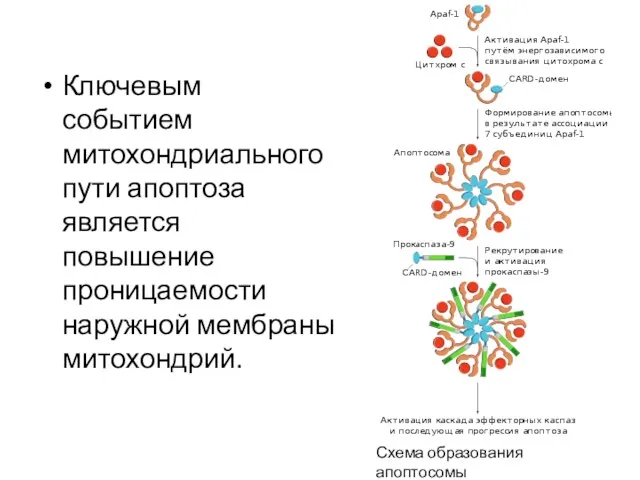
- 12. Ключевым событием митохондриального пути апоптоза является повышение проницаемости наружной мембраны митохондрий. Схема образования апоптосомы
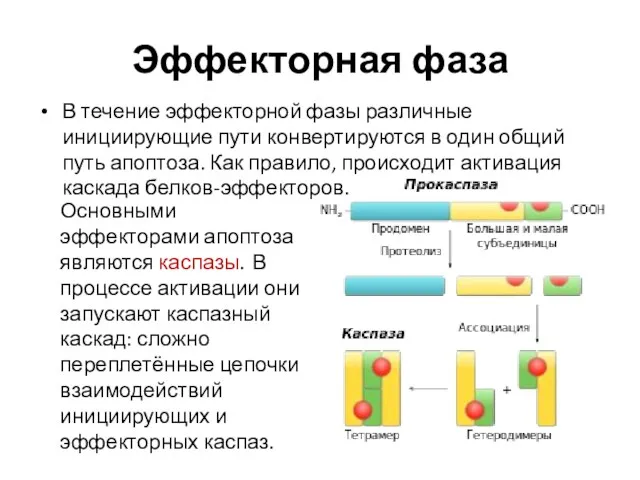
- 13. Эффекторная фаза В течение эффекторной фазы различные инициирующие пути конвертируются в один общий путь апоптоза. Как
- 14. Деградационная фаза Итогом программируемой клеточной гибели вне зависимости от изначального инициирующего воздействия является деградация клетки путём
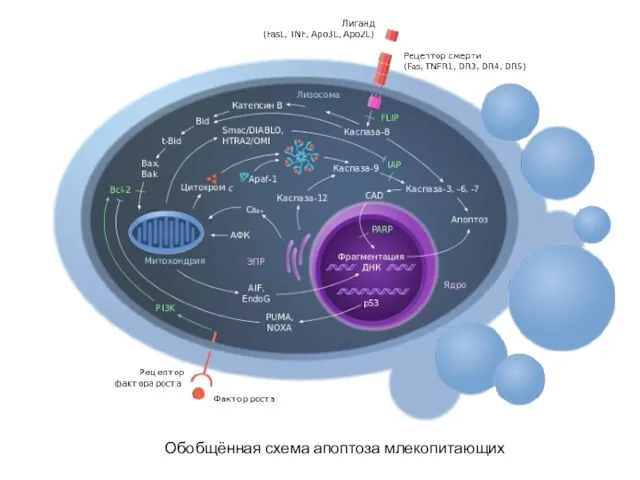
- 15. Обобщённая схема апоптоза млекопитающих
- 16. Регуляция апоптоза Белки семейства Bcl-2 являются основными регуляторами митохондриального пути апоптоза. Они оказывают решающее воздействие на
- 17. Роль апоптоза в организме: Одной из главных функций апоптоза в организме является поддержание клеточного гомеостаза. Обеспечивается
- 18. Редукция хвоста у головастика при превращении в лягушку: Головастик паракринии Лягушонок с остатками хвоста У животных
- 19. Автономный апоптоз Морфогенетический апоптоз участвует в разрушении различных тканевых зачатков. Его нарушение приводит к синдактилии, расщеплению
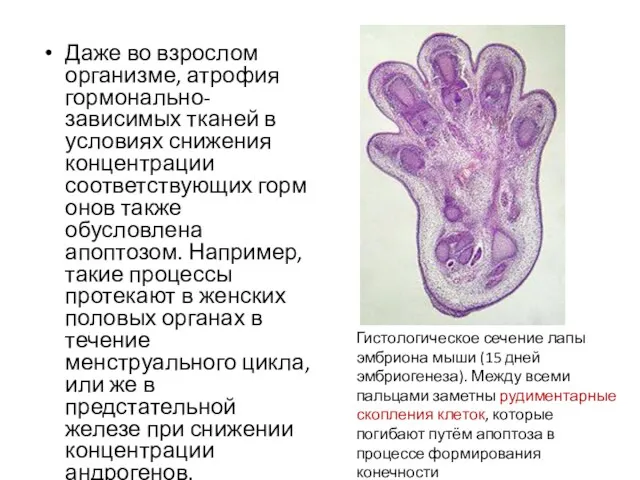
- 20. Даже во взрослом организме, атрофия гормонально-зависимых тканей в условиях снижения концентрации соответствующих гормонов также обусловлена апоптозом.
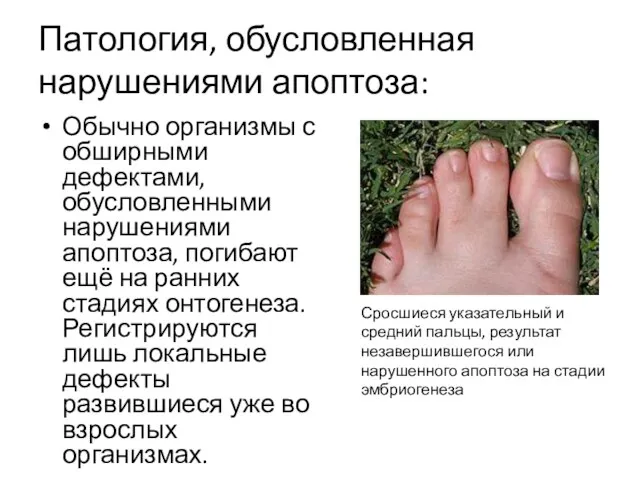
- 21. Патология, обусловленная нарушениями апоптоза: Обычно организмы с обширными дефектами, обусловленными нарушениями апоптоза, погибают ещё на ранних
- 22. Патологические процессы развиваются в случае подавления или усиления апоптоза. При недостаточности апоптоза прогрессируют аутоиммунные процессы и
- 24. Вывод: Апопотоз для организма играет боьшую роль, выполняя защитный механизм. Но также, апоптоз может нарушаться и
- 26. Скачать презентацию
















 Влияние геомагнитного поля на состояние сердечно-сосудистой системы человека в условиях космического полета
Влияние геомагнитного поля на состояние сердечно-сосудистой системы человека в условиях космического полета Кишечные инфекции
Кишечные инфекции Посттравматическое стрессовое расстройство
Посттравматическое стрессовое расстройство Диета при сердечно-сосудистых заболеваниях
Диета при сердечно-сосудистых заболеваниях Современный взгляд на проблему лечения инфекции нижних мочевыводящих путей
Современный взгляд на проблему лечения инфекции нижних мочевыводящих путей Дәрігер-мейірбике-науқас қарым-қатынасы
Дәрігер-мейірбике-науқас қарым-қатынасы Профессиональные заболевания медицинских работников
Профессиональные заболевания медицинских работников История развития Сестринского дела
История развития Сестринского дела Хроническая венозная недостаточность
Хроническая венозная недостаточность Сестринский уход при анемиях
Сестринский уход при анемиях Хирургиялық ақпараттар,компьютерлік технология және телемедицина
Хирургиялық ақпараттар,компьютерлік технология және телемедицина Мышцы верхних и нижних конечностей человека
Мышцы верхних и нижних конечностей человека Реанимация новорожденных
Реанимация новорожденных СУ при различных заболеваниях и состояниях. Клиническая фармакология
СУ при различных заболеваниях и состояниях. Клиническая фармакология Дәрілік заттар жарнамаcының дұрыс емеc жүргізілу белгілері
Дәрілік заттар жарнамаcының дұрыс емеc жүргізілу белгілері Сушка ЛРС
Сушка ЛРС Еңбек гигиенасындағы зертханалық зерттеулердің техникасы
Еңбек гигиенасындағы зертханалық зерттеулердің техникасы Тағамдық қауіпсіздік және оның бағалау критерийлері
Тағамдық қауіпсіздік және оның бағалау критерийлері Процессный анализ в деятельности врача. Обеспечение безопасности пациентов
Процессный анализ в деятельности врача. Обеспечение безопасности пациентов Секвенирование ДНК по Сэнгеру. Курс 3 ЦИОП Медицина будущего
Секвенирование ДНК по Сэнгеру. Курс 3 ЦИОП Медицина будущего Ингаляционная анестезия и мониторинг низкого потока
Ингаляционная анестезия и мониторинг низкого потока Язвенная болезнь желудка и двенадцатиперстной кишки
Язвенная болезнь желудка и двенадцатиперстной кишки Современные подходы к антибактериальной терапии при сесписе
Современные подходы к антибактериальной терапии при сесписе ВКР: Роль медицинской сестры в проведении реабилитационных мероприятий при заболеваниях органов дыхания у детей
ВКР: Роль медицинской сестры в проведении реабилитационных мероприятий при заболеваниях органов дыхания у детей Психотропные средства
Психотропные средства Общая фармакология. Фармакокинетика
Общая фармакология. Фармакокинетика Правила проведения коррекции частичного съемного протеза. Фазы адаптации к съемным протезам
Правила проведения коррекции частичного съемного протеза. Фазы адаптации к съемным протезам Валидация очистки оборудования. Отчет о валидации очистки оборудования
Валидация очистки оборудования. Отчет о валидации очистки оборудования