Проект на тему: Диагностика наследственных заболеваний. Молекулярно-генетические факторы высокого риска развития тромбоза презентация
Содержание
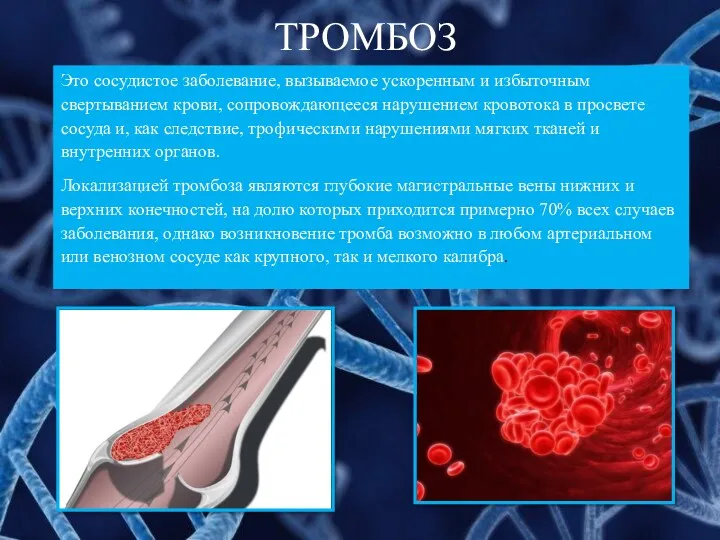
- 2. ТРОМБОЗ Это сосудистое заболевание, вызываемое ускоренным и избыточным свертыванием крови, сопровождающееся нарушением кровотока в просвете сосуда
- 3. АКТУАЛЬНОСТЬ ПРОБЛЕМЫ: Венозные тромбозы и легочная эмболия являются важной проблемой современной медицины, значение которой в практике
- 4. ФАКТОРЫ РИСКА РАЗВИТИЯ ТРОМБОЗА Травма Хирургическое вмешательство Пожилой возраст Беременность Постельный режим Генетическая предрасположенность
- 5. ЦЕЛЬ РАБОТЫ: 1.Исследовать основные генетические факторы развития тромбоза 2.Освоить методы молекулярно-генетической диагностики наследственной предрасположенности.
- 6. НАИБОЛЕЕ РАСПРОСТРАНЕННЫЕ ГЕННЫЕ МАРКЕРЫ НАСЛЕДСТВЕННЫХ ТРОМБОФИЛИЙ Метилентетрагидрофолатредуктаза (MTHFR) является ключевым звеном фолатного цикла и катализирует реакцию
- 7. НАИБОЛЕЕ РАСПРОСТРАНЕННЫЕ ГЕННЫЕ МАРКЕРЫ НАСЛЕДСТВЕННЫХ ТРОМБОФИЛИЙ Фактор Лейдена (FV) происходит замена аргинина на глутамин в позиции
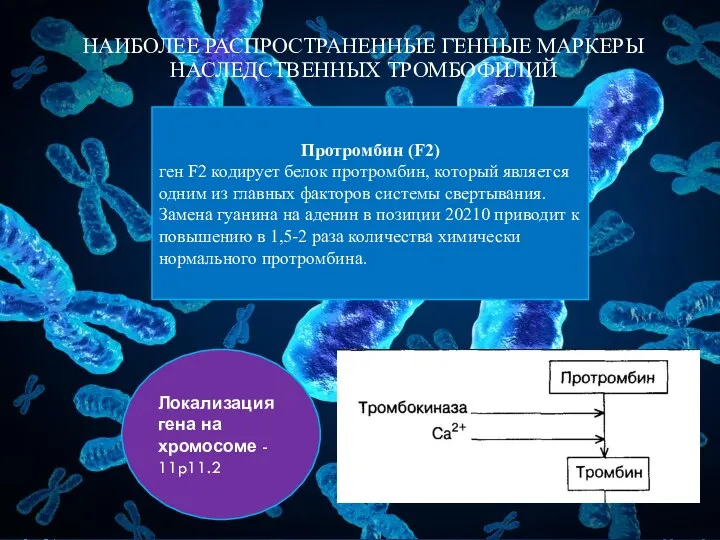
- 8. НАИБОЛЕЕ РАСПРОСТРАНЕННЫЕ ГЕННЫЕ МАРКЕРЫ НАСЛЕДСТВЕННЫХ ТРОМБОФИЛИЙ Протромбин (F2) ген F2 кодирует белок протромбин, который является одним
- 9. ВЫДЕЛЕНИЕ ДНК 1. В 2 эппендорфа налить по 300 мкл лизирующего раствора, 20 мкл. сорбента, 100
- 10. ПОЛИМЕРАЗНАЯ ЦЕПНАЯ РЕАКЦИЯ Полимеразная цепная реакция (ПЦР) — экспериментальный метод молекулярной биологии, позволяющий добиться значительного увеличения
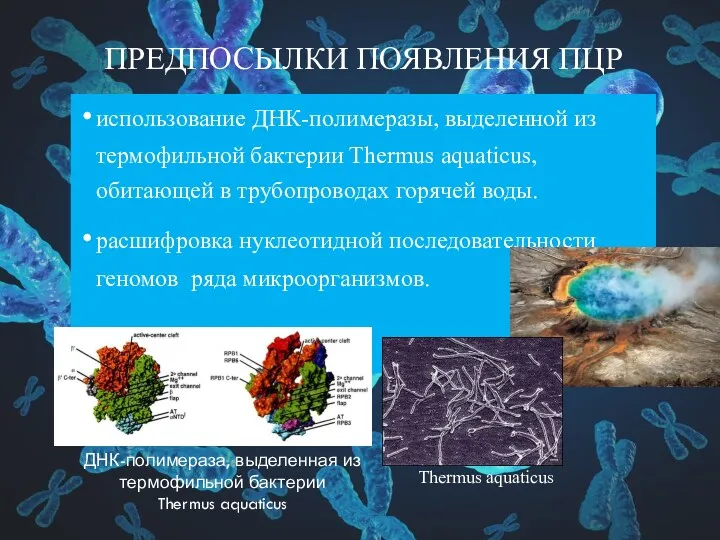
- 11. ПРЕДПОСЫЛКИ ПОЯВЛЕНИЯ ПЦР использование ДНК-полимеразы, выделенной из термофильной бактерии Thermus aquaticus, обитающей в трубопроводах горячей воды.
- 12. ПРОВЕДЕНИЕ ПЦР Подготовить реагенты. В пустой эппендорф налить 17, 5 мкл разбавителя; Добавить 2,5 мкл. реакционной
- 13. ЭЛЕКТРОФОРЕЗ Электрофорез фрагментов ДНК — разделение фрагментов по молекулярной массе и электрическому заряду в агарозном геле.
- 14. ПРОВЕДЕНИЕ ЭЛЕКТРОФОРЕЗА Варим 3% агарозу . Ставим в колбе в микроволновую печь для размешивания и разогревания;
- 15. РЕЗУЛЬТАТЫ Ген F2 Ген FV Ген MTHFR
- 16. ЗАКЛЮЧЕНИЕ 1. Освоили некоторые методы молекулярно-генетической диагностики наследственной предрасположенности 2. Научились описывать полученные результаты.
- 18. Скачать презентацию












 Лейкокория у детей
Лейкокория у детей Методика исследования периферических и внутригрудных лимфатических узлов
Методика исследования периферических и внутригрудных лимфатических узлов Инфекционные болезни - чума
Инфекционные болезни - чума Наложение шин на руку
Наложение шин на руку Сердечно-легочная реанимация
Сердечно-легочная реанимация Жүктілікпен байланысты гипертензиясы Ерте токсикоздар
Жүктілікпен байланысты гипертензиясы Ерте токсикоздар Воздействие на поведение водителя психотропных, наркотических веществ, алкоголя и медицинских препаратов
Воздействие на поведение водителя психотропных, наркотических веществ, алкоголя и медицинских препаратов Косметические средства ухода за кожей детей при аномалиях конституции
Косметические средства ухода за кожей детей при аномалиях конституции Diet and teen health
Diet and teen health Зрительный нерв. Заболевания зрительного нерва
Зрительный нерв. Заболевания зрительного нерва Реанимационная помощь
Реанимационная помощь Дәрілік заттардың әсерінің ағза қасиеттеріне тәуелділігі. Фармакологиялық әсердің дәрілік заттардың қасиеттері мен қолдану
Дәрілік заттардың әсерінің ағза қасиеттеріне тәуелділігі. Фармакологиялық әсердің дәрілік заттардың қасиеттері мен қолдану Antimicrobial drugs
Antimicrobial drugs Снотворные и противосудорожные средства. Противопаркинсонические средства
Снотворные и противосудорожные средства. Противопаркинсонические средства Предмет и задачи медицинской микробиологии. История микробиологии. Медицинская микробиология XXI века
Предмет и задачи медицинской микробиологии. История микробиологии. Медицинская микробиология XXI века Ошибки диагностики и лечения при сочетанной травме
Ошибки диагностики и лечения при сочетанной травме Профилактика стоматологических заболеваний в раннем детском возрасте
Профилактика стоматологических заболеваний в раннем детском возрасте Вскармливание детей грудного возраста. Раздел 1.Лекция 6
Вскармливание детей грудного возраста. Раздел 1.Лекция 6 Современные направления пластической хирургии в акушерстве и гинекологии
Современные направления пластической хирургии в акушерстве и гинекологии Местные анестетики
Местные анестетики Всероссийский день трезвости
Всероссийский день трезвости ВКР: Анализ работы медсестры процедурного кабинета хирургического отделения стационара
ВКР: Анализ работы медсестры процедурного кабинета хирургического отделения стационара Врожденные аномалии грудной клетки
Врожденные аномалии грудной клетки Вреден ли фаст-фуд для нашего здоровья
Вреден ли фаст-фуд для нашего здоровья Здоровый образ жизни и профилактика основных неинфекционных заболеваний
Здоровый образ жизни и профилактика основных неинфекционных заболеваний Қазіргі заманғы денсаулық сақтау, әлемдік тенденция, дамыған елдер
Қазіргі заманғы денсаулық сақтау, әлемдік тенденция, дамыған елдер Иммуногенез бұзылуының морфологиясы. Тимустың, шеткері лимфалық тіндердің иммунгенез бұзылғандағы өзгерістері
Иммуногенез бұзылуының морфологиясы. Тимустың, шеткері лимфалық тіндердің иммунгенез бұзылғандағы өзгерістері Жүкті студенттердің медико-әлеуметтік аспектілері
Жүкті студенттердің медико-әлеуметтік аспектілері