Содержание
- 2. Дисклеймер Информация предоставлена в качестве информационной и образовательной поддержки врачей. Мнения, высказанные на слайдах и в
- 3. Декларация заинтересованности Чтение лекций Astellas, bioMerieux, MSD, Pfizer Экспертные консультации Angelini, Astellas, MSD, Pfizer, Р-Фарм, Алкеми
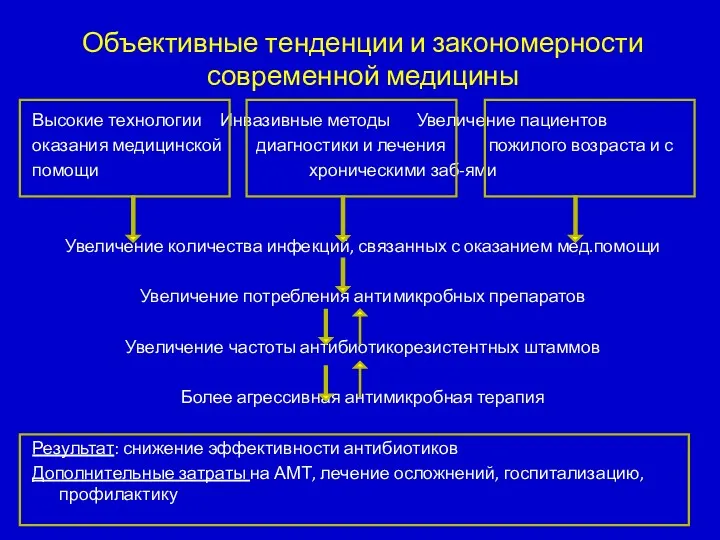
- 4. Объективные тенденции и закономерности современной медицины Высокие технологии Инвазивные методы Увеличение пациентов оказания медицинской диагностики и
- 5. Инфекции, вызванные условно-патогенными микроорганизмами Внебольничные Связанные с оказанием медицинской помощи (Community-acquired) (Healthcare-associated) - нозокомиальные инфекции -
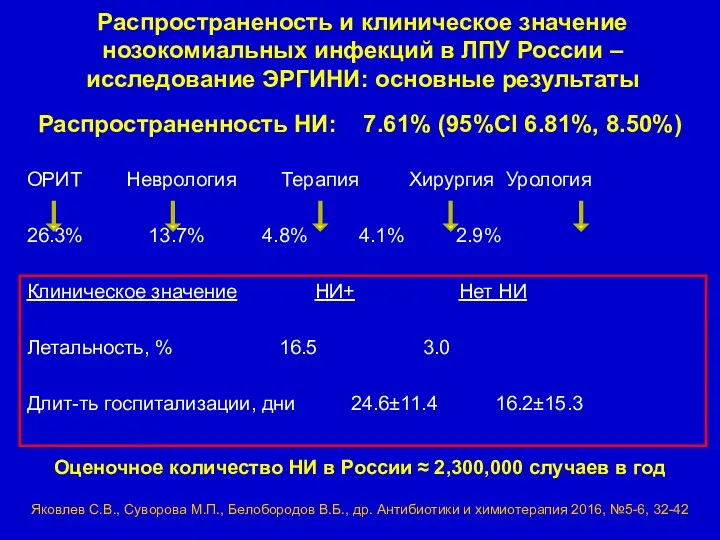
- 6. Распространеность и клиническое значение нозокомиальных инфекций в ЛПУ России – исследование ЭРГИНИ: основные результаты Распространенность НИ:
- 7. Локализация и этиология НИ в ЛПУ РФ: исследование ЭРГИНИ Локализация Возбудители Нижние ДП 42.4% Klebsiella spp.
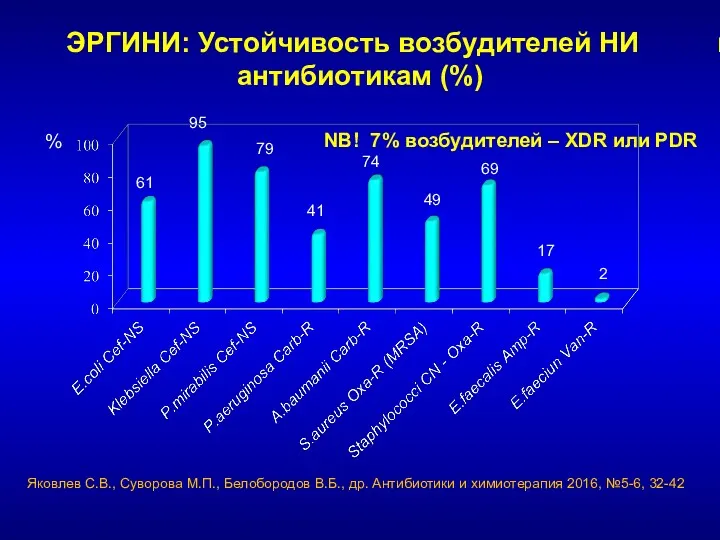
- 8. ЭРГИНИ: Устойчивость возбудителей НИ к антибиотикам (%) 61 95 79 41 74 % NB! 7% возбудителей
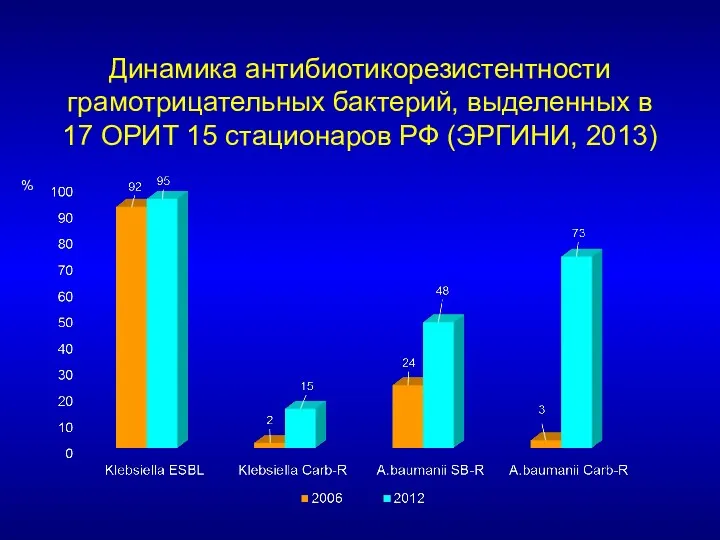
- 9. Динамика антибиотикорезистентности грамотрицательных бактерий, выделенных в 17 ОРИТ 15 стационаров РФ (ЭРГИНИ, 2013) %
- 10. Оценка угроз антибиотикорезистентности CDC и приоритеты ВОЗ в разработки новых АМП Неотложные угрозы Enterobacteriaceae – Carb-R
- 11. К этим терминам придется привыкать Полирезистентность (MDR) Высокая резистентность (XDR) Панрезистентность (PDR)
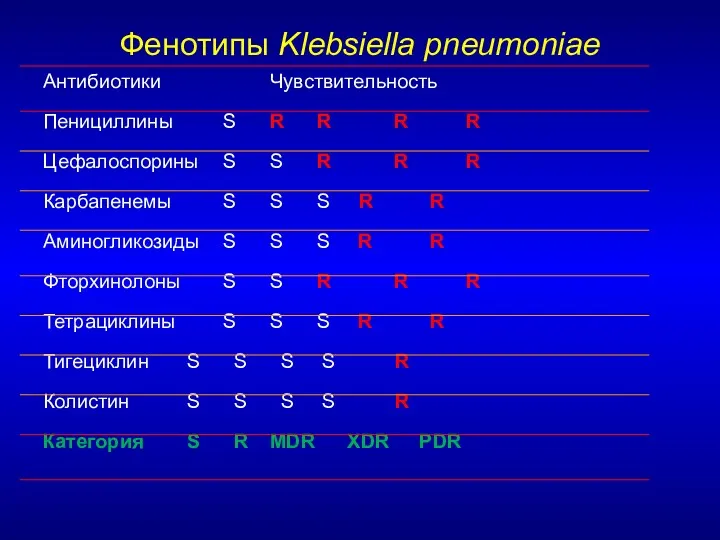
- 12. Фенотипы Klebsiella pneumoniae Антибиотики Чувствительность Пенициллины S R R R R Цефалоспорины S S R R
- 13. Программы «Antibiotic Stewardship» Стратегическая цель Оптимизация применения АМП в стационарах Сдерживание антибиотикорезистентности «Организованная интервенция, направленная на
- 14. Программа СКАТ – инструмент внедрения рациональной АМТ и сдерживания антибиотикорезистентности в ЛПУ Стратегия Контроля Антимикробной Терапии
- 15. www.antimicrob.net www.nasci.ru
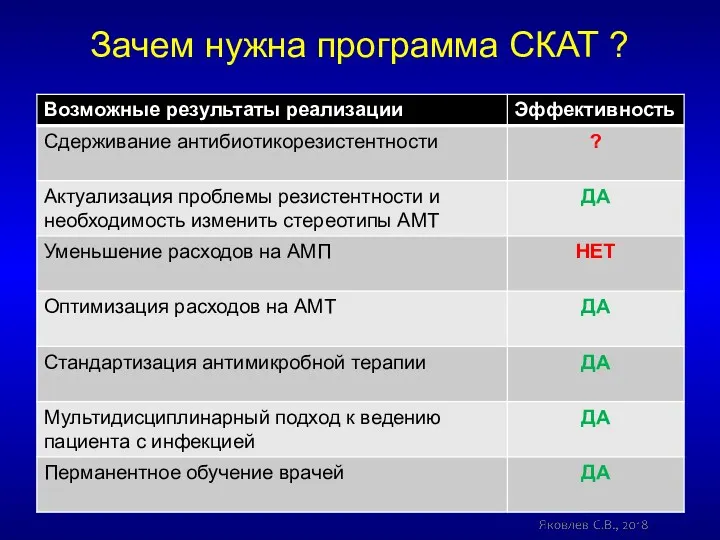
- 16. Зачем нужна программа СКАТ ?
- 17. Что нового в рекомендациях 2018 года? Данные о распространенности и клиническом значении нозокомиальных инфекций в стационарах
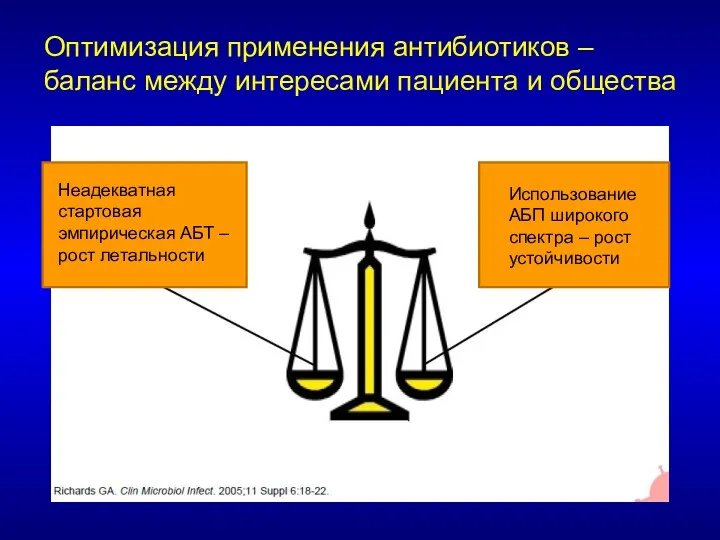
- 18. Неадекватная стартовая эмпирическая АБТ – рост летальности Использование АБП широкого спектра – рост устойчивости Оптимизация применения
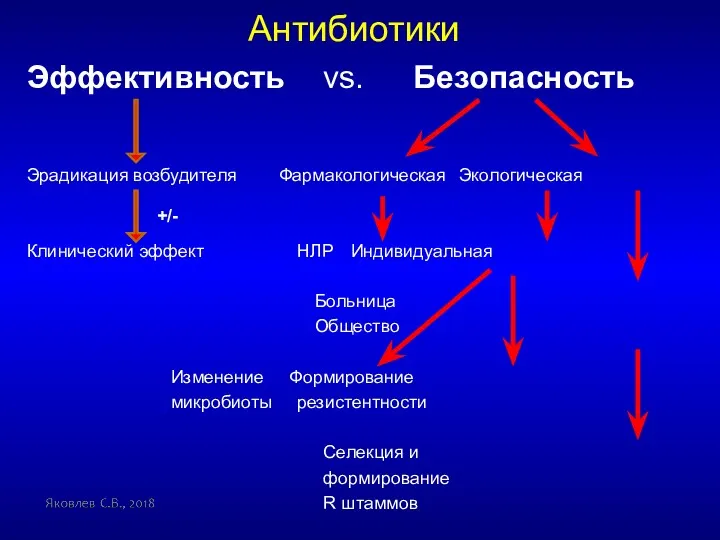
- 19. Антибиотики Эффективность vs. Безопасность Эрадикация возбудителя Фармакологическая Экологическая Клинический эффект НЛР Индивидуальная Больница Общество Изменение Формирование
- 20. Рационализация применения антибиотиков Ограничение использования антибиотиков, провоцирующих селекцию антибиотикорезистентных штаммов Антибиотико-ассоциированная резистентность – сопутствующий ущерб (Collateral
- 21. Факторы риска P.aeruginosa и выбор АБТ Длительное нахождение в ОРИТ (> 5 суток), ИВЛ Иммуносупрессия (цитостатики,
- 22. Использование эртапенема позволяет уменьшить устойчивость P. aeruginosa к АП карбапенемам и другим АБП Снижение частоты выделения
- 23. Условия достижения адекватной антимикробной терапии сепсиса Принятие решения о назначении антибиотика Диагностика инфекции – оценка SIRS,
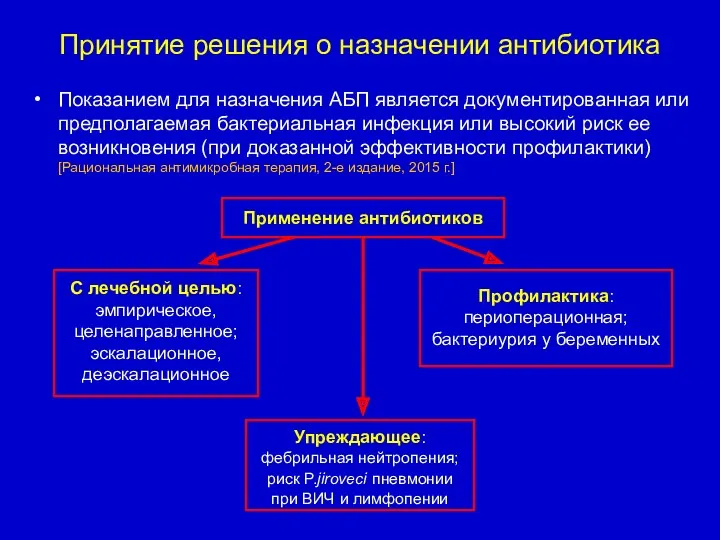
- 24. Принятие решения о назначении антибиотика Показанием для назначения АБП является документированная или предполагаемая бактериальная инфекция или
- 25. Принятие решения о назначении антибиотика Показанием для назначения АБП является документированная или предполагаемая бактериальная инфекция или
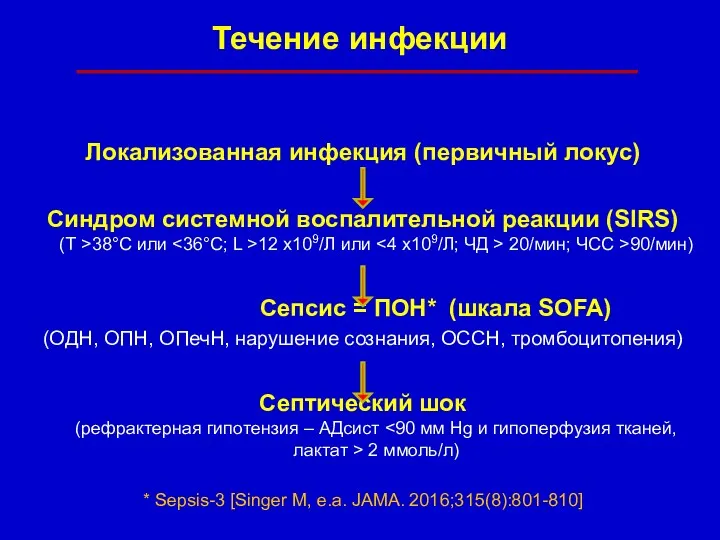
- 26. Течение инфекции Локализованная инфекция (первичный локус) Синдром системной воспалительной реакции (SIRS) (Т >38°C или 12 х109/Л
- 27. Естественное течение инфекции Локализованная инфекция (первичный локус) Синдром системной воспалительной реакции (SIRS) (Т >38°C или 12
- 28. Естественное течение инфекции Локализованная инфекция (первичный локус) Синдром системной воспалительной реакции (SIRS) (Т >38°C или 12
- 29. В какие сроки Вы хотели бы получить результат микробиологического исследования (микроб и чувствительность)? 5 дней 3
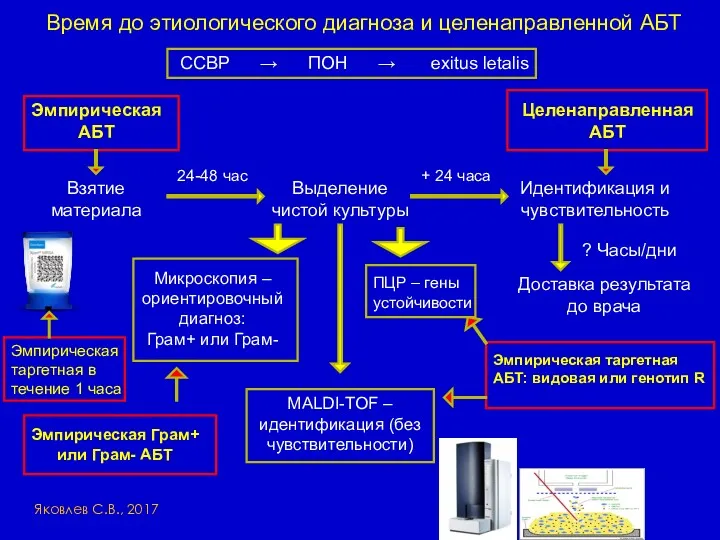
- 30. Время до этиологического диагноза и целенаправленной АБТ Взятие материала Выделение чистой культуры Идентификация и чувствительность 24-48
- 31. Оптимизация микробиологической диагностики Классическая микробиология Более точная идентификация и чувствительность Анализатор гемокультур – время Автоматические анализаторы
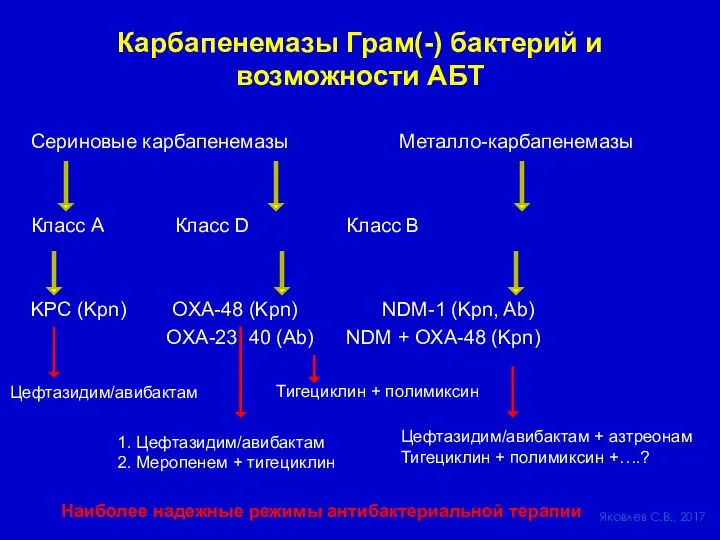
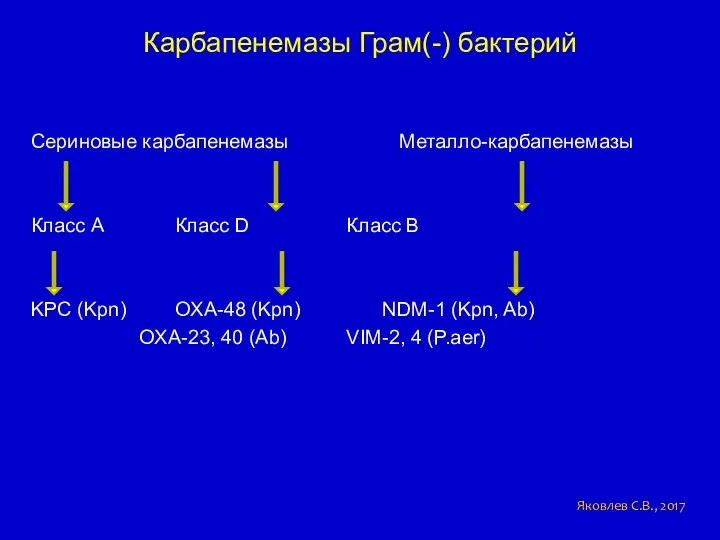
- 32. Карбапенемазы Грам(-) бактерий и возможности АБТ Сериновые карбапенемазы Металло-карбапенемазы Класс А Класс D Класс В KPC
- 33. Условия достижения адекватной антимикробной терапии сепсиса Принятие решения о назначении антибиотика Диагностика инфекции – оценка SIRS,
- 34. Основное правило антимикробной терапии сепсиса / септического шока Адекватная терапия должна быть начата в течение первого
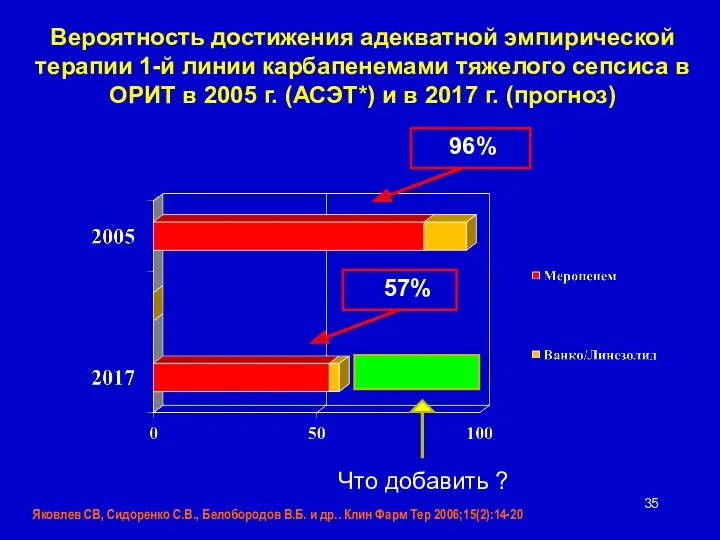
- 35. Вероятность достижения адекватной эмпирической терапии 1-й линии карбапенемами тяжелого сепсиса в ОРИТ в 2005 г. (АСЭТ*)
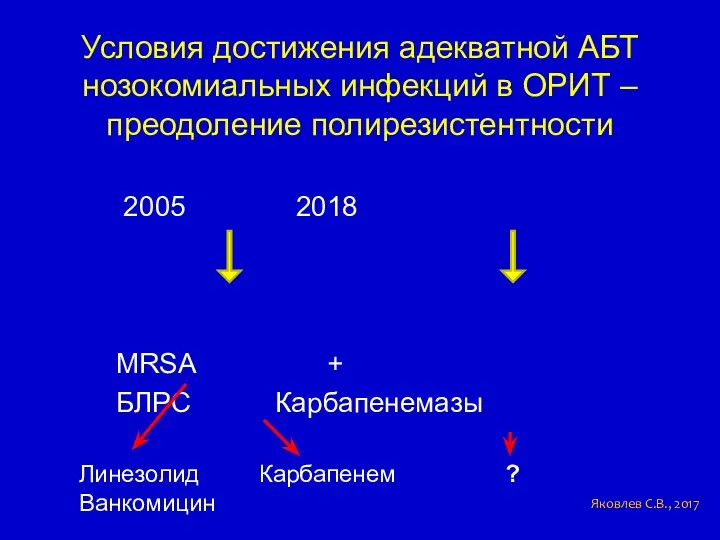
- 36. Условия достижения адекватной АБТ нозокомиальных инфекций в ОРИТ – преодоление полирезистентности 2005 2018 MRSA + БЛРС
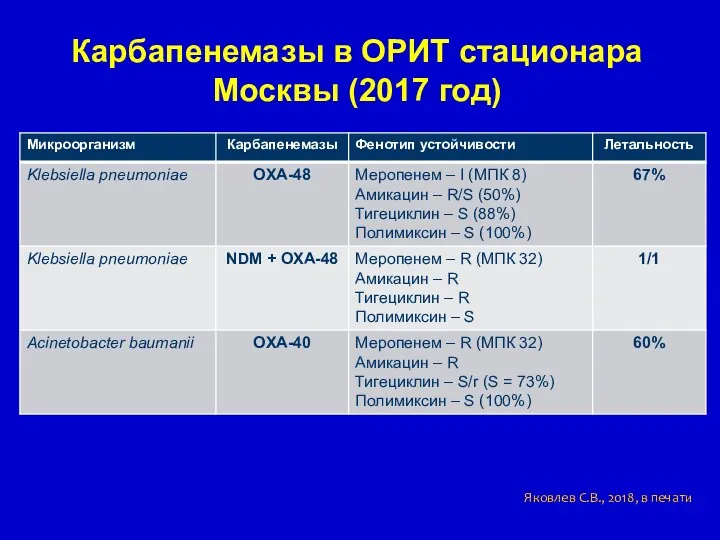
- 37. Карбапенемазы в ОРИТ стационара Москвы (2017 год) Яковлев С.В., 2018, в печати
- 38. Стратификация госпитализированных пациентов по риску антибиотикорезистентности и инвазивного кандидоза – повышение вероятности адекватной эмпирической АМТ Типы
- 39. При внебольничных инфекциях (БЛРС) Применение антибиотиков в предшествующие 3 месяца Госпитализация в течение 2 и более
- 40. Тип I и II - Внебольничные инфекции Тип I: Внебольничные инфекции без риска полирезистентных возбудителей (БЛРС)
- 41. Тип III - Нозокомиальные инфекции IIIa: НИ ранние, вне ОРИТ, без предшествующих АБП – риск БЛРС
- 42. Факторы риска инвазивного кандидоза – показание для эмпирического назначения антифунгальных средств (1 + 2 +/- 3)
- 43. Условия достижения адекватной антимикробной терапии сепсиса Принятие решения о назначении антибиотика Диагностика инфекции – оценка SIRS,
- 44. Правила целенаправленной АБТ Оценка клинической значимости выделенного микроорганизма Знание основных механизмов антибиотикорезистентности Выбор оптимального антибиотика из
- 45. Сложности оценки клинической значимости условно-патогенных бактерий с низкой вирулентностью Кровь: CNS, Corynebacterium spp. Аспират трахеи/БАЛ: Candida
- 46. Оценивать микроорганизм и пациента! БАЛ: Candida albicans 108 КОЕ/мл в монокультуре; сохранение ССВР на фоне антибиотиков
- 47. Сложности лечения стафилококковых инфекций Клиническая эффективность антистафилококковых антибиотиков не всегда коррелирует с данными чувствительности in vitro
- 48. Тактика ведения больных с первичной или вторичной S.aureus бактериемией Положительная гемокультура S.aureus (однократно!) Немедленная Повторные Обследование
- 49. Предикторы осложненной стафилококковой бактериемии (формирование вторичных очагов) Факторы риска Относительный риск Внебольничная бактериемия 3.08 Кожная сыпь
- 50. Предикторы осложненной стафилококковой бактериемии (формирование вторичных очагов) Факторы риска Относительный риск Внебольничная бактериемия 3.08 Кожная сыпь
- 51. Пациент с ангиогенным сепсисом. Из крови в двух флаконах отмечен рост Staphylococcus aureus со следующим фенотипом
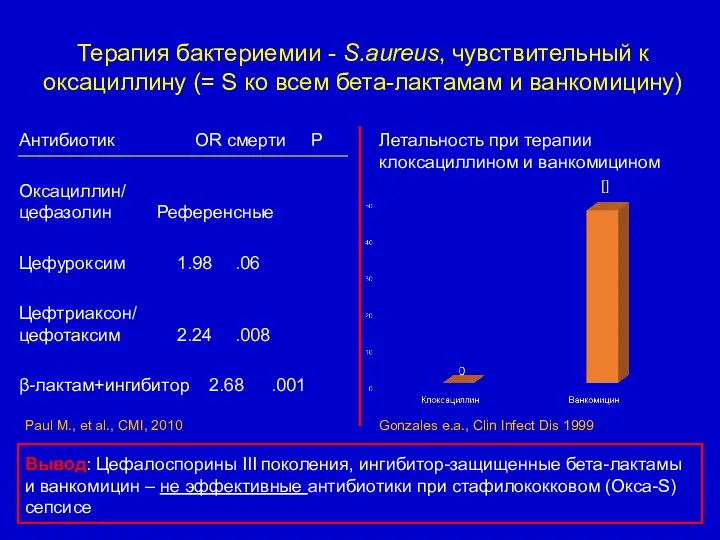
- 52. Терапия бактериемии - S.aureus, чувствительный к оксациллину (= S ко всем бета-лактамам и ванкомицину) Антибиотик OR
- 53. Стафилококковые инфекции (длительность АБТ при бактериемии 14-28 дней) Staphylococcus aureus Чувств. к оксациллину Устойч. к оксациллину
- 54. MRSA M Methicillin R Resistant S Staphylococcus A Aureus Устойчивость к метициллину = устойчивость к оксациллину
- 55. Анти-MRSA антибиотики Ванкомицин Телаванцин Далбаванцин Линезолид Тедизолид Даптомицин Цефтаролин Тигециклин Гликопептиды Оксазолидиноны Липопептид Цефалоспорин Эффективность других
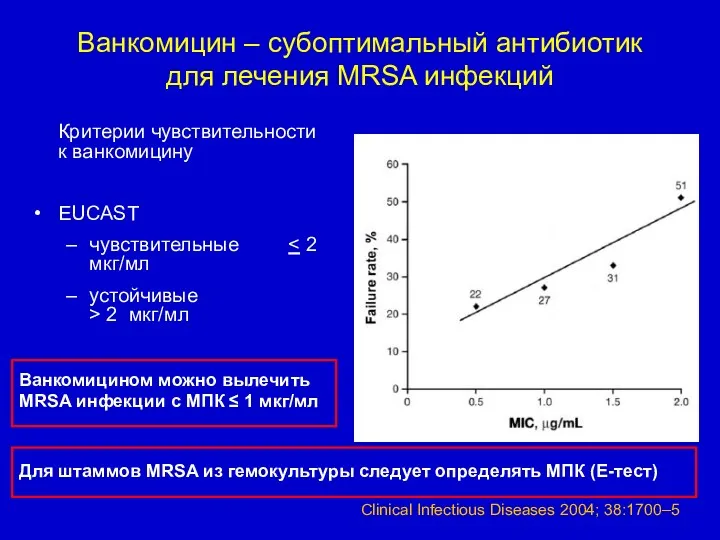
- 56. Ванкомицин – субоптимальный антибиотик для лечения MRSA инфекций Критерии чувствительности к ванкомицину EUCAST чувствительные устойчивые >
- 57. Лечение MRSA сепсиса – альтернатива ванкомицину при МПК > 1 мкг/мл Локализация инфекции – первичный очаг
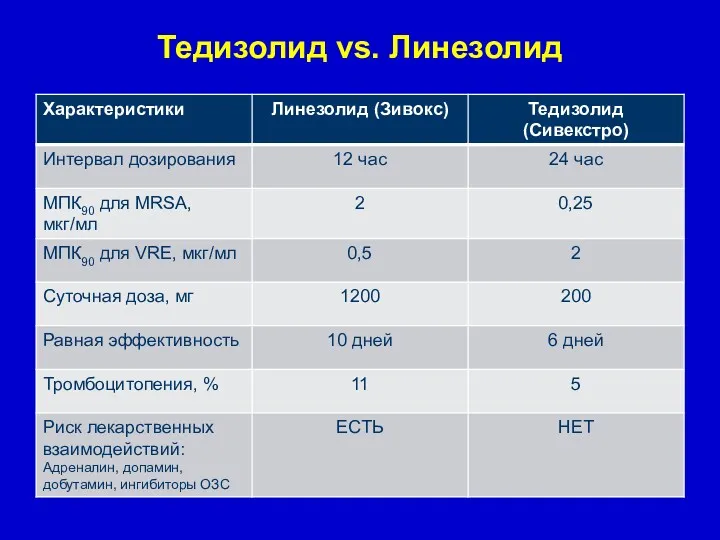
- 58. Тедизолид vs. Линезолид
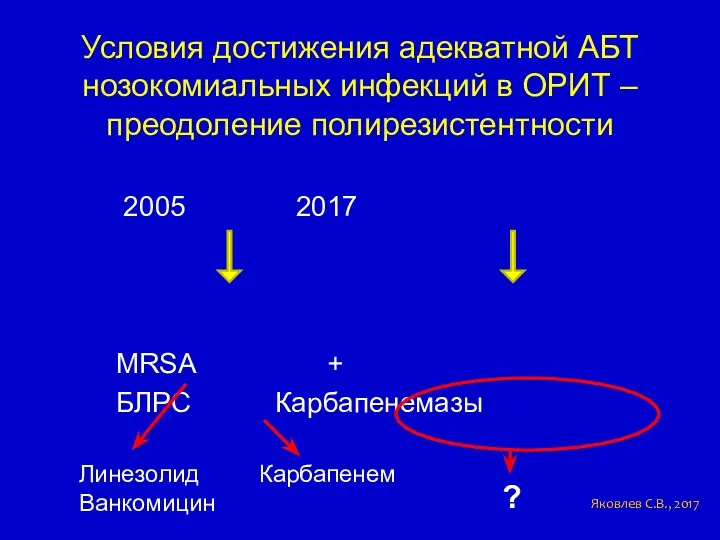
- 59. Условия достижения адекватной АБТ нозокомиальных инфекций в ОРИТ – преодоление полирезистентности 2005 2017 MRSA + БЛРС
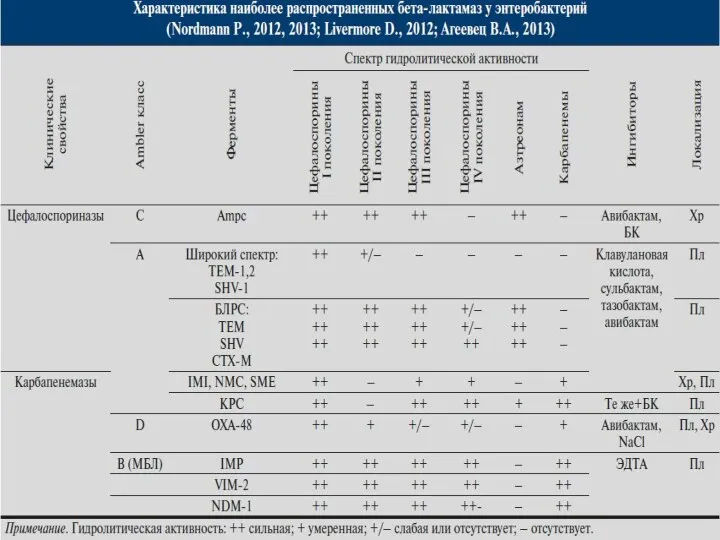
- 60. Проблемы устойчивости Enterobacteralis Наиболее важные бета-лактамазы Klebsiella pn. & E.coli ESBL группа А AmpC группа С
- 61. Карбапенемазы Грам(-) бактерий Сериновые карбапенемазы Металло-карбапенемазы Класс А Класс D Класс В KPC (Kpn) OXA-48 (Kpn)
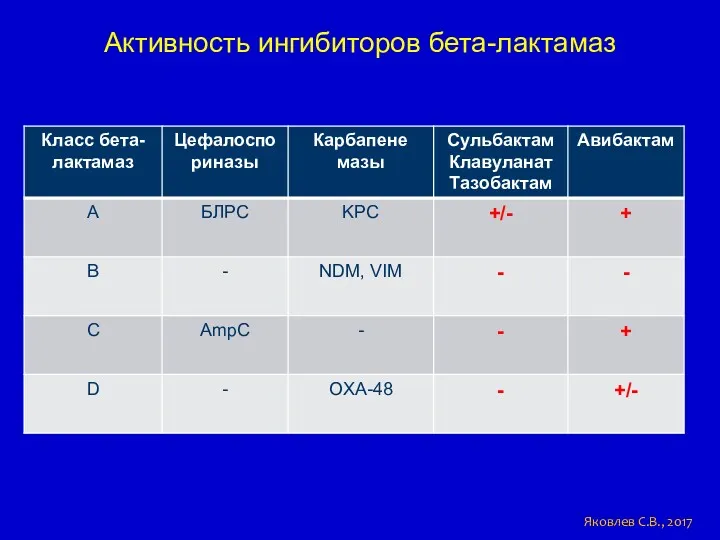
- 63. Активность ингибиторов бета-лактамаз Яковлев С.В., 2017
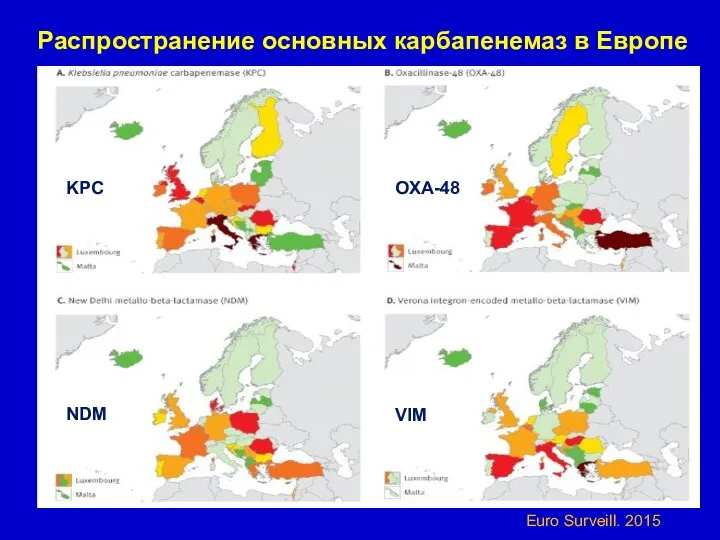
- 64. Распространение основных карбапенемаз в Европе Euro Surveill. 2015 KPC OXA-48 NDM VIM
- 65. CRE и летальность Нозокомиальная пневмония с бактериемией, вызванная Kpn NDM-1+ Общая летальность 72% Атрибутивная летальность 50%
- 66. CRE и летальность Нозокомиальная пневмония с бактериемией, вызванная Kpn NDM-1+ Общая летальность 72% Атрибутивная летальность 50%
- 67. Как повысить вероятность адекватной терапии против Carb-R энтеробактерий? Микробиологам: При оценке чувствительности использовать правила EUCAST Фенотипическая
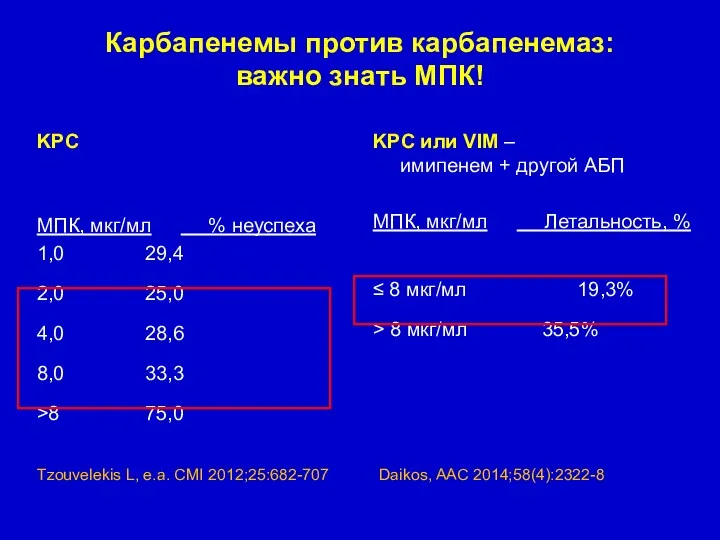
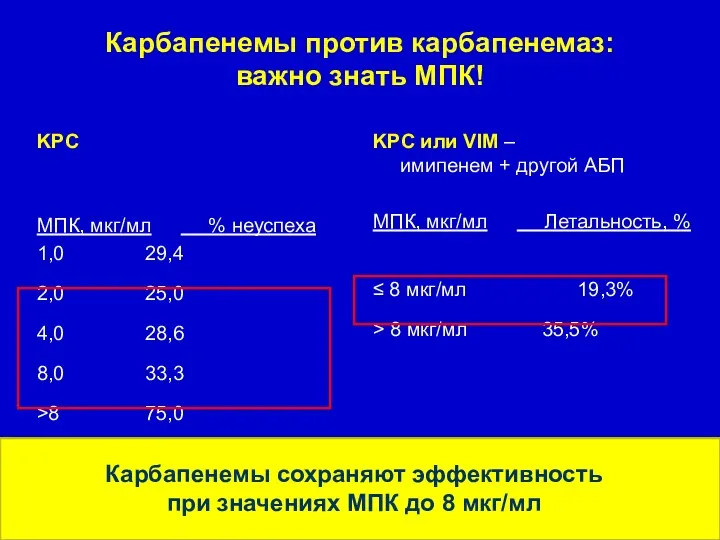
- 68. Карбапенемы против карбапенемаз: важно знать МПК! KPC МПК, мкг/мл % неуспеха 1,0 29,4 2,0 25,0 4,0
- 69. Карбапенемы против карбапенемаз: важно знать МПК! KPC МПК, мкг/мл % неуспеха 1,0 29,4 2,0 25,0 4,0
- 70. Ретроспективный анализ результатов лечения инфекций, вызванных K.pneumoniae – KPC и/или VIM [Daikos, AAC 2014;58(4):2322-8] 205 пациентов;
- 71. Рекомендация Выделение карбапенем-резистентных энтеробактерий или ацинетобактерий – показание для комбинированной АБТ !
- 72. Возможности АБТ инфекций, вызванных карбапенем-резистентными энтеробактериями Базовые антибиотики АБП для комбинаций Меропенем и дорипенем Гентамицин и
- 73. Pseudomonas aeruginosa – перспективы АБТ Цефтолозан/тазобактам (Зербакса) Зарегистрирован в РФ ноябрь 2018 Преодолевает большинство механизмов устойчивости
- 74. Условия достижения адекватной антимикробной терапии сепсиса Принятие решения о назначении антибиотика Диагностика инфекции – оценка SIRS,
- 75. Дозирование антибиотиков: особые категории пациентов Дети Почечная недостаточность Печеночная недостаточность Ожирение или дефицит массы тела Лечение
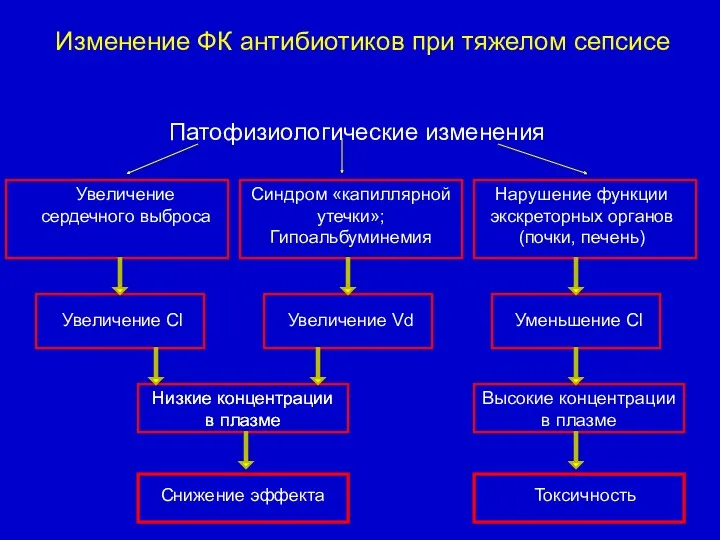
- 76. Изменение ФК антибиотиков при тяжелом сепсисе Патофизиологические изменения Увеличение сердечного выброса Синдром «капиллярной утечки»; Гипоальбуминемия Нарушение
- 77. The DALI Study Вывод: стандартное дозирование антибиотика (ИМП) в ОРИТ не позволяет достичь целевого параметра фармакодинамики
- 78. Тяжелый сепсис: эндотелиальная дисфункция – синдром капиллярной утечки Дозу каких антибиотиков следует увеличить? Пенициллины Цефалоспорины Карбапенемы
- 79. Знание фармакодинамики – оптимизация применения антибиотиков Бета-лактамы – время зависимые антибиотики Предиктор эффекта: [T > МПК]
- 80. Оптимизация дозирования антибиотиков у тяжелых пациентов Назначать максимально рекомендуемую дозу АБП Увеличение дозы при клиренсе креатинина
- 81. Факторы, способствующие росту антибиотикорезистентности в ЛПУ Избыточное использование антибиотиков в стационаре Превалирование необоснованной профилактики Продленные курсы
- 82. Факторы, способствующие росту антибиотикорезистентности в ЛПУ Избыточное использование антибиотиков Превалирование необоснованной профилактики Нерациональное применение антибиотиков Превалирование
- 84. Скачать презентацию























































 Металлы и сплавы, применяемые в ортопедической стоматологии, общие сведения, классификация сплавов
Металлы и сплавы, применяемые в ортопедической стоматологии, общие сведения, классификация сплавов Переломы и вывихи
Переломы и вывихи Неотложные состояния в гинекологии. Маточные кровотечения
Неотложные состояния в гинекологии. Маточные кровотечения Мелкоклеточный рак лёгких
Мелкоклеточный рак лёгких Философия сестринского дела
Философия сестринского дела Клинические формы первичного и вторичного туберкулеза
Клинические формы первичного и вторичного туберкулеза Гонококова та хламідійна інфекція
Гонококова та хламідійна інфекція Верхушечный периодонтит
Верхушечный периодонтит Санитария және гигиена бұйымдарының жіктелуі және сипаттамасы. Медициналық техника. Стандарттау
Санитария және гигиена бұйымдарының жіктелуі және сипаттамасы. Медициналық техника. Стандарттау Тахикардия по механизму re-entry
Тахикардия по механизму re-entry Жұқпалы үрдіс патофизиологиясы. Сепсис және сепсистік сілейменің патогенезі
Жұқпалы үрдіс патофизиологиясы. Сепсис және сепсистік сілейменің патогенезі Іріңді тендовагинит
Іріңді тендовагинит Природне вигодовування дітей раннього віку
Природне вигодовування дітей раннього віку Физические упражнения для детей грудного возраста
Физические упражнения для детей грудного возраста Принципы оказания паллиативной помощи
Принципы оказания паллиативной помощи Подпороговое восприятие и его использование
Подпороговое восприятие и его использование Развитие фармацевтической деонтологии
Развитие фармацевтической деонтологии Шовный материал. История возникновения.Современные виды шовного материала
Шовный материал. История возникновения.Современные виды шовного материала Бронхоэктатикалық ауру, диагностикасы және емдеу әдістері
Бронхоэктатикалық ауру, диагностикасы және емдеу әдістері Спадковість і патологія. Лекція 4
Спадковість і патологія. Лекція 4 Лекция 16. Антигипертензивные средства
Лекция 16. Антигипертензивные средства Эндокринное бесплодие у женщин
Эндокринное бесплодие у женщин Особенности ухода за пожилыми, в том числе и на дому. Уход за тяжелобольными и умирающими. Сестринский уход
Особенности ухода за пожилыми, в том числе и на дому. Уход за тяжелобольными и умирающими. Сестринский уход Ликбез на тему ВИЧ/СПИД
Ликбез на тему ВИЧ/СПИД Қызылша (morbilli)
Қызылша (morbilli) Государственная программа развития здравоохранения Республики Казахстан Денсаулық
Государственная программа развития здравоохранения Республики Казахстан Денсаулық Современные способы обработки рук хирурга и операционного поля
Современные способы обработки рук хирурга и операционного поля Аралас Т- және В-иммундық тапшылықтар
Аралас Т- және В-иммундық тапшылықтар