Строение иммунной системы, механизм иммуногенеза. Использование иммунных реакций, диагностика инфекционных заболеваний. (Тема 2) презентация
Содержание
- 2. Инфекция (от лат. infectio – заражение) или инфекционный процесс - совокупность реакций восприимчивого макроорганизма на внедрение
- 3. Условия развития инфекционного процесса 1. Факторы патогенности (вирулентности) 2. Количество микроорганизмов Адгезия: специфическая и неспецифическая способность
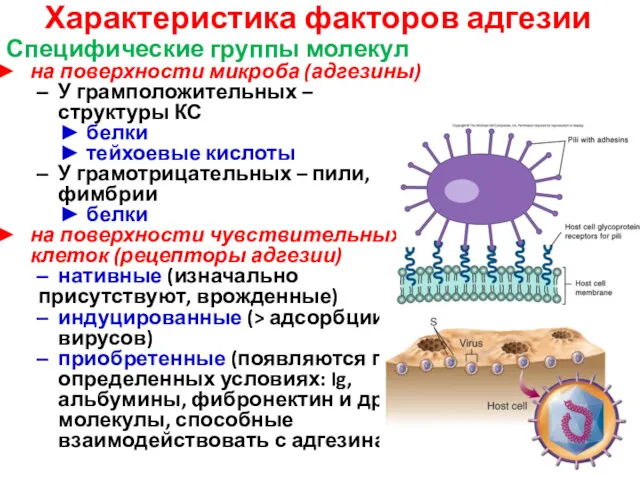
- 4. Характеристика факторов адгезии Специфические группы молекул на поверхности микроба (адгезины) У грамположительных – структуры КС белки
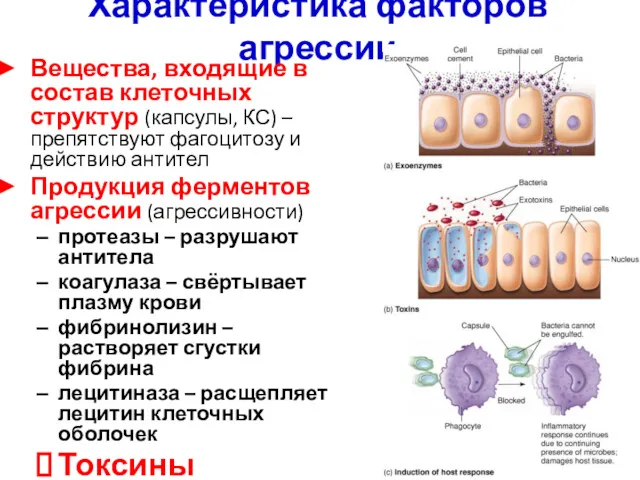
- 5. Характеристика факторов агрессии Вещества, входящие в состав клеточных структур (капсулы, КС) – препятствуют фагоцитозу и действию
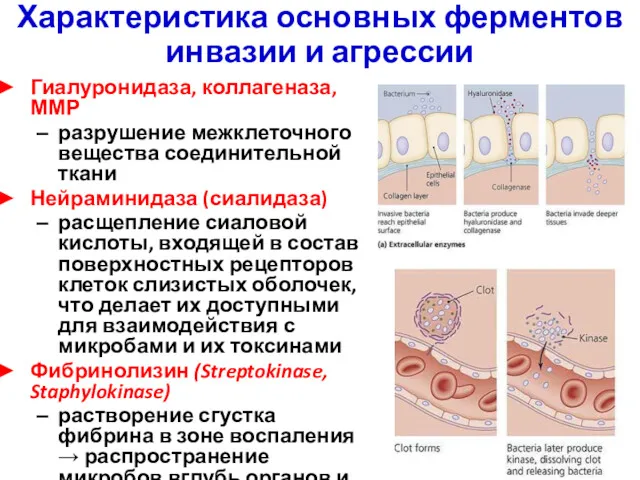
- 6. Характеристика основных ферментов инвазии и агрессии Гиалуронидаза, коллагеназа, ММР разрушение межклеточного вещества соединительной ткани Нейраминидаза (сиалидаза)
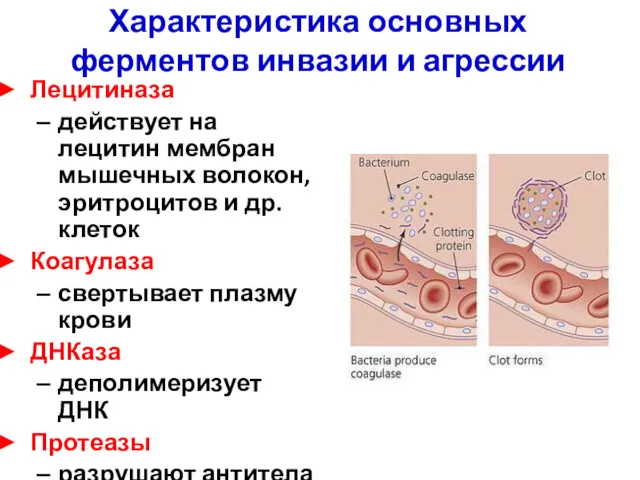
- 7. Характеристика основных ферментов инвазии и агрессии Лецитиназа действует на лецитин мембран мышечных волокон, эритроцитов и др.
- 8. 1. Эндотоксины характерны только для Грам- бактерий, экзотоксины характерны для всех бактерий вне зависимости от того
- 9. Классификация экзотоксинов по механизму действия Экзотоксины по характеру действия можно разделить на 5 групп: 1. Повреждающие
- 10. Возбудители инфекционных болезней: Прионы; Вирусы; Бактерии; Грибы Возбудители инвазионных болезней: - простейшие; - гельминты; - паразитические
- 11. Стадии инфекционного процесса: 1. Проникновение микроорганизма в макроорганизм 2. Образование ферментов, токсинов и др. продуктов 3.
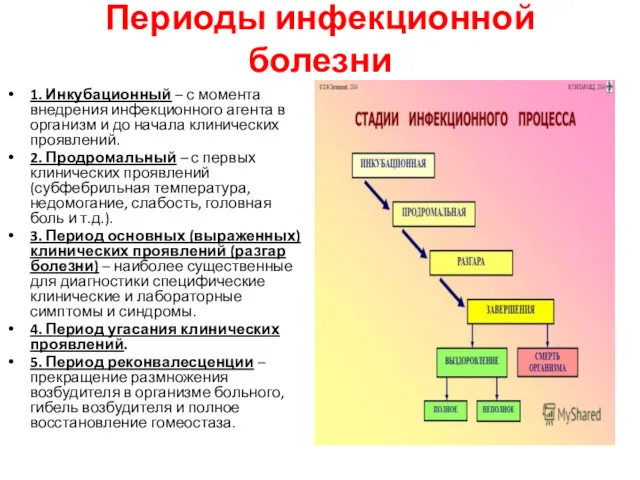
- 12. Периоды инфекционной болезни 1. Инкубационный – с момента внедрения инфекционного агента в организм и до начала
- 13. По происхождению инфекции 1. Экзогенная инфекция - возникает при попадании возбудителя в организм извне. 2. Эндогенная
- 14. По локализации патогена в организме: Местная или очаговая инфекция имеет место, когда возбудитель локализуется в определенном
- 15. Формы инфекции Классификация по локализации возбудителя в организме хозяина очаговая (местная) – микроб не распространяется по
- 16. Формы инфекции Классификация по повторным проявлениям заболевания, вызванного тем же или другим возбудителем вторичная (присоединение инфекции,
- 17. Формы инфекции Классификация по клиническим проявлениям манифестная (выраженная характерная симптоматика) стертая (характерная симптоматика слабо выражена) атипичная
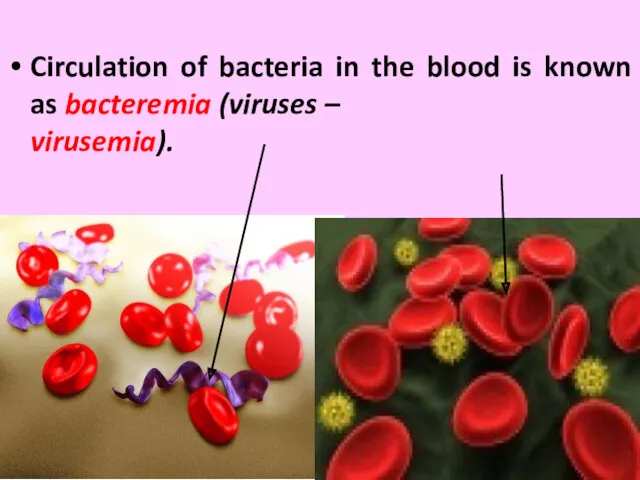
- 18. Клинические формы инфекционного процесса: Бактериемия (вирусемия) - возбудитель, распространяясь по крови, не размножается в ней. Кровь
- 19. Circulation of bacteria in the blood is known as bacteremia (viruses – virusemia).
- 20. Моноинфекция – заболевание, вызванное одним видом микроорганизмов. Микстинфекция - заболевание, вызванное двумя или более видами микроорганизмов
- 21. По длительности течения : Острые инфекции протекают непродолжительное время, их срок исчисляется днями, неделями (грипп, корь,
- 22. Формы инфекционного процесса 1. Носительство - возбудитель размножается, циркулирует в организме, происходит формирование иммунитета и очищение
- 23. Механизмы персистенции бактерий и их защита от иммунных воздействий макроорганизма: 1) факторы, „экранирующие” клеточную стенку бактерий;
- 24. Классификация заболеваемости по распространению и охвату территории *эндемия (встречается только в определенной местности). *спорадическая (отдельные случаи,
- 25. Эпидемический процесс возникает и поддерживается непрерывностью взаимодействия трех основных движущих его сил (факторов, звеньев): Источника возбудителя
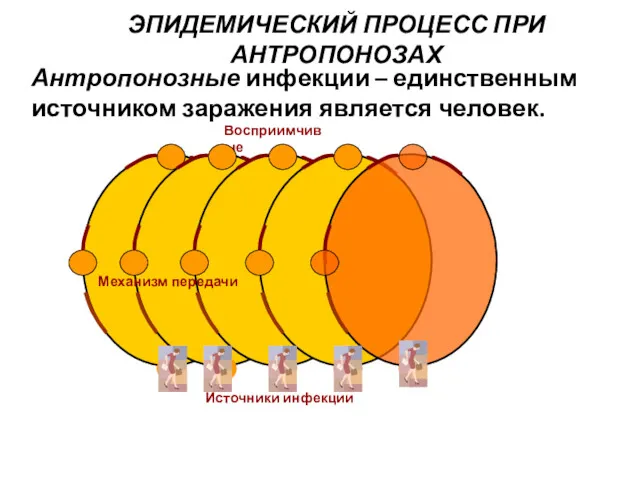
- 26. ЭПИДЕМИЧЕСКИЙ ПРОЦЕСС ПРИ АНТРОПОНОЗАХ Восприимчивые Источники инфекции Механизм передачи Антропонозные инфекции – единственным источником заражения является
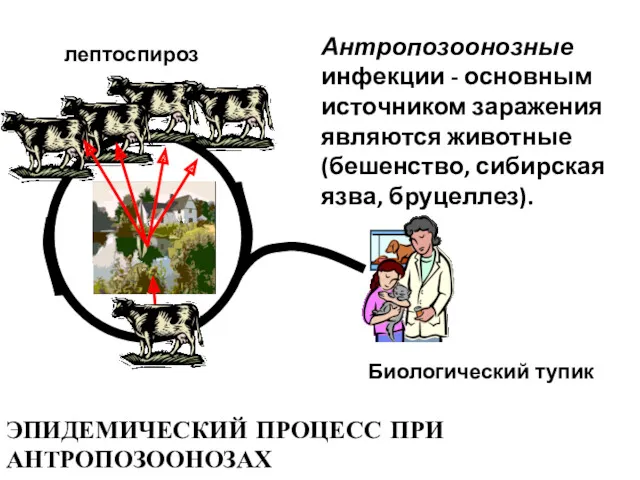
- 27. ЭПИДЕМИЧЕСКИЙ ПРОЦЕСС ПРИ АНТРОПОЗООНОЗАХ лептоспироз Биологический тупик Антропозоонозные инфекции - основным источником заражения являются животные (бешенство,
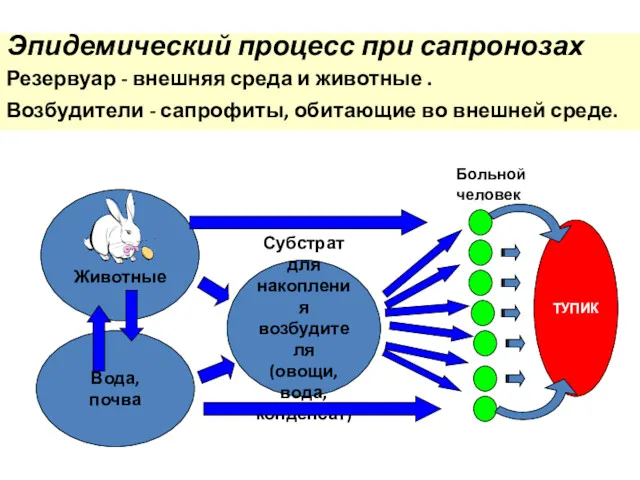
- 28. Эпидемический процесс при сапронозах Резервуар - внешняя среда и животные . Возбудители - сапрофиты, обитающие во
- 29. Классификация инфекций по механизму, путям передачи и воротам инфекции 1. Фекально-оральный механизм передачи Пути передачи: алиментарный
- 30. Классификация инфекций по механизму, путям передачи и воротам инфекции 3. Кровяной механизм передачи Пути передачи: укус
- 31. Классификация инфекций по механизму, путям передачи и воротам инфекции 5. Контактный механизм передачи Пути передачи: раневой
- 32. Иммунитет – это устойчивость организма, его способность противостоять патогенным болезнетворным микробам, токсинам, а также воздействию чужеродных
- 33. Из истории: Первое применение вакцинации Иммунология как определенное направление исследований возникла из практической необходимости борьбы с
- 34. На смену инокуляции пришел метод вакцинации (от лат. vacca - корова), разработанный в конце XVIIIв. английским
- 35. ИСТОРИЯ Рождение инфекционной иммунологии связывают с именем выдающегося французского ученого Луи Пастера (Louis Paster). Первый шаг
- 36. Хотя Пастер считается основателем инфекционной иммунологии, он ничего не знал о факторах, включенных в процесс защиты
- 37. В 1883 году он сделал первое сообщение по фагоцитарной (клеточной) теории иммунитета на съезде врачей и
- 38. Параллельно с Мечниковым разрабатывал свою теорию иммунной защиты от инфекции немецкий фармаколог Пауль Эрлих. Он знал
- 39. Прозорливость Эрлиха поражает, поскольку с некоторыми изменениями эта в целом умозрительная теория подтвердилась в настоящее время.
- 40. Именно он в значительной степени определил лицо современной иммунологии. Рассматривая иммунитет как реакцию, направленную на дифференциацию
- 41. Особого внимания заслуживают взгляды Бернета на иммунитет как на такую реакцию организма, которая отличает все "свое"
- 42. Большой вклад в становление современной иммунологии внесли также Роберт Кох (Robert Koch; 1843-1910), открывший возбудитель туберкулеза
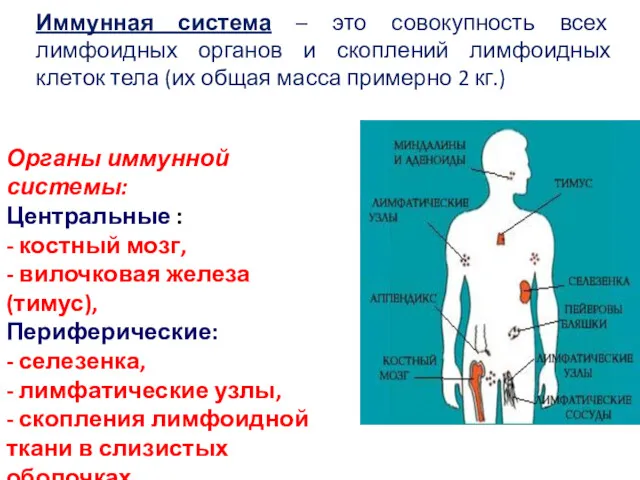
- 43. Иммунная система – это совокупность всех лимфоидных органов и скоплений лимфоидных клеток тела (их общая масса
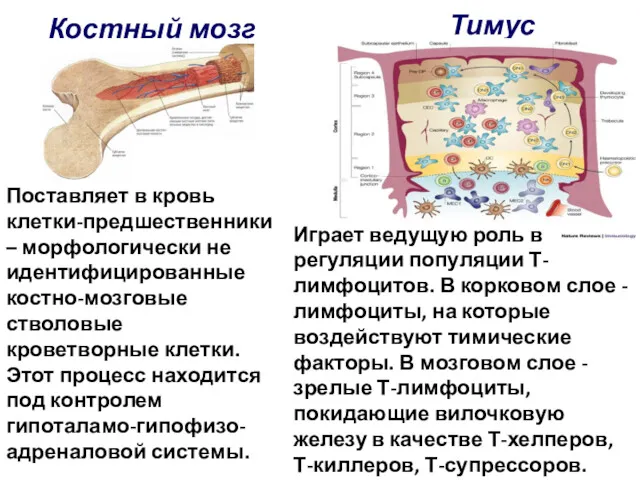
- 44. Костный мозг Поставляет в кровь клетки-предшественники – морфологически не идентифицированные костно-мозговые стволовые кроветворные клетки. Этот процесс
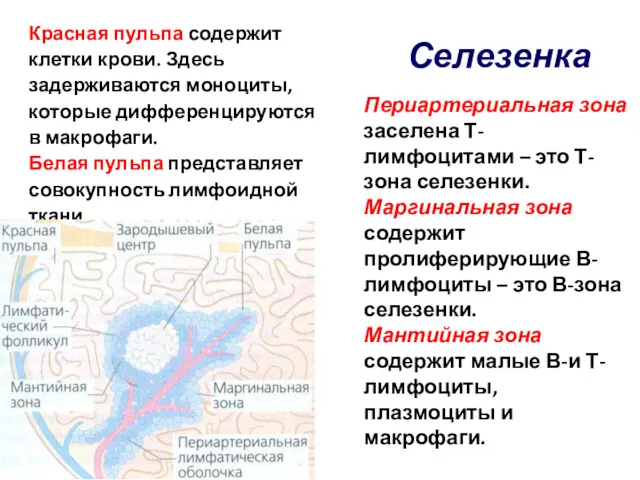
- 45. Селезенка Красная пульпа содержит клетки крови. Здесь задерживаются моноциты, которые дифференцируются в макрофаги. Белая пульпа представляет
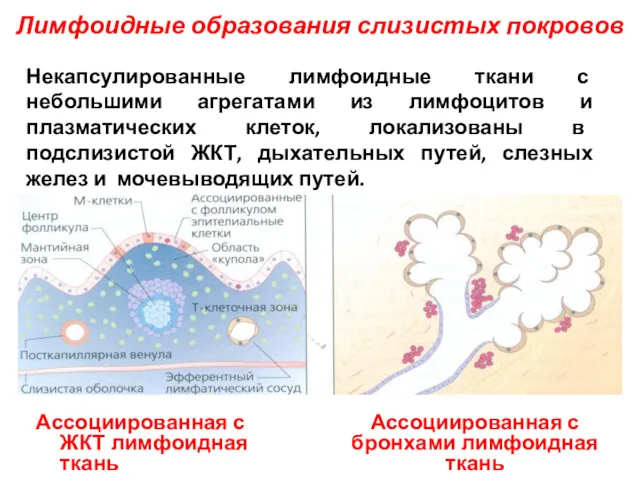
- 46. Лимфоидные образования слизистых покровов Некапсулированные лимфоидные ткани с небольшими агрегатами из лимфоцитов и плазматических клеток, локализованы
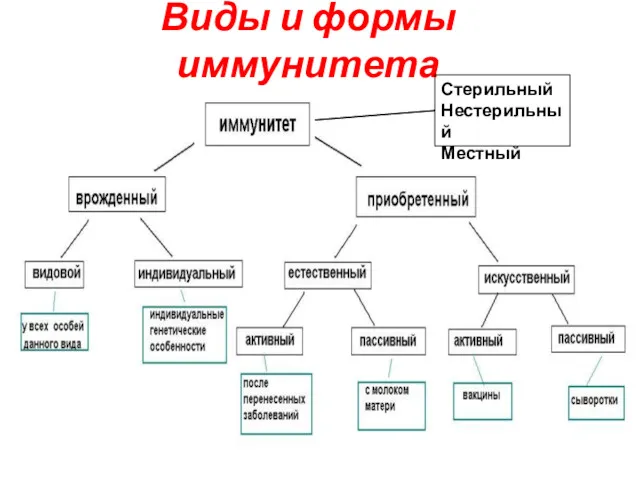
- 47. Виды и формы иммунитета Стерильный Нестерильный Местный
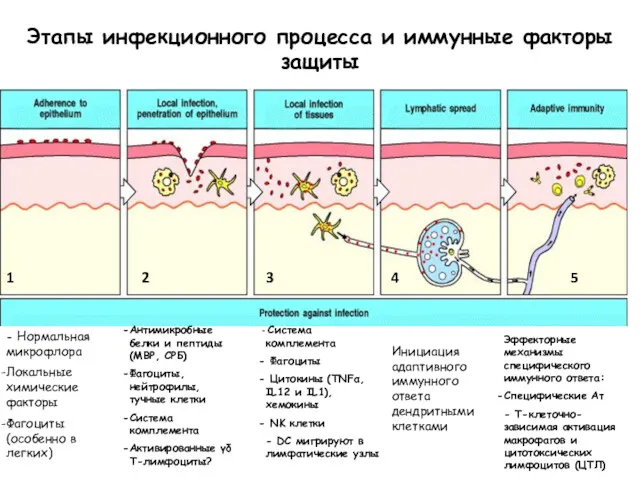
- 49. Этапы инфекционного процесса и иммунные факторы защиты - Нормальная микрофлора Локальные химические факторы Фагоциты (особенно в
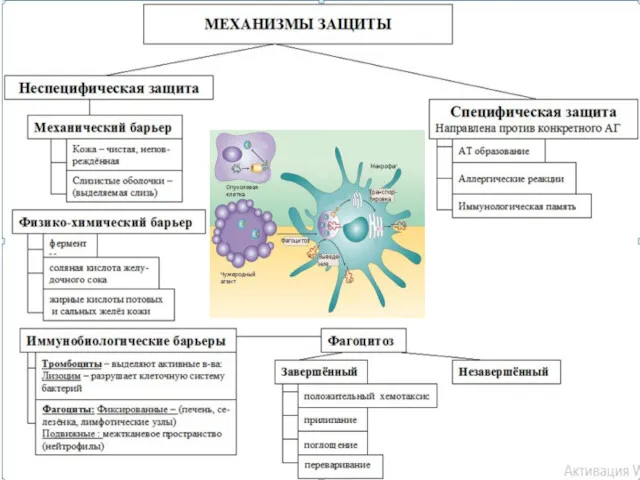
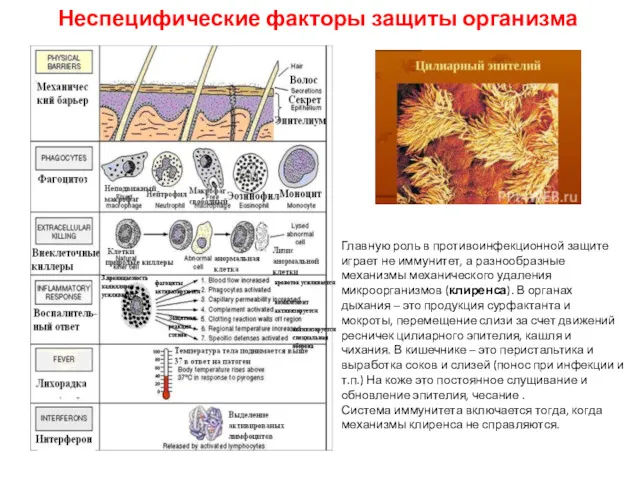
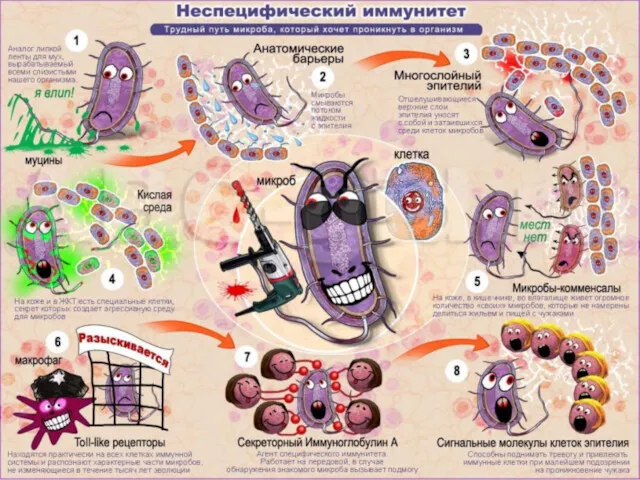
- 50. Неспецифические факторы защиты организма Главную роль в противоинфекционной защите играет не иммунитет, а разнообразные механизмы механического
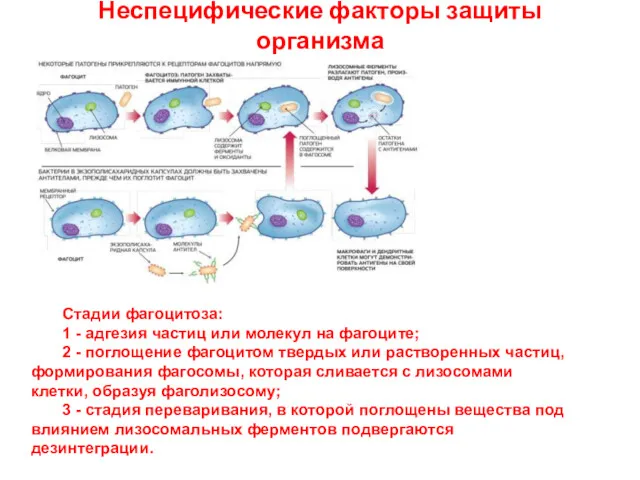
- 51. Неспецифические факторы защиты организма Стадии фагоцитоза: 1 - адгезия частиц или молекул на фагоците; 2 -
- 52. Неспецифические факторы защиты организма
- 53. Антигены- это любые вещества, содержащиеся в микроорганизмах и других клетках или выделяемые ими, которые несут признаки
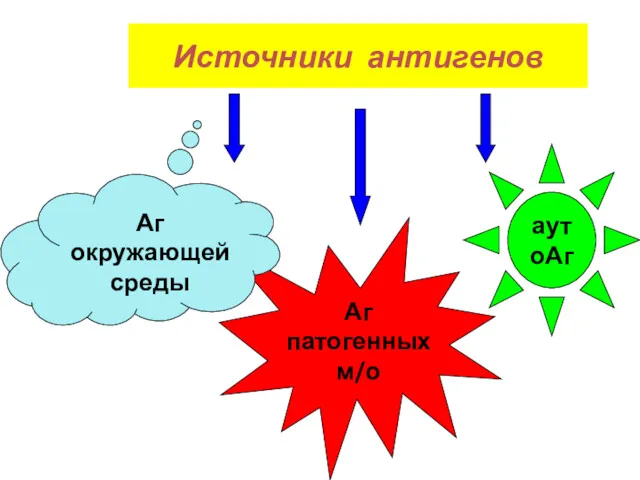
- 54. Источники антигенов Аг патогенных м/о аутоАг Аг окружающей среды
- 55. По происхождению: Эндогенные. 2. Экзогенные. По химической природе: 1. Белковые (обладают наибольшей иммуногенностью). 2. Небелковые (углеводы,
- 56. По характеру иммунного ответа: 1) тимусзависимые антигены (иммунный ответ зависит от активного участия Т-лимфоцитов); 2) тимуснезависимые
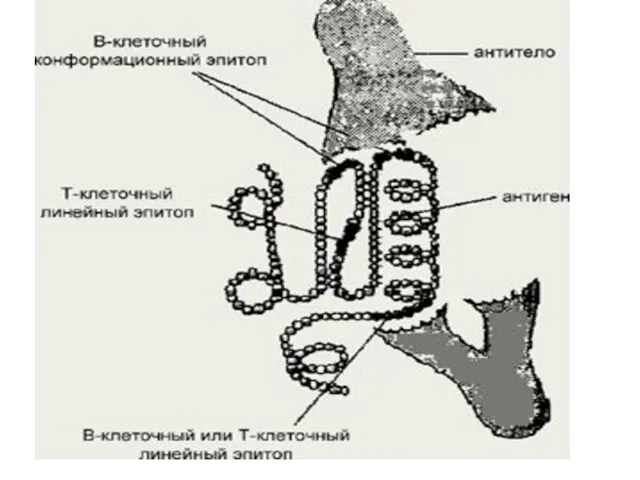
- 57. Эпитоп (антигенная детерминанта) — часть макромолекулы антигена, которая распознаётся иммунной системой (Ат, В-, Т-лимфоцитами). Линейные эпитопы
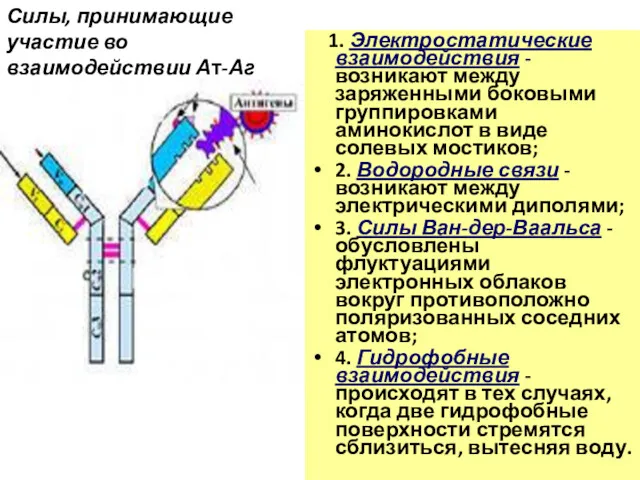
- 58. 1. Электростатические взаимодействия - возникают между заряженными боковыми группировками аминокислот в виде солевых мостиков; 2. Водородные
- 60. Инфекционные антигены – это антигены бактерий, вирусов, грибов, простейших. 1) группоспецифические (встречаются у разных видов одного
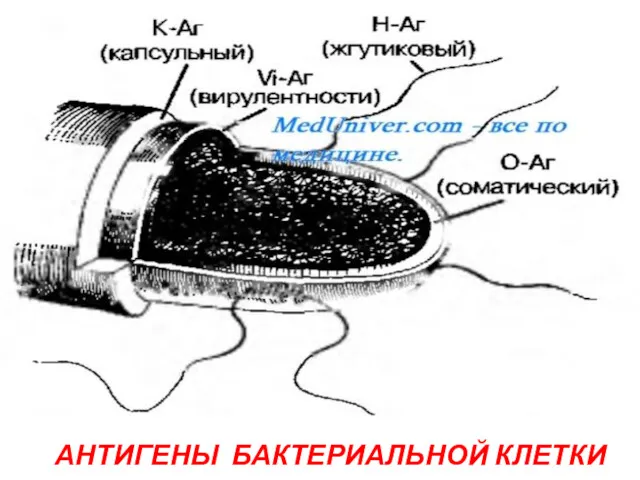
- 61. В зависимости от локализации в бактериальной клетке Аг – клеточные структуры 1) О – Аг –
- 62. АНТИГЕНЫ БАКТЕРИАЛЬНОЙ КЛЕТКИ
- 63. Протективные антигены – совокупность антигенных детерминант (эпитопов), которые вызывают наиболее сильный иммунный ответ, что предохраняет организм
- 64. Иммунологическая реактивность (иммунный ответ) – это распознавание генетически чужеродных АГ и специфическое реагирование с ними: Блокирование
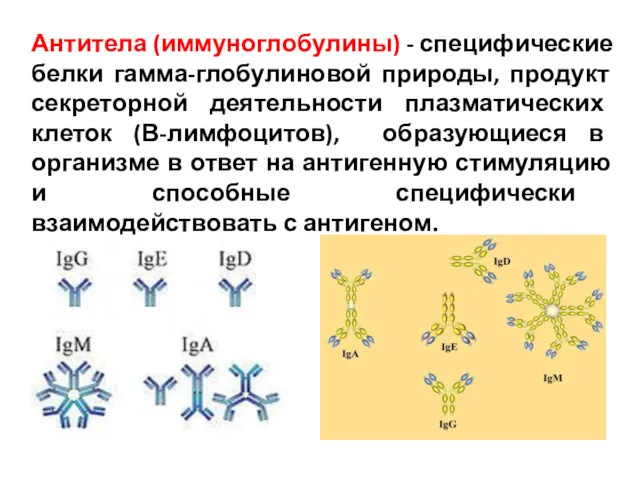
- 66. Антитела (иммуноглобулины) - специфические белки гамма-глобулиновой природы, продукт секреторной деятельности плазматических клеток (В-лимфоцитов), образующиеся в организме
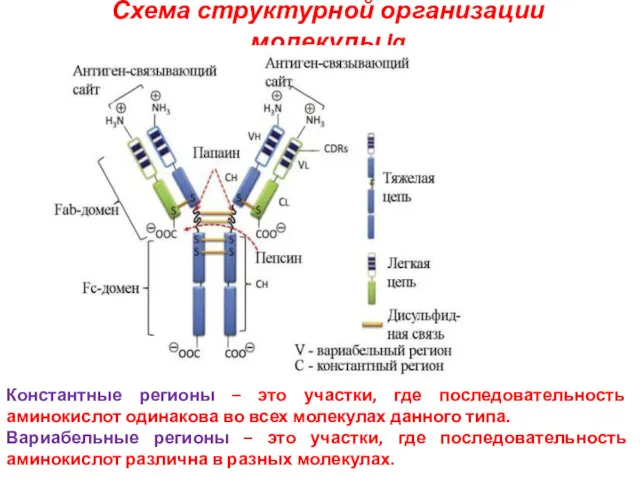
- 67. Схема структурной организации молекулы Ig Константные регионы – это участки, где последовательность аминокислот одинакова во всех
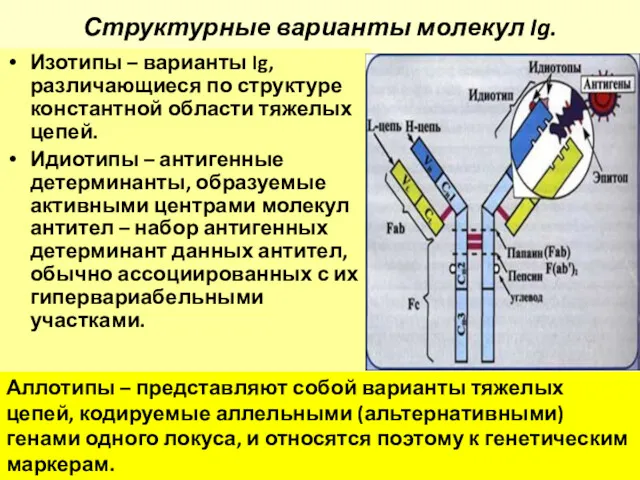
- 68. Структурные варианты молекул Ig. Изотипы – варианты Ig, различающиеся по структуре константной области тяжелых цепей. Идиотипы
- 69. Ig G (IgG 1, IgG 2, IgG 3, IgG 4) Мономер. Концентрация в крови – 8-
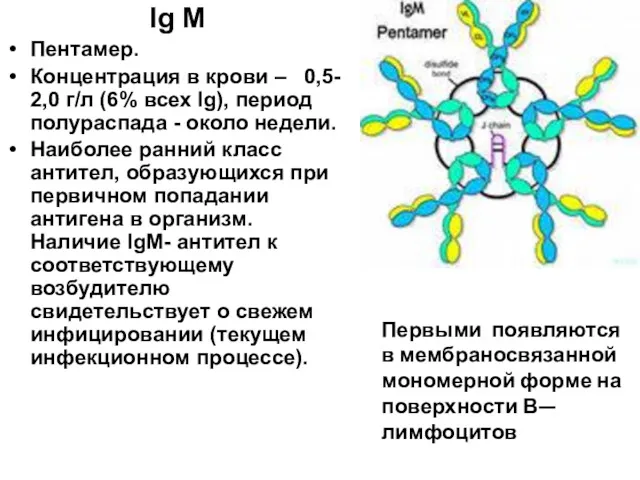
- 70. Первыми появляются в мембраносвязанной мономерной форме на поверхности В—лимфоцитов Ig М Пентамер. Концентрация в крови –
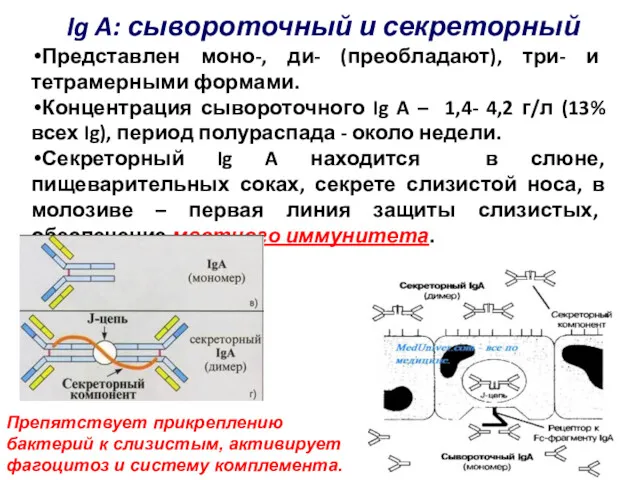
- 71. Ig A: сывороточный и секреторный Представлен моно-, ди- (преобладают), три- и тетрамерными формами. Концентрация сывороточного Ig
- 72. Ig D Мономер. 0,1% всех Ig, период полураспада - около 2-3 суток. IgD и IgM находятся
- 73. Основная физиологическая функция – защита слизистых оболочек организма путем локальной активации факторов плазмы крови и эффекторных
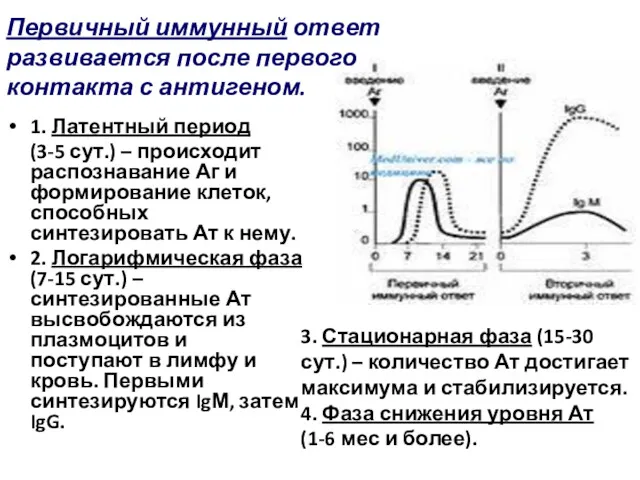
- 75. 1. Латентный период (3-5 сут.) – происходит распознавание Аг и формирование клеток, способных синтезировать Ат к
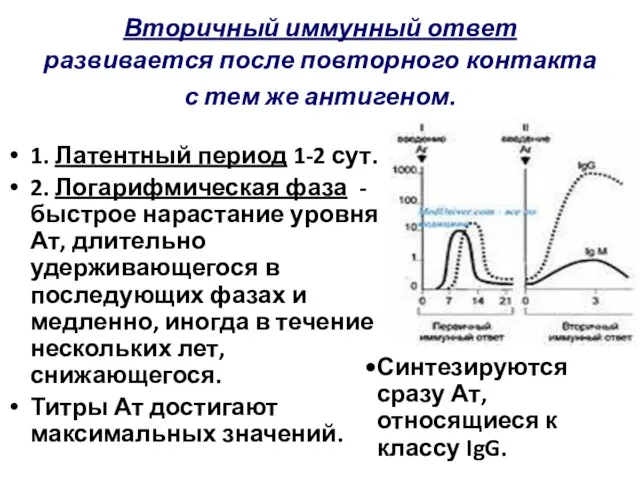
- 76. Вторичный иммунный ответ развивается после повторного контакта с тем же антигеном. 1. Латентный период 1-2 сут.
- 77. Основную роль в реализации иммунных функций играют: 1. Макрофаги, а также другие антигенпрезентирующие клетки (дендритные). 2.
- 78. 1) захват нативного (неизмененного) антигенного материала путем фагоцитоза, пиноцитоза или рецепторно-опосредованного эндоцитоза; 2) частичный протеолиз эндогенного
- 79. 5) экспрессия на поверхности клетки добавочных молекул, усиливающих процесс взаимодействия с лимфоцитами; 6) секреция растворимых медиаторов
- 80. Функции T-лимфоцитов 1) с помощью имеющихся на их поверхности Т-клеточных рецепторов (ТКР) обеспечивают специфическое распознавание антигенных
- 81. Фазы образования Т-лимфоцитов Антиген-независимая фаза образования T-клеток осуществляется последовательно в костном мозге и тимусе. Антиген-зависимая фаза
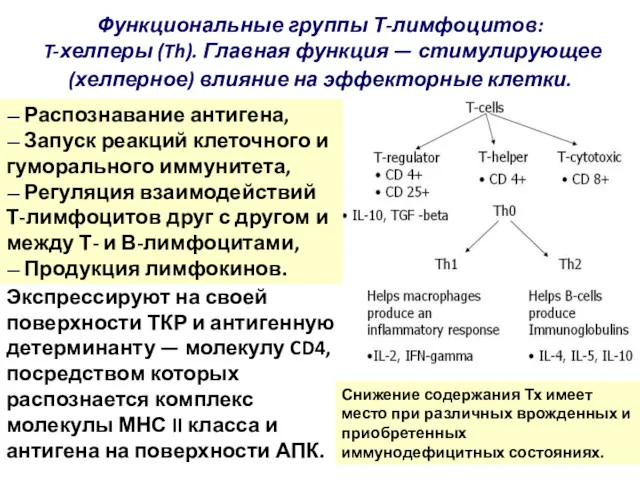
- 82. Функциональные группы Т-лимфоцитов: T-хелперы (Th). Главная функция — стимулирующее (хелперное) влияние на эффекторные клетки. Экспрессируют на
- 83. — индукторы T-хелперов (ИТх) – начинают функционировать спустя 16-20 ч после появления чужеродного материала. Реагируя на
- 84. Цитотоксические лейкоциты - клетки-эффекторы — ЦТЛ - Т-киллеры (Тк). Непосредственно осуществляют защитные реакции посредством ТКР и
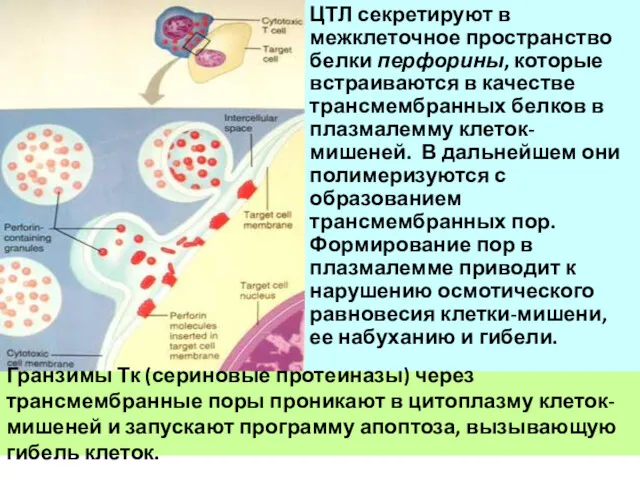
- 85. ЦТЛ секретируют в межклеточное пространство белки перфорины, которые встраиваются в качестве трансмембранных белков в плазмалемму клеток-мишеней.
- 86. Клетки -регуляторы – T-супрессоры(Тс). На поверхности имеют молекулы CD4, CD 25. Распознают эпитопы антигенов в комбинации
- 87. В-система специфической иммунной защиты Функции В-лимфоцитов : 1) распознавание антигенов иммуноглобулиновыми рецепторами; 2) обеспечение реакций гуморального
- 88. В—клетка памяти (Вп) — долгоживущая клетка, обеспечивающая быструю пролиферацию и дифференцировку В-лимфоцитов в плазмоциты при повторном
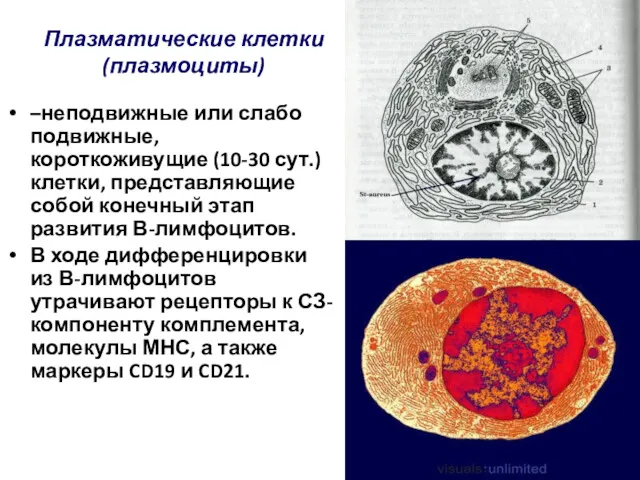
- 89. Плазматические клетки (плазмоциты) –неподвижные или слабо подвижные, короткоживущие (10-30 сут.) клетки, представляющие собой конечный этап развития
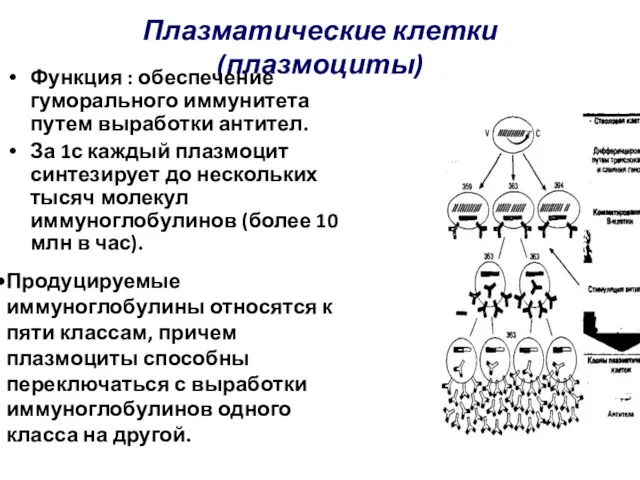
- 90. Плазматические клетки (плазмоциты) Функция : обеспечение гуморального иммунитета путем выработки антител. За 1с каждый плазмоцит синтезирует
- 91. Типы антигенов, участвующих в активации В-лимфоцитов 1). Тимуснезависимые антигены обоих типов вызывают преимущественный синтез IgM, а
- 92. СЕРОЛОГИЧЕСКИЕ РЕАКЦИИ
- 93. Серологические реакции – это реакции между антигенами и антителами in vitro . Цели применения: серодиагностика бактериальных
- 94. Классификация серологических реакций в зависимости от характера и физического состояния антигена Прямые серологические реакции, основанные на
- 95. Титр сыворотки – это наиболее высокое разведение сыворотки (наименьшее количество антител), при котором данная серологическая реакция
- 96. Серологические реакции Реакция агглютинации Реакция преципитации Реакции нейтрализации Реакция связывания комплемента Реакция иммунофлюоресценции Радиоиммунологический анализ Иммуноферментный
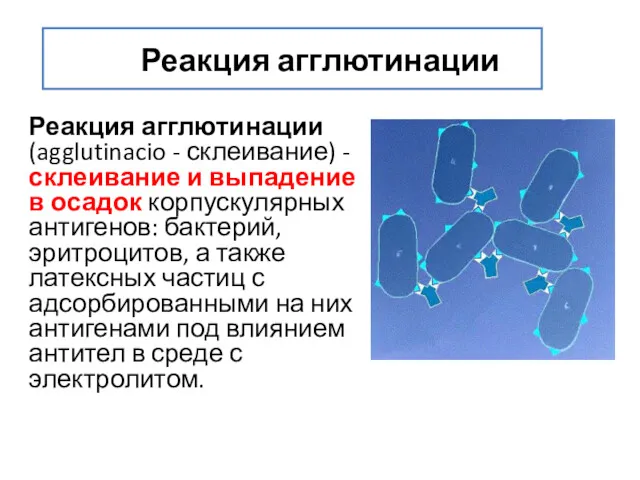
- 97. Реакция агглютинации Реакция агглютинации (agglutinacio - склеивание) - склеивание и выпадение в осадок корпускулярных антигенов: бактерий,
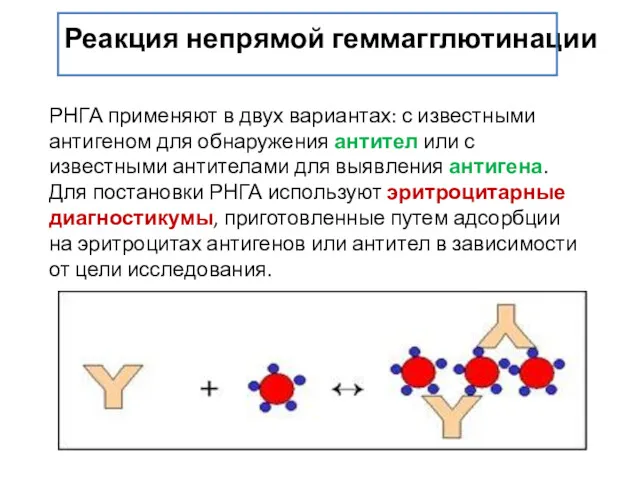
- 98. Реакция непрямой геммагглютинации РНГА применяют в двух вариантах: с известными антигеном для обнаружения антител или с
- 99. В положительных случаях в лунке осадок имеет вид тонкой пленки из склеивающихся эритроцитов (зонтик).
- 100. Реакция преципитации Принцип: При взаимодействиии растворимого антигена с антителом в присутствии электролитов (NaCl) образуется комплекс Аг-Ат
- 101. Варианты реакции преципитации в жидкой среде - по типу реакции флокуляции , кольцепреципитации. в плотной среде
- 102. Реакция кольцепреципитации Образование комплекса АГ-АТ - + Реакцию проводят путем наслаивания на иммунную сыворотку антигена
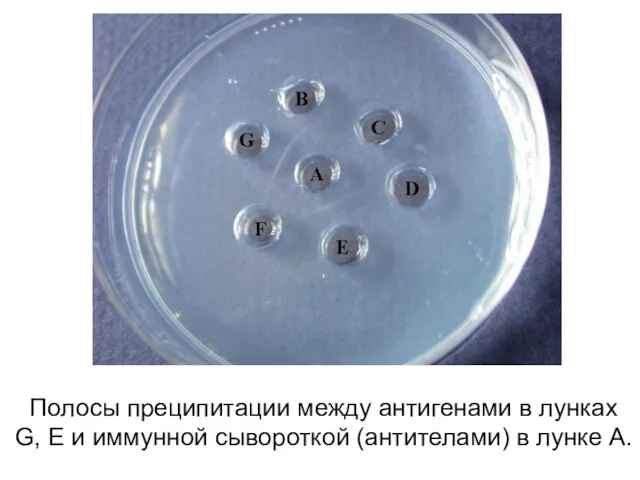
- 103. Реакция проводится в агаре на стеклах или в чашках Петри . В разные лунки в агаре
- 104. Полосы преципитации между антигенами в лунках G, E и иммунной сывороткой (антителами) в лунке A.
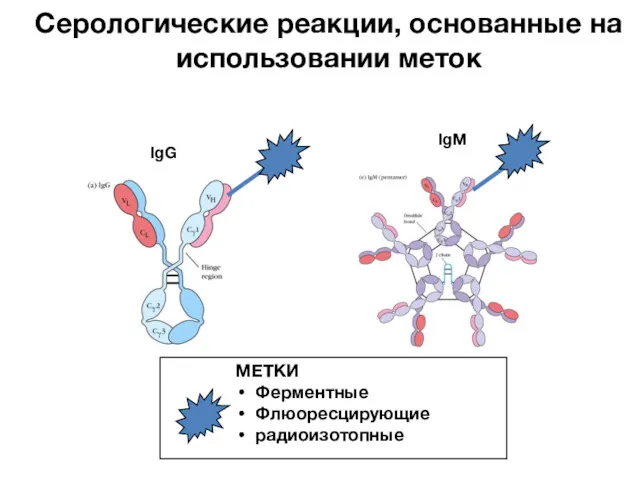
- 105. IgG IgM Серологические реакции, основанные на использовании меток МЕТКИ Ферментные Флюоресцирующие радиоизотопные
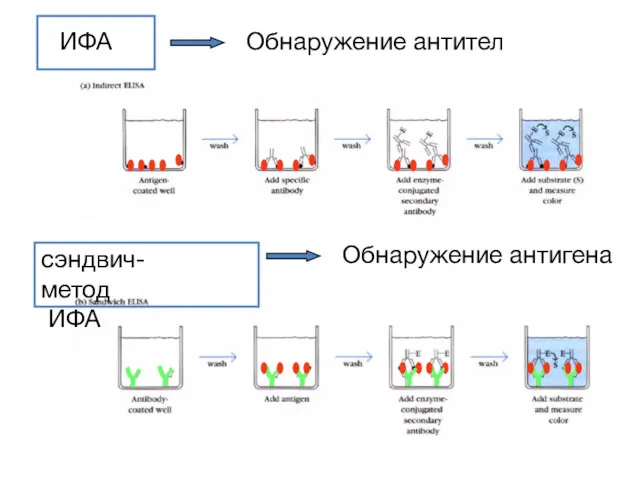
- 106. Иммуноферментный анализ (ИФА или ΕLISA) Метод ИФА или ELISA – это серологическая реакция , в которой
- 107. ИФА сэндвич-метод ИФА Обнаружение антител Обнаружение антигена
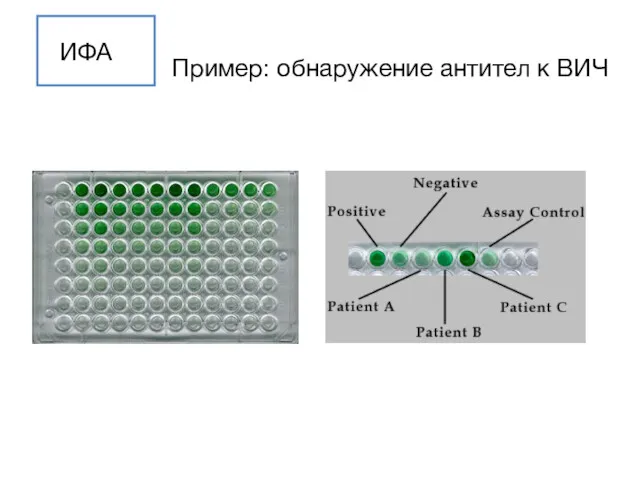
- 108. ИФА Пример: обнаружение антител к ВИЧ
- 109. Реакция иммунофлуоресценции (РИФ) РИФ основана на соединении антигенов бактерий и вирусов со специфическими антителами, меченными флюоресцирующими
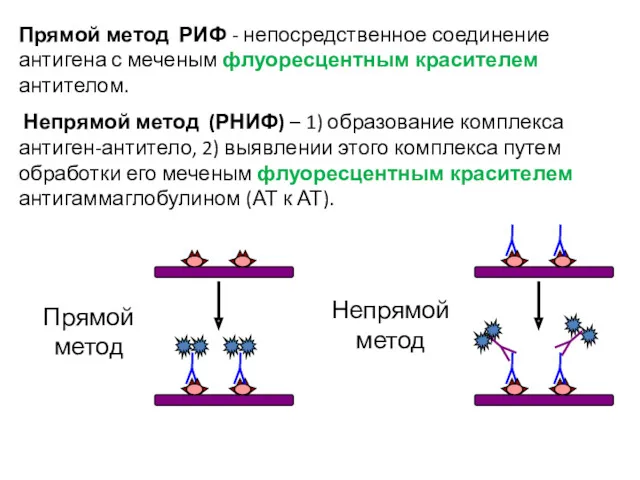
- 111. Прямой метод РИФ - непосредственное соединение антигена с меченым флуоресцентным красителем антителом. Непрямой метод (РНИФ) –
- 112. Люминесцентный микроскоп
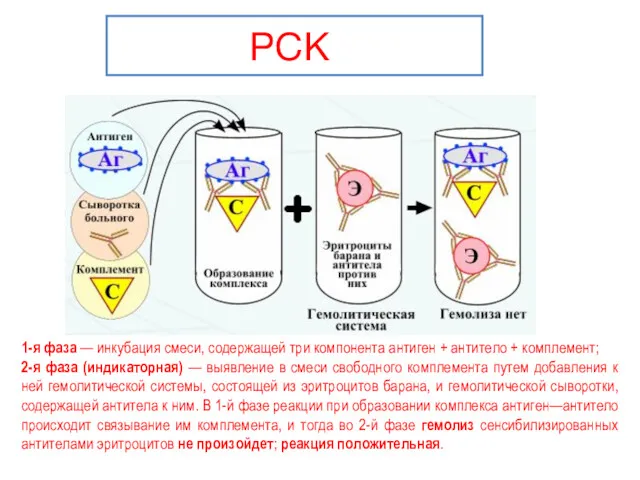
- 113. Реакция связывания комплемента РСК основывается на способности комплемента связываться с комплексом АГ + АТ . Реакция
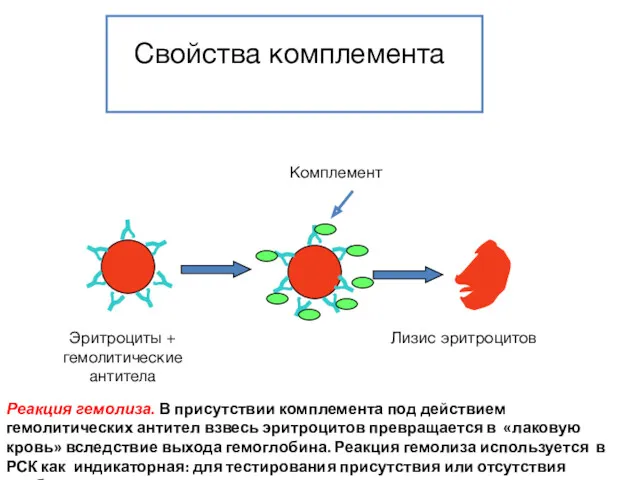
- 114. Свойства комплемента Реакция гемолиза. В присутствии комплемента под действием гемолитических антител взвесь эритроцитов превращается в «лаковую
- 115. РСК 1-я фаза — инкубация смеси, содержащей три компонента антиген + антитело + комплемент; 2-я фаза
- 117. Скачать презентацию




































































 Florence Nightingale
Florence Nightingale Магнітні бурі і їхній вплив на здоров'я людина
Магнітні бурі і їхній вплив на здоров'я людина Показания к оперативному лечению. Методы предоперационного обследования
Показания к оперативному лечению. Методы предоперационного обследования Симптоматическое и климатическое бесплодие
Симптоматическое и климатическое бесплодие Мәдениеттің даму заңдылықтары
Мәдениеттің даму заңдылықтары Клиническая эффективность комплексного лечения больных с дорсалгией
Клиническая эффективность комплексного лечения больных с дорсалгией Группа антибиотиков макролиды
Группа антибиотиков макролиды Огнестрельные переломы черепа
Огнестрельные переломы черепа Синдромы ЖКТ
Синдромы ЖКТ Старение кожи. Факторы старения
Старение кожи. Факторы старения Профессия - врач-хирург
Профессия - врач-хирург Противоинфекционный иммунитет: определение, типы, виды, механизмы
Противоинфекционный иммунитет: определение, типы, виды, механизмы Синдром Конна
Синдром Конна Заболеваемость, инвалидность населения. Общие положения регистрации
Заболеваемость, инвалидность населения. Общие положения регистрации Гонорея и негонорейные уретриты
Гонорея и негонорейные уретриты Спинальная травма
Спинальная травма Найбільш поширені вроджені вади серця у дітей
Найбільш поширені вроджені вади серця у дітей Основы управления в здравоохранении
Основы управления в здравоохранении Наркомания. Влияние наркотиков на организм человека
Наркомания. Влияние наркотиков на организм человека Плоскостопие у детей и взрослых
Плоскостопие у детей и взрослых Парафинотерапия. Механизм действия
Парафинотерапия. Механизм действия Здоровый день - здоровая жизнь
Здоровый день - здоровая жизнь Жоғарға ми қызметінің бұзылулары
Жоғарға ми қызметінің бұзылулары Збудник туберкульозу. Патогенні мікобактерії
Збудник туберкульозу. Патогенні мікобактерії Фоновые, предраковые заболевания, доброкачественные и злокачественные опухоли вульвы, влагалища
Фоновые, предраковые заболевания, доброкачественные и злокачественные опухоли вульвы, влагалища Общая реакция организма на травму
Общая реакция организма на травму Микроциркуляция. Транскапиллярный обмен. Лимфообращение
Микроциркуляция. Транскапиллярный обмен. Лимфообращение Язва желудка и 12-перстной кишки
Язва желудка и 12-перстной кишки