Техника определения группы крови, резус-фактора, проведение проб на совместимость по системе АВО и резус-фактору презентация
Содержание
- 2. Техника определения группы крови, резус-фактора, проведение проб на совместимость по системе АВО и резус-фактору.
- 3. α β О А β В α АВ 0 (I) группа (II) группа (III) группа (IV)
- 4. В 1981 году для типирования групп крови были предложены моноклональные антитела, т.е. происходящие из одного клона
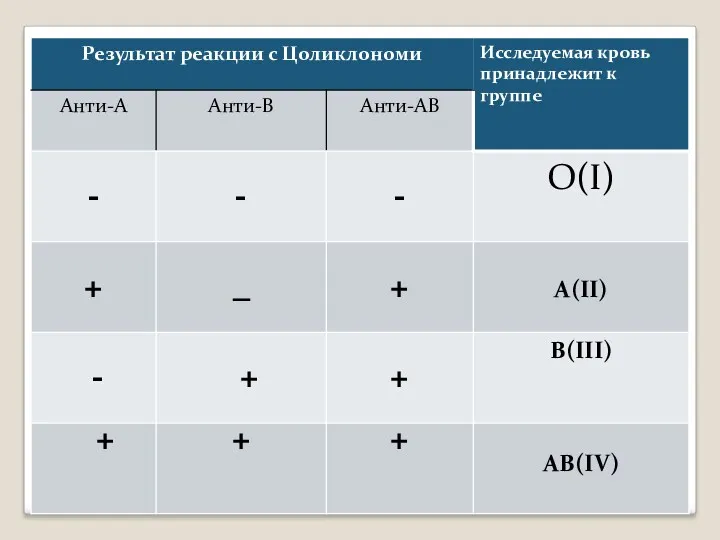
- 5. Определение группы крови АВО моноклональными антителами 1.Групповая принадлежность крови определяется реакцией агглютинации при помощи реактивов, содержащих
- 7. Определение резус принадлежности исследуемой крови с помощью цоликлонов анти-D супер Наносят большую каплю (около 0,1 мл)
- 8. Анти – D супер Rh(+) положительный Rh(-) отрицательный Система Резус
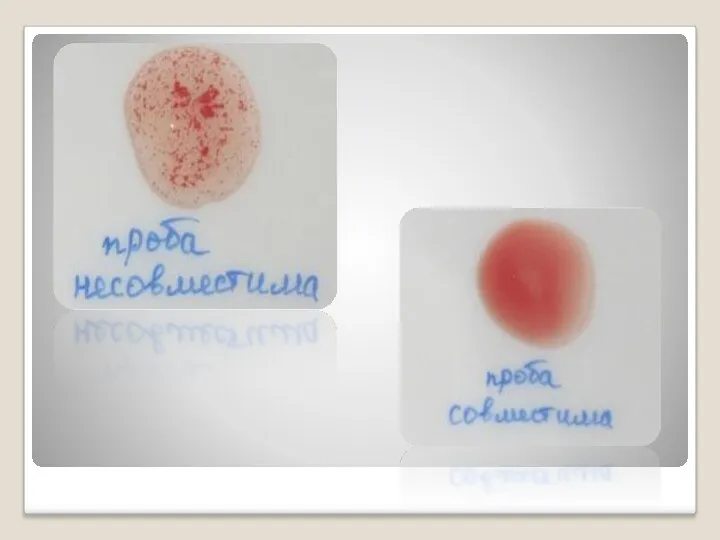
- 9. Проба на совместимость по группам крови системы АВ0 На пластинку наносят 2-3 капли сыворотки реципиента и
- 11. Инструкция по применению компонентов крови «Перед переливанием контейнер с трансфузионной средой (эритроцитная масса или взвесь, плазма
- 12. Селиванов Е.А. и cоавт. Трансфузиология 2001;4:61-64 Размораживание плазмы методом теплообмена (+37°С/20 мин) приводит к снижению активности
- 13. Hardy J.-F. ISBT Science Series 2007:2;168-177 Гипотермия – один факторов, ответственных за развитие коагулопатии при массивной
- 14. Гипотермия, вызванная быстрым введением большого объема холодной крови, способна вызвать нарушения ритма сердца и даже остановку
- 15. По приказу №666: При трансфузии эритроцитсодержащих компонентов в плановом или экстренном порядке врач, выполняющий трансфузию, независимо
- 16. 4.перед каждой трансфузией перепроверяет группу крови у реципиента по системе AB0 и сверить полученный результат с
- 17. При трансфузии других компонентов крови, врач, выполняющий трансфузию, определяет группу крови АВ0 и резус-принадлежность реципиента и
- 18. Пробы на совместимость по группам крови системы АВ0 выполняются с сывороткой крови больного, которую получают путем
- 19. Перед переливанием контейнер с трансфузионной средой (ЭМ или ЭВ) извлекается из холодильника и выдерживается при комнатной
- 20. Биологическая проба проводится перед началом любой трансфузии и перед каждой новой дозой компонентов или препаратов, в
- 21. При проведении биологической пробы однократно переливается 60 капель (два–три миллилитра) в течение одной–двух минут, затем переливание
- 22. При появлении во время проведения биологической пробы озноба, боли в пояснице, чувства жара и стеснения в
- 23. Не допускается введение в контейнер с эритроцитсодержащим компонентом крови каких-либо других медикаментов или растворов, кроме стерильного
- 24. Для контроля в случае возникновения реакций и осложнений после окончания переливания донорский контейнер с небольшим количеством
- 25. В случае развития осложнений во время биологической пробы, во время трансфузии или после неё, делается подробная
- 26. После трансфузии: 1)реципиентом соблюдается в течение двух часов постельный режим; реципиент после окончания переливания находится под
- 27. Скорость переливания ЭМ составляет 2–5 мл/кг массы тела в час под обязательным контролем показателей гемодинамики и
- 29. Скачать презентацию
























 Эссенциальная артериальная гипертензия
Эссенциальная артериальная гипертензия Ревматоидный артрит
Ревматоидный артрит Макропрепараты по модулям
Макропрепараты по модулям Харчові отруєння
Харчові отруєння Мышцы нижней конечности. Мышцы тазового пояса. Мышцы свободной нижней конечности
Мышцы нижней конечности. Мышцы тазового пояса. Мышцы свободной нижней конечности Хронический гнойный мезотимпанит у детей
Хронический гнойный мезотимпанит у детей Зәр шығару жүйесі
Зәр шығару жүйесі Жүрек- өкпелік реанимация
Жүрек- өкпелік реанимация Геморрагическая лихорадка Эбола
Геморрагическая лихорадка Эбола Парадонт құрылымы. Қызыл иек сұйықтығы. Қызыл иек жүлгесі. Қызыл иек ультра құрылымы
Парадонт құрылымы. Қызыл иек сұйықтығы. Қызыл иек жүлгесі. Қызыл иек ультра құрылымы Пневматоракс и его виды. Опасность проникающих ранений грудной клетки, механизм нарушения дыхания
Пневматоракс и его виды. Опасность проникающих ранений грудной клетки, механизм нарушения дыхания Презентация санаториев-профилакториев Казахстана от профсоюза КәсіпҚазақмыс на 2018 год
Презентация санаториев-профилакториев Казахстана от профсоюза КәсіпҚазақмыс на 2018 год Заболевания зрительного нерва и сетчатой оболочки. Патология глаз при общих соматических заболеваниях
Заболевания зрительного нерва и сетчатой оболочки. Патология глаз при общих соматических заболеваниях Жүрек автономдығының механизмі
Жүрек автономдығының механизмі Жаңа дәрілік заттардың клиникаға дейінгі зерттеулері
Жаңа дәрілік заттардың клиникаға дейінгі зерттеулері Нейроинфекция
Нейроинфекция Осанка. Позвоночный столб
Осанка. Позвоночный столб Туберкулез кезіндегі жүктілік
Туберкулез кезіндегі жүктілік Гигиенические требования к планировке и содержания детских и подростковых учреждениях
Гигиенические требования к планировке и содержания детских и подростковых учреждениях Гендік мутация
Гендік мутация Лекарственные растения
Лекарственные растения Искусственный интеллект в медицине
Искусственный интеллект в медицине Заболевание пищевода
Заболевание пищевода Харчові добавки. Е-числа
Харчові добавки. Е-числа Современные методы диагностики и лечения пострадавших с тяжелой политравмой в травматологическом центре
Современные методы диагностики и лечения пострадавших с тяжелой политравмой в травматологическом центре Профилактика и лечение видов мастита у крупного рогатого скота
Профилактика и лечение видов мастита у крупного рогатого скота Стабилизация растворов для инъекций
Стабилизация растворов для инъекций Коллективное медицинское страхование работников АК Узбектелеком
Коллективное медицинское страхование работников АК Узбектелеком