Содержание
- 2. Наприкінці XX, початку XXI століття у зв’язку зі значиним ростом арсеналу нових лікарських засобів постало питання
- 3. безпідставний ріст вартості ліків, збільшення розриву між ресурсами лікувальних закладів і витратами на придбання ліків вимагали
- 4. Фармацевтична біоетика – галузь біоетики, що вивчає моральні, правові, соціальні, екологічні, біологічні і юридичні проблеми, що
- 5. ЗАДАЧІ БІОЕТИКИ 1. Формування: - біоетичної концепції провізора в системі «фармацевтичний робітник і суспільство»; - біоетичних
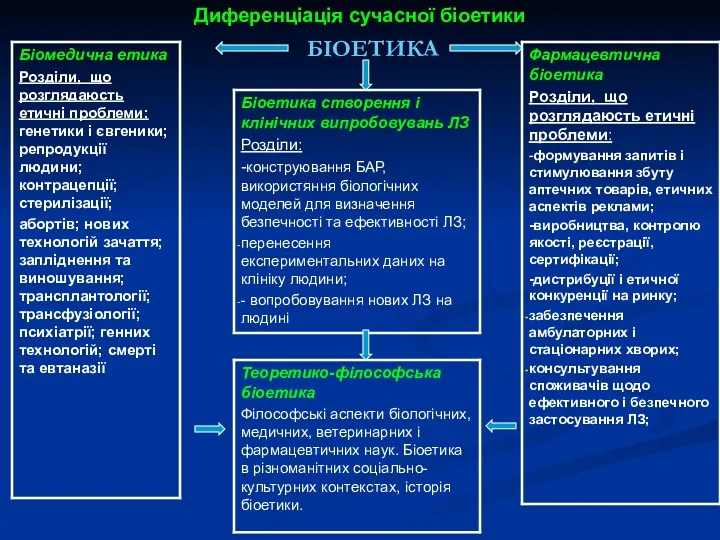
- 6. Диференціація сучасної біоетики БІОЕТИКА
- 7. ХАРАКТЕРИСТИКА СУЧАСНОГО ЛІКАРСЬКОГО РИНКУ З ПОЗИЦІЇ БІОЕТИКИ ТА ЗХИСТУ ПРАВ СПОЖИВАЧІВ. ФАРМАКОНАГЛЯД В даний час: найбільш
- 8. Групування ЛЗ за ступенем доведеності ефективності і характеристикою безпечності ЛЗ 1. Категорія А – ЛЗ, ефективність
- 9. У ДРУГІЙ ПОЛОВИНІ XX СТОЛІТТЯ ЗАГОСТРИЛАСЬ СИТУАЦІЯ В ГАЛУЗІ БЕЗПЕКИ ЗАСТОСУВАННЯ ЛЗ. Постійно збільшується число повідомлень
- 10. ЗАДАЧАМИ ФАРМАКОНАГЛЯДУ є системне рішення, що забезпечує: створення національної служби фармаконагляду; навчання та підготовка спеціалістів охорони
- 11. ОБ’ЄКТОМ ВИВЧЕННЯ ФАРМАКОНАГЛЯДУ Є: недостатня вивченість ЛЗ; недостатня інформованість медичних і фармацевтичних роботників і споживачів фармацевтичної
- 12. Ким здійснюється фармаконагляд в Україні? п. 1.3. Здійснення нагляду за побічними реакціями лікарських засобів, дозволених до
- 13. Действующая система фармаконадзора в Украине Приказ МЗ № 898 от 27.12.06 г. Міністерство охорони здоров’я Украины
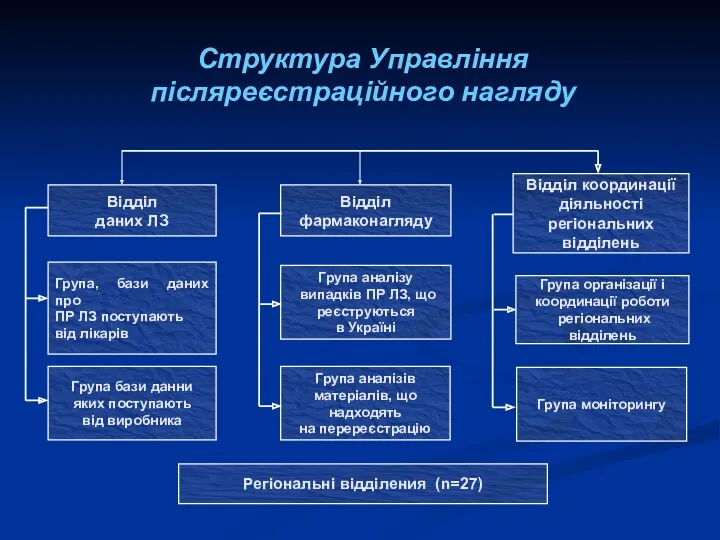
- 14. Структура Управління післяреєстраційного нагляду
- 15. Основні напрямки роботи системи фармаконагляду в Україні Інформаційне і методичне забезпечення системи охорони здоров’я з питань
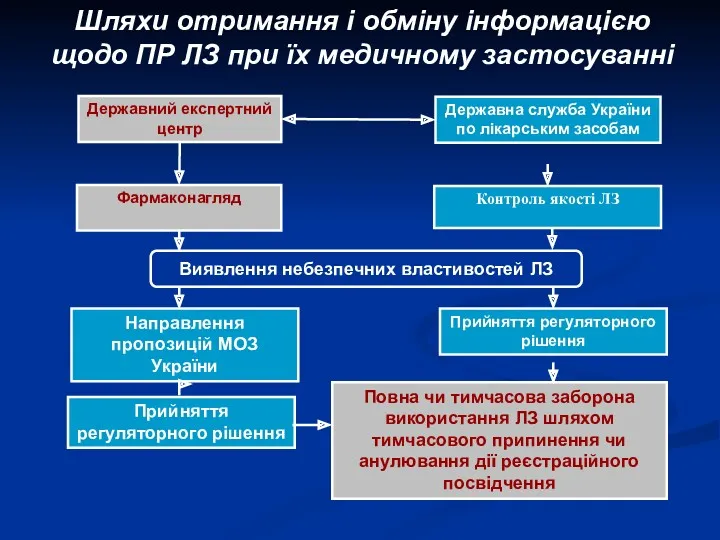
- 16. Шляхи отримання і обміну інформацією щодо ПР ЛЗ при їх медичному застосуванні
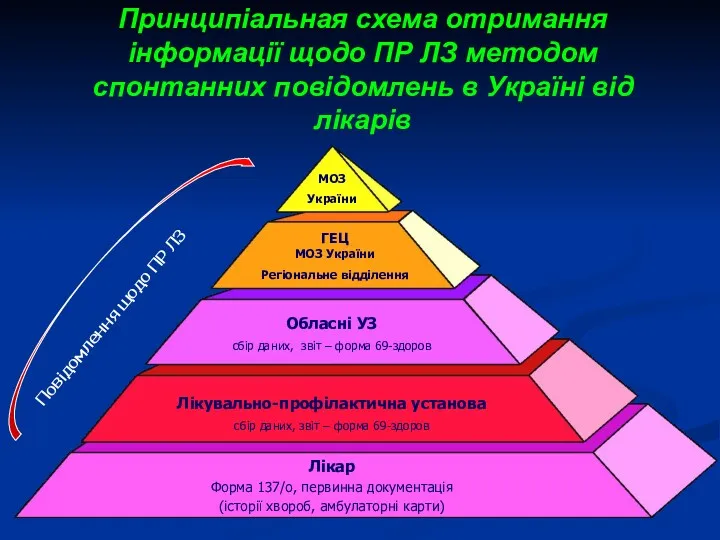
- 17. Принципіальная схема отримання інформації щодо ПР ЛЗ методом спонтанних повідомлень в Україні від лікарів
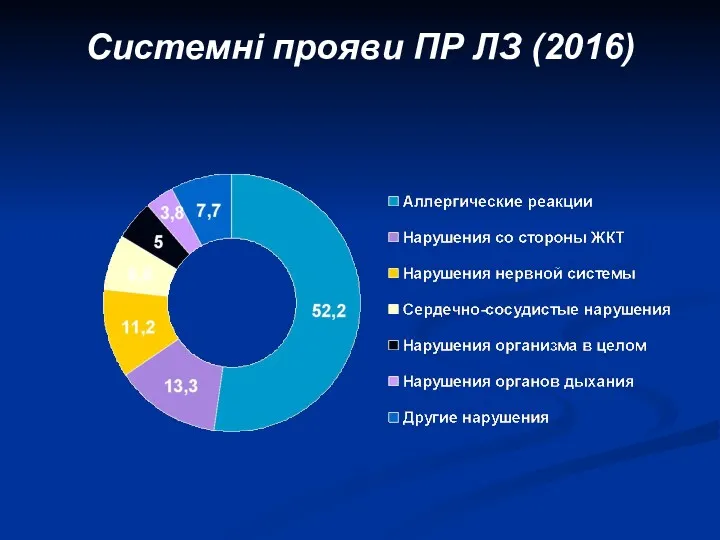
- 18. Системні прояви ПР ЛЗ (2016)
- 19. Розподіл ПР ЛЗ за ступенем серйозності (2010) 79,5% – несерйозні ПР 20,5% – серйозні ПР 7,3%
- 20. Критерії оцінки безпеки ЛЗ Частота ПР Співвідношення кількості непередбачених до передбачених ПР, серйозних до несерйозних ПР
- 21. Частота ПР Більше 10% - дуже часті, які потребують обов’язкового проведення профілю безпечності ЛЗ або негайного
- 22. Причини, за якими вносяться зміни і доповнення в інформацію щодо безпечності ЛЗ при проведенні експертизи перереєстраційних
- 23. Взаємодія формулярної системи і фармаконагляду Міністерство охорони здоров’я України Державний експертний центр Управління післяреєстрационного нагляду Регіональний
- 25. Скачать презентацию

















 Деонтология, этика ұғымдары. Дәрігер деонтологиясы. Медициналық деонтология түрлері
Деонтология, этика ұғымдары. Дәрігер деонтологиясы. Медициналық деонтология түрлері Основы оказания первой помощи на поиске, юридические аспекты, базовые алгоритмы. ПО Лиза Алерт
Основы оказания первой помощи на поиске, юридические аспекты, базовые алгоритмы. ПО Лиза Алерт Наследственные болезни человека. Наследственные заболевания человека
Наследственные болезни человека. Наследственные заболевания человека Тиреотоксикоз
Тиреотоксикоз Ударно-волновая терапия в косметологии
Ударно-волновая терапия в косметологии Методы исследования почек и мочевыводящих путей
Методы исследования почек и мочевыводящих путей Морфологические группы лекарственного растительного сырья и их особенности
Морфологические группы лекарственного растительного сырья и их особенности Первая помощь при укусах насекомых
Первая помощь при укусах насекомых Туа пайда болған пилоростеноз
Туа пайда болған пилоростеноз Компьютер и здоровье ребенка
Компьютер и здоровье ребенка Сезімталдықтың нейрогендік бұзылыстары, түрлері; даму механизмдері. Ауырсыну сезімі, анықтамасы және сипаттамасы Ауырсыну сезі
Сезімталдықтың нейрогендік бұзылыстары, түрлері; даму механизмдері. Ауырсыну сезімі, анықтамасы және сипаттамасы Ауырсыну сезі Зоонозды инфекцияларға сипаттама
Зоонозды инфекцияларға сипаттама Инородные тела дыхательных путей у детей
Инородные тела дыхательных путей у детей Заболевания органов дыхания. Пневмонии
Заболевания органов дыхания. Пневмонии Хейлиты и предраковые заболевания слизистой оболочки
Хейлиты и предраковые заболевания слизистой оболочки Геморрагический инсульт
Геморрагический инсульт Antimicrobial drugs
Antimicrobial drugs Properties of heart and vessels in children
Properties of heart and vessels in children Особенности познавательных процессов у лиц с ДЦП
Особенности познавательных процессов у лиц с ДЦП Кровотечения. Виды кровотечений, их признаки
Кровотечения. Виды кровотечений, их признаки Токсоплазмоз
Токсоплазмоз Патогенез лихорадки при инфекции и принципы жаропонижающей терапии у детей
Патогенез лихорадки при инфекции и принципы жаропонижающей терапии у детей Гострий герпетичний стоматит
Гострий герпетичний стоматит Безопасное материнство и эффективный перинатальный уход: нужны ли изменения
Безопасное материнство и эффективный перинатальный уход: нужны ли изменения Фотометрия. Клинический спектрофотометр
Фотометрия. Клинический спектрофотометр Бактериальный вагиноз
Бактериальный вагиноз Изменения слизистой оболочки полости рта при заболеваниях нервной системы, желудочно-кишечного тракта и кроветворной системы
Изменения слизистой оболочки полости рта при заболеваниях нервной системы, желудочно-кишечного тракта и кроветворной системы Принципы оказания помощи при остром нарушении мозгового кровообращения
Принципы оказания помощи при остром нарушении мозгового кровообращения