Содержание
- 2. Что такое алкадиены? Алкадиены – углеводороды, молекулы которых содержат две двойные связи. общая формула: CnH2n-2 Названия
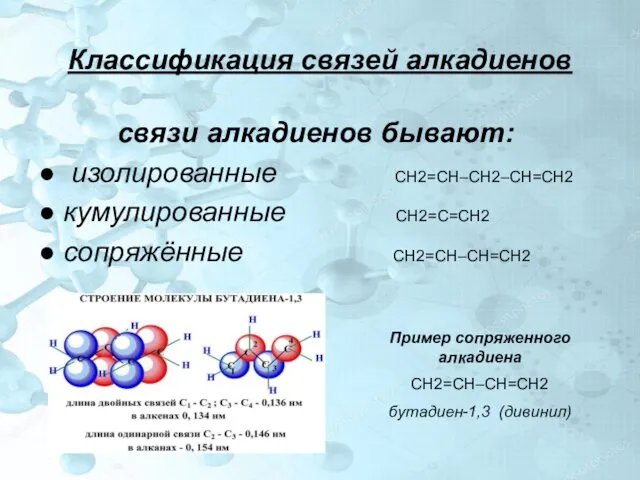
- 3. Классификация связей алкадиенов связи алкадиенов бывают: ● изолированные СН2=СН–СН2–СН=СН2 ● кумулированные СН2=С=СН2 ● сопряжённые СН2=СН–СН=СН2 Пример
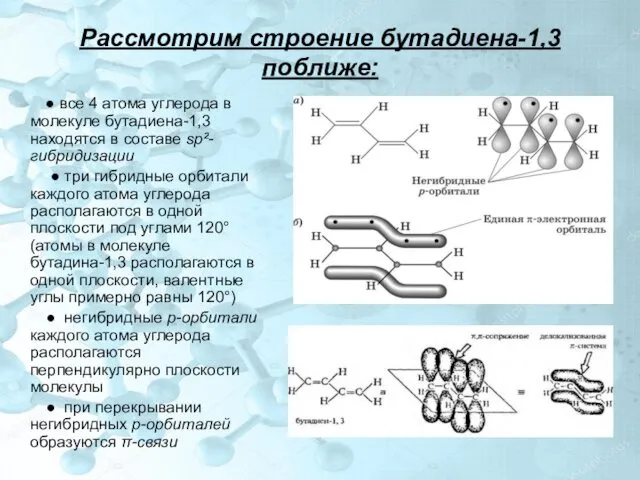
- 4. Рассмотрим строение бутадиена-1,3 поближе: ● все 4 атома углерода в молекуле бутадиена-1,3 находятся в составе sp²-гибридизации
- 5. Химические свойства алкадиенов Химические свойства алкадиенов похожи на свойства алкенов. Алкадиены также легко вступают в реакции
- 6. Реакции присоединения Для алкадиенов характерны реакции присоединения по одной из двойных связей С=С, либо по обоим
- 7. Окисление алкадиенов Реакции окисления в органической химии сопровождаются увеличением. В зависимости от интенсивности и условий окисление
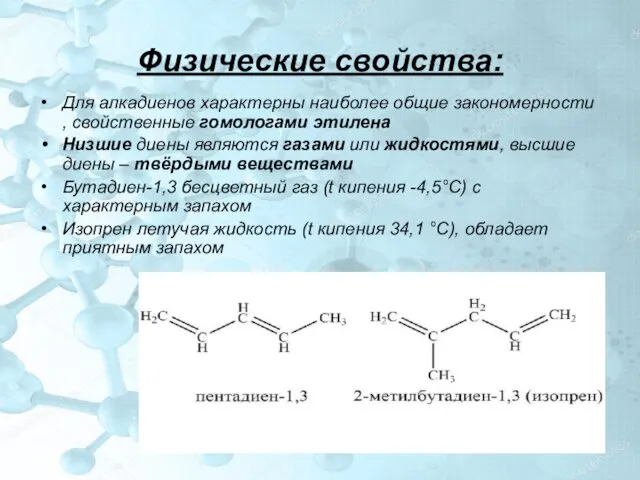
- 8. Физические свойства: Для алкадиенов характерны наиболее общие закономерности , свойственные гомологами этилена Низшие диены являются газами
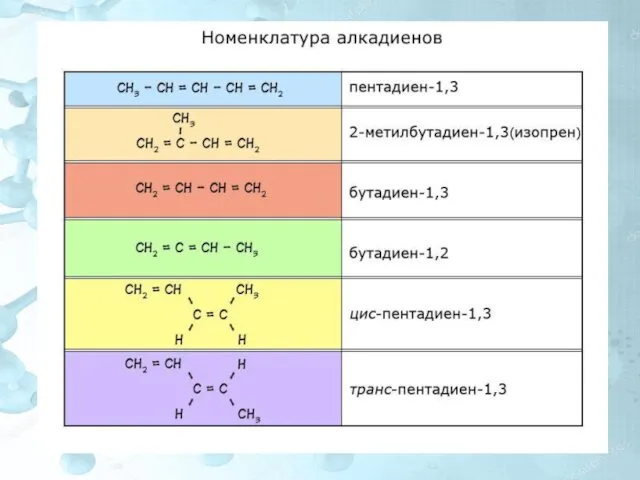
- 9. Номенклатура алкадиенов По правилам ИЮПАК главная цепь молекулы алкадиена должна включать обе двойные связи. Нумерация атомов
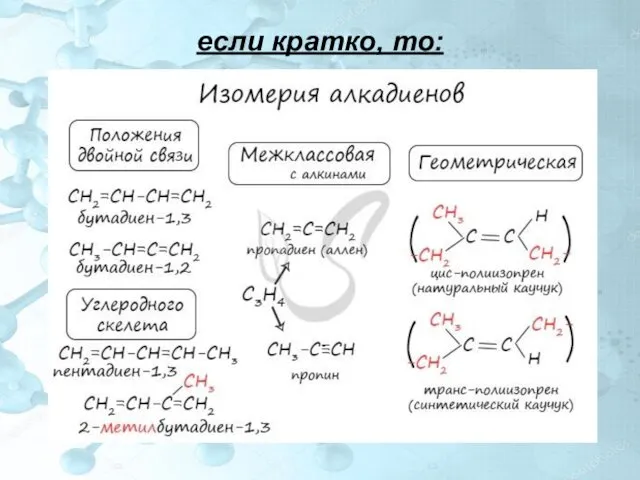
- 11. Изомерия алкадиенов 1)Структурная изомерия Для алкенов характерна структурная изомерия – изомерия углеродного скелета, изомерия положения кратных
- 12. 2)Пространственная изомерия Для некоторых алкадиенов характерна пространственная изомерия: цис-транс-изомерия и оптическая. Цис-транс-изомерия обусловлена отсутствием вращения по
- 13. если кратко, то:
- 15. Скачать презентацию






 Карта мира перед II Мировой войной
Карта мира перед II Мировой войной Краеведение. Город Колпино.
Краеведение. Город Колпино. ПРЕЗЕНТАЦИЯ СЕНСОРНОЕ РАЗВИТИЕ
ПРЕЗЕНТАЦИЯ СЕНСОРНОЕ РАЗВИТИЕ Вирусные гепатиты с фекально-оральным механизмом передачи
Вирусные гепатиты с фекально-оральным механизмом передачи Подготовка к ГИА. Решение текстовых задач
Подготовка к ГИА. Решение текстовых задач Типология обществ
Типология обществ Церковь в честь Сретения Господня на подворье Иоанно-Предтеченского Леушинского женского монастыря в г. Череповце
Церковь в честь Сретения Господня на подворье Иоанно-Предтеченского Леушинского женского монастыря в г. Череповце Трудовое законодательство
Трудовое законодательство Платежный баланс Статистическая система мирохозяйственных связей
Платежный баланс Статистическая система мирохозяйственных связей Обследование больных. Алгоритм действий
Обследование больных. Алгоритм действий Методы диагностики неисправностей асинхронных машин (машин переменного тока)
Методы диагностики неисправностей асинхронных машин (машин переменного тока) Круговорот веществ - основа целостности биосферы
Круговорот веществ - основа целостности биосферы Презентация Величина тормозного пути транспортного средства
Презентация Величина тормозного пути транспортного средства Ледяные композиции (круглые скульптуры, сказочные замки)
Ледяные композиции (круглые скульптуры, сказочные замки) Знания в твоих руках
Знания в твоих руках На XX Международных духовно-образовательных Рождественских Чтениях
На XX Международных духовно-образовательных Рождественских Чтениях Электровоз ВЛ-10 КРП
Электровоз ВЛ-10 КРП Термин Программная инженерия (software engineering)
Термин Программная инженерия (software engineering) 20230914_ploshchadi_prezentatsiya
20230914_ploshchadi_prezentatsiya Международные стандарты в сфере разрешения таможенных споров. (Лекция 12)
Международные стандарты в сфере разрешения таможенных споров. (Лекция 12) Языковые паттерны (предикаты)
Языковые паттерны (предикаты) лекция 1
лекция 1 Призма
Призма Новогодняя сказка
Новогодняя сказка Аппликация Новогоднее приглашение Диск
Аппликация Новогоднее приглашение Диск Введение в профиль (электроэнергетику). Лекция 4
Введение в профиль (электроэнергетику). Лекция 4 ZCTS 2014 (ZCTS)
ZCTS 2014 (ZCTS) Реки
Реки