Содержание
- 2. Гидратация алкенов Идёт в кислой среде как сопряженное присоединение: ОКСОНИЕВЫЙ ИОН ОКСОНИЕВЫЙ ИОН ТРЕТ-БУТИЛОВЫЙ СПИРТ На
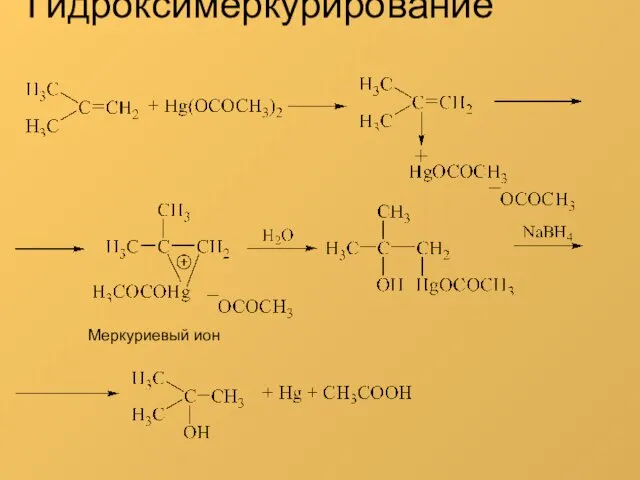
- 3. Гидроксимеркурирование Меркуриевый ион
- 4. Алкоксимеркурирование Если в реакции гидроксимеркурирования к образовавшемуся карб-катиону добавить вместо воды спирт, то в результате реакции
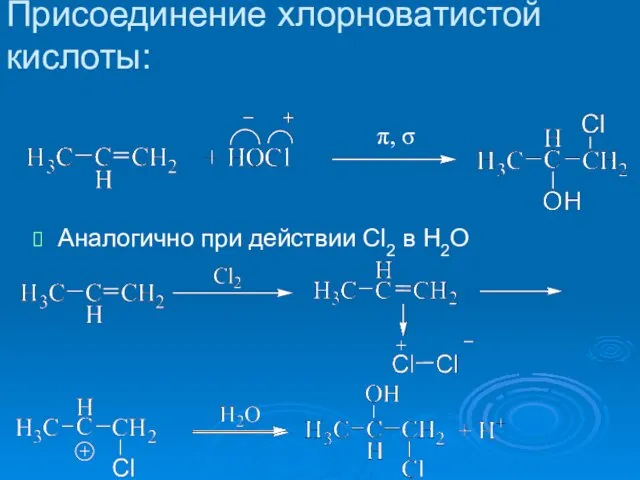
- 5. Присоединение хлорноватистой кислоты: Аналогично при действии Cl2 в H2O π, σ
- 6. Гидроборирование (присоединение гидридов бора к алкенам) В качестве гидроборирующего агента используют диборан B2H6 Диборан в обычных
- 7. При гидроборировании несимметричных олефинов атом бора идет к концевому (терминальному) атому углерода. Гидроборирование протекает как цис-присоединение.
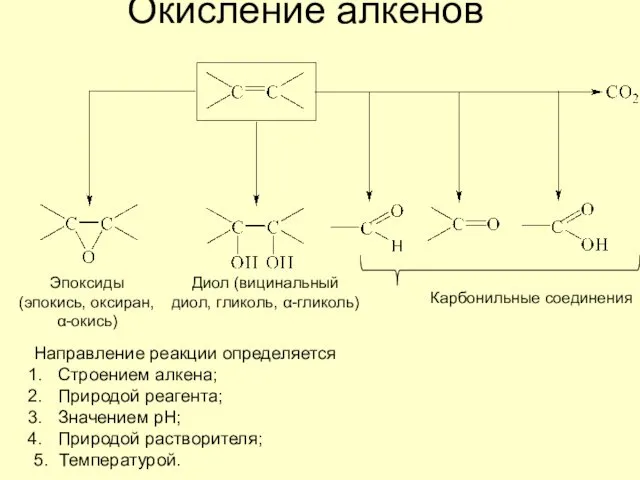
- 8. Окисление алкенов Диол (вицинальный диол, гликоль, α-гликоль) Эпоксиды (эпокись, оксиран, α-окись) Карбонильные соединения Направление реакции определяется
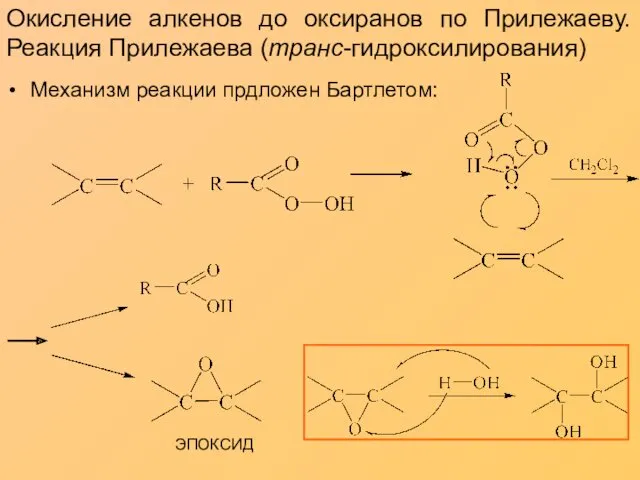
- 9. Окисление алкенов до оксиранов по Прилежаеву. Реакция Прилежаева (транс-гидроксилирования) Механизм реакции прдложен Бартлетом: ЭПОКСИД
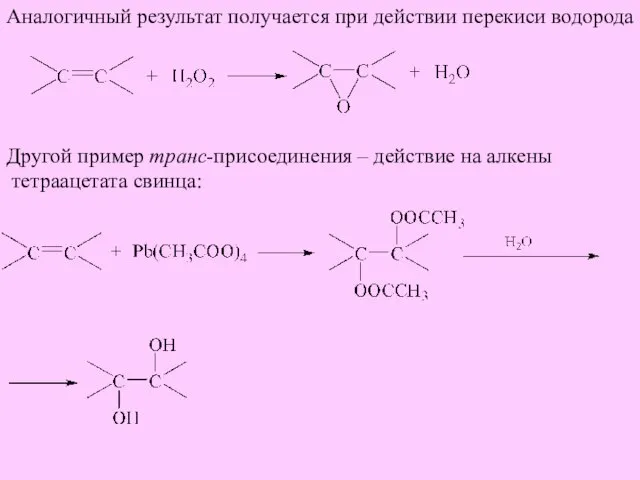
- 10. Аналогичный результат получается при действии перекиси водорода Другой пример транс-присоединения – действие на алкены тетраацетата свинца:
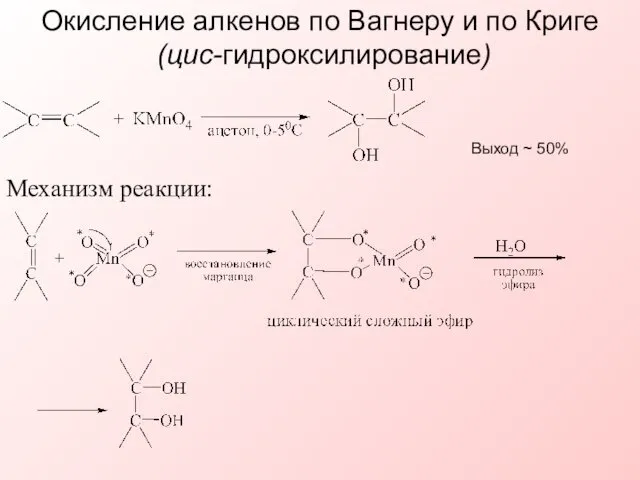
- 11. Окисление алкенов по Вагнеру и по Криге (цис-гидроксилирование) Выход ~ 50% Механизм реакции:
- 12. В тех случаях когда необходимо провести цис-гидроксилирование алкена с высоким выходом и «чисто» , используют OsO4
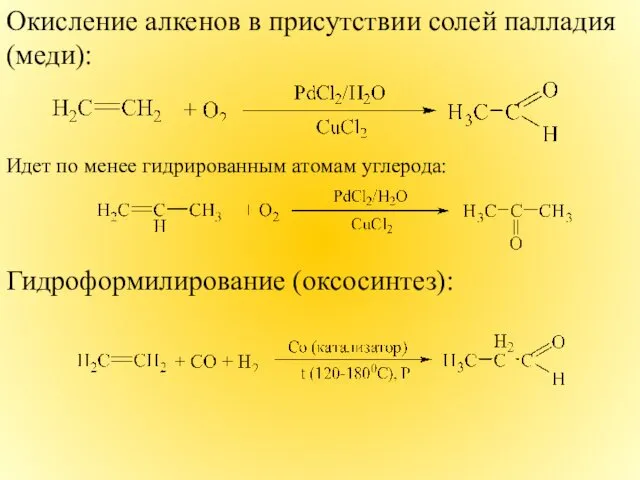
- 13. Окисление алкенов в присутствии солей палладия (меди): Идет по менее гидрированным атомам углерода: Гидроформилирование (оксосинтез):
- 14. Озонирование (озонолиз) Озон – сильный окислитель. Реагирует с алкенами с образованием озонидов. Молекула озона имеет угловую
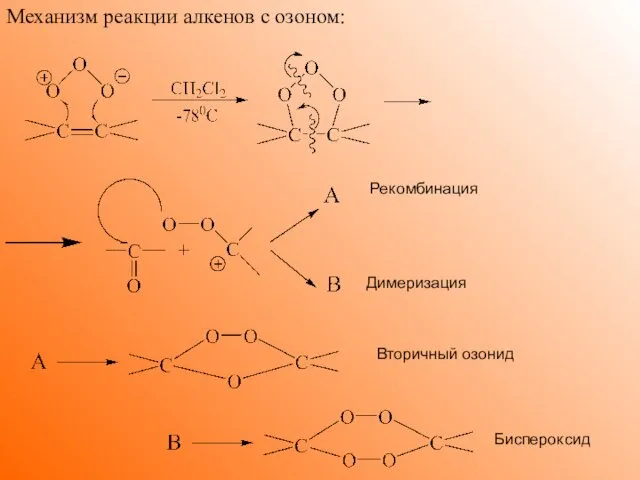
- 15. Механизм реакции алкенов с озоном: Рекомбинация Димеризация Вторичный озонид Биспероксид
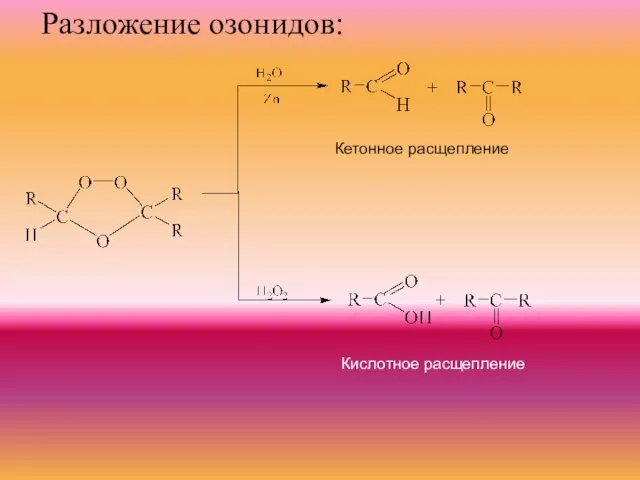
- 16. Разложение озонидов: Кетонное расщепление Кислотное расщепление
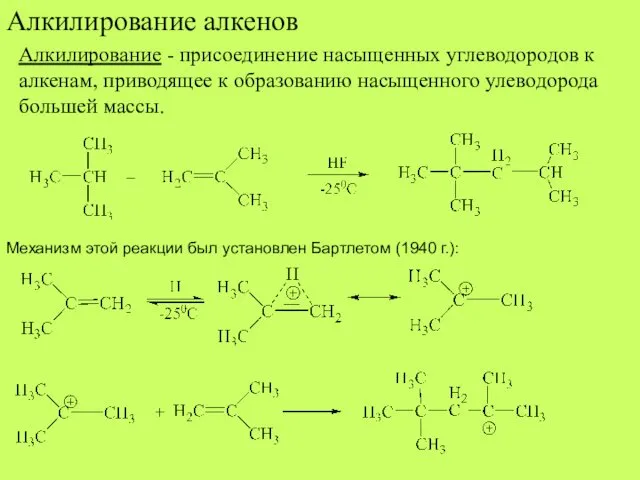
- 17. Алкилирование алкенов Алкилирование - присоединение насыщенных углеводородов к алкенам, приводящее к образованию насыщенного улеводорода большей массы.
- 18. Бартлет показал, что карбокатионы способны отрывать водород от насыщенных углеводородов, имеющих третичный углеродный атом и т.д.
- 19. Полимеризация олефинов Катионная полимеризация: Полимеризация – процесс получения высокомолекулярных соединений, при котором молекула полимера (макромолекула) образуется
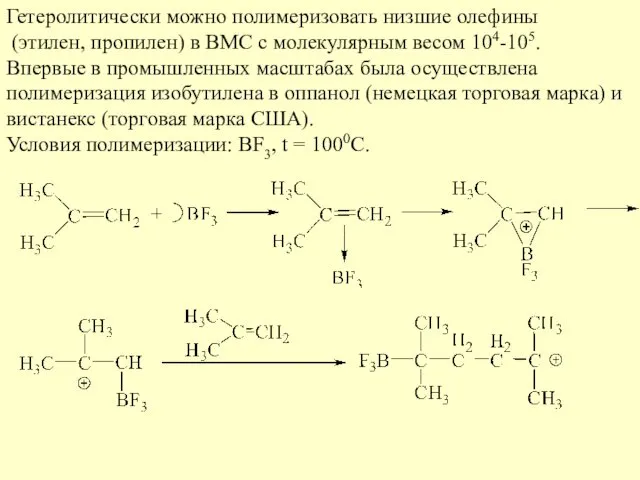
- 20. Гетеролитически можно полимеризовать низшие олефины (этилен, пропилен) в ВМС с молекулярным весом 104-105. Впервые в промышленных
- 22. Скачать презентацию








 Адаптированная программа дошкольного образования для детей с задержкой психического развития
Адаптированная программа дошкольного образования для детей с задержкой психического развития Материалы к Празднику знаний -1сентября Диск
Материалы к Празднику знаний -1сентября Диск Внеклассное мероприятие Вежливые слова
Внеклассное мероприятие Вежливые слова Своя игра (игра-соревнование)
Своя игра (игра-соревнование) Мировая экономика
Мировая экономика Азбука безопасности. Словарик
Азбука безопасности. Словарик هوش مصنوعی
هوش مصنوعی 20231026_osobennosti_organizatsii_olimpiad_po_informatike
20231026_osobennosti_organizatsii_olimpiad_po_informatike Презентация к практическому занятию по химии в 5 классе.
Презентация к практическому занятию по химии в 5 классе. D элементтеріне жалпы сипаттама
D элементтеріне жалпы сипаттама Разработка системы автоматического регулирования питания барабанного котельного агрегата водой (на материалах АО ССГПО)
Разработка системы автоматического регулирования питания барабанного котельного агрегата водой (на материалах АО ССГПО) Русь в правление Ивана Грозного (1533 - 1584)
Русь в правление Ивана Грозного (1533 - 1584) Медико-демографические проблемы населения России
Медико-демографические проблемы населения России Мультибрендовая платформа FROZA. Автозапчасти и аксессуары для авто, мото, грузовой и спецтехники
Мультибрендовая платформа FROZA. Автозапчасти и аксессуары для авто, мото, грузовой и спецтехники Modern construction technologies
Modern construction technologies Новая система обращения с твердыми коммунальными отходами
Новая система обращения с твердыми коммунальными отходами Социальная сеть Facebook
Социальная сеть Facebook Интеллектуальная игра Пентагон
Интеллектуальная игра Пентагон Загадки про грибы
Загадки про грибы Понятие и сущность международного права. (Лекция 1)
Понятие и сущность международного права. (Лекция 1) Подготовка деталей перед сборкой и сваркой. Сборка и сварка
Подготовка деталей перед сборкой и сваркой. Сборка и сварка Великобритания во второй половине XX века
Великобритания во второй половине XX века презентация №Фенол
презентация №Фенол Индекс экономической безопасности
Индекс экономической безопасности Балалардағы экг ерекшеліктері.Жүрек тондарының пайда болу механизмдері
Балалардағы экг ерекшеліктері.Жүрек тондарының пайда болу механизмдері Определение надежности, безотказности, работоспособности, долговечности, ремонтопригодности
Определение надежности, безотказности, работоспособности, долговечности, ремонтопригодности Семья.Семейные ценности.
Семья.Семейные ценности. Возбудитель коклюша Bordetella pertussis
Возбудитель коклюша Bordetella pertussis